دوره 33، شماره 10 - ( دی 1404 )
جلد 33 شماره 10 صفحات 9508-9495 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Sharifi Z, Kaki A. Investigation of the Changes in CXCL-14 and EPDR1 Gene Expression in Response to Aerobic Exercise in an Induced Obesity Animal Model. JSSU 2026; 33 (10) :9495-9508
URL: http://jssu.ssu.ac.ir/article-1-6490-fa.html
URL: http://jssu.ssu.ac.ir/article-1-6490-fa.html
شریفی زهرا، کاکی احمد. بررسی تغییرات بیان ژنهای CXCL-14 و EPDR1 در پاسخ به تمرین هوازی در مدل حیوانی چاقی القاشده. مجله علمي پژوهشي دانشگاه علوم پزشكي شهید صدوقی يزد. 1404; 33 (10) :9495-9508
متن کامل [PDF 955 kb]
(159 دریافت)
| چکیده (HTML) (362 مشاهده)
References:
1- Aparecida Silveira E, Vaseghi G, de Carvalho Santos AS, Kliemann N, Masoudkabir F, Noll M, et al. Visceral Obesity and Its Shared Role in Cancer and Cardiovascular Disease: A Scoping Review of the Pathophysiology and Pharmacological Treatments. Int J Mol Sci 2020; 21(23): 9042.
2- Lee M-J, Kim J. The Pathophysiology of Visceral Adipose Tissues in Cardiometabolic Diseases. Biochem pharmacol 2024; 222: 116116.
3- Pinckard KM, Stanford KI. The Heartwarming Effect of Brown Adipose Tissue. Mol Pharmacol 2022; 102(1): 460-71.
4- Ghesmati Z, Rashid M, Fayezi S, Gieseler F, Alizadeh E, Darabi M. An Update on the Secretory Functions of Brown, White, And Beige Adipose Tissue: Towards Therapeutic Applications. Rev Endocr Metab Disord 2024; 25(2): 279-308.
5- Villarroya J, Cereijo R, Giralt M, Villarroya F. Secretory Proteome of Brown Adipocytes in Response to Camp-Mediated Thermogenic Activation. Front physiol 2019; 10: 67.
6- Zhang J, Kibret BG, Vatner DE, Vatner SF. The Role of Brown Adipose Tissue in Mediating Healthful Longevity. J Cardiovasc Aging 2024; 4(2): 17.
7- Coassolo L, Dannieskiold-Samsøe NB, Zhao M, Allen H, Svensson KJ. New Players of the Adipose Secretome: Therapeutic Opportunities and Challenges. Curr Opin Pharmacol 2022; 67: 102302.
8- Cereijo R, Gavaldà-Navarro A, Cairó M, Quesada-López T, Villarroya J, Morón-Ros S, et al. CXCL14, A Brown Adipokine that Mediates Brown-Fat-To-Macrophage Communication in Thermogenic Adaptation. Cell Metab 2018; 28(5): 750-63.
9- Cereijo R, Quesada-López T, Gavaldà-Navarro A, Tarascó J, Pellitero S, Reyes M, et al. The Chemokine CXCL14 Is Negatively Associated with Obesity and Concomitant Type-2 Diabetes in Humans. Int J Obes (Lond) 2021; 45(3): 706-10.
10- Takahashi M, Takahashi Y, Takahashi K, Zolotaryov FN, Hong KS, Iida K, et al. CXCL14 Enhances Insulin-Dependent Glucose Uptake in Adipocytes and Is Related to High-Fat Diet-Induced Obesity. Biochem Biophys Res Commun 2007; 364(4): 1037-42
11- Deshmukh AS, Peijs L, Beaudry JL, Jespersen NZ, Nielsen CH, Ma T, et al. Proteomics-Based Comparative Mapping of the Secretomes of Human Brown and White Adipocytes Reveals EPDR1 as a Novel Batokine. Cell Metab 2019; 30(5): 963-75.
12- Wei Y, Xiong ZJ, Li J, Zou C, Cairo CW, Klassen JS, et al. Crystal Structures of Human Lysosomal EPDR1 Reveal Homology with the Superfamily of Bacterial Lipoprotein Transporters. Commun Biol 2019; 2(1): 52.
13- Engin B, Willis SA, Malaikah S, Sargeant JA, Yates T, Gray LJ, et al. The Effect of Exercise Training on Adipose Tissue Insulin Sensitivity: A Systematic Review and Meta‐Analysis. Obes Rev 2022; 23(7): e13445.
14- Guo Q, Li N, Shi H, Gan Y, Wang W, Jia J, et al. Aerobic Exercise Prevents High-Fat-Diet-Induced Adipose Tissue Dysfunction in Male Mice. Nutrients 2024; 16(20): 3451.
15- Ringholm S, Grunnet Knudsen J, Leick L, Lundgaard A, Munk Nielsen M, Pilegaard H. PGC-1α Is Required for Exercise-And Exercise Training-Induced UCP1 Up-Regulation in Mouse White Adipose Tissue. PloS one 2013; 8(5): e64123.
16- Mu W-J, Zhu J-Y, Chen M, Guo L. Exercise-Mediated Browning of White Adipose Tissue: Its Significance, Mechanism and Effectiveness. Int J Mol Sci 2021; 22(21): 11512.
17- Young MF, Valaris S, Wrann CD. A Role For FNDC5/Irisin in the Beneficial Effects of Exercise on the Brain and in Neurodegenerative Diseases. Prog Cardiovasc Dis 2019; 62(2): 172-8.
18- Shi H, Hao X, Sun Y, Zhao Y, Wang Y, Cao X, et al. Exercise‐Inducible Circulating Extracellular Vesicle Irisin Promotes Browning and the Thermogenic Program in White Adipose Tissue. Acta Physiol 2024; 240(3): e14103.
19- Milton-Laskibar I, Marcos-Zambrano LJ, Gómez-Zorita S, Fernández-Quintela A, Carrillo de Santa Pau E, Martínez JA, et al. Gut Microbiota Induced by Pterostilbene and Resveratrol in High-Fat-High-Fructose Fed Rats: Putative Role in Steatohepatitis Onset. Nutrients 2021; 13(5): 1738.
20- Rocha-Rodrigues S, Rodríguez A, Gouveia AM, Gonçalves IO, Becerril S, Ramírez B, et al. Effects of Physical Exercise on Myokines Expression and Brown Adipose-Like Phenotype Modulation in Rats Fed a High-Fat Diet. Life Sciences 2016; 165: 100-8.
21- Alradi M, Askari H, Shaw M, Bhavsar JD, Kingham BF, Polson SW, et al. A Long-Term High-Fat Diet Induces Differential Gene Expression Changes in Spatially Distinct Adipose Tissue of Male Mice. Physiol Genomics 2024; 56(12): 819-32.
22- Kiran S, Rakib A, Kodidela S, Kumar S, Singh UP. High-Fat Diet-Induced Dysregulation of Immune Cells Correlates with Macrophage Phenotypes and Chronic Inflammation in Adipose Tissue. Cells 2022; 11(8): 1327.
23- Feillet‐Coudray C, Fouret G, Vigor C, Bonafos B, Jover B, Blachnio‐Zabielska A, et al. Long‐Term Measures of Dyslipidemia, Inflammation, and Oxidative Stress in Rats Fed a High‐Fat/High‐Fructose Diet. Lipids 2019; 54(1): 81-97.
24- Singh S, Sharma A, Guru B, Ahmad S, Gulzar F, Kumar P, et al. Fructose-Mediated NLRP3 Activation Induces Inflammation and Lipogenesis in Adipose Tissue. J Nutr Biochem 2022; 107: 109080.
25- Tourniaire F, Romier-Crouzet B, Lee JH, Marcotorchino J, Gouranton E, Salles J, et al. Chemokine Expression in Inflamed Adipose Tissue is Mainly Mediated by Nf-Κb. PloS one 2013; 8(6): e66515.
26- Nara N, Nakayama Y, Okamoto S, Tamura H, Kiyono M, Muraoka M, et al. Disruption of Cxc Motif Chemokine Ligand-14 in Mice Ameliorates Obesity-Induced Insulin Resistance. J Biol Chem 2007; 282(42): 30794-803.
27- Tanegashima K, Okamoto S, Nakayama Y, Taya C, Shitara H, Ishii R, et al. CXCL14 Deficiency in Mice Attenuates Obesity and Inhibits Feeding Behavior in A Novel Environment. PloS one 2010; 5(4): e10321.
28- Atanes P, Hawkes RG, Olaniru OE, Ruz-Maldonado I, Amisten S, Persaud SJ. CXCL14 Inhibits Insulin Secretion Independently of CXCR4 or CXCR7 Receptor Activation or Camp Inhibition. Cell Physiol Biochem 2019; 52(4): 879-92.
29- Franczyk MP, He M, Yoshino J. Removal of Epididymal Visceral Adipose Tissue Prevents Obesity-Induced Multi-Organ Insulin Resistance in Male Mice. J Endocrine Society 2021; 5(5): bvab024.
30- Cataldo LR, Gao Q, Argemi-Muntadas L, Hodek O, Cowan E, Hladkou S, et al. The Human Batokine EPDR1 Regulates Β-Cell Metabolism and Function. Mol Metab 2022; 66: 101629.
31- Fu P, Zhu R, Jia J, Hu Y, Wu C, Cieszczyk P, et al. Aerobic Exercise Promotes the Functions of Brown Adipose Tissue in Obese Mice Via a Mechanism Involving COX2 in the VEGF Signaling Pathway. Nutr Metab 2021; 18(1): 56.
32- McKie GL, Wright DC. Biochemical Adaptations in White Adipose Tissue Following Aerobic Exercise: from Mitochondrial Biogenesis to Browning. Biochem J 2020; 477(6): 1061-81.
33- Zhang Y, Xie C, Wang H, Foss RM, Clare M, George EV, et al. Irisin Exerts Dual Effects on Browning and Adipogenesis of Human White Adipocytes. Am J Physiol Endocrinol Metab 2016; 311(2): E530-41.
34- Roca-Rivada A, Castelao C, Senin LL, Landrove MO, Baltar J, Crujeiras AB, et al. FNDC5/Irisin Is Not Only a Myokine but Also an Adipokine. PloS one 2013; 8(4): e60563.
35- Powers SK, Jackson MJ. Exercise-Induced Oxidative Stress: Cellular Mechanisms and Impact on Muscle Force Production. Physiol Rev 2008; 88(4): 1243-76.
36- Voisin S, Eynon N, Yan X, Bishop D. Exercise Training and DNA Methylation in Humans. Acta Physiol 2015; 213(1): 39-59.
37- Barres R, Yan J, Egan B, Treebak JT, Rasmussen M, Fritz T, et al. Acute Exercise Remodels Promoter Methylation in Human Skeletal Muscle. Cell Metab 2012; 15(3): 405-11.
38- Pedersen BK. Anti‐Inflammatory Effects of Exercise: Role in Diabetes and Cardiovascular Disease. Eur J Clin Invest 2017; 47(8): 600-11.
39- Stanford KI, Goodyear LJ. Exercise Regulation of Adipose Tissue. Adipocyte 2016; 5(2): 153-62.
40- Ntanasis-Stathopoulos J, Tzanninis J, Philippou A, Koutsilieris M. Epigenetic Regulation on Gene Expression Induced by Physical Exercise. J Musculoskelet Neuronal Interact 2013; 13(2): 133-46.
41- Improta Caria AC, Nonaka CKV, Pereira CS, Soares MBP, Macambira SG, Souza BSdF. Exercise Training-Induced Changes in Micrornas: Beneficial Regulatory Effects in Hypertension, Type 2 Diabetes, and Obesity. Int J Mol Sci 2018; 19(11): 3608.
متن کامل: (82 مشاهده)
مقدمه
چاقی، بهعنوان یکی از چالشهای اساسی نظامهای سلامت در قرن بیستویکم، با روندی فزاینده در سطح جهانی، بهویژه در کشورهای در حال توسعه، مطرح است و پیامدهای گستردهای در بروز و گسترش بیماریهای مزمن ناشی از سبک زندگی مدرن به همراه دارد. این پدیده، که از آن بهعنوان یک اختلال پیچیده متابولیکی یاد میشود، عمدتاً با تجمع غیرعادی و مفرط چربی بدن، بهویژه در نواحی احشایی، شناخته میشود و با طیف متنوعی از اختلالات متابولیکی و التهابی، از جمله دیابت نوع ۲، سندرم متابولیک، بیماریهای قلبیعروقی، مقاومت به انسولین، ناهنجاریهای لیپیدی و التهاب مزمن خفیف همراه است (3-1). در سالهای اخیر، پژوهشگران دریافتهاند که بافت چربی صرفاً یک مخزن انرژی غیرفعال نیست، بلکه یک بافت فعال متابولیک و غدد درونریز محسوب میشود که طیف وسیعی از مولکولهای پیامرسان نظیر آدیپوکاینها، سایتوکاینها و اخیراً "باتوکینها" را تولید میکند (5, 4). از میان انواع بافت چربی، بافت چربی قهوهای(Brown Adipose Tissue) به دلیل نقش برجستهای که در تولید گرما (ترموژنز وابسته به Uncoupling Protein 1) و تنظیم تعادل انرژی ایفا میکند، مورد توجه گسترده قرار گرفته است (6). اما علاوه بر نقش ترموژنیک، Brown Adipose Tissue از طریق ترشح مولکولهایی با عملکرد شبههورمونی موسوم به باتوکینها (Batokines)، در تنظیم متابولیسم گلوکز و چربی، حساسیت انسولینی، و عملکرد سیستم ایمنی و قلبی-عروقی نقش دارد (7, 4). در میان ترکیبات ترشحشده از بافت چربی قهوهای، دو مولکول CXCL-14 و EPDR1 بهعنوان عوامل میانجی نوظهور در تنظیم فرآیندهای متابولیکی و ایمنی شناخته شدهاند که نقش بالقوهای در هموستاز انرژی، تعادل التهابی و سازوکارهای سلولی مرتبط با اختلالات متابولیک ایفا میکنند (9, 8). ژن CXCL-14، که یکی از اعضای خانواده کموکاینها محسوب میشود، یک کموتاکسین فاقد گیرنده شناختهشده اختصاصی است که بیان گستردهای در بافتهای متابولیک از جمله بافت چربی قهوهای دارد (10). شواهد تجربی نشان میدهد که این مولکول نقش مؤثری در تنظیم مهاجرت ماکروفاژها به بافتهای محیطی، حفظ حساسیت به انسولین در محیط متابولیک و کاهش التهاب مزمن با درجه پایین ایفا مینماید (9). بهویژه، دادههای حاصل از مدلهای حیوانی و سلولی بیانگر آناند که CXCL-14 ممکن است از طریق میانجیگری در تعاملات سلولهای ایمنی و آدیپوسیتها، در کنترل پاسخهای التهابی و بهبود عملکرد متابولیکی در شرایط مرتبط با چاقی نقش داشته باشد (11, 10). از سوی دیگر، ژن EPDR1 که به خانواده پروتئینهای مرتبط با اپندیمین (Ependymin-related proteins) تعلق دارد، بهعنوان مولکولی با نقشهای چندگانه در فرآیندهای زیستی نظیر تمایز سلولی، تنظیم چسبندگی بین سلولی و احتمالاً تنظیم فعالیت متابولیکی بافت چربی قهوهای شناخته میشود (12). با وجود شناسایی بیان این ژن در بافتهای متابولیک و گزارشهایی از نقش آن در سازوکارهای سلولی مرتبط با تعادل انرژی، دانش کنونی در خصوص عملکرد دقیق EPDR1، بهویژه در شرایط پاتولوژیک مانند چاقی القاشده ناشی از رژیم غذایی پرچرب، همچنان ناکافی و پراکنده باقی مانده است (13). از طرف دیگر، یافتههای حاصل از مطالعات تجربی گوناگون بهوضوح نشان میدهد که فعالیت بدنی منظم، بهویژه تمرینات هوازی، از ظرفیت بالایی برای تعدیل فرآیندهای التهابی مزمن، ارتقای حساسیت به انسولین، افزایش مصرف انرژی و بهبود عملکرد فیزیولوژیک بافت چربی برخوردار است (15, 14). تمرین هوازی از طریق فعال کردن مسیرهای مولکولی متعدد از جمله فعالسازی آنزیم AMPK، افزایش بیان فاکتور تنظیمی PGC-1α، مهار مسیر التهابی NF-κB، و القای بیان ژنهای مرتبط با ترموژنز نظیر UCP1، به بازآرایی متابولیکی و ساختاری در بافتهای چربی سفید و قهوهای منجر میشود (17, 16). علاوهبر این، ورزش هوازی با افزایش ترشح میوکاینهایی چون FNDC5 و محصول آن یعنی آیریزین از عضلات اسکلتی، میتواند موجب تحریک عملکرد ترموژنیک BAT و القای تغییرات فنوتیپی در WAT به سوی قهوهای شدن (browning) گردد (19, 18). این اثرات چندمسیره، ورزش را بهعنوان یک مداخله غیر دارویی مؤثر در تنظیم عملکرد بافت چربی و بهبود اختلالات متابولیکی ناشی از چاقی، در کانون توجه پژوهشهای اخیر قرار داده است. با وجود پیشرفتهای موجود، هنوز خلأهای جدی در شناخت دقیق مکانیسمهای مولکولی اثر تمرین هوازی بر بیان ژنهای خاص در BAT بهویژه ژنهای تازه شناساییشدهای مانند CXCL-14 و EPDR1 وجود دارد. بیشتر مطالعات تمرکز خود را بر ژنهای کلاسیک نظیر UCP1، PRDM16 و PGC-1α معطوف کردهاند و کمتر به نقش عوامل تازه شناساییشدهای پرداختهاند که میتوانند اهداف بالقوهای برای درمان چاقی و بیماریهای متابولیک محسوب شوند. ازاینرو، این مطالعه با هدف بررسی تأثیر تمرینات هوازی بر تغییرات بیان ژنهای CXCL-14 و EPDR1 در مدل حیوانی چاقی القاشده با رژیم پرچرب طراحی گردید. انجام این پژوهش میتواند درک عمیقتری از نقش این ژنها در تنظیم عملکرد متابولیکی و ایمنی بافت چربی فراهم سازد و سازوکارهای مولکولی دخیل در پاسخ به مداخلات ورزشی را روشنتر نماید.
روش بررسی
در این پژوهش تجربی، 32 سر موش صحرایی نر نژاد ویستار 8 هفتگی با محدوده وزنی 5/2±198 گرم از مرکز تکثیر حیوانات آزمایشگاهی دانشگاه علوم پزشکی جندیشاپور اهواز تهیه و در گروههای چهارتایی در قفسهای استاندارد پلیکربنات در شرایط دمایی 2±22 درجه سانتیگراد و رطوبت نسبی 40 تا 60 درصد، تحت چرخه 12:12 ساعت تاریکی – روشنایی و با دسترسی آزاد به آب و غذا نگهداری شدند. بعد از گذشت دو هفته تطابق با محیط جدید آزمایشگاه و تغذیه از رژیم غذایی استاندارد (20٪ کیلوکالری از چربی، 20٪ پروتئین و 60٪ کربوهیدرات که 3/1 کیلوکالری بهازای هر گرم انرژی داشت)، موشها به طور تصادفی به دو گروه رژیم غذایی استاندارد (12 سر) و گروه رژیم غذایی پرچرب (20 سر) تقسیم شدند در مرحله اول، 24 هفته موشها گروه رژیم غذایی پرچرب، تحت رژیم غذایی 60 درصد چربی و 25 درصد فروکتوز قرار گرفتند. سپس برای بررسی تأیید القاء چاقی، از هر گروه 4 سر موش انتخاب و شاخصهای تنسنجی و پارامترهای بیوشیمیایی خون مورد ارزیابی قرار گرفت. پس از احراز چاقی در گروه رژیم غذایی پر چرب، موشها بهطور تصادفی به سه گروه (8 = n)؛ گروه شاهد Normal (غذای استاندارد)، گروه رژیم غذایی پرچرب HFD و گروه رژیم غذایی پرچرب و تمرین هوازی THFD دستهبندی شدند. تمام مراحل پژوهش، محققان با رعایت اصول اخلاقی کار با حیوانات، طبق دستورالعملهای اخلاقی مؤسسات ملی برای مراقبت و استفاده از حیوانات آزمایشگاهی (برابر با پروتکل هلسینکی 2006) مصوب دانشگاه آزاد اسلامی واحد اهواز با کد (IR.IAU.AHVAZ.REC.1404.125) تصویب و انجام شد. القاء چاقی: بهمنظور القای چاقی از رژیم غذایی 60 درصد چربی حاوی 25 درصد فروکتوز استفاده شد. برای ساخت 100 کیلوگرم پلت پرچرب 60 درصد (شرکت زیست فن آوران رویان اصفهان)، 45 کیلوگرم پودر پلت استاندارد با 30 کیلوگرم چربی حیوانی (حاصل از آبکردن دنبه گاو و روغن دانۀ سویا) ترکیب و به شکل پلت استاندارد قالبزده شد و تا پایان دوره تحقیق در اختیار گروههای رژیم پرچرب قرار گرفت. همچنین برای تهیه محلول 25 درصد حجمی فروکتوز؛ از رابطه (۱۰۰ × حجم محلول (میلیلیتر) / حجم حلشونده (میلیلیتر) = درصد حجمی) استفاده شد. 250 میلیلیتر مایع فروکتوز را در 750 میلیلیتر آب حل تا محلول 25 درصد حجمی فروکتوز به دست آید. محلول فروکتوز، بهصورت روزانه تهیه و به طور آزاد، از ابتدا تا پایان دوره پژوهش در اختیار موشها گروه رژیم پرچرب قرار میگرفت (20).
پروتکل تمرین هوازی: پس از حصول چاقی در موشها، پروتکل تمرین هوازی به مدت 8 هفته انجام شد. در پژوهش حاضر پروتکل تمرین هوازی، بر اساس مطالعه سیلویا روچا و همکاران در سال 2016 استفاده شد؛ بدینصورت که گروه رژیم غذایی پرچرب و تمرین هوازی THFD در معرض تمرین نوار گردان، 5 جلسه در هفته و به مدت 8 هفته قرار گرفتند. تمام جلسات تمرینی در پایان سیکل خواب حیوانات و بین ساعت 16 تا 18 عصر برگزار شد. سرعت و مدت تمرین نوار گردان به تدریج افزایش یافته و از 15 متر در دقیقه به مدت 30 دقیقه در هفته اول، 16 متر در دقیقه برای 35 دقیقه در هفته دوم، 18متر در دقیقه40 دقیقه در هفته سوم، 20 متر در دقیقه برای 45 دقیقه در هفته چهارم، به 21 متر در دقیقه 50 دقیقه در هفته پنجم و 23 متر در دقیقه 55 دقیقه در هفته ششم، 25 متر در دقیقه 60 دقیقه در هفته هفتم و هفته هشتم افزایش یافت. جهت رسیدن سازگاریهای بهدست آمده به حالت یکنواخت، تمامی متغیرهای تمرینی درهفته های پایانی ثابت نگهداشته شد (21)(جدول 1).
جدول 1: پروتکل تمرین هوازی
.JPG)
اندازهگیری شاخصهای تنسنجی: اندازهگیری شاخصهای تنسنجی شامل؛ وزن، دور شکم، دور سینه، نسبت دور شکم بهدور سینه، طول بدن، شاخص توده بدن و شاخص Lee در سه زمان؛ ابتدای دوره، هفته 24 ام و پایان دوره، در یک روز مشخص، از همه حیوانات در تمام گروهها انجام شد.
اندازه گیری وزن بدن (W): برای اندازه گیری وزن موشها از ترازوی دیجیتال موش آزمایشگاهی (شرکت کیمیا کهربای مبین، ساخت کشور ایران) جهت وزن کشی استفاده شد. دور شکم (AC): بلافاصله جلوی پای عقب در بخش بزرگترین ناحیه شکم، برای دور شکم به سانتی متر اندازه گیری شد. دور سینه (TC): بلافاصله پشت دست جلو به سانتی متر برای دور سینه اندازه گیری شد. نسبت دور شکم به دور سینه (AC/TC): اندازه دور شکم را بر اندازه دور سینه تقسیم و نسبت آن به دست آمد. طول بدن (L): طول بدن از نوک بینی تا مقعد به سانتی متر اندازه گیری شد. شاخص توده بدن (BMI): وزن بدن به گرم تقسیم بر طول بدن از بینی تا مقعد به توان دو به سانتی متر به عنوان شاخص توده بدن محاسبه شد.
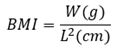
شاخص Lee: شاخص لی به عنوان شاخصی از ترکیب بدنی در جوندگان با استفاده از فرمول؛ ریشه مکعب وزن بدن به گرم تقسیم بر طول بدن از بینی تا مقعد به سانتی متر محاسبه شد.
.JPG)
سنجش پروفایلهای لیپیدی (Lipid Profile): اندازهگیری سطوح سرمی پارامترهای بیوشیمیایی لیپیدی شامل؛ تری گلیسیرید، کلسترول تام، کلسترول HDL و کلسترول LDL بعد از 24 هفته مصرف غذای پر چرب به همراه فروکتوز از گروه رژیم غذایی پرچرب (4 سر) و گروه شاهد (4 سر) اندازه گیری شد. ابتدا موشها به مدت 12 ساعت محرومیت از غذا، توسط تزریق درون صفاقی ترکیب از کتامین90 (میلیگرم /کیلوگرم) و زایلازین 10(میلیگرم /کیلوگرم) بیهوش، سپس قفسه سینه حیوان شکافته و 5 میلی لیتر نمونه خون به طور مستقیم از قلب موشها گرفته شد و در لولههای پلاستیکی حاوی ژل Clot جمعآوری شد. پس از انعقاد خون، نمونههای خون با سرعت 4000 دور در دقیقه و به مدت 15 دقیقه سانتریفیوژ گردید، سرم آن جداسازی و در اپندورفهای مخصوص قرار داده شد. میزانتری گلیسیرید به روش آنزیماتیک (لیپاز برای تبدیل تری گلیسیرید به گلیسرول) و کلسترول به روش آنزیماتیک کلسترول استراز (لیپاز برای تبدیل تری گلیسرید به گلیسرول) و کلسترول HDL توسط روش رسوبی آنزیمی (همگی تستها با به کارگیری کیتهای تجاری شرکت بوتیک که مورد تایید آزمایشگاه مرجع سلامت ایران بود و با دستگاه اتوآنالایزر (Hitachi,japan) تعیین شد) و کلسترول LDL توسط فرمول فریدوالد (Friedewald equation) (LDL-C = TC - (HDL-C) - (TG/5) محاسبه شد.
استخراج نمونه و روش اندازهگیری: در پایان دوره بعد از اجرای هشت هفته برنامه تمرینی، همه موشها، 48 ساعت پس از آخرین جلسه، بیهوش، کشته و جراحی شدند. تحت شرایط استریل بافت چربی احشایی تشریح و استخراج گردید و پس از شستشو با نرمال سالین، با ترازوی دیجیتال (با دقت اندازهگیری 0/001 گرم) وزن شد، یک بخش از آن بهعنوان نمونه، برای آزمایشهای سلولی و مولکولی به روش ریل تایم، بلافاصله در نیتروژن مایع منجمد و نمونهها تا زمان انجام آزمایشهای ملکولی در فریزر 80- درجه سانتیگراد نگهداری شدند.
Real Time-PCR: حدود 50 میلیگرم از بافت چربی احشایی جهت استخراج RNA کل به نسبت 1 به 10 با استفاده از کیت QIAzol Lysis Reagent هموژن گردید. بهمنظور برداشتن اجزای پروتئینی محصول در دمای 4 درجه سانتیگراد، به مدت 10 دقیقه، با دور g12000 سانتریفیوژ شد. سپس به نسبت 1 به 0/5 با محلول کلروفرم مخلوط و به مدت 15 ثانیه بهشدت تکان داده شد. محصول در دمای 4 درجه سانتیگراد، به مدت 15 دقیقه، با 12000 (دور در دقیقه) سانتریفیوژ و بخش معدنی و آبی از هم جدا شدند. بخش محتوی RNA برداشته و با نسبت یک به نیم با محلول ایزوپروپانول مخلوط و به مدت ده دقیقه در دمای اتاق نگهداری و سپس در دمای 4 درجه سانتیگراد، به مدت 10 دقیقه، با 12000 سانتریفیوژ شد. پلت حاوی RNA با محلول اتانول شستشو داده شد و سپس در ۲۰ میکرولیتر آب بدون RNase حل گردید. غلظت RNA موردسنجش واقع شد طبق شرکت (Eppendorf - Germany) و به نسبت 260 به 280 بین 1/8 تا 2 بهعنوان تلخیص مطلوب تعریف گردید. سنتز cDNA تکرشتهای از پرایمر (Oligo dt MWG-Biotech, Germany) و آنزیم نسخهبرداری معکوس (Fermentas) و بر اساس پروتکل مربوطه انجام شد. از تکنیک RT-qPCR جهت تأیید بیان ژنهای CXCL-14 و EPDR1 بهصورت کمی استفاده شد، هر واکنش PCR با استفاده از دستگاه (PCR master mix Applied Biosystems) و SYBR Green در دستگاه ABI Step One (Applied Biosystems, Sequence Detection Systems. Foster City, CA) طبق پروتکل شرکت سازنده انجام گرفت. 40 سیکل برای هر چرخه Real-Time PCR در نظر گرفته شد و دماهای هر سیکل شامل 94 درجه سانتیگراد برای 20 ثانیه، 60-58 درجه سانتیگراد برای 30 ثانیه و 72 درجه سانتیگراد برای 30 ثانیه تنظیم شدند. ضمن اینکه از GAPDH بهعنوان ژن مرجع استفاده گردید. نسبت بیان ژنهای موردبررسی در این مطالعه، با روش مقایسهای چرخه آستانه (Thereshold Cycle(CT)) مورد ارزیابی قرار گرفتند. با استفاده از قرار دادن داده¬ها در فرمول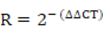 میزان بیان ژن هدف با ژن مرجع نرمالیز شده و بیان ژنهای گروه سالم بهعنوان کالیبراتور در نظر گرفته شد. مشخصات پرایمرهای سنتز شده در جدول 2 ذکر شده است.
میزان بیان ژن هدف با ژن مرجع نرمالیز شده و بیان ژنهای گروه سالم بهعنوان کالیبراتور در نظر گرفته شد. مشخصات پرایمرهای سنتز شده در جدول 2 ذکر شده است.
تجزیه و تحلیل آماری
جهت تعیین نرمال بودن دادهها از آزمون کلوموگروف - اسمیرنوف استفاده شد. برای بررسی معنیدار بودن اختلاف بین گروهها از تحلیل واریانس یکطرفه و در صورت معنی-داری، جهت تعیین تفاوت بین میانگینهای دوگروهی از آزمون تعقیبی توکی استفاده شد. تجزیهوتحلیل دادهها با استفاده از نرمافزار SPSS version 16 در سطح معنیداری (0.05 > P) انجام شد.
نتایج
نتایج حاصل از مقایسه شاخصهای تنسنجی شامل وزن بدن، دور شکم، دور سینه، نسبت دور شکم بهدور سینه، طول بدن، شاخص توده بدنی (BMI) و شاخص لی (Lee index) در دو بازه زمانی ابتدای مطالعه و هفته بیست و چهارم نشان داد که بین گروه دریافتکننده رژیم غذایی پرچرب (HFD) با رژیم غذایی شاهد (Normal) تفاوت معناداری وجود دارد. (P=0/001) این تفاوت معنادار بیانگر تأثیر رژیم غذایی پرچرب بر افزایش شاخصهای تنسنجی در طول دوره مطالعه است. در هفتههای پایانی مطالعه، نتایج تحلیل واریانس یکطرفه نشان داد که میانگین تغییرات شاخصهای تنسنجی (شامل وزن بدن، دور شکم، دور سینه، نسبت دور شکم بهدور سینه، طول بدن، شاخص توده بدنی و شاخص لی) در گروه دریافتکننده رژیم غذایی پرچرب همراه با تمرین هوازی (THFD)، در مقایسه با گروه دریافتکننده تنها رژیم پرچرب (HFD) به طور معناداری کمتر بود. (P=0/001) (جدول 3). پس از القای چاقی از طریق مصرف رژیم غذایی پرچرب همراه با فروکتوز، سطوح سرمی شاخصهای لیپیدی شامل تری گلیسیرید، کلسترول تام، کلسترول لیپوپروتئین با چگالی بالا و لیپوپروتئین با چگالی پایین در هفته بیست و چهارم در گروههای دریافتکننده رژیم پرچرب (HFD) و گروه شاهد (Normal) مورد سنجش قرار گرفت. نتایج تحلیل آماری نشان داد که سطوح تری گلیسیرید، کلسترول تام و LDL-C در گروه HFD به طور معناداری نسبت به گروه شاهد افزایش یافتهاند، درحالیکه میزان HDL-C کاهش معناداری نشان داد (P=0.001) (جدول 4). بر اساس نتایج حاصل از بررسی میانگین مقادیر نسبی بیان ژن CXCL-14 در بافت چربی احشایی، مشاهده شد که مصرف بلندمدت رژیم غذایی پرچرب همراه با فروکتوز منجر به کاهش معنادار میزان بیان این ژن در گروه HFD در مقایسه با گروه شاهد با رژیم غذایی نرمال شد (P=0/001). در مقابل، مداخله ورزشی تمرین هوازی در گروه THFD منجر به افزایش معنادار بیان ژن CXCL-14 در مقایسه با گروه HFD شد (P=0/001) (نمودار 1). بر اساس نتایج حاصل از بررسی میانگین مقادیر نسبی بیان ژن EPDR1 در بافت چربی احشایی، مشاهده شد که مصرف بلندمدت رژیم غذایی پرچرب همراه با فروکتوز منجر به کاهش معنادار میزان بیان این ژن در گروه HFD در مقایسه با گروه شاهد با رژیم غذایی نرمال شد (P=0/001). در مقابل، مداخله ورزشی تمرین هوازی در گروه THFD منجر به افزایش معنادار بیان ژن EPDR1 در مقایسه با گروه HFD شد (P=0/001) (نمودار2).
جدول 2: مشخصات توالی پرایمرهای ژنهای مورد استفاده در پژوهش
.JPG)
جدول 3: میانگین و انحراف معیار شاخصهای تن سنجی در موشهای گروههای مختلف
.JPG)
جدول 4: میانگین و انحراف معیار پروفایلهای لیپیدی، بعد از 24 هفته مصرف غذای پر چرب به همراه فروکتوز در گروه رژیم غذایی پرچرب (4 سر) و گروه شاهد (4 سر)
.JPG)
کلیه مقادیر جدول به صورت انحراف استاندارد ± میانگین میباشند. * اختلاف معنیدار با گروه شاهد (۰٫۰۵ > P)
گروه رژیم غذایی پرچرب HFD، گروه شاهد Normal، کلسترول تام TC، تری گلیسیرید TG ، لیپوپروتئین با چگالی بالا HDL-C و لیپوپروتئین با چگالی کم LDL-C
.JPG)
نمودار 1: مقایسه میانگین تغییرات میزان بیان ژن CXCL-14 در گروههای مختلف
* اختلاف معنیدار با گروه شاهد (۰٫۰۵ > P) † اختلاف معنیدار با گروه رژیم غذایی پرچرب (۰٫۰۵ > P) گروه رژیم غذایی پرچرب HFD، گروه رژیم غذایی پر چرب و تمرین هوازیTHFD، گروه شاهد Normal
.JPG)
نمودار 2: مقایسه میانگین تغییرات میزان بیان ژن EPDR1 در موشهای گروههای مختلف
* اختلاف معنیدار با گروه کنترل (۰٫۰۵ > P) † اختلاف معنیدار با گروه رژیم غذایی پرچرب (۰٫۰۵ > P) گروه رژیم غذایی پرچرب HFD، گروه رژیم غذایی پر چرب و تمرین هوازیTHFD، گروه شاهد Normal
بحث
یافتههای این پژوهش بهروشنی نشان داد که مصرف بلندمدت رژیم غذایی پرچرب همراه با فروکتوز، موجب بروز چاقی واضح و اختلالات متابولیکی در موشهای صحرایی نر گردید؛ بهطوریکه افزایش معناداری در شاخصهای تنسنجی و پروفایلهای لیپیدی مشاهده شد. این اختلالات متابولیکی با کاهش معنادار بیان ژنهای CXCL-14 و EPDR1 در بافت چربی احشایی همراه بود. این نتایج با پیشینهی پژوهشهایی که نقش مخرب رژیمهای غذایی پرچرب را بر تنظیم ژنهای مرتبط با متابولیسم، التهاب و عملکرد سلولی گزارش کردهاند، همراستا است (23, 22). در حالیکه تمرین هوازی منظم توانست بهطور معناداری موجب افزایش بیان این ژنها در گروه تحت رژیم پرچرب گردد. این نتایج نهتنها بیانگر اثرات نامطلوب تغذیه ناسالم، بلکه مؤید نقش تنظیمی و جبرانی فعالیت هوازی در بازآرایی مسیرهای مولکولی مرتبط با عملکرد بافت چربی است. رژیمهای غذایی پرچرب و حاوی قندهای ساده مانند فروکتوز، موجب افزایش التهاب مزمن با شدت پایین، افزایش تولید رادیکالهای آزاد، اختلال در عملکرد میتوکندریایی و فعالسازی مسیرهای التهابی مانند NF-κB و JNK در بافت چربی میشوند (25, 24). این احتمال وجود دارد که این وضعیت منجر به افزایش نفوذ سلولهای ایمنی مانند ماکروفاژهای M1 به بافت چربی و تولید سایتوکاینهای التهابی (TNF-α، IL-6، MCP-1) شده و با سرکوب ژنهای تنظیمکنندهی ضدالتهاب و متابولیسم مانند CXCL-14 و EPDR1 همراه باشد (27, 26). مطالعات نشان دادهاند که کاهش بیان CXCL-14 میتواند منجر به اختلال در هموستاز سلولهای ایمنی، کاهش مهار پاسخهای التهابی و افزایش مقاومت به انسولین گردد (29, 28). بهبیان دیگر، ژن EPDR1 که اخیراً نقش آن در فرآیندهایی همچون تنظیم اتصال بینسلولی، تمایز سلولی و متابولیسم چربی شناسایی شده است، در وضعیت چاقی با کاهش بیان همراه میباشد (30, 8). این ژن در بافت چربی قهوهای فعال بوده و بهنظر میرسد نقش مهمی در حفظ عملکرد متابولیکی و تنظیم انرژی ایفا میکند (31). کاهش بیان EPDR1 در گروه HFD میتواند نشاندهنده اختلال در هموستاز بافتی، ظرفیت ترموژنیک و پاسخهای سازشی سلولهای چربی باشد (12). بهطور کلی، این احتمال وجود دارد که چاقی بهعنوان یک وضعیت التهابی-متابولیکی، از طریق مکانیسمهای متعددی شامل التهاب، استرس اکسیداتیو، تغییرات اپیژنتیکی و اختلال در سیگنالینگ سلولی، باعث تنظیم منفی ژنهای کلیدی مانند CXCL-14 و EPDR1 شده باشد. کاهش بیان این ژنها نهتنها بهعنوان نشانهای از آسیب بافت چربی، بلکه بهعنوان عاملی مؤثر در پیشرفت اختلالات متابولیکی عمل میکنند. ازاینرو، مداخلات غیر دارویی که قادر باشند، مسیرهای تنظیمی این ژنها را بازیابی نمایند، میتوانند ابزار مؤثری در کنترل چاقی و پیامدهای آن باشند. در پژوهش حاضر مشاهده شد که تمرین هوازی، منجر به افزایش معنادار بیان ژنهای CXCL-14 و EPDR1 در بافت چربی احشایی موشهای چاق گردید. این تغییرات میتواند حاصل اثرات تعدیلگر تمرین هوازی بر مسیرهای زیر باشد: تمرین هوازی، بهویژه با شدت متوسط تا بالا، موجب افزایش نسبت AMP/ATP در سلولها شده و در نتیجه AMPK را فعال میکند. این آنزیم بهعنوان یک حسگر انرژی، چندین عملکرد کلیدی در بهبود متابولیسم دارد، از جمله: افزایش اکسیداسیون اسیدهای چرب، مهار سنتز لیپید و گلوکونئوژنز، تحریک بیوژنز میتوکندری و با مهار مسیر NF-κB موجب کاهش التهاب مزمن میشود و احتمالاً با کاهش عوامل مهارکنندهی رونویسی ژنهای CXCL-14 و EPDR1، موجب افزایش بیان این ژنها میگردد (32). از طرفی افزایش بیان PGC-1α در پاسخ به تمرین، میتواند به افزایش بیان EPDR1 و بازآرایی ساختار بافت چربی کمک نماید (33). همچنین ترشح میوکاینها نظیر FNDC5/آیریزین در نتیجه تمرینات هوازی می تواند با اثر بر بافت چربی، نهتنها موجب قهوهای شدن چربی سفید شود، بلکه بیان فاکتورهای ترموژنیک از جمله CXCL-14 و احتمالاً EPDR1 را نیز تحریک کند (34). برخی مطالعات نشان دادهاند که آیریزین میتواند بیان ژنهای ضدالتهابی مانند CXCL-14 و نیز ژنهایی که در بازسازی ساختاری بافت چربی نقش دارند مانند EPDR1 را افزایش دهد (35). این احتمال وجود دارد که فعالیتهای هوازی با کاهش استرس اکسیداتیو و مهار مسیرهای التهابی NF-κB و JNK، موجب کاهش بیان سایتوکاینهای مخرب و ایجاد شرایطی مناسب برای افزایش بیان ژنهای تنظیمکننده ضدالتهاب و افزایش بیان ژنهای تنظیمکننده متابولیسم مانند EPDR1 و CXCL-14 کمک میکند (36). تمرین هوازی میتواند از طریق تغییر در متیلاسیون DNA، استیلاسیون هیستونها و تنظیم بیان microRNAها، مسیرهای اپیژنتیکی را نیز تنظیم کند (37). برخی مطالعات نشان دادهاند که ورزش میتواند با کاهش متیلاسیون پروموتر ژنهای متابولیکی و افزایش در دسترس بودن کروماتین، بیان ژنهایی نظیر EPDR1 را افزایش دهد (38). در مجموع، تمرین هوازی از طریق فعالسازی همزمان چندین مسیر مولکولی کلیدی، از جمله AMPK، PGC-1α، مهار NF-κB و افزایش ترشح میوکاینهایی نظیر آیریزین، قادر است؛ التهاب بافت چربی را کاهش دهد،اکسیداسیون چربی و ترموژنز را افزایش دهد، بیان ژنهای محافظتی مانند CXCL-14 و EPDR1 را تعدیل کند (40, 39). این مسیرها، هم در سطح رونویسی و هم در سطح اپیژنتیک عمل کرده و با تنظیم بیان این ژنها، در بازگرداندن تعادل متابولیکی و ایمنی در شرایط چاقی، نقش مؤثری ایفا میکنند (41). بنابراین، تمرین هوازی نهتنها یک ابزار فیزیولوژیک، بلکه یک مداخله مولکولی هدفمند برای بهبود اختلالات ناشی از چاقی است. این مطالعه برای نخستین بار بهطور همزمان تغییرات بیان ژنهای CXCL-14 و EPDR1 را در پاسخ به تمرین هوازی در مدل چاقی القاشده بررسی کرده است. برخلاف بیشتر مطالعات که بر ژنهای شناختهشدهتری چون UCP1، PRDM16 و PPARγ تمرکز دارند، یافتههای این تحقیق افق جدیدی در بررسی نقش ژنهای کمتر شناختهشده ولی مؤثر در تنظیم پاسخهای متابولیکی و ایمنی بافت چربی گشوده است. افزایش بیان این دو ژن در گروه تمرین، احتمالاً از طریق بازسازی ساختاری و عملکردی بافت چربی، افزایش ظرفیت اکسیداتیو، تحریک بیوژنز میتوکندری و کاهش پاسخهای التهابی محقق شده است. این یافتهها تأکیدی مجدد بر نقش تمرین هوازی بهعنوان مداخلهای مؤثر و ایمن برای تعدیل پیامدهای مولکولی چاقی دارد. با این وجود، این مطالعه دارای محدودیتهایی است؛ از جمله استفاده از مدل حیوانی و تمرکز صرف بر بافت چربی احشایی. همچنین، مسیرهای سیگنالینگ دقیق میان EPDR1 و تنظیمات ایمنیمتابولیکی هنوز بهطور کامل مشخص نشده است. بنابراین در پژوهشهای آینده، از تکنیکهای پیشرفته مانند سرکوب بیان ژن، آنالیز فسفوریلاسیون پروتئینها و مطالعات انسانی، مکانیسمهای دقیقتر تنظیم ژنهای مذکور در پاسخ به ورزش و چاقی بررسی شود.
نتیجهگیری
پژوهش حاضر نشان داد که رژیم پرچرب همراه با فروکتوز موجب بروز چاقی و اختلالات متابولیکی همراه با کاهش بیان ژنهای CXCL-14 و EPDR1 در بافت چربی احشایی میشود. در مقابل، تمرین هوازی با افزایش معنادار بیان این ژنها و بهبود شاخصهای تنسنجی و پروفایل لیپیدی، بخشی از اثرات منفی رژیم پرچرب را تعدیل کرد. این یافتهها اهمیت تمرین هوازی را بهعنوان یک مداخله غیردارویی مؤثر در بازگرداندن تنظیم متابولیکی و ایمنی بافت چربی در شرایط چاقی برجسته میسازد. همچنین، ژنهای CXCL-14 و EPDR1 میتوانند بهعنوان نشانگرهای زیستی حساس برای ارزیابی اثربخشی مداخلات ورزشی در مدیریت چاقی در نظر گرفته شوند. در مجموع، یافتههای این مطالعه بر اهمیت نقش ورزش هوازی در بهبود تنظیم ژنهای متابولیکی و ایمنی در بافت چربی تأکید مینمایند لذا پیشنهاد میشود باتوجهبه پیچیدگی سازوکارهای مولکولی دخیل در چاقی، بررسی دقیقتر این مسیرها در مطالعات آینده، بهویژه در مدلهای انسانی، مورد مطالعه قرار گیرد.
سپاسگزاری
این مقاله برگرفته از پایاننامه کارشناسیارشد رشته فیزیولوژی ورزشی است. نگارندگان از همکاری اعضای محترم هیئتعلمی و کارشناسان آزمایشگاه دانشگاه آزاد اسلامی واحد اهواز قدردانی مینمایند.
حامی مالی: ندارد.
تعارض در منافع: وجود ندارد
ملاحظات اخلاقی
پروپوزال این تحقیق توسط دانشگاه آزاد اسلامی واحد اهواز تایید شده است. (کد اخلاق:IR.IAU.AHVAZ.REC.1403.039 )
مشارکت نویسندگان
زهرا شریفی، نویسنده اول، در ایدهپردازی، طراحی اولیه مطالعه، جمعآوری دادهها و تهیه پیشنویس اولیه مقاله مشارکت داشته است. احمد کاکی، نویسنده مسئول، در نهاییسازی طرح پژوهش، نظارت بر اجرای مطالعه، تجزیهوتحلیل دادهها و تفسیر یافتهها نقش داشته است. هر دو نویسنده در نگارش، ویرایش علمی و بازنگری نهایی مقاله و همچنین پاسخگویی به سوالات مرتبط با مقاله سهیم هستند.
چاقی، بهعنوان یکی از چالشهای اساسی نظامهای سلامت در قرن بیستویکم، با روندی فزاینده در سطح جهانی، بهویژه در کشورهای در حال توسعه، مطرح است و پیامدهای گستردهای در بروز و گسترش بیماریهای مزمن ناشی از سبک زندگی مدرن به همراه دارد. این پدیده، که از آن بهعنوان یک اختلال پیچیده متابولیکی یاد میشود، عمدتاً با تجمع غیرعادی و مفرط چربی بدن، بهویژه در نواحی احشایی، شناخته میشود و با طیف متنوعی از اختلالات متابولیکی و التهابی، از جمله دیابت نوع ۲، سندرم متابولیک، بیماریهای قلبیعروقی، مقاومت به انسولین، ناهنجاریهای لیپیدی و التهاب مزمن خفیف همراه است (3-1). در سالهای اخیر، پژوهشگران دریافتهاند که بافت چربی صرفاً یک مخزن انرژی غیرفعال نیست، بلکه یک بافت فعال متابولیک و غدد درونریز محسوب میشود که طیف وسیعی از مولکولهای پیامرسان نظیر آدیپوکاینها، سایتوکاینها و اخیراً "باتوکینها" را تولید میکند (5, 4). از میان انواع بافت چربی، بافت چربی قهوهای(Brown Adipose Tissue) به دلیل نقش برجستهای که در تولید گرما (ترموژنز وابسته به Uncoupling Protein 1) و تنظیم تعادل انرژی ایفا میکند، مورد توجه گسترده قرار گرفته است (6). اما علاوه بر نقش ترموژنیک، Brown Adipose Tissue از طریق ترشح مولکولهایی با عملکرد شبههورمونی موسوم به باتوکینها (Batokines)، در تنظیم متابولیسم گلوکز و چربی، حساسیت انسولینی، و عملکرد سیستم ایمنی و قلبی-عروقی نقش دارد (7, 4). در میان ترکیبات ترشحشده از بافت چربی قهوهای، دو مولکول CXCL-14 و EPDR1 بهعنوان عوامل میانجی نوظهور در تنظیم فرآیندهای متابولیکی و ایمنی شناخته شدهاند که نقش بالقوهای در هموستاز انرژی، تعادل التهابی و سازوکارهای سلولی مرتبط با اختلالات متابولیک ایفا میکنند (9, 8). ژن CXCL-14، که یکی از اعضای خانواده کموکاینها محسوب میشود، یک کموتاکسین فاقد گیرنده شناختهشده اختصاصی است که بیان گستردهای در بافتهای متابولیک از جمله بافت چربی قهوهای دارد (10). شواهد تجربی نشان میدهد که این مولکول نقش مؤثری در تنظیم مهاجرت ماکروفاژها به بافتهای محیطی، حفظ حساسیت به انسولین در محیط متابولیک و کاهش التهاب مزمن با درجه پایین ایفا مینماید (9). بهویژه، دادههای حاصل از مدلهای حیوانی و سلولی بیانگر آناند که CXCL-14 ممکن است از طریق میانجیگری در تعاملات سلولهای ایمنی و آدیپوسیتها، در کنترل پاسخهای التهابی و بهبود عملکرد متابولیکی در شرایط مرتبط با چاقی نقش داشته باشد (11, 10). از سوی دیگر، ژن EPDR1 که به خانواده پروتئینهای مرتبط با اپندیمین (Ependymin-related proteins) تعلق دارد، بهعنوان مولکولی با نقشهای چندگانه در فرآیندهای زیستی نظیر تمایز سلولی، تنظیم چسبندگی بین سلولی و احتمالاً تنظیم فعالیت متابولیکی بافت چربی قهوهای شناخته میشود (12). با وجود شناسایی بیان این ژن در بافتهای متابولیک و گزارشهایی از نقش آن در سازوکارهای سلولی مرتبط با تعادل انرژی، دانش کنونی در خصوص عملکرد دقیق EPDR1، بهویژه در شرایط پاتولوژیک مانند چاقی القاشده ناشی از رژیم غذایی پرچرب، همچنان ناکافی و پراکنده باقی مانده است (13). از طرف دیگر، یافتههای حاصل از مطالعات تجربی گوناگون بهوضوح نشان میدهد که فعالیت بدنی منظم، بهویژه تمرینات هوازی، از ظرفیت بالایی برای تعدیل فرآیندهای التهابی مزمن، ارتقای حساسیت به انسولین، افزایش مصرف انرژی و بهبود عملکرد فیزیولوژیک بافت چربی برخوردار است (15, 14). تمرین هوازی از طریق فعال کردن مسیرهای مولکولی متعدد از جمله فعالسازی آنزیم AMPK، افزایش بیان فاکتور تنظیمی PGC-1α، مهار مسیر التهابی NF-κB، و القای بیان ژنهای مرتبط با ترموژنز نظیر UCP1، به بازآرایی متابولیکی و ساختاری در بافتهای چربی سفید و قهوهای منجر میشود (17, 16). علاوهبر این، ورزش هوازی با افزایش ترشح میوکاینهایی چون FNDC5 و محصول آن یعنی آیریزین از عضلات اسکلتی، میتواند موجب تحریک عملکرد ترموژنیک BAT و القای تغییرات فنوتیپی در WAT به سوی قهوهای شدن (browning) گردد (19, 18). این اثرات چندمسیره، ورزش را بهعنوان یک مداخله غیر دارویی مؤثر در تنظیم عملکرد بافت چربی و بهبود اختلالات متابولیکی ناشی از چاقی، در کانون توجه پژوهشهای اخیر قرار داده است. با وجود پیشرفتهای موجود، هنوز خلأهای جدی در شناخت دقیق مکانیسمهای مولکولی اثر تمرین هوازی بر بیان ژنهای خاص در BAT بهویژه ژنهای تازه شناساییشدهای مانند CXCL-14 و EPDR1 وجود دارد. بیشتر مطالعات تمرکز خود را بر ژنهای کلاسیک نظیر UCP1، PRDM16 و PGC-1α معطوف کردهاند و کمتر به نقش عوامل تازه شناساییشدهای پرداختهاند که میتوانند اهداف بالقوهای برای درمان چاقی و بیماریهای متابولیک محسوب شوند. ازاینرو، این مطالعه با هدف بررسی تأثیر تمرینات هوازی بر تغییرات بیان ژنهای CXCL-14 و EPDR1 در مدل حیوانی چاقی القاشده با رژیم پرچرب طراحی گردید. انجام این پژوهش میتواند درک عمیقتری از نقش این ژنها در تنظیم عملکرد متابولیکی و ایمنی بافت چربی فراهم سازد و سازوکارهای مولکولی دخیل در پاسخ به مداخلات ورزشی را روشنتر نماید.
روش بررسی
در این پژوهش تجربی، 32 سر موش صحرایی نر نژاد ویستار 8 هفتگی با محدوده وزنی 5/2±198 گرم از مرکز تکثیر حیوانات آزمایشگاهی دانشگاه علوم پزشکی جندیشاپور اهواز تهیه و در گروههای چهارتایی در قفسهای استاندارد پلیکربنات در شرایط دمایی 2±22 درجه سانتیگراد و رطوبت نسبی 40 تا 60 درصد، تحت چرخه 12:12 ساعت تاریکی – روشنایی و با دسترسی آزاد به آب و غذا نگهداری شدند. بعد از گذشت دو هفته تطابق با محیط جدید آزمایشگاه و تغذیه از رژیم غذایی استاندارد (20٪ کیلوکالری از چربی، 20٪ پروتئین و 60٪ کربوهیدرات که 3/1 کیلوکالری بهازای هر گرم انرژی داشت)، موشها به طور تصادفی به دو گروه رژیم غذایی استاندارد (12 سر) و گروه رژیم غذایی پرچرب (20 سر) تقسیم شدند در مرحله اول، 24 هفته موشها گروه رژیم غذایی پرچرب، تحت رژیم غذایی 60 درصد چربی و 25 درصد فروکتوز قرار گرفتند. سپس برای بررسی تأیید القاء چاقی، از هر گروه 4 سر موش انتخاب و شاخصهای تنسنجی و پارامترهای بیوشیمیایی خون مورد ارزیابی قرار گرفت. پس از احراز چاقی در گروه رژیم غذایی پر چرب، موشها بهطور تصادفی به سه گروه (8 = n)؛ گروه شاهد Normal (غذای استاندارد)، گروه رژیم غذایی پرچرب HFD و گروه رژیم غذایی پرچرب و تمرین هوازی THFD دستهبندی شدند. تمام مراحل پژوهش، محققان با رعایت اصول اخلاقی کار با حیوانات، طبق دستورالعملهای اخلاقی مؤسسات ملی برای مراقبت و استفاده از حیوانات آزمایشگاهی (برابر با پروتکل هلسینکی 2006) مصوب دانشگاه آزاد اسلامی واحد اهواز با کد (IR.IAU.AHVAZ.REC.1404.125) تصویب و انجام شد. القاء چاقی: بهمنظور القای چاقی از رژیم غذایی 60 درصد چربی حاوی 25 درصد فروکتوز استفاده شد. برای ساخت 100 کیلوگرم پلت پرچرب 60 درصد (شرکت زیست فن آوران رویان اصفهان)، 45 کیلوگرم پودر پلت استاندارد با 30 کیلوگرم چربی حیوانی (حاصل از آبکردن دنبه گاو و روغن دانۀ سویا) ترکیب و به شکل پلت استاندارد قالبزده شد و تا پایان دوره تحقیق در اختیار گروههای رژیم پرچرب قرار گرفت. همچنین برای تهیه محلول 25 درصد حجمی فروکتوز؛ از رابطه (۱۰۰ × حجم محلول (میلیلیتر) / حجم حلشونده (میلیلیتر) = درصد حجمی) استفاده شد. 250 میلیلیتر مایع فروکتوز را در 750 میلیلیتر آب حل تا محلول 25 درصد حجمی فروکتوز به دست آید. محلول فروکتوز، بهصورت روزانه تهیه و به طور آزاد، از ابتدا تا پایان دوره پژوهش در اختیار موشها گروه رژیم پرچرب قرار میگرفت (20).
پروتکل تمرین هوازی: پس از حصول چاقی در موشها، پروتکل تمرین هوازی به مدت 8 هفته انجام شد. در پژوهش حاضر پروتکل تمرین هوازی، بر اساس مطالعه سیلویا روچا و همکاران در سال 2016 استفاده شد؛ بدینصورت که گروه رژیم غذایی پرچرب و تمرین هوازی THFD در معرض تمرین نوار گردان، 5 جلسه در هفته و به مدت 8 هفته قرار گرفتند. تمام جلسات تمرینی در پایان سیکل خواب حیوانات و بین ساعت 16 تا 18 عصر برگزار شد. سرعت و مدت تمرین نوار گردان به تدریج افزایش یافته و از 15 متر در دقیقه به مدت 30 دقیقه در هفته اول، 16 متر در دقیقه برای 35 دقیقه در هفته دوم، 18متر در دقیقه40 دقیقه در هفته سوم، 20 متر در دقیقه برای 45 دقیقه در هفته چهارم، به 21 متر در دقیقه 50 دقیقه در هفته پنجم و 23 متر در دقیقه 55 دقیقه در هفته ششم، 25 متر در دقیقه 60 دقیقه در هفته هفتم و هفته هشتم افزایش یافت. جهت رسیدن سازگاریهای بهدست آمده به حالت یکنواخت، تمامی متغیرهای تمرینی درهفته های پایانی ثابت نگهداشته شد (21)(جدول 1).
جدول 1: پروتکل تمرین هوازی
.JPG)
اندازهگیری شاخصهای تنسنجی: اندازهگیری شاخصهای تنسنجی شامل؛ وزن، دور شکم، دور سینه، نسبت دور شکم بهدور سینه، طول بدن، شاخص توده بدن و شاخص Lee در سه زمان؛ ابتدای دوره، هفته 24 ام و پایان دوره، در یک روز مشخص، از همه حیوانات در تمام گروهها انجام شد.
اندازه گیری وزن بدن (W): برای اندازه گیری وزن موشها از ترازوی دیجیتال موش آزمایشگاهی (شرکت کیمیا کهربای مبین، ساخت کشور ایران) جهت وزن کشی استفاده شد. دور شکم (AC): بلافاصله جلوی پای عقب در بخش بزرگترین ناحیه شکم، برای دور شکم به سانتی متر اندازه گیری شد. دور سینه (TC): بلافاصله پشت دست جلو به سانتی متر برای دور سینه اندازه گیری شد. نسبت دور شکم به دور سینه (AC/TC): اندازه دور شکم را بر اندازه دور سینه تقسیم و نسبت آن به دست آمد. طول بدن (L): طول بدن از نوک بینی تا مقعد به سانتی متر اندازه گیری شد. شاخص توده بدن (BMI): وزن بدن به گرم تقسیم بر طول بدن از بینی تا مقعد به توان دو به سانتی متر به عنوان شاخص توده بدن محاسبه شد.
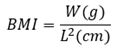
شاخص Lee: شاخص لی به عنوان شاخصی از ترکیب بدنی در جوندگان با استفاده از فرمول؛ ریشه مکعب وزن بدن به گرم تقسیم بر طول بدن از بینی تا مقعد به سانتی متر محاسبه شد.
.JPG)
سنجش پروفایلهای لیپیدی (Lipid Profile): اندازهگیری سطوح سرمی پارامترهای بیوشیمیایی لیپیدی شامل؛ تری گلیسیرید، کلسترول تام، کلسترول HDL و کلسترول LDL بعد از 24 هفته مصرف غذای پر چرب به همراه فروکتوز از گروه رژیم غذایی پرچرب (4 سر) و گروه شاهد (4 سر) اندازه گیری شد. ابتدا موشها به مدت 12 ساعت محرومیت از غذا، توسط تزریق درون صفاقی ترکیب از کتامین90 (میلیگرم /کیلوگرم) و زایلازین 10(میلیگرم /کیلوگرم) بیهوش، سپس قفسه سینه حیوان شکافته و 5 میلی لیتر نمونه خون به طور مستقیم از قلب موشها گرفته شد و در لولههای پلاستیکی حاوی ژل Clot جمعآوری شد. پس از انعقاد خون، نمونههای خون با سرعت 4000 دور در دقیقه و به مدت 15 دقیقه سانتریفیوژ گردید، سرم آن جداسازی و در اپندورفهای مخصوص قرار داده شد. میزانتری گلیسیرید به روش آنزیماتیک (لیپاز برای تبدیل تری گلیسیرید به گلیسرول) و کلسترول به روش آنزیماتیک کلسترول استراز (لیپاز برای تبدیل تری گلیسرید به گلیسرول) و کلسترول HDL توسط روش رسوبی آنزیمی (همگی تستها با به کارگیری کیتهای تجاری شرکت بوتیک که مورد تایید آزمایشگاه مرجع سلامت ایران بود و با دستگاه اتوآنالایزر (Hitachi,japan) تعیین شد) و کلسترول LDL توسط فرمول فریدوالد (Friedewald equation) (LDL-C = TC - (HDL-C) - (TG/5) محاسبه شد.
استخراج نمونه و روش اندازهگیری: در پایان دوره بعد از اجرای هشت هفته برنامه تمرینی، همه موشها، 48 ساعت پس از آخرین جلسه، بیهوش، کشته و جراحی شدند. تحت شرایط استریل بافت چربی احشایی تشریح و استخراج گردید و پس از شستشو با نرمال سالین، با ترازوی دیجیتال (با دقت اندازهگیری 0/001 گرم) وزن شد، یک بخش از آن بهعنوان نمونه، برای آزمایشهای سلولی و مولکولی به روش ریل تایم، بلافاصله در نیتروژن مایع منجمد و نمونهها تا زمان انجام آزمایشهای ملکولی در فریزر 80- درجه سانتیگراد نگهداری شدند.
Real Time-PCR: حدود 50 میلیگرم از بافت چربی احشایی جهت استخراج RNA کل به نسبت 1 به 10 با استفاده از کیت QIAzol Lysis Reagent هموژن گردید. بهمنظور برداشتن اجزای پروتئینی محصول در دمای 4 درجه سانتیگراد، به مدت 10 دقیقه، با دور g12000 سانتریفیوژ شد. سپس به نسبت 1 به 0/5 با محلول کلروفرم مخلوط و به مدت 15 ثانیه بهشدت تکان داده شد. محصول در دمای 4 درجه سانتیگراد، به مدت 15 دقیقه، با 12000 (دور در دقیقه) سانتریفیوژ و بخش معدنی و آبی از هم جدا شدند. بخش محتوی RNA برداشته و با نسبت یک به نیم با محلول ایزوپروپانول مخلوط و به مدت ده دقیقه در دمای اتاق نگهداری و سپس در دمای 4 درجه سانتیگراد، به مدت 10 دقیقه، با 12000 سانتریفیوژ شد. پلت حاوی RNA با محلول اتانول شستشو داده شد و سپس در ۲۰ میکرولیتر آب بدون RNase حل گردید. غلظت RNA موردسنجش واقع شد طبق شرکت (Eppendorf - Germany) و به نسبت 260 به 280 بین 1/8 تا 2 بهعنوان تلخیص مطلوب تعریف گردید. سنتز cDNA تکرشتهای از پرایمر (Oligo dt MWG-Biotech, Germany) و آنزیم نسخهبرداری معکوس (Fermentas) و بر اساس پروتکل مربوطه انجام شد. از تکنیک RT-qPCR جهت تأیید بیان ژنهای CXCL-14 و EPDR1 بهصورت کمی استفاده شد، هر واکنش PCR با استفاده از دستگاه (PCR master mix Applied Biosystems) و SYBR Green در دستگاه ABI Step One (Applied Biosystems, Sequence Detection Systems. Foster City, CA) طبق پروتکل شرکت سازنده انجام گرفت. 40 سیکل برای هر چرخه Real-Time PCR در نظر گرفته شد و دماهای هر سیکل شامل 94 درجه سانتیگراد برای 20 ثانیه، 60-58 درجه سانتیگراد برای 30 ثانیه و 72 درجه سانتیگراد برای 30 ثانیه تنظیم شدند. ضمن اینکه از GAPDH بهعنوان ژن مرجع استفاده گردید. نسبت بیان ژنهای موردبررسی در این مطالعه، با روش مقایسهای چرخه آستانه (Thereshold Cycle(CT)) مورد ارزیابی قرار گرفتند. با استفاده از قرار دادن داده¬ها در فرمول
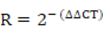 میزان بیان ژن هدف با ژن مرجع نرمالیز شده و بیان ژنهای گروه سالم بهعنوان کالیبراتور در نظر گرفته شد. مشخصات پرایمرهای سنتز شده در جدول 2 ذکر شده است.
میزان بیان ژن هدف با ژن مرجع نرمالیز شده و بیان ژنهای گروه سالم بهعنوان کالیبراتور در نظر گرفته شد. مشخصات پرایمرهای سنتز شده در جدول 2 ذکر شده است.تجزیه و تحلیل آماری
جهت تعیین نرمال بودن دادهها از آزمون کلوموگروف - اسمیرنوف استفاده شد. برای بررسی معنیدار بودن اختلاف بین گروهها از تحلیل واریانس یکطرفه و در صورت معنی-داری، جهت تعیین تفاوت بین میانگینهای دوگروهی از آزمون تعقیبی توکی استفاده شد. تجزیهوتحلیل دادهها با استفاده از نرمافزار SPSS version 16 در سطح معنیداری (0.05 > P) انجام شد.
نتایج
نتایج حاصل از مقایسه شاخصهای تنسنجی شامل وزن بدن، دور شکم، دور سینه، نسبت دور شکم بهدور سینه، طول بدن، شاخص توده بدنی (BMI) و شاخص لی (Lee index) در دو بازه زمانی ابتدای مطالعه و هفته بیست و چهارم نشان داد که بین گروه دریافتکننده رژیم غذایی پرچرب (HFD) با رژیم غذایی شاهد (Normal) تفاوت معناداری وجود دارد. (P=0/001) این تفاوت معنادار بیانگر تأثیر رژیم غذایی پرچرب بر افزایش شاخصهای تنسنجی در طول دوره مطالعه است. در هفتههای پایانی مطالعه، نتایج تحلیل واریانس یکطرفه نشان داد که میانگین تغییرات شاخصهای تنسنجی (شامل وزن بدن، دور شکم، دور سینه، نسبت دور شکم بهدور سینه، طول بدن، شاخص توده بدنی و شاخص لی) در گروه دریافتکننده رژیم غذایی پرچرب همراه با تمرین هوازی (THFD)، در مقایسه با گروه دریافتکننده تنها رژیم پرچرب (HFD) به طور معناداری کمتر بود. (P=0/001) (جدول 3). پس از القای چاقی از طریق مصرف رژیم غذایی پرچرب همراه با فروکتوز، سطوح سرمی شاخصهای لیپیدی شامل تری گلیسیرید، کلسترول تام، کلسترول لیپوپروتئین با چگالی بالا و لیپوپروتئین با چگالی پایین در هفته بیست و چهارم در گروههای دریافتکننده رژیم پرچرب (HFD) و گروه شاهد (Normal) مورد سنجش قرار گرفت. نتایج تحلیل آماری نشان داد که سطوح تری گلیسیرید، کلسترول تام و LDL-C در گروه HFD به طور معناداری نسبت به گروه شاهد افزایش یافتهاند، درحالیکه میزان HDL-C کاهش معناداری نشان داد (P=0.001) (جدول 4). بر اساس نتایج حاصل از بررسی میانگین مقادیر نسبی بیان ژن CXCL-14 در بافت چربی احشایی، مشاهده شد که مصرف بلندمدت رژیم غذایی پرچرب همراه با فروکتوز منجر به کاهش معنادار میزان بیان این ژن در گروه HFD در مقایسه با گروه شاهد با رژیم غذایی نرمال شد (P=0/001). در مقابل، مداخله ورزشی تمرین هوازی در گروه THFD منجر به افزایش معنادار بیان ژن CXCL-14 در مقایسه با گروه HFD شد (P=0/001) (نمودار 1). بر اساس نتایج حاصل از بررسی میانگین مقادیر نسبی بیان ژن EPDR1 در بافت چربی احشایی، مشاهده شد که مصرف بلندمدت رژیم غذایی پرچرب همراه با فروکتوز منجر به کاهش معنادار میزان بیان این ژن در گروه HFD در مقایسه با گروه شاهد با رژیم غذایی نرمال شد (P=0/001). در مقابل، مداخله ورزشی تمرین هوازی در گروه THFD منجر به افزایش معنادار بیان ژن EPDR1 در مقایسه با گروه HFD شد (P=0/001) (نمودار2).
جدول 2: مشخصات توالی پرایمرهای ژنهای مورد استفاده در پژوهش
.JPG)
جدول 3: میانگین و انحراف معیار شاخصهای تن سنجی در موشهای گروههای مختلف
.JPG)
جدول 4: میانگین و انحراف معیار پروفایلهای لیپیدی، بعد از 24 هفته مصرف غذای پر چرب به همراه فروکتوز در گروه رژیم غذایی پرچرب (4 سر) و گروه شاهد (4 سر)
.JPG)
کلیه مقادیر جدول به صورت انحراف استاندارد ± میانگین میباشند. * اختلاف معنیدار با گروه شاهد (۰٫۰۵ > P)
گروه رژیم غذایی پرچرب HFD، گروه شاهد Normal، کلسترول تام TC، تری گلیسیرید TG ، لیپوپروتئین با چگالی بالا HDL-C و لیپوپروتئین با چگالی کم LDL-C
.JPG)
نمودار 1: مقایسه میانگین تغییرات میزان بیان ژن CXCL-14 در گروههای مختلف
* اختلاف معنیدار با گروه شاهد (۰٫۰۵ > P) † اختلاف معنیدار با گروه رژیم غذایی پرچرب (۰٫۰۵ > P) گروه رژیم غذایی پرچرب HFD، گروه رژیم غذایی پر چرب و تمرین هوازیTHFD، گروه شاهد Normal
.JPG)
نمودار 2: مقایسه میانگین تغییرات میزان بیان ژن EPDR1 در موشهای گروههای مختلف
* اختلاف معنیدار با گروه کنترل (۰٫۰۵ > P) † اختلاف معنیدار با گروه رژیم غذایی پرچرب (۰٫۰۵ > P) گروه رژیم غذایی پرچرب HFD، گروه رژیم غذایی پر چرب و تمرین هوازیTHFD، گروه شاهد Normal
بحث
یافتههای این پژوهش بهروشنی نشان داد که مصرف بلندمدت رژیم غذایی پرچرب همراه با فروکتوز، موجب بروز چاقی واضح و اختلالات متابولیکی در موشهای صحرایی نر گردید؛ بهطوریکه افزایش معناداری در شاخصهای تنسنجی و پروفایلهای لیپیدی مشاهده شد. این اختلالات متابولیکی با کاهش معنادار بیان ژنهای CXCL-14 و EPDR1 در بافت چربی احشایی همراه بود. این نتایج با پیشینهی پژوهشهایی که نقش مخرب رژیمهای غذایی پرچرب را بر تنظیم ژنهای مرتبط با متابولیسم، التهاب و عملکرد سلولی گزارش کردهاند، همراستا است (23, 22). در حالیکه تمرین هوازی منظم توانست بهطور معناداری موجب افزایش بیان این ژنها در گروه تحت رژیم پرچرب گردد. این نتایج نهتنها بیانگر اثرات نامطلوب تغذیه ناسالم، بلکه مؤید نقش تنظیمی و جبرانی فعالیت هوازی در بازآرایی مسیرهای مولکولی مرتبط با عملکرد بافت چربی است. رژیمهای غذایی پرچرب و حاوی قندهای ساده مانند فروکتوز، موجب افزایش التهاب مزمن با شدت پایین، افزایش تولید رادیکالهای آزاد، اختلال در عملکرد میتوکندریایی و فعالسازی مسیرهای التهابی مانند NF-κB و JNK در بافت چربی میشوند (25, 24). این احتمال وجود دارد که این وضعیت منجر به افزایش نفوذ سلولهای ایمنی مانند ماکروفاژهای M1 به بافت چربی و تولید سایتوکاینهای التهابی (TNF-α، IL-6، MCP-1) شده و با سرکوب ژنهای تنظیمکنندهی ضدالتهاب و متابولیسم مانند CXCL-14 و EPDR1 همراه باشد (27, 26). مطالعات نشان دادهاند که کاهش بیان CXCL-14 میتواند منجر به اختلال در هموستاز سلولهای ایمنی، کاهش مهار پاسخهای التهابی و افزایش مقاومت به انسولین گردد (29, 28). بهبیان دیگر، ژن EPDR1 که اخیراً نقش آن در فرآیندهایی همچون تنظیم اتصال بینسلولی، تمایز سلولی و متابولیسم چربی شناسایی شده است، در وضعیت چاقی با کاهش بیان همراه میباشد (30, 8). این ژن در بافت چربی قهوهای فعال بوده و بهنظر میرسد نقش مهمی در حفظ عملکرد متابولیکی و تنظیم انرژی ایفا میکند (31). کاهش بیان EPDR1 در گروه HFD میتواند نشاندهنده اختلال در هموستاز بافتی، ظرفیت ترموژنیک و پاسخهای سازشی سلولهای چربی باشد (12). بهطور کلی، این احتمال وجود دارد که چاقی بهعنوان یک وضعیت التهابی-متابولیکی، از طریق مکانیسمهای متعددی شامل التهاب، استرس اکسیداتیو، تغییرات اپیژنتیکی و اختلال در سیگنالینگ سلولی، باعث تنظیم منفی ژنهای کلیدی مانند CXCL-14 و EPDR1 شده باشد. کاهش بیان این ژنها نهتنها بهعنوان نشانهای از آسیب بافت چربی، بلکه بهعنوان عاملی مؤثر در پیشرفت اختلالات متابولیکی عمل میکنند. ازاینرو، مداخلات غیر دارویی که قادر باشند، مسیرهای تنظیمی این ژنها را بازیابی نمایند، میتوانند ابزار مؤثری در کنترل چاقی و پیامدهای آن باشند. در پژوهش حاضر مشاهده شد که تمرین هوازی، منجر به افزایش معنادار بیان ژنهای CXCL-14 و EPDR1 در بافت چربی احشایی موشهای چاق گردید. این تغییرات میتواند حاصل اثرات تعدیلگر تمرین هوازی بر مسیرهای زیر باشد: تمرین هوازی، بهویژه با شدت متوسط تا بالا، موجب افزایش نسبت AMP/ATP در سلولها شده و در نتیجه AMPK را فعال میکند. این آنزیم بهعنوان یک حسگر انرژی، چندین عملکرد کلیدی در بهبود متابولیسم دارد، از جمله: افزایش اکسیداسیون اسیدهای چرب، مهار سنتز لیپید و گلوکونئوژنز، تحریک بیوژنز میتوکندری و با مهار مسیر NF-κB موجب کاهش التهاب مزمن میشود و احتمالاً با کاهش عوامل مهارکنندهی رونویسی ژنهای CXCL-14 و EPDR1، موجب افزایش بیان این ژنها میگردد (32). از طرفی افزایش بیان PGC-1α در پاسخ به تمرین، میتواند به افزایش بیان EPDR1 و بازآرایی ساختار بافت چربی کمک نماید (33). همچنین ترشح میوکاینها نظیر FNDC5/آیریزین در نتیجه تمرینات هوازی می تواند با اثر بر بافت چربی، نهتنها موجب قهوهای شدن چربی سفید شود، بلکه بیان فاکتورهای ترموژنیک از جمله CXCL-14 و احتمالاً EPDR1 را نیز تحریک کند (34). برخی مطالعات نشان دادهاند که آیریزین میتواند بیان ژنهای ضدالتهابی مانند CXCL-14 و نیز ژنهایی که در بازسازی ساختاری بافت چربی نقش دارند مانند EPDR1 را افزایش دهد (35). این احتمال وجود دارد که فعالیتهای هوازی با کاهش استرس اکسیداتیو و مهار مسیرهای التهابی NF-κB و JNK، موجب کاهش بیان سایتوکاینهای مخرب و ایجاد شرایطی مناسب برای افزایش بیان ژنهای تنظیمکننده ضدالتهاب و افزایش بیان ژنهای تنظیمکننده متابولیسم مانند EPDR1 و CXCL-14 کمک میکند (36). تمرین هوازی میتواند از طریق تغییر در متیلاسیون DNA، استیلاسیون هیستونها و تنظیم بیان microRNAها، مسیرهای اپیژنتیکی را نیز تنظیم کند (37). برخی مطالعات نشان دادهاند که ورزش میتواند با کاهش متیلاسیون پروموتر ژنهای متابولیکی و افزایش در دسترس بودن کروماتین، بیان ژنهایی نظیر EPDR1 را افزایش دهد (38). در مجموع، تمرین هوازی از طریق فعالسازی همزمان چندین مسیر مولکولی کلیدی، از جمله AMPK، PGC-1α، مهار NF-κB و افزایش ترشح میوکاینهایی نظیر آیریزین، قادر است؛ التهاب بافت چربی را کاهش دهد،اکسیداسیون چربی و ترموژنز را افزایش دهد، بیان ژنهای محافظتی مانند CXCL-14 و EPDR1 را تعدیل کند (40, 39). این مسیرها، هم در سطح رونویسی و هم در سطح اپیژنتیک عمل کرده و با تنظیم بیان این ژنها، در بازگرداندن تعادل متابولیکی و ایمنی در شرایط چاقی، نقش مؤثری ایفا میکنند (41). بنابراین، تمرین هوازی نهتنها یک ابزار فیزیولوژیک، بلکه یک مداخله مولکولی هدفمند برای بهبود اختلالات ناشی از چاقی است. این مطالعه برای نخستین بار بهطور همزمان تغییرات بیان ژنهای CXCL-14 و EPDR1 را در پاسخ به تمرین هوازی در مدل چاقی القاشده بررسی کرده است. برخلاف بیشتر مطالعات که بر ژنهای شناختهشدهتری چون UCP1، PRDM16 و PPARγ تمرکز دارند، یافتههای این تحقیق افق جدیدی در بررسی نقش ژنهای کمتر شناختهشده ولی مؤثر در تنظیم پاسخهای متابولیکی و ایمنی بافت چربی گشوده است. افزایش بیان این دو ژن در گروه تمرین، احتمالاً از طریق بازسازی ساختاری و عملکردی بافت چربی، افزایش ظرفیت اکسیداتیو، تحریک بیوژنز میتوکندری و کاهش پاسخهای التهابی محقق شده است. این یافتهها تأکیدی مجدد بر نقش تمرین هوازی بهعنوان مداخلهای مؤثر و ایمن برای تعدیل پیامدهای مولکولی چاقی دارد. با این وجود، این مطالعه دارای محدودیتهایی است؛ از جمله استفاده از مدل حیوانی و تمرکز صرف بر بافت چربی احشایی. همچنین، مسیرهای سیگنالینگ دقیق میان EPDR1 و تنظیمات ایمنیمتابولیکی هنوز بهطور کامل مشخص نشده است. بنابراین در پژوهشهای آینده، از تکنیکهای پیشرفته مانند سرکوب بیان ژن، آنالیز فسفوریلاسیون پروتئینها و مطالعات انسانی، مکانیسمهای دقیقتر تنظیم ژنهای مذکور در پاسخ به ورزش و چاقی بررسی شود.
نتیجهگیری
پژوهش حاضر نشان داد که رژیم پرچرب همراه با فروکتوز موجب بروز چاقی و اختلالات متابولیکی همراه با کاهش بیان ژنهای CXCL-14 و EPDR1 در بافت چربی احشایی میشود. در مقابل، تمرین هوازی با افزایش معنادار بیان این ژنها و بهبود شاخصهای تنسنجی و پروفایل لیپیدی، بخشی از اثرات منفی رژیم پرچرب را تعدیل کرد. این یافتهها اهمیت تمرین هوازی را بهعنوان یک مداخله غیردارویی مؤثر در بازگرداندن تنظیم متابولیکی و ایمنی بافت چربی در شرایط چاقی برجسته میسازد. همچنین، ژنهای CXCL-14 و EPDR1 میتوانند بهعنوان نشانگرهای زیستی حساس برای ارزیابی اثربخشی مداخلات ورزشی در مدیریت چاقی در نظر گرفته شوند. در مجموع، یافتههای این مطالعه بر اهمیت نقش ورزش هوازی در بهبود تنظیم ژنهای متابولیکی و ایمنی در بافت چربی تأکید مینمایند لذا پیشنهاد میشود باتوجهبه پیچیدگی سازوکارهای مولکولی دخیل در چاقی، بررسی دقیقتر این مسیرها در مطالعات آینده، بهویژه در مدلهای انسانی، مورد مطالعه قرار گیرد.
سپاسگزاری
این مقاله برگرفته از پایاننامه کارشناسیارشد رشته فیزیولوژی ورزشی است. نگارندگان از همکاری اعضای محترم هیئتعلمی و کارشناسان آزمایشگاه دانشگاه آزاد اسلامی واحد اهواز قدردانی مینمایند.
حامی مالی: ندارد.
تعارض در منافع: وجود ندارد
ملاحظات اخلاقی
پروپوزال این تحقیق توسط دانشگاه آزاد اسلامی واحد اهواز تایید شده است. (کد اخلاق:IR.IAU.AHVAZ.REC.1403.039 )
مشارکت نویسندگان
زهرا شریفی، نویسنده اول، در ایدهپردازی، طراحی اولیه مطالعه، جمعآوری دادهها و تهیه پیشنویس اولیه مقاله مشارکت داشته است. احمد کاکی، نویسنده مسئول، در نهاییسازی طرح پژوهش، نظارت بر اجرای مطالعه، تجزیهوتحلیل دادهها و تفسیر یافتهها نقش داشته است. هر دو نویسنده در نگارش، ویرایش علمی و بازنگری نهایی مقاله و همچنین پاسخگویی به سوالات مرتبط با مقاله سهیم هستند.
References:
1- Aparecida Silveira E, Vaseghi G, de Carvalho Santos AS, Kliemann N, Masoudkabir F, Noll M, et al. Visceral Obesity and Its Shared Role in Cancer and Cardiovascular Disease: A Scoping Review of the Pathophysiology and Pharmacological Treatments. Int J Mol Sci 2020; 21(23): 9042.
2- Lee M-J, Kim J. The Pathophysiology of Visceral Adipose Tissues in Cardiometabolic Diseases. Biochem pharmacol 2024; 222: 116116.
3- Pinckard KM, Stanford KI. The Heartwarming Effect of Brown Adipose Tissue. Mol Pharmacol 2022; 102(1): 460-71.
4- Ghesmati Z, Rashid M, Fayezi S, Gieseler F, Alizadeh E, Darabi M. An Update on the Secretory Functions of Brown, White, And Beige Adipose Tissue: Towards Therapeutic Applications. Rev Endocr Metab Disord 2024; 25(2): 279-308.
5- Villarroya J, Cereijo R, Giralt M, Villarroya F. Secretory Proteome of Brown Adipocytes in Response to Camp-Mediated Thermogenic Activation. Front physiol 2019; 10: 67.
6- Zhang J, Kibret BG, Vatner DE, Vatner SF. The Role of Brown Adipose Tissue in Mediating Healthful Longevity. J Cardiovasc Aging 2024; 4(2): 17.
7- Coassolo L, Dannieskiold-Samsøe NB, Zhao M, Allen H, Svensson KJ. New Players of the Adipose Secretome: Therapeutic Opportunities and Challenges. Curr Opin Pharmacol 2022; 67: 102302.
8- Cereijo R, Gavaldà-Navarro A, Cairó M, Quesada-López T, Villarroya J, Morón-Ros S, et al. CXCL14, A Brown Adipokine that Mediates Brown-Fat-To-Macrophage Communication in Thermogenic Adaptation. Cell Metab 2018; 28(5): 750-63.
9- Cereijo R, Quesada-López T, Gavaldà-Navarro A, Tarascó J, Pellitero S, Reyes M, et al. The Chemokine CXCL14 Is Negatively Associated with Obesity and Concomitant Type-2 Diabetes in Humans. Int J Obes (Lond) 2021; 45(3): 706-10.
10- Takahashi M, Takahashi Y, Takahashi K, Zolotaryov FN, Hong KS, Iida K, et al. CXCL14 Enhances Insulin-Dependent Glucose Uptake in Adipocytes and Is Related to High-Fat Diet-Induced Obesity. Biochem Biophys Res Commun 2007; 364(4): 1037-42
11- Deshmukh AS, Peijs L, Beaudry JL, Jespersen NZ, Nielsen CH, Ma T, et al. Proteomics-Based Comparative Mapping of the Secretomes of Human Brown and White Adipocytes Reveals EPDR1 as a Novel Batokine. Cell Metab 2019; 30(5): 963-75.
12- Wei Y, Xiong ZJ, Li J, Zou C, Cairo CW, Klassen JS, et al. Crystal Structures of Human Lysosomal EPDR1 Reveal Homology with the Superfamily of Bacterial Lipoprotein Transporters. Commun Biol 2019; 2(1): 52.
13- Engin B, Willis SA, Malaikah S, Sargeant JA, Yates T, Gray LJ, et al. The Effect of Exercise Training on Adipose Tissue Insulin Sensitivity: A Systematic Review and Meta‐Analysis. Obes Rev 2022; 23(7): e13445.
14- Guo Q, Li N, Shi H, Gan Y, Wang W, Jia J, et al. Aerobic Exercise Prevents High-Fat-Diet-Induced Adipose Tissue Dysfunction in Male Mice. Nutrients 2024; 16(20): 3451.
15- Ringholm S, Grunnet Knudsen J, Leick L, Lundgaard A, Munk Nielsen M, Pilegaard H. PGC-1α Is Required for Exercise-And Exercise Training-Induced UCP1 Up-Regulation in Mouse White Adipose Tissue. PloS one 2013; 8(5): e64123.
16- Mu W-J, Zhu J-Y, Chen M, Guo L. Exercise-Mediated Browning of White Adipose Tissue: Its Significance, Mechanism and Effectiveness. Int J Mol Sci 2021; 22(21): 11512.
17- Young MF, Valaris S, Wrann CD. A Role For FNDC5/Irisin in the Beneficial Effects of Exercise on the Brain and in Neurodegenerative Diseases. Prog Cardiovasc Dis 2019; 62(2): 172-8.
18- Shi H, Hao X, Sun Y, Zhao Y, Wang Y, Cao X, et al. Exercise‐Inducible Circulating Extracellular Vesicle Irisin Promotes Browning and the Thermogenic Program in White Adipose Tissue. Acta Physiol 2024; 240(3): e14103.
19- Milton-Laskibar I, Marcos-Zambrano LJ, Gómez-Zorita S, Fernández-Quintela A, Carrillo de Santa Pau E, Martínez JA, et al. Gut Microbiota Induced by Pterostilbene and Resveratrol in High-Fat-High-Fructose Fed Rats: Putative Role in Steatohepatitis Onset. Nutrients 2021; 13(5): 1738.
20- Rocha-Rodrigues S, Rodríguez A, Gouveia AM, Gonçalves IO, Becerril S, Ramírez B, et al. Effects of Physical Exercise on Myokines Expression and Brown Adipose-Like Phenotype Modulation in Rats Fed a High-Fat Diet. Life Sciences 2016; 165: 100-8.
21- Alradi M, Askari H, Shaw M, Bhavsar JD, Kingham BF, Polson SW, et al. A Long-Term High-Fat Diet Induces Differential Gene Expression Changes in Spatially Distinct Adipose Tissue of Male Mice. Physiol Genomics 2024; 56(12): 819-32.
22- Kiran S, Rakib A, Kodidela S, Kumar S, Singh UP. High-Fat Diet-Induced Dysregulation of Immune Cells Correlates with Macrophage Phenotypes and Chronic Inflammation in Adipose Tissue. Cells 2022; 11(8): 1327.
23- Feillet‐Coudray C, Fouret G, Vigor C, Bonafos B, Jover B, Blachnio‐Zabielska A, et al. Long‐Term Measures of Dyslipidemia, Inflammation, and Oxidative Stress in Rats Fed a High‐Fat/High‐Fructose Diet. Lipids 2019; 54(1): 81-97.
24- Singh S, Sharma A, Guru B, Ahmad S, Gulzar F, Kumar P, et al. Fructose-Mediated NLRP3 Activation Induces Inflammation and Lipogenesis in Adipose Tissue. J Nutr Biochem 2022; 107: 109080.
25- Tourniaire F, Romier-Crouzet B, Lee JH, Marcotorchino J, Gouranton E, Salles J, et al. Chemokine Expression in Inflamed Adipose Tissue is Mainly Mediated by Nf-Κb. PloS one 2013; 8(6): e66515.
26- Nara N, Nakayama Y, Okamoto S, Tamura H, Kiyono M, Muraoka M, et al. Disruption of Cxc Motif Chemokine Ligand-14 in Mice Ameliorates Obesity-Induced Insulin Resistance. J Biol Chem 2007; 282(42): 30794-803.
27- Tanegashima K, Okamoto S, Nakayama Y, Taya C, Shitara H, Ishii R, et al. CXCL14 Deficiency in Mice Attenuates Obesity and Inhibits Feeding Behavior in A Novel Environment. PloS one 2010; 5(4): e10321.
28- Atanes P, Hawkes RG, Olaniru OE, Ruz-Maldonado I, Amisten S, Persaud SJ. CXCL14 Inhibits Insulin Secretion Independently of CXCR4 or CXCR7 Receptor Activation or Camp Inhibition. Cell Physiol Biochem 2019; 52(4): 879-92.
29- Franczyk MP, He M, Yoshino J. Removal of Epididymal Visceral Adipose Tissue Prevents Obesity-Induced Multi-Organ Insulin Resistance in Male Mice. J Endocrine Society 2021; 5(5): bvab024.
30- Cataldo LR, Gao Q, Argemi-Muntadas L, Hodek O, Cowan E, Hladkou S, et al. The Human Batokine EPDR1 Regulates Β-Cell Metabolism and Function. Mol Metab 2022; 66: 101629.
31- Fu P, Zhu R, Jia J, Hu Y, Wu C, Cieszczyk P, et al. Aerobic Exercise Promotes the Functions of Brown Adipose Tissue in Obese Mice Via a Mechanism Involving COX2 in the VEGF Signaling Pathway. Nutr Metab 2021; 18(1): 56.
32- McKie GL, Wright DC. Biochemical Adaptations in White Adipose Tissue Following Aerobic Exercise: from Mitochondrial Biogenesis to Browning. Biochem J 2020; 477(6): 1061-81.
33- Zhang Y, Xie C, Wang H, Foss RM, Clare M, George EV, et al. Irisin Exerts Dual Effects on Browning and Adipogenesis of Human White Adipocytes. Am J Physiol Endocrinol Metab 2016; 311(2): E530-41.
34- Roca-Rivada A, Castelao C, Senin LL, Landrove MO, Baltar J, Crujeiras AB, et al. FNDC5/Irisin Is Not Only a Myokine but Also an Adipokine. PloS one 2013; 8(4): e60563.
35- Powers SK, Jackson MJ. Exercise-Induced Oxidative Stress: Cellular Mechanisms and Impact on Muscle Force Production. Physiol Rev 2008; 88(4): 1243-76.
36- Voisin S, Eynon N, Yan X, Bishop D. Exercise Training and DNA Methylation in Humans. Acta Physiol 2015; 213(1): 39-59.
37- Barres R, Yan J, Egan B, Treebak JT, Rasmussen M, Fritz T, et al. Acute Exercise Remodels Promoter Methylation in Human Skeletal Muscle. Cell Metab 2012; 15(3): 405-11.
38- Pedersen BK. Anti‐Inflammatory Effects of Exercise: Role in Diabetes and Cardiovascular Disease. Eur J Clin Invest 2017; 47(8): 600-11.
39- Stanford KI, Goodyear LJ. Exercise Regulation of Adipose Tissue. Adipocyte 2016; 5(2): 153-62.
40- Ntanasis-Stathopoulos J, Tzanninis J, Philippou A, Koutsilieris M. Epigenetic Regulation on Gene Expression Induced by Physical Exercise. J Musculoskelet Neuronal Interact 2013; 13(2): 133-46.
41- Improta Caria AC, Nonaka CKV, Pereira CS, Soares MBP, Macambira SG, Souza BSdF. Exercise Training-Induced Changes in Micrornas: Beneficial Regulatory Effects in Hypertension, Type 2 Diabetes, and Obesity. Int J Mol Sci 2018; 19(11): 3608.
نوع مطالعه: پژوهشي |
موضوع مقاله:
فیزیولوژی ورزش
دریافت: 1404/5/13 | پذیرش: 1404/11/15 | انتشار: 1404/11/15
دریافت: 1404/5/13 | پذیرش: 1404/11/15 | انتشار: 1404/11/15
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |







