دوره 33، شماره 8 - ( آبان 1404 )
جلد 33 شماره 8 صفحات 9279-9269 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Gheibollahi H, Moradi H. Conservative Management of a Parakeratinized Odontogenic Keratocyst in the Anterior Maxilla: A Case Report. JSSU 2025; 33 (8) :9269-9279
URL: http://jssu.ssu.ac.ir/article-1-6501-fa.html
URL: http://jssu.ssu.ac.ir/article-1-6501-fa.html
غیب اللهی حامد، مرادی حامد. مدیریت محافظهکارانه کیست ادونتوژنیک کراتوسیستیک پاراکراتینیزه در ناحیه قدامی ماگزیلا: گزارش مورد. مجله علمي پژوهشي دانشگاه علوم پزشكي شهید صدوقی يزد. 1404; 33 (8) :9269-9279
واژههای کلیدی: کیست ادونتوژنیک کراتوسیستیک، پاراکراتینیزه، مارسوپیالیزاسیون، انوکلیشن، ماگزیلا، درمان محافظهکارانه
متن کامل [PDF 783 kb]
(138 دریافت)
| چکیده (HTML) (280 مشاهده)
متن کامل: (55 مشاهده)
مقدمه
کیست ادونتوژنیک کراتوسیستیک (Odontogenic Keratocyst – OKC) یک ضایعه فکی با منشأ ادونتوژنیک و ماهیت تکاملی است که به دلیل رفتار شبهنئوپلاستیک، پتانسیل رشد موضعی تهاجمی، و نرخ بالای عود مورد توجه قرار گرفته است. این ضایعه نخستین بار توسط Philipsen در سال ۱۹۵۶ توصیف شد (1) و از آن زمان تاکنون در طبقهبندیهای مختلف سازمان جهانی بهداشت (WHO) با دیدگاههای گوناگون مورد بررسی قرار گرفته است. در سال ۲۰۰۵، OKC در رده تومورهای ادونتوژنیک با عنوان keratocystic odontogenic tumor (KCOT) قرار گرفت، اما در نسخه چهارم طبقهبندی WHO (2017) (2) مجدداً به گروه کیستهای تکاملی بازگردانده شد و این جایگاه در بهروزرسانی پنجم WHO در سال 2022 نیز تأیید شد (3). دادههای ژنومیک اخیر نشان میدهد که محور Sonic Hedgehog و بهویژه ژن transmembrane receptor Patched 1 (PTCH1) در پاتوژنز OKC نقش محوری دارد، تغییرات PTCH1 در اکثریت موارد سندرمی و همچنین طیف وسیعی از موارد غیرسندرمی گزارش شده است، در برخی مطالعات تا حدود هشتاد تا نود درصد. افزون برPTCH1، شواهدی از فعال شدن اجزای مسیر HH (Hedgehoge) مانند transmembrane G protein-coupled receptor Smoothened (SMO) وglioma-associated oncogene homolog 1 (GLI1)و افزایش بیان اهداف پایین دستی نظیر cyclin D1 و bcl-2 نیز دیده شده است که با ظرفیت تکثیر اپیتلیوم و رفتار بالینی تهاجمیتر ارتباط دارد (4). علاوه بر جهش، الگوهای ژنومی مشخصی مانند copy-neutral LOH در بازوی 9q با درگیری جایگاه PTCH1 و حتی NOTCH1 در هر سه مورد سندرمی و اغلب موارد غیرسندرمی گزارش شده است، همچنین LOH در 16p11.2 و تغییرات در 22q11.23 و 10 q22.1 نیز در هر دو گروه دیده شده است، که همپوشانی و در عین حال تمایز مولکولی بین فرمهای سندرمی و غیرسندرمی را نشان میدهد. این یافتهها بر ضرورت توجه به زیستشناسی مولکولی در تصمیمگیری درمانی و پایش پیگیری تاکید میکند (5). از نظر بافتشناسی، OKCبه دو نوع پاراکراتینیزه و ارتوکراتینیزه تقسیم میشود که نوع پاراکراتینیزه شیوع بیشتری دارد و از نظر بالینی رفتار تهاجمیتری نشان میدهد (6،1). ویژگیهای هیستوپاتولوژیک آن شامل اپیتلیوم سنگفرشی مطبق با لایه بازال نردبانیشکل، سطح مواج، کراتین داخل لومن و فقدان رتپگ (Rete Pegs) است. همین ویژگیها موجب دشواری در برداشت کامل ضایعه و افزایش خطر عود آن شدهاند (7،2). مطالعات اپیدمیولوژیک بینالمللی نشان دادهاند که این ضایعه بیشتر در ناحیه خلفی مندیبل رخ میدهد اما بر اساس مطالعه گذشتهنگر ۳۱ ساله در دانشگاه علوم پزشکی تهران، حدود ۳۲% از OKCها در فک بالا و از میان آنها ۴۲% در ناحیه قدامی ماگزیلا قرار داشتهاند، که نشان میدهد در جمعیت ایرانی نیز این محل از شیوع قابلتوجهی برخوردار است (8).
انتخاب روش درمان برای OKC بر اساس اندازه، محل ضایعه، سن بیمار، نوع بافتشناسی و خطر عود صورت میگیرد. روشهای مختلفی از جمله انوکلیشن ساده، انوکلیشن همراه با peripheral ostectomyدکامپرشن، مارسوپیالیزاسیون و حتی رزکسیون وسیع پیشنهاد شدهاند. در سالهای اخیر، درمانهای مرحلهای شامل مارسوپیالیزاسیون اولیه و انوکلیشن تأخیری بهعنوان گزینهای محافظهکارانه برای ضایعات بزرگ یا واقع در نواحی حساس معرفی شدهاند (10،9). مطالعات اخیرا، بر برجسته شدن فرآیندهای سازماندهی ماتریکس خارجسلولی، سازماندهی فیبریلهای کلاژن و چسبندگی سلولی در OKC دلالت دارند، در حالیکه مسیرهای دفاع ضد ویروسی و پاسخ به اینترفرون گاما در ژنهای پایینتنظیم شده غالب است. این الگو میتواند با تغییرات بافتی پس از دکامپرشن و تاثیر آن بر تسهیل برداشت نهایی همسو باشد و منطق رویکرد مرحلهای را تقویت کند (12،11). مطالعاتی در زمینه بررسی و مقایسه روشهای درمانی OKC انجام شده است. در مطالعه مروری و متاآنالیز Silva و همکاران، گرچه اختلاف معناداری از نظر آماری بین دو گروه مارسوپیالیزاسیون + انوکلیشن تأخیری و انوکلیشن تنها دیده نشد، ولی گروه اول نرخ عود کمتری را تجربه کرده بودند (13). مطالعه Khalil و همکاران نیز گزارش موفقیتآمیز یک درمان مرحلهای شامل مارسوپیالیزاسیون اولیه و انوکلیشن همراه با برداشت محیطی در یک مورد OKC بزرگ را ارائه کرد (14).
مطالعه Nasrollahi نیز در ایران نشان داد که این رویکرد میتواند منجر به بازسازی مناسب استخوان و عدم عود در پیگیری طولانیمدت شود (15). با توجه به رفتار بیولوژیک ویژه OKC و چالشهای درمانی در مجاورت ساختارهای حیاتی، رویکرد مرحلهای شامل دکامپرشن یا مارسوپیالیزاسیون و سپس انوکلیشن، به تنهایی یا همراه برداشت محیطی، در سالهای اخیر برای کاهش اندازه ضایعه، تسهیل جراحی قطعی و احتمالاً کاهش عود مطرح شده است. شواهد متاآنالیز نشان میدهد که مارسوپیالیزاسیون به دنبال انوکلیشن طی ۱۲ تا ۱۸ ماه میتواند نسبت به انوکلیشن تنها، عود را کاهش دهد، اگرچه نیاز به مطالعات بیشتر باقی است (13). در برخی مطالعات آدجوانتها و رویکردهای جراحی با نرخ عود بسیار پایین گزارش شدهاند. استفاده موضعی از پنج فلورواوراسیل پس از انوکلیشن و برداشت محیطی در تنها مطالعه مرور ۲۰۲۴ بدون عود ثبت شده است، هرچند تعداد نمونه محدود بوده است. در برخی مجموعهها، انوکلیشن همراه برداشت محیطی یا حتی رزکشن نیز بدون عود گزارش شده، اما تهاجمی بودن و عوارض رزکشن، کاربرد روتین آن را محدود میکند. بهطورکلی، دکامپرشن و مارسوپیالیزاسیون با موربیدیتی کمتر، کوچک شدن ضایعه و تسهیل برداشت نهایی همراه است، ولی به همکاری بیمار و پیگیری منظم نیاز دارد (16). در مطالعه حاضر، موردی نادر از OKC پاراکراتینیزه در ناحیه قدامی ماگزیلا گزارش میشود که تحت درمان مرحلهای شامل مارسوپیالیزاسیون اولیه و انوکلیشن تأخیری قرار گرفته است. مستندسازی این مورد میتواند به درک بهتر رفتار بالینی این ضایعه در محل غیرشایع و اثربخشی درمان محافظهکارانه مرحلهای کمک کند.
گزارش مورد : بیمار مردی ۵۷ ساله، بدون سابقه بیماری سیستمیک خاص، با شکایت تورم مزمن، بدون درد و با رشد آهسته در ناحیه قدامی ماگزیلا از 1سال گذشته در اسفندماه 1402 به درمانگاه دندانپزشکی مراجعه کرده و پس از بیوپسی و شک به OKC بیمار توسط دندانپزشک به سرویس جراحی دهان و فک و صورت بیمارستان شهید رهنمون یزد ارجاع داده شد. تورم طی یک سال گذشته بهتدریج افزایش یافته بود و با مصرف دارو یا اقدامات دندانی پیشین بهبود نیافته بود. بیمار سابقه ضربه یا جراحی قبلی در این ناحیه نداشت. در معاینه خارجدهانی، تورم غیرقرینه در ناحیه زیر بینی و لب فوقانی مشاهده شد که موجب برهمخوردن خفیف تقارن صورت شده بود. پوست روی ناحیه متورم طبیعی و فاقد تغییر رنگ یا زخم بود (شکل 1و2) (نمای تحتانی صورت نیز برجستگی پایه بینی و ناحیه سابنازال را تأیید کرد. در معاینه داخلدهانی، تورم سفت و بدون درد در مخاط لبی ماگزیلا از ناحیه مولر دوم سمت راست تا مولر دوم سمت چپ دیده شد. مخاط روی ضایعه اندکی قرمزتر از مخاط مجاور بود، ولی زخم، ترشح یا التهاب حاد مشاهده نشد (شکل 3). رادیوگرافی پانورامیک اولیه، ضایعهای رادیولوسنت، تکحفرهای و با حدود مشخص را در ناحیه قدام وخلف ماگزیلا نشان داد که از دندان مولردوم سمت راست تا مولر دوم سمت چپ امتداد داشت و منجر به نازکشدگی قابلتوجه کورتکس قدامی شده بود (شکل ۴). ارزیابی تکمیلی باCBCT، ضایعهای با گسترش وسیع (2*3*4 سانتیمتر) در محور قدامی-خلفی فک بالا را تأیید کرد که بدون درگیری سینوس فکی یا کف بینی بود. دیوارههای استخوانی پالاتال و باکال در محل ضایعه نازک شده اما پیوسته بودند. جابهجایی اندک ریشههای دندانهای مجاور بدون تحلیل ریشه مشاهده شد (شکل 5). با توجه به ویژگیهای بالینی و تصویربرداری، تشخیصهای افتراقی شامل آملوبلاستوما، کیست مجرای نازوپالاتین و OKC مطرح شد. بیوپسی انسیزیونی از ضایعه انجام و نمونه جهت بررسی هیستوپاتولوژیک ارسال شد. گزارش پاتولوژی نشان داد که ضایعه دارای اپیتلیوم سنگفرشی مطبق پاراکراتینیزه با سطح مواج و چینخورده، بدون رتپگ، و لایه بازال نردبانی با سلولهای استوانهای پلاریزه است. کراتین فراوان در لومن مشاهده شد و میتوز در لایههای بازال و پارابازال وجود داشت. این ویژگیها با تشخیص OKC نوع پاراکراتینیزه مطابقت داشتند (شکل 7). با توجه به محل ضایعه، اندازه نسبتاً بزرگ آن، و نزدیکی به ساختارهای حیاتی مانند حفره بینی و قاعده سینوس، تصمیم به انجام درمان مرحلهای گرفته شد. در مرحله اول، مارسوپیالیزاسیون تحت بیهوشی عمومی با اینتوباسیون نازال انجام شد. برش وستیبولار دوطرفه در قدام ماگزیلا ایجاد و پس از بازکردن دیواره کیست، دو عدد درن نلاتون در طرفین ضایعه قرار داده شد. بخیه لبههای مخاطی به دیواره کیست با نخ سلیک ۰-۲ انجام و مخاط با ویکریل ۰-۳ سوچور شد. شستشوی کامل با نرمالسالین انجام شد و پانسمان داخل حفره با گاز استریل صورت گرفت (شکل 8). تا زمان حضور بیمار در بیمارستان شستشو توسط پزشک انجام شد و نهایتا پس از آموزش شستشو به بیمار و اطمینان از آموزش وی بیمار مرخص گردید. در پیگیریهای انجام شده در فواصل دو هفته، یک ماه، سه ماه و شش ماه، بیمار بدون علائم عود، درد یا ترشح باقی ماند. تورم بهتدریج کاهش یافت و نمای مخاطی ناحیه به وضعیت نرمال نزدیک شد. گرافی پانورامیک پیگیری شش ماهه کاهش چشمگیر اندازه ضایعه و افزایش تراکم استخوان را نشان داد (شکل 9). با توجه به پاسخ مناسب ضایعه به مرحله اول درمان، برنامهریزی برای انجام انوکلیشن تأخیری به همراه برداشت محیطی (Peripheral Ostectomy) پس از شش ماه انجام شد. در مرحله دوم تحت بیهوشی عمومی، با ایجاد یک برش وستیبولار و نمایان شدن ناحیه ضایعه، پوشش ضایعه از دیوارههای استخوانی جدا گردید. بهمنظور برداشت استخوان مجاور پوشش کیستیک، از فرز جراحی استفاده شد. پس از انجام انوکلیشن، حفره با ژلفوم پر گردید و برشها با نخ بخیه ۴-۰ پرولن بسته شدند. هدف از این اقدام، حذف کامل اپیتلیوم باقیمانده و کاهش خطر عود ضایعه در بلندمدت خواهد بود.
.JPG)
شکل 2و1: نمای روبهرو از صورت بیمار پیش از جراحی، با تورم خفیف در ناحیه قدامی ماگزیلا (لب فوقانی سمت راست بیمار) و نمای تحتانی از صورت بیمار، نشاندهنده گسترش تورم به ناحیه پایه بینی و قدام ماگزیلا.
.JPG)
شکل3: نمای داخلدهانی بیمار قبل از انجام مارسوپیالیزاسیون. تورم مخاطی با رنگ قرمزتر نسبت به مخاط نرمال در ناحیه قدامی ماگزیلا قابل مشاهده است.
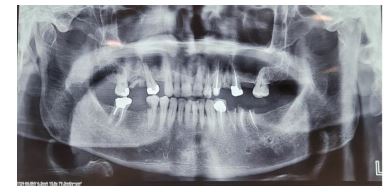
شکل 4: نمای پانورامیک قبل از انجام مارسوپیالیزاسیون که ضایعه رادیولوسنت تکحفرهای در ناحیه قدامی و خلفی ماگزیلا را نشان میدهد. محدوده ضایعه از مولردوم راست تا ناحیه مولردوم چپ امتداد دارد و نازکشدگی کورتکس قابل مشاهده است.
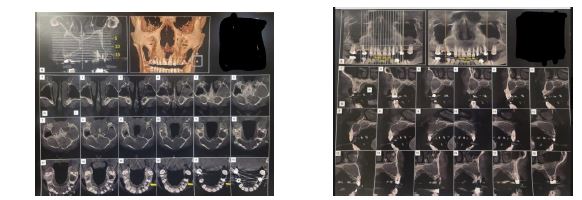
شکل 6و5 : تصاویر CBCT در محور کرونال و ساژیتال؛ تأیید نازکشدگی کورتکس بدون درگیری سینوس یا بینی.
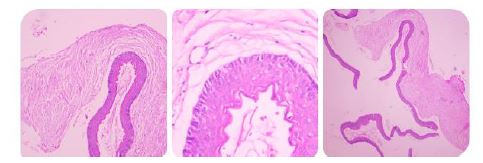
شکل7: تصاویر پاتولوژیH&E
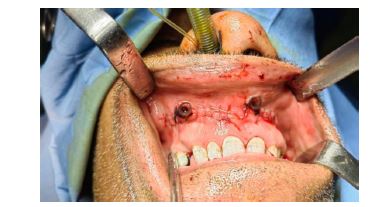
شکل8: نمای داخل دهانی حین جراحی مارسوپیالیزاسیون در ناحیه قدامی ماگزیلا. دو پنجره در دیواره ضایعه ایجاد شده و توسط بخیه به مخاط دهان متصل شدهاند. پانسمان داخل حفره پس از عمل انجام شده است.
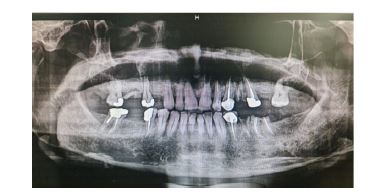
شکل9: نمای پانورامیک شش ماه پس از مارسوپیالیزاسیون، نشاندهنده کاهش چشمگیر حجم ضایعه، افزایش تراکم استخوانی و عدم عود ضایعه در ناحیه قدامی ماگزیلا.
بحث
کیست ادونتوژنیک کراتوسیستیک (OKC) به دلیل ویژگیهای تهاجمی، شیوع نسبی بالا و رفتار بالینی غیرقابل پیشبینی، یکی از چالشبرانگیزترین ضایعات در حوزه جراحی فک و صورت بهشمار میرود (3). OKC ها تمایل به عود دارند و عوامل خطری مانند سن کمتر، چندحفرهای بودن، اندازه بزرگتر و طول قدامی ـ خلفی بیشتر، احتمال عود را بالا میبرد. بنابراین انتخاب رویکرد مرحلهای یا قطعی باید بر اساس این عوامل و موقعیت آناتومیک انجام شود (16). ساختار هیستوپاتولوژیک خاص آن، از جمله اپیتلیوم سنگفرشی مطبق با لایه بازال نردبانی و کراتین در لومن، احتمال باقیماندن بقایای بافتی پس از درمان و در نتیجه، عود ضایعه را افزایش میدهد (3،9). در این مطالعه، کیستی از نوع پاراکراتینیزه OKC در ناحیه نسبتاً نادر قدامی ماگزیلا گزارش شد که با رویکرد مرحلهای محافظهکارانه، شامل مارسوپیالیزاسیون اولیه و انوکلیشن تأخیری، مدیریت گردید. ناحیه قدامی ماگزیلا، اگرچه در مطالعات بینالمللی بهندرت بهعنوان محل اصلی OKC ذکر میشود، اما در مطالعه گذشتهنگر انجام شده در دانشگاه تهران، 42% از OKCهای فک بالا در این ناحیه قرار داشتند که نشان میدهد این محل در جمعیت ایرانی نیز حائز اهمیت است (6). در کنار بررسیهای کلینیکی، تصویربرداری و هیستوپاتولوژیک، ارزیابی احتمال سندرمی بودن کیستهای ادونتوژنیک کراتوسیستیک بهویژه در بیماران جوان، دارای ضایعات متعدد یا موارد عودشونده اهمیت دارد. یکی از مهمترین سندرمهای مرتبط باOKC، سندرم کارسینومای بازالسل نئووئید (Nevoid Basal Cell Carcinoma Syndrome – NBCCS) است که در آن جهش در ژن PTCH1 منجر به فعالشدن غیرطبیعی مسیر سیگنالینگ Hedgehog میشود. این مسیر در پاتوژنز ضایعات کراتوسیستیک نقش مؤثر دارد و زمینهساز تهاجم بیشتر و پتانسیل عود بالا خواهد بود (12). در برخی مطالعات، استفاده از درمانهای هدفمند مولکولی نظیر Vismodegib برای موارد مقاوم یا سندرمی پیشنهاد شده است، هرچند کاربرد بالینی آن هنوز در مرحله تحقیقاتی قرار دارد (15). یافتههای بیوانفورماتیکی جدید نیز نشان میدهد که ژنهای بالارونده در OKC بیشتر با سازماندهی ماتریکس خارج سلولی و فیبریلهای کلاژن ارتباط دارند، در حالیکه ژنهای پایینرونده با پاسخهای دفاعی ضد ویروسی و فعالسازی اینترفرون گاما مرتبط هستند. این الگو با تغییرات بافتی پس از دکامپرشن قابل جمع است و میتواند منطق رویکرد مرحلهای را تقویت کند (16). برآیند شواهد نشان میدهد که در ضایعات واقع در نواحی حساس مانند قدام ماگزیلا، بهکارگیری درمان مرحلهای با هدف کاهش حجم ضایعه و تسهیل برداشت قطعی، در کنار در نظر گرفتن عوامل خطر عود و امکان استفاده از آدجوانتها، میتواند انتخابی منطقی باشد. با این حال، ضرورت پیگیری بلندمدت و اجرای مطالعات آیندهنگر برای استانداردسازی پروتکلها پابرجاست (16،17). در مطالعه حاضر، با توجه به محل منفرد ضایعه، عدم وجود سابقه خانوادگی مشابه، و عدم وجود سایر علائم سندرمی (نظیر کیستهای پلانتار، کلسیفیکاسیون فالکس سربری، یا اختلالات اسکلتی)، بیمار جهت اطمینان به مشاوره ژنتیک ارجاع داده شد. پس از انجام بررسیهای تخصصی توسط متخصص ژنتیک، احتمال ارتباط ضایعه با NBCCS (Non Basal Cell Carcinoma) رد گردید. این اقدام از آن جهت اهمیت دارد که شناسایی فرمهای سندرمی OKC مستلزم برنامهریزی درمانی، پیگیریهای گستردهتر و غربالگری سایر اعضای خانواده خواهد بود (18). یکی از اصلیترین اهداف درمان، کاهش خطر عود با حفظ حداقل تهاجم است. درمان مرحلهای در سالهای اخیر توجه بسیاری را به خود جلب کرده است. در متاآنالیز انجامشده توسط Silva و همکاران، گرچه تفاوت آماری معناداری بین انوکلیشن تنها و انوکلیشن پس از مارسوپیالیزاسیون یافت نشد، اما نرخ عود در افرادیکه انوکلیشن پس از مارسوپیالیزاسیون انجام داده بودند بهطور نسبی کمتر بود، که نشان از پتانسیل مؤثر این روش دارد. این متاآنالیز همچنین بازه زمانی 12 تا 18 ماه را برای مرحله اول توصیه کرده است، کاهش حجم ضایعه و تسهیل برداشت نهایی را میتوان در این فاصله انتظار داشت. این مطالعه همچنین تأکید میکند که کاهش فشار داخل کیست با مارسوپیالیزاسیون میتواند منجر به تغییرات اپیتلیال و کاهش پتانسیل تهاجمی ضایعه شود (13). همسویی با این نتایج را میتوان در مطالعه Khalil و همکاران نیز مشاهده کرد، که در آن یک مورد OKC وسیع در ناحیه راموس مندیبل با استفاده از مارسوپیالیزاسیون اولیه و انوکلیشن همراه با برداشت محیطی (peripheral ostectomy) بدون عود و با بازسازی کامل استخوان طی پیگیری ۳۶ ماهه درمان شد (14،5). یافتههای مطالعه حاضر با نتایج این گزارش همراستا است؛ بهویژه از آن جهت که کاهش چشمگیر اندازه ضایعه و تراکم استخوانی پس از مرحله اول درمان مشاهده شد. تغییر دیدگاه نسبت به OKC طی دو دهه اخیر، از طبقهبندی آن بهعنوان تومور (KCOT) در سال ۲۰۰۵ تا بازگشت آن به گروه کیستهای تکاملی در طبقهبندیWHO 2017، در نتیجه مشاهده شواهد پاتولوژیک و بالینی مانند تغییرات ساختاری اپیتلیوم پس از دکامپرشن صورت گرفته است (19،10،3). این شواهد پایهای برای اثبات اثربخشی درمانهای محافظهکارانه مرحلهای بودهاند.
مارسوپیالیزاسیون در مطالعات اخیر نهتنها بهعنوان روشی کمتهاجم جهت کاهش حجم ضایعه و حفظ ساختارهای حیاتی (مانند سینوس ماگزیلاری و عصب آلوئولار تحتانی) مطرح شده، بلکه اثر آن در تحریک استئوژنز نیز مورد تأکید قرار گرفته است (1). این ویژگیها در مورد حاضر، که ضایعه به ناحیه پایه بینی و استخوانهای قدامی ماگزیلا گسترش یافته بود، اهمیت مضاعفی پیدا میکند. با این حال، باید تأکید کرد که مارسوپیالیزاسیون بهتنهایی درمان قطعی محسوب نمیشود، چرا که اپیتلیوم ادونتوژنیک ممکن است در دیواره کیست باقی بماند و زمینهساز عود در آینده شود. بنابراین، مرحله دوم درمان در قالب انوکلیشن همراه با برداشت محیطی انجام شد، تا تمامی بافتهای باقیمانده حذف شوند. در روش برداشت محیطی، حدود ۱.۵ تا ۲ میلیمتر از استخوان اطراف محل ضایعه با ابزار دوار برداشته میشود تا خطر عود به حداقل برسد. مطالعات متعدد از جمله بررسی Kolokythas و همکاران نیز نشان دادهاند که افزودن برداشت محیطی به انوکلیشن موجب کاهش معنادار نرخ عود OKC شده و حتی در برخی مطالعات، نرخ عود صفر گزارش شده است (20). در مطالعه نصرالهی و علیرضایی نیز گزارش شد که استفاده از دکامپرشن اولیه و انوکلیشن تأخیری در یک OKC پاراکراتینیزه در فک پایین، باعث تغییر در ساختار اپیتلیال، کاهش ضخامت جداره کیست و تسهیل در برداشت کامل آن گردید. همچنین، در پیگیری ۲۸ ماهه هیچ نشانهای از عود مشاهده نشد (15). از دیدگاه پاتولوژیک نیز، مطالعات نشان دادهاند که کاهش فشار داخل کیست، تغییراتی در الگوی کراتینیزاسیون و سلولهای بازال ایجاد میکند که میتواند باعث کاهش توان نفوذ و تکثیر سلولهای اپیتلیال شود (4). برخی نویسندگان معتقدند که مارسوپیالیزاسیون نهتنها از نظر مکانیکی باعث کاهش حجم ضایعه میشود، بلکه تأثیر بیولوژیک نیز در ساختار بافت دارد (22،21). در این مطالعه، پس از انجام مرحله اول درمان، بیمار بدون درد، ترشح یا شواهد بالینی عود باقی ماند و در گرافی پیگیری، بازسازی تدریجی استخوان مشاهده شد. پاسخ به درمان اولیه موفقیتآمیز بوده و روند پیشرفت درمان مرحلهای را تأیید میکند. با توجه به شواهد حاصل از مطالعات مشابه، میتوان امیدوار بود که تکمیل درمان با روشهای مکمل، احتمال عود را به حداقل خواهد رساند. در مجموع، رویکرد مرحلهای در مدیریت OKC بهویژه در نواحی آناتومیک حساس مانند قدام ماگزیلا میتواند گزینهای مناسب و کمعارضه باشد. با اینحال، تصمیمگیری درمانی باید مبتنی بر فاکتورهای بالینی، پاتولوژیک و میزان درگیری استخوان باشد و انجام پیگیریهای درازمدت و ثبت نتایج نهایی، برای اثبات اثربخشی این رویکرد ضروری است.
نتیجهگیری
در این مطالعه، مدیریت مرحلهای یک مورد نادر از OKC پاراکراتینیزه در ناحیه قدامی ماگزیلا با موفقیت پشت سر گذاشته است. کاهش چشمگیر اندازه ضایعه، عدم علائم عود و بازسازی استخوانی در گرافی پیگیری، اثربخشی اولیه درمان محافظهکارانه را نشان میدهد. با توجه به نزدیکی ضایعه به ساختارهای حیاتی، این رویکرد با حداقل تهاجم، جایگزین مناسبی برای رزکسیون وسیع محسوب میشود. با اینحال، پیگیری طولانیمدت برای ارزیابی قطعی موفقیت ضروری است.
سپاسگزاری
نویسندگان از بیمار و خانواده ایشان بهخاطر همکاری در تهیه این گزارش مورد کمال تشکر را دارند.
حامی مالی: ندارد
تعارض در منافع:وجود ندارد
ملاحظات اخلاقی
این گزارش مورد با رضایت آگاهانه از بیمار جهت قراردهی تصاویر و معرفی ایشان، همچنین کد اخلاق با شماره IR.SSU.SRH.REC.1404.006 از بیمارستان شهید رهنمون یزد دریافت شد.
مشارکت نویسندگان
دکتر حامد غیباللهی در ارائه ایده، دکتر حامد مرادی در طراحی مطالعه، دکتر حامد مرادی در جمعآوری دادهها، دکتر حامد غیباللهی در تجزیه و تحلیل دادهها مشارکت داشته و همه نویسندگان در تدوین، ویرایش اولیه و نهایی مقاله و پاسخگویی به سوالات مرتبط با مقاله سهیم هستند.
کیست ادونتوژنیک کراتوسیستیک (Odontogenic Keratocyst – OKC) یک ضایعه فکی با منشأ ادونتوژنیک و ماهیت تکاملی است که به دلیل رفتار شبهنئوپلاستیک، پتانسیل رشد موضعی تهاجمی، و نرخ بالای عود مورد توجه قرار گرفته است. این ضایعه نخستین بار توسط Philipsen در سال ۱۹۵۶ توصیف شد (1) و از آن زمان تاکنون در طبقهبندیهای مختلف سازمان جهانی بهداشت (WHO) با دیدگاههای گوناگون مورد بررسی قرار گرفته است. در سال ۲۰۰۵، OKC در رده تومورهای ادونتوژنیک با عنوان keratocystic odontogenic tumor (KCOT) قرار گرفت، اما در نسخه چهارم طبقهبندی WHO (2017) (2) مجدداً به گروه کیستهای تکاملی بازگردانده شد و این جایگاه در بهروزرسانی پنجم WHO در سال 2022 نیز تأیید شد (3). دادههای ژنومیک اخیر نشان میدهد که محور Sonic Hedgehog و بهویژه ژن transmembrane receptor Patched 1 (PTCH1) در پاتوژنز OKC نقش محوری دارد، تغییرات PTCH1 در اکثریت موارد سندرمی و همچنین طیف وسیعی از موارد غیرسندرمی گزارش شده است، در برخی مطالعات تا حدود هشتاد تا نود درصد. افزون برPTCH1، شواهدی از فعال شدن اجزای مسیر HH (Hedgehoge) مانند transmembrane G protein-coupled receptor Smoothened (SMO) وglioma-associated oncogene homolog 1 (GLI1)و افزایش بیان اهداف پایین دستی نظیر cyclin D1 و bcl-2 نیز دیده شده است که با ظرفیت تکثیر اپیتلیوم و رفتار بالینی تهاجمیتر ارتباط دارد (4). علاوه بر جهش، الگوهای ژنومی مشخصی مانند copy-neutral LOH در بازوی 9q با درگیری جایگاه PTCH1 و حتی NOTCH1 در هر سه مورد سندرمی و اغلب موارد غیرسندرمی گزارش شده است، همچنین LOH در 16p11.2 و تغییرات در 22q11.23 و 10 q22.1 نیز در هر دو گروه دیده شده است، که همپوشانی و در عین حال تمایز مولکولی بین فرمهای سندرمی و غیرسندرمی را نشان میدهد. این یافتهها بر ضرورت توجه به زیستشناسی مولکولی در تصمیمگیری درمانی و پایش پیگیری تاکید میکند (5). از نظر بافتشناسی، OKCبه دو نوع پاراکراتینیزه و ارتوکراتینیزه تقسیم میشود که نوع پاراکراتینیزه شیوع بیشتری دارد و از نظر بالینی رفتار تهاجمیتری نشان میدهد (6،1). ویژگیهای هیستوپاتولوژیک آن شامل اپیتلیوم سنگفرشی مطبق با لایه بازال نردبانیشکل، سطح مواج، کراتین داخل لومن و فقدان رتپگ (Rete Pegs) است. همین ویژگیها موجب دشواری در برداشت کامل ضایعه و افزایش خطر عود آن شدهاند (7،2). مطالعات اپیدمیولوژیک بینالمللی نشان دادهاند که این ضایعه بیشتر در ناحیه خلفی مندیبل رخ میدهد اما بر اساس مطالعه گذشتهنگر ۳۱ ساله در دانشگاه علوم پزشکی تهران، حدود ۳۲% از OKCها در فک بالا و از میان آنها ۴۲% در ناحیه قدامی ماگزیلا قرار داشتهاند، که نشان میدهد در جمعیت ایرانی نیز این محل از شیوع قابلتوجهی برخوردار است (8).
انتخاب روش درمان برای OKC بر اساس اندازه، محل ضایعه، سن بیمار، نوع بافتشناسی و خطر عود صورت میگیرد. روشهای مختلفی از جمله انوکلیشن ساده، انوکلیشن همراه با peripheral ostectomyدکامپرشن، مارسوپیالیزاسیون و حتی رزکسیون وسیع پیشنهاد شدهاند. در سالهای اخیر، درمانهای مرحلهای شامل مارسوپیالیزاسیون اولیه و انوکلیشن تأخیری بهعنوان گزینهای محافظهکارانه برای ضایعات بزرگ یا واقع در نواحی حساس معرفی شدهاند (10،9). مطالعات اخیرا، بر برجسته شدن فرآیندهای سازماندهی ماتریکس خارجسلولی، سازماندهی فیبریلهای کلاژن و چسبندگی سلولی در OKC دلالت دارند، در حالیکه مسیرهای دفاع ضد ویروسی و پاسخ به اینترفرون گاما در ژنهای پایینتنظیم شده غالب است. این الگو میتواند با تغییرات بافتی پس از دکامپرشن و تاثیر آن بر تسهیل برداشت نهایی همسو باشد و منطق رویکرد مرحلهای را تقویت کند (12،11). مطالعاتی در زمینه بررسی و مقایسه روشهای درمانی OKC انجام شده است. در مطالعه مروری و متاآنالیز Silva و همکاران، گرچه اختلاف معناداری از نظر آماری بین دو گروه مارسوپیالیزاسیون + انوکلیشن تأخیری و انوکلیشن تنها دیده نشد، ولی گروه اول نرخ عود کمتری را تجربه کرده بودند (13). مطالعه Khalil و همکاران نیز گزارش موفقیتآمیز یک درمان مرحلهای شامل مارسوپیالیزاسیون اولیه و انوکلیشن همراه با برداشت محیطی در یک مورد OKC بزرگ را ارائه کرد (14).
مطالعه Nasrollahi نیز در ایران نشان داد که این رویکرد میتواند منجر به بازسازی مناسب استخوان و عدم عود در پیگیری طولانیمدت شود (15). با توجه به رفتار بیولوژیک ویژه OKC و چالشهای درمانی در مجاورت ساختارهای حیاتی، رویکرد مرحلهای شامل دکامپرشن یا مارسوپیالیزاسیون و سپس انوکلیشن، به تنهایی یا همراه برداشت محیطی، در سالهای اخیر برای کاهش اندازه ضایعه، تسهیل جراحی قطعی و احتمالاً کاهش عود مطرح شده است. شواهد متاآنالیز نشان میدهد که مارسوپیالیزاسیون به دنبال انوکلیشن طی ۱۲ تا ۱۸ ماه میتواند نسبت به انوکلیشن تنها، عود را کاهش دهد، اگرچه نیاز به مطالعات بیشتر باقی است (13). در برخی مطالعات آدجوانتها و رویکردهای جراحی با نرخ عود بسیار پایین گزارش شدهاند. استفاده موضعی از پنج فلورواوراسیل پس از انوکلیشن و برداشت محیطی در تنها مطالعه مرور ۲۰۲۴ بدون عود ثبت شده است، هرچند تعداد نمونه محدود بوده است. در برخی مجموعهها، انوکلیشن همراه برداشت محیطی یا حتی رزکشن نیز بدون عود گزارش شده، اما تهاجمی بودن و عوارض رزکشن، کاربرد روتین آن را محدود میکند. بهطورکلی، دکامپرشن و مارسوپیالیزاسیون با موربیدیتی کمتر، کوچک شدن ضایعه و تسهیل برداشت نهایی همراه است، ولی به همکاری بیمار و پیگیری منظم نیاز دارد (16). در مطالعه حاضر، موردی نادر از OKC پاراکراتینیزه در ناحیه قدامی ماگزیلا گزارش میشود که تحت درمان مرحلهای شامل مارسوپیالیزاسیون اولیه و انوکلیشن تأخیری قرار گرفته است. مستندسازی این مورد میتواند به درک بهتر رفتار بالینی این ضایعه در محل غیرشایع و اثربخشی درمان محافظهکارانه مرحلهای کمک کند.
گزارش مورد : بیمار مردی ۵۷ ساله، بدون سابقه بیماری سیستمیک خاص، با شکایت تورم مزمن، بدون درد و با رشد آهسته در ناحیه قدامی ماگزیلا از 1سال گذشته در اسفندماه 1402 به درمانگاه دندانپزشکی مراجعه کرده و پس از بیوپسی و شک به OKC بیمار توسط دندانپزشک به سرویس جراحی دهان و فک و صورت بیمارستان شهید رهنمون یزد ارجاع داده شد. تورم طی یک سال گذشته بهتدریج افزایش یافته بود و با مصرف دارو یا اقدامات دندانی پیشین بهبود نیافته بود. بیمار سابقه ضربه یا جراحی قبلی در این ناحیه نداشت. در معاینه خارجدهانی، تورم غیرقرینه در ناحیه زیر بینی و لب فوقانی مشاهده شد که موجب برهمخوردن خفیف تقارن صورت شده بود. پوست روی ناحیه متورم طبیعی و فاقد تغییر رنگ یا زخم بود (شکل 1و2) (نمای تحتانی صورت نیز برجستگی پایه بینی و ناحیه سابنازال را تأیید کرد. در معاینه داخلدهانی، تورم سفت و بدون درد در مخاط لبی ماگزیلا از ناحیه مولر دوم سمت راست تا مولر دوم سمت چپ دیده شد. مخاط روی ضایعه اندکی قرمزتر از مخاط مجاور بود، ولی زخم، ترشح یا التهاب حاد مشاهده نشد (شکل 3). رادیوگرافی پانورامیک اولیه، ضایعهای رادیولوسنت، تکحفرهای و با حدود مشخص را در ناحیه قدام وخلف ماگزیلا نشان داد که از دندان مولردوم سمت راست تا مولر دوم سمت چپ امتداد داشت و منجر به نازکشدگی قابلتوجه کورتکس قدامی شده بود (شکل ۴). ارزیابی تکمیلی باCBCT، ضایعهای با گسترش وسیع (2*3*4 سانتیمتر) در محور قدامی-خلفی فک بالا را تأیید کرد که بدون درگیری سینوس فکی یا کف بینی بود. دیوارههای استخوانی پالاتال و باکال در محل ضایعه نازک شده اما پیوسته بودند. جابهجایی اندک ریشههای دندانهای مجاور بدون تحلیل ریشه مشاهده شد (شکل 5). با توجه به ویژگیهای بالینی و تصویربرداری، تشخیصهای افتراقی شامل آملوبلاستوما، کیست مجرای نازوپالاتین و OKC مطرح شد. بیوپسی انسیزیونی از ضایعه انجام و نمونه جهت بررسی هیستوپاتولوژیک ارسال شد. گزارش پاتولوژی نشان داد که ضایعه دارای اپیتلیوم سنگفرشی مطبق پاراکراتینیزه با سطح مواج و چینخورده، بدون رتپگ، و لایه بازال نردبانی با سلولهای استوانهای پلاریزه است. کراتین فراوان در لومن مشاهده شد و میتوز در لایههای بازال و پارابازال وجود داشت. این ویژگیها با تشخیص OKC نوع پاراکراتینیزه مطابقت داشتند (شکل 7). با توجه به محل ضایعه، اندازه نسبتاً بزرگ آن، و نزدیکی به ساختارهای حیاتی مانند حفره بینی و قاعده سینوس، تصمیم به انجام درمان مرحلهای گرفته شد. در مرحله اول، مارسوپیالیزاسیون تحت بیهوشی عمومی با اینتوباسیون نازال انجام شد. برش وستیبولار دوطرفه در قدام ماگزیلا ایجاد و پس از بازکردن دیواره کیست، دو عدد درن نلاتون در طرفین ضایعه قرار داده شد. بخیه لبههای مخاطی به دیواره کیست با نخ سلیک ۰-۲ انجام و مخاط با ویکریل ۰-۳ سوچور شد. شستشوی کامل با نرمالسالین انجام شد و پانسمان داخل حفره با گاز استریل صورت گرفت (شکل 8). تا زمان حضور بیمار در بیمارستان شستشو توسط پزشک انجام شد و نهایتا پس از آموزش شستشو به بیمار و اطمینان از آموزش وی بیمار مرخص گردید. در پیگیریهای انجام شده در فواصل دو هفته، یک ماه، سه ماه و شش ماه، بیمار بدون علائم عود، درد یا ترشح باقی ماند. تورم بهتدریج کاهش یافت و نمای مخاطی ناحیه به وضعیت نرمال نزدیک شد. گرافی پانورامیک پیگیری شش ماهه کاهش چشمگیر اندازه ضایعه و افزایش تراکم استخوان را نشان داد (شکل 9). با توجه به پاسخ مناسب ضایعه به مرحله اول درمان، برنامهریزی برای انجام انوکلیشن تأخیری به همراه برداشت محیطی (Peripheral Ostectomy) پس از شش ماه انجام شد. در مرحله دوم تحت بیهوشی عمومی، با ایجاد یک برش وستیبولار و نمایان شدن ناحیه ضایعه، پوشش ضایعه از دیوارههای استخوانی جدا گردید. بهمنظور برداشت استخوان مجاور پوشش کیستیک، از فرز جراحی استفاده شد. پس از انجام انوکلیشن، حفره با ژلفوم پر گردید و برشها با نخ بخیه ۴-۰ پرولن بسته شدند. هدف از این اقدام، حذف کامل اپیتلیوم باقیمانده و کاهش خطر عود ضایعه در بلندمدت خواهد بود.
.JPG)
شکل 2و1: نمای روبهرو از صورت بیمار پیش از جراحی، با تورم خفیف در ناحیه قدامی ماگزیلا (لب فوقانی سمت راست بیمار) و نمای تحتانی از صورت بیمار، نشاندهنده گسترش تورم به ناحیه پایه بینی و قدام ماگزیلا.
.JPG)
شکل3: نمای داخلدهانی بیمار قبل از انجام مارسوپیالیزاسیون. تورم مخاطی با رنگ قرمزتر نسبت به مخاط نرمال در ناحیه قدامی ماگزیلا قابل مشاهده است.

شکل 4: نمای پانورامیک قبل از انجام مارسوپیالیزاسیون که ضایعه رادیولوسنت تکحفرهای در ناحیه قدامی و خلفی ماگزیلا را نشان میدهد. محدوده ضایعه از مولردوم راست تا ناحیه مولردوم چپ امتداد دارد و نازکشدگی کورتکس قابل مشاهده است.

شکل 6و5 : تصاویر CBCT در محور کرونال و ساژیتال؛ تأیید نازکشدگی کورتکس بدون درگیری سینوس یا بینی.

شکل7: تصاویر پاتولوژیH&E

شکل8: نمای داخل دهانی حین جراحی مارسوپیالیزاسیون در ناحیه قدامی ماگزیلا. دو پنجره در دیواره ضایعه ایجاد شده و توسط بخیه به مخاط دهان متصل شدهاند. پانسمان داخل حفره پس از عمل انجام شده است.

شکل9: نمای پانورامیک شش ماه پس از مارسوپیالیزاسیون، نشاندهنده کاهش چشمگیر حجم ضایعه، افزایش تراکم استخوانی و عدم عود ضایعه در ناحیه قدامی ماگزیلا.
بحث
کیست ادونتوژنیک کراتوسیستیک (OKC) به دلیل ویژگیهای تهاجمی، شیوع نسبی بالا و رفتار بالینی غیرقابل پیشبینی، یکی از چالشبرانگیزترین ضایعات در حوزه جراحی فک و صورت بهشمار میرود (3). OKC ها تمایل به عود دارند و عوامل خطری مانند سن کمتر، چندحفرهای بودن، اندازه بزرگتر و طول قدامی ـ خلفی بیشتر، احتمال عود را بالا میبرد. بنابراین انتخاب رویکرد مرحلهای یا قطعی باید بر اساس این عوامل و موقعیت آناتومیک انجام شود (16). ساختار هیستوپاتولوژیک خاص آن، از جمله اپیتلیوم سنگفرشی مطبق با لایه بازال نردبانی و کراتین در لومن، احتمال باقیماندن بقایای بافتی پس از درمان و در نتیجه، عود ضایعه را افزایش میدهد (3،9). در این مطالعه، کیستی از نوع پاراکراتینیزه OKC در ناحیه نسبتاً نادر قدامی ماگزیلا گزارش شد که با رویکرد مرحلهای محافظهکارانه، شامل مارسوپیالیزاسیون اولیه و انوکلیشن تأخیری، مدیریت گردید. ناحیه قدامی ماگزیلا، اگرچه در مطالعات بینالمللی بهندرت بهعنوان محل اصلی OKC ذکر میشود، اما در مطالعه گذشتهنگر انجام شده در دانشگاه تهران، 42% از OKCهای فک بالا در این ناحیه قرار داشتند که نشان میدهد این محل در جمعیت ایرانی نیز حائز اهمیت است (6). در کنار بررسیهای کلینیکی، تصویربرداری و هیستوپاتولوژیک، ارزیابی احتمال سندرمی بودن کیستهای ادونتوژنیک کراتوسیستیک بهویژه در بیماران جوان، دارای ضایعات متعدد یا موارد عودشونده اهمیت دارد. یکی از مهمترین سندرمهای مرتبط باOKC، سندرم کارسینومای بازالسل نئووئید (Nevoid Basal Cell Carcinoma Syndrome – NBCCS) است که در آن جهش در ژن PTCH1 منجر به فعالشدن غیرطبیعی مسیر سیگنالینگ Hedgehog میشود. این مسیر در پاتوژنز ضایعات کراتوسیستیک نقش مؤثر دارد و زمینهساز تهاجم بیشتر و پتانسیل عود بالا خواهد بود (12). در برخی مطالعات، استفاده از درمانهای هدفمند مولکولی نظیر Vismodegib برای موارد مقاوم یا سندرمی پیشنهاد شده است، هرچند کاربرد بالینی آن هنوز در مرحله تحقیقاتی قرار دارد (15). یافتههای بیوانفورماتیکی جدید نیز نشان میدهد که ژنهای بالارونده در OKC بیشتر با سازماندهی ماتریکس خارج سلولی و فیبریلهای کلاژن ارتباط دارند، در حالیکه ژنهای پایینرونده با پاسخهای دفاعی ضد ویروسی و فعالسازی اینترفرون گاما مرتبط هستند. این الگو با تغییرات بافتی پس از دکامپرشن قابل جمع است و میتواند منطق رویکرد مرحلهای را تقویت کند (16). برآیند شواهد نشان میدهد که در ضایعات واقع در نواحی حساس مانند قدام ماگزیلا، بهکارگیری درمان مرحلهای با هدف کاهش حجم ضایعه و تسهیل برداشت قطعی، در کنار در نظر گرفتن عوامل خطر عود و امکان استفاده از آدجوانتها، میتواند انتخابی منطقی باشد. با این حال، ضرورت پیگیری بلندمدت و اجرای مطالعات آیندهنگر برای استانداردسازی پروتکلها پابرجاست (16،17). در مطالعه حاضر، با توجه به محل منفرد ضایعه، عدم وجود سابقه خانوادگی مشابه، و عدم وجود سایر علائم سندرمی (نظیر کیستهای پلانتار، کلسیفیکاسیون فالکس سربری، یا اختلالات اسکلتی)، بیمار جهت اطمینان به مشاوره ژنتیک ارجاع داده شد. پس از انجام بررسیهای تخصصی توسط متخصص ژنتیک، احتمال ارتباط ضایعه با NBCCS (Non Basal Cell Carcinoma) رد گردید. این اقدام از آن جهت اهمیت دارد که شناسایی فرمهای سندرمی OKC مستلزم برنامهریزی درمانی، پیگیریهای گستردهتر و غربالگری سایر اعضای خانواده خواهد بود (18). یکی از اصلیترین اهداف درمان، کاهش خطر عود با حفظ حداقل تهاجم است. درمان مرحلهای در سالهای اخیر توجه بسیاری را به خود جلب کرده است. در متاآنالیز انجامشده توسط Silva و همکاران، گرچه تفاوت آماری معناداری بین انوکلیشن تنها و انوکلیشن پس از مارسوپیالیزاسیون یافت نشد، اما نرخ عود در افرادیکه انوکلیشن پس از مارسوپیالیزاسیون انجام داده بودند بهطور نسبی کمتر بود، که نشان از پتانسیل مؤثر این روش دارد. این متاآنالیز همچنین بازه زمانی 12 تا 18 ماه را برای مرحله اول توصیه کرده است، کاهش حجم ضایعه و تسهیل برداشت نهایی را میتوان در این فاصله انتظار داشت. این مطالعه همچنین تأکید میکند که کاهش فشار داخل کیست با مارسوپیالیزاسیون میتواند منجر به تغییرات اپیتلیال و کاهش پتانسیل تهاجمی ضایعه شود (13). همسویی با این نتایج را میتوان در مطالعه Khalil و همکاران نیز مشاهده کرد، که در آن یک مورد OKC وسیع در ناحیه راموس مندیبل با استفاده از مارسوپیالیزاسیون اولیه و انوکلیشن همراه با برداشت محیطی (peripheral ostectomy) بدون عود و با بازسازی کامل استخوان طی پیگیری ۳۶ ماهه درمان شد (14،5). یافتههای مطالعه حاضر با نتایج این گزارش همراستا است؛ بهویژه از آن جهت که کاهش چشمگیر اندازه ضایعه و تراکم استخوانی پس از مرحله اول درمان مشاهده شد. تغییر دیدگاه نسبت به OKC طی دو دهه اخیر، از طبقهبندی آن بهعنوان تومور (KCOT) در سال ۲۰۰۵ تا بازگشت آن به گروه کیستهای تکاملی در طبقهبندیWHO 2017، در نتیجه مشاهده شواهد پاتولوژیک و بالینی مانند تغییرات ساختاری اپیتلیوم پس از دکامپرشن صورت گرفته است (19،10،3). این شواهد پایهای برای اثبات اثربخشی درمانهای محافظهکارانه مرحلهای بودهاند.
مارسوپیالیزاسیون در مطالعات اخیر نهتنها بهعنوان روشی کمتهاجم جهت کاهش حجم ضایعه و حفظ ساختارهای حیاتی (مانند سینوس ماگزیلاری و عصب آلوئولار تحتانی) مطرح شده، بلکه اثر آن در تحریک استئوژنز نیز مورد تأکید قرار گرفته است (1). این ویژگیها در مورد حاضر، که ضایعه به ناحیه پایه بینی و استخوانهای قدامی ماگزیلا گسترش یافته بود، اهمیت مضاعفی پیدا میکند. با این حال، باید تأکید کرد که مارسوپیالیزاسیون بهتنهایی درمان قطعی محسوب نمیشود، چرا که اپیتلیوم ادونتوژنیک ممکن است در دیواره کیست باقی بماند و زمینهساز عود در آینده شود. بنابراین، مرحله دوم درمان در قالب انوکلیشن همراه با برداشت محیطی انجام شد، تا تمامی بافتهای باقیمانده حذف شوند. در روش برداشت محیطی، حدود ۱.۵ تا ۲ میلیمتر از استخوان اطراف محل ضایعه با ابزار دوار برداشته میشود تا خطر عود به حداقل برسد. مطالعات متعدد از جمله بررسی Kolokythas و همکاران نیز نشان دادهاند که افزودن برداشت محیطی به انوکلیشن موجب کاهش معنادار نرخ عود OKC شده و حتی در برخی مطالعات، نرخ عود صفر گزارش شده است (20). در مطالعه نصرالهی و علیرضایی نیز گزارش شد که استفاده از دکامپرشن اولیه و انوکلیشن تأخیری در یک OKC پاراکراتینیزه در فک پایین، باعث تغییر در ساختار اپیتلیال، کاهش ضخامت جداره کیست و تسهیل در برداشت کامل آن گردید. همچنین، در پیگیری ۲۸ ماهه هیچ نشانهای از عود مشاهده نشد (15). از دیدگاه پاتولوژیک نیز، مطالعات نشان دادهاند که کاهش فشار داخل کیست، تغییراتی در الگوی کراتینیزاسیون و سلولهای بازال ایجاد میکند که میتواند باعث کاهش توان نفوذ و تکثیر سلولهای اپیتلیال شود (4). برخی نویسندگان معتقدند که مارسوپیالیزاسیون نهتنها از نظر مکانیکی باعث کاهش حجم ضایعه میشود، بلکه تأثیر بیولوژیک نیز در ساختار بافت دارد (22،21). در این مطالعه، پس از انجام مرحله اول درمان، بیمار بدون درد، ترشح یا شواهد بالینی عود باقی ماند و در گرافی پیگیری، بازسازی تدریجی استخوان مشاهده شد. پاسخ به درمان اولیه موفقیتآمیز بوده و روند پیشرفت درمان مرحلهای را تأیید میکند. با توجه به شواهد حاصل از مطالعات مشابه، میتوان امیدوار بود که تکمیل درمان با روشهای مکمل، احتمال عود را به حداقل خواهد رساند. در مجموع، رویکرد مرحلهای در مدیریت OKC بهویژه در نواحی آناتومیک حساس مانند قدام ماگزیلا میتواند گزینهای مناسب و کمعارضه باشد. با اینحال، تصمیمگیری درمانی باید مبتنی بر فاکتورهای بالینی، پاتولوژیک و میزان درگیری استخوان باشد و انجام پیگیریهای درازمدت و ثبت نتایج نهایی، برای اثبات اثربخشی این رویکرد ضروری است.
نتیجهگیری
در این مطالعه، مدیریت مرحلهای یک مورد نادر از OKC پاراکراتینیزه در ناحیه قدامی ماگزیلا با موفقیت پشت سر گذاشته است. کاهش چشمگیر اندازه ضایعه، عدم علائم عود و بازسازی استخوانی در گرافی پیگیری، اثربخشی اولیه درمان محافظهکارانه را نشان میدهد. با توجه به نزدیکی ضایعه به ساختارهای حیاتی، این رویکرد با حداقل تهاجم، جایگزین مناسبی برای رزکسیون وسیع محسوب میشود. با اینحال، پیگیری طولانیمدت برای ارزیابی قطعی موفقیت ضروری است.
سپاسگزاری
نویسندگان از بیمار و خانواده ایشان بهخاطر همکاری در تهیه این گزارش مورد کمال تشکر را دارند.
حامی مالی: ندارد
تعارض در منافع:وجود ندارد
ملاحظات اخلاقی
این گزارش مورد با رضایت آگاهانه از بیمار جهت قراردهی تصاویر و معرفی ایشان، همچنین کد اخلاق با شماره IR.SSU.SRH.REC.1404.006 از بیمارستان شهید رهنمون یزد دریافت شد.
مشارکت نویسندگان
دکتر حامد غیباللهی در ارائه ایده، دکتر حامد مرادی در طراحی مطالعه، دکتر حامد مرادی در جمعآوری دادهها، دکتر حامد غیباللهی در تجزیه و تحلیل دادهها مشارکت داشته و همه نویسندگان در تدوین، ویرایش اولیه و نهایی مقاله و پاسخگویی به سوالات مرتبط با مقاله سهیم هستند.
References:
1- Philipsen HP. OM Keratocyster (Kolesten-Tomer). Tandlaegebladet 1956; 60: 963-80.[Danish]
2- El-Naggar AK، Chan JKC، Grandis JR، Takata T، Slootweg PJ، ed. WHO Classification of Head and Neck Tumours. 4th ed. IARC; 2017.
3- Valdivia ADCM، Ramos-Ibarra ML، Franco-Barrera MJ، Arias-Ruiz LF، García-Cruz JM، Torres-Bugarín O. What Is Currently Known about Odontogenic Keratocysts? Oral Health & Preventive Dentistry 2022; 20: b3240829.
4- Ambele MA، Van Zyl A، Pepper MS، Van Heerden MB، Van Heerden WF. Amplification of 3q26. 2، 5q14. 3، 8q24. 3، 8q22. 3، and 14q32. 33 are Possible Common Genetic Alterations in Oral Cancer Patients. Front Oncol 2020; 10: 683.
5- Ambele MA، Robinson L، van Heerden MB، Pepper MS، van Heerden WF. Comparative Molecular Genetics of Odontogenic Keratocysts in Sporadic and Syndromic Patients. Mod Pathol 2023; 36(1): 100002.
6- Nakamura N، Mitsuyasu T، Mitsuyasu Y، Taketomi T، Higuchi Y، Ohishi M. Marsupialization for Odontogenic Keratocysts: Long-Term Follow-Up Analysis of the Effects and Changes in Growth Characteristics. Oral Surgery، Oral Medicine، Oral Pathology، Oral Radiology، and Endodontology 2002; 94(5): 543-53.
7- de Vicente JC، Torre-Iturraspe A، Gutiérrez AM، Lequerica-Fernández P. Immunohistochemical Comparative Study of the Odontogenic Keratocysts and Other Odontogenic Lesions. Med Oral Patol Oral Cir Bucal 2010; 15(5): e709-15.
8- Elah-e-Ain N، Nooshin J، Eshghyar N، Jalayer Naderi N، Sarraf P. Odontogenic Keratocyst: A 31- Year Retrospective Study in The Oral and Maxillofacial Pathology Department، Faculty of Dentistry، Tehran University of Medical Sciences. J Dent Med-tums 2005; 18 (1): 56-60. [Persian]
9- Pogrel MA. Decompression and Marsupialization as a Treatment for the Odontogenic Keratocyst. Oral Maxillofac Surg Clin North Am 2003; 15(3): 415-27.
10- Brøndum N، Jensen VJ. Recurrence of Keratocysts and Decompression Treatment: A Long-Term Follow-Up of Forty-Four Cases. Oral surgery، oral medicine، oral pathology 1991; 72(3): 265-9.
11- Ramírez-Martínez CM، Legorreta-Villegas I، Mejía-Velázquez CP، Portilla-Robertson J، Gaitán-Cepeda LA، Paramo-Sánchez JT، et al. In Silico Analysis of Genes Associated with the Pathogenesis of Odontogenic Keratocyst. Int J Mol Sci 2024; 25(4): 2379.
12- Mascitti M، Togni L، Balercia A، Balercia P، Rubini C، Santarelli A. P53-Family Proteins in Odontogenic Cysts: An Immunohistochemical Study. Appl Immunohistochem Mol Morphol 2020; 28(5): 369-75.
13- Slusarenko da Silva Y، Stoelinga PJ، Naclério-Homem MD. Recurrence of Nonsyndromic Odontogenic Keratocyst after Marsupialization and Delayed Enucleation Vs. Enucleation Alone: A Systematic Review and Meta-Analysis. Oral and Maxillofacial Surgery 2019; 23(1): 1-1.
14- Khalil A، Albash Z، Sleman N، Sayegh W. Marsupialization and Peripheral Ostectomy for the Management of Large Odontogenic Keratocyst: A Case Report. J Surgical Case Rep 2023; 2023(3): Rjad119.
15- Mohammadi N، Nasrollahi M. Conservative Management of a Large Keratocystic Odontogenic Tumor. Journal of Research in Dental Sciences 2016; 13(1): 54-8.
16- Dioguardi M، Quarta C، Sovereto D، Caloro GA، Ballini A، Aiuto R، et al. Factors and Management Techniques in Odontogenic Keratocysts: A Systematic Review. European Journal of Medical Research 2024; 29(1): 287.
17- Moellmann HL، Parviz A، Goldmann-Kirn M، Rana M، Rana M. Comparison of Five Different Treatment Approaches of Mandibular Keratocystic Odontogenic Keratocyst (OKC): A Retrospective Recurrence Analysis of Clinical and Radiographic Parameters. J Maxillofacial Oral Surgery 2024; 23(1): 145-51.
18- Evans DG، Ladusans EJ، Rimmer S، Burnell LD، Thakker N، Farndon PA. Complications of the Naevoid Basal Cell Carcinoma Syndrome: Results of a Population-Based Study. J Medical Genetics 1993; 30(6): 460-4.
19- Tang JY، Mackay-Wiggan JM، Aszterbaum M، Yauch RL، Lindgren J، Chang K، et al. Inhibiting the Hedgehog Pathway in Patients with the Basal-Cell Nevus Syndrome. N Engl J Med 2012; 366(23): 2180-8.
20- Kimonis VE، Goldstein AM، Pastakia B، Yang ML، Kase R، DiGiovanna JJ، et al. Clinical Manifestations in 105 Persons with Nevoid Basal Cell Carcinoma Syndrome. American J Med Genetics 1997; 69(3): 299-308.
21- Maurette PE، Jorge J، de Moraes M. Conservative Treatment Protocol of Odontogenic Keratocyst: A Preliminary Study. J Oral Maxillofac Surg 2006; 64(3): 379-83.
1- Philipsen HP. OM Keratocyster (Kolesten-Tomer). Tandlaegebladet 1956; 60: 963-80.[Danish]
2- El-Naggar AK، Chan JKC، Grandis JR، Takata T، Slootweg PJ، ed. WHO Classification of Head and Neck Tumours. 4th ed. IARC; 2017.
3- Valdivia ADCM، Ramos-Ibarra ML، Franco-Barrera MJ، Arias-Ruiz LF، García-Cruz JM، Torres-Bugarín O. What Is Currently Known about Odontogenic Keratocysts? Oral Health & Preventive Dentistry 2022; 20: b3240829.
4- Ambele MA، Van Zyl A، Pepper MS، Van Heerden MB، Van Heerden WF. Amplification of 3q26. 2، 5q14. 3، 8q24. 3، 8q22. 3، and 14q32. 33 are Possible Common Genetic Alterations in Oral Cancer Patients. Front Oncol 2020; 10: 683.
5- Ambele MA، Robinson L، van Heerden MB، Pepper MS، van Heerden WF. Comparative Molecular Genetics of Odontogenic Keratocysts in Sporadic and Syndromic Patients. Mod Pathol 2023; 36(1): 100002.
6- Nakamura N، Mitsuyasu T، Mitsuyasu Y، Taketomi T، Higuchi Y، Ohishi M. Marsupialization for Odontogenic Keratocysts: Long-Term Follow-Up Analysis of the Effects and Changes in Growth Characteristics. Oral Surgery، Oral Medicine، Oral Pathology، Oral Radiology، and Endodontology 2002; 94(5): 543-53.
7- de Vicente JC، Torre-Iturraspe A، Gutiérrez AM، Lequerica-Fernández P. Immunohistochemical Comparative Study of the Odontogenic Keratocysts and Other Odontogenic Lesions. Med Oral Patol Oral Cir Bucal 2010; 15(5): e709-15.
8- Elah-e-Ain N، Nooshin J، Eshghyar N، Jalayer Naderi N، Sarraf P. Odontogenic Keratocyst: A 31- Year Retrospective Study in The Oral and Maxillofacial Pathology Department، Faculty of Dentistry، Tehran University of Medical Sciences. J Dent Med-tums 2005; 18 (1): 56-60. [Persian]
9- Pogrel MA. Decompression and Marsupialization as a Treatment for the Odontogenic Keratocyst. Oral Maxillofac Surg Clin North Am 2003; 15(3): 415-27.
10- Brøndum N، Jensen VJ. Recurrence of Keratocysts and Decompression Treatment: A Long-Term Follow-Up of Forty-Four Cases. Oral surgery، oral medicine، oral pathology 1991; 72(3): 265-9.
11- Ramírez-Martínez CM، Legorreta-Villegas I، Mejía-Velázquez CP، Portilla-Robertson J، Gaitán-Cepeda LA، Paramo-Sánchez JT، et al. In Silico Analysis of Genes Associated with the Pathogenesis of Odontogenic Keratocyst. Int J Mol Sci 2024; 25(4): 2379.
12- Mascitti M، Togni L، Balercia A، Balercia P، Rubini C، Santarelli A. P53-Family Proteins in Odontogenic Cysts: An Immunohistochemical Study. Appl Immunohistochem Mol Morphol 2020; 28(5): 369-75.
13- Slusarenko da Silva Y، Stoelinga PJ، Naclério-Homem MD. Recurrence of Nonsyndromic Odontogenic Keratocyst after Marsupialization and Delayed Enucleation Vs. Enucleation Alone: A Systematic Review and Meta-Analysis. Oral and Maxillofacial Surgery 2019; 23(1): 1-1.
14- Khalil A، Albash Z، Sleman N، Sayegh W. Marsupialization and Peripheral Ostectomy for the Management of Large Odontogenic Keratocyst: A Case Report. J Surgical Case Rep 2023; 2023(3): Rjad119.
15- Mohammadi N، Nasrollahi M. Conservative Management of a Large Keratocystic Odontogenic Tumor. Journal of Research in Dental Sciences 2016; 13(1): 54-8.
16- Dioguardi M، Quarta C، Sovereto D، Caloro GA، Ballini A، Aiuto R، et al. Factors and Management Techniques in Odontogenic Keratocysts: A Systematic Review. European Journal of Medical Research 2024; 29(1): 287.
17- Moellmann HL، Parviz A، Goldmann-Kirn M، Rana M، Rana M. Comparison of Five Different Treatment Approaches of Mandibular Keratocystic Odontogenic Keratocyst (OKC): A Retrospective Recurrence Analysis of Clinical and Radiographic Parameters. J Maxillofacial Oral Surgery 2024; 23(1): 145-51.
18- Evans DG، Ladusans EJ، Rimmer S، Burnell LD، Thakker N، Farndon PA. Complications of the Naevoid Basal Cell Carcinoma Syndrome: Results of a Population-Based Study. J Medical Genetics 1993; 30(6): 460-4.
19- Tang JY، Mackay-Wiggan JM، Aszterbaum M، Yauch RL، Lindgren J، Chang K، et al. Inhibiting the Hedgehog Pathway in Patients with the Basal-Cell Nevus Syndrome. N Engl J Med 2012; 366(23): 2180-8.
20- Kimonis VE، Goldstein AM، Pastakia B، Yang ML، Kase R، DiGiovanna JJ، et al. Clinical Manifestations in 105 Persons with Nevoid Basal Cell Carcinoma Syndrome. American J Med Genetics 1997; 69(3): 299-308.
21- Maurette PE، Jorge J، de Moraes M. Conservative Treatment Protocol of Odontogenic Keratocyst: A Preliminary Study. J Oral Maxillofac Surg 2006; 64(3): 379-83.
22- Kolokythas A، Fernandes RP، Pazoki A، Ord RA. Odontogenic Keratocyst: To Decompress or Not to Decompress? A Comparative Study of Decompression and Enucleation Versus Resection/Peripheral Ostectomy. J Oral Maxillofac Surg 2007; 65(4): 640-4.
نوع مطالعه: گزارش مورد |
موضوع مقاله:
دندانپزشکی
دریافت: 1404/6/4 | پذیرش: 1404/6/24 | انتشار: 1404/8/15
دریافت: 1404/6/4 | پذیرش: 1404/6/24 | انتشار: 1404/8/15
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |







