دوره 33، شماره 4 - ( تیر 1404 )
جلد 33 شماره 4 صفحات 8984-8974 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Mohammadi F, Rouhi L. Evaluation of Spirulina Platensis Extract Effect on the Expression Level of Apoptosis-Related Gene (Drp1) and Regulation Programmed Cell Death in Human Gastric Adenocarcinoma Cell Line (AGS). JSSU 2025; 33 (4) :8974-8984
URL: http://jssu.ssu.ac.ir/article-1-6384-fa.html
URL: http://jssu.ssu.ac.ir/article-1-6384-fa.html
محمدی فرخنده، روحی لیلا. بررسی اثر عصاره اسپیرولینا پلاتنسیس بر میزان بیان ژن آپوپتوزی Drp1 و تنظیم مرگ سلولی برنامهریزی شده در رده سلولی آدنوکارسینومای معده انسان (AGS). مجله علمي پژوهشي دانشگاه علوم پزشكي شهید صدوقی يزد. 1404; 33 (4) :8974-8984
متن کامل [PDF 638 kb]
(303 دریافت)
| چکیده (HTML) (770 مشاهده)
متن کامل: (321 مشاهده)
مقدمه
سرطان در کشورهای توسعه یافته و در حال توسعه به ترتیب اولین و دومین عامل مرگ میباشد. سرطان معده در جهان به عنوان پنجمین سرطان شایع و چهارمین عامل مرگ بر اثر سرطان شناخته میشود (1). این سرطان از دسته سرطانهایی است که به آرامی و طی سالیان رشد میکند، اما قبل از آنکه به معنای واقعی بروز نماید، تغییراتی در لایههای معده ظاهر میگردد، ولی متاسفانه علائم چندانی را در این مرحله بهدنبال نداشته و به همین دلیل این نوع بدخیمی به سختی در مراحل ابتدایی تشخیص داده میشود. این در حالی است که اگر بدخیمیهای معده در مراحل اولیه کشف و درمان شوند، روند بهبود برای مبتلایان فراهم میگردد (3,2). بروز تدریجی چندین جهش در ژنهای کنترل کننده مسیرهای حیاتی سلول از جمله رشد، نمو و مرگ برنامهریزی شده سلولی باعث تولید تودههای توموری در بافت معده میشود، که از قوانین تکاملی حاکم بر ماهیت پر سلولی یک موجود زنده پیروی نکرده و با کسب ویژگیهایی از جمله عدم توجه به فاکتورهای رشد داخلی و خارجی، توانایی تکثیر خود به خودی، فرار از آپوپتوز و متاستاز سرطان معده را ایجاد میکنند (4,5). در طی سالهای اخیر، دانش و درک ما از فرآیندهای مولکولی که موجب بروز و پیشرفت سرطان میشوند، به میزان قابلتوجهی افزایش یافته است. این امر منجر به توسعه درمانهای هدفمند شده است که این فرآیندهای مولکولی را مختل مینمایند. از جمله این دستاوردهای علمی برای درمان سرطان معده میتوان به جراحی، پرتودرمانی، شیمیدرمانی، ایمنیدرمانی و استفاده از داروها اشاره کرد. اما با توجه به عوارض جانبی داروهای شیمیایی و همچنین اثرات منفی بر سایر بافتها و سلولهای بدن، امروزه استفاده از ترکیبات طبیعی بهعنوان دارو به دنبال دارا بودن اثرات جانبی کمتر در مقایسه با ترکیبات شمیایی، بیشتر مورد توجه قرار گرفته است (6,7). در این میان آبزیان دریائی بهواسطه فراوانی و تنوع بسیار بالای آنها همواره قابلتوجه قرار گرفتهاند. یکی از مهم-ترین این آبزیان که از سوی محققان علوم تغذیه به آن اشاره شده است و کشفیات زیادی در خصوص خواص تغذیهای و دارویی آن موجود میباشد، جلبک سبز- آبی اسپیرولینا پلاتنسیس است. اسپیرولینا یکی از نوید بخشترین ریزجلبکها میباشد که از سوی سازمان بهداشت جهانی بهعنوان بهترین راه حل درمانی برای فردا و پرسشنامه به عنوان غذای برتر اعلام گردیده است. فواید و برتری این ریزجلبک نسبت به سایر منابع غذایی گیاهی و دیگر جلبکها بسیار زیاد و قابلتوجه میباشد. اسپیرولینا پلاتنسیس به صورت بالقوه منبع بزرگی از ترکیباتی بوده که می¬توانند جهت تولید مواد اولیه فرآوردههای غذایی استفاده شوند. کاربرد اسپیرولینا پلاتنسیس و متابولیتهای آن روند جالبی در بهبود ارزش فراوردههای غذایی سالم ایجاد کرده است. اسپیرولینا غنیترین افزودنی به لحاظ پروتئینی، اسیدهای چرب ضروری نظیر گامالینولنیک، ویتامینها خصوصا ویتامین B12 و پیش ساز ویتامین A، مواد معدنی بخصوص آهن و کلسیم و رنگدانههایی از جمله فایکوسیانین و سولفولیپیدها میباشد. نداشتن دیواره سلولی سلولزی باعث جذب راحتتر مواد مغذی آن شده است. کم بودن میزان اسید نوکلئیک (کمتر از 4%) اسپیرولینا، یکی دیگر از برتریهای این ریز جلبک نسبت به سایر منابع پروتئینی مشابه میباشد. اسپیرولینا به دلیل داشتن اجزا و ترکیبات آنتیاکسیدانی مانند فایکوسیانین، سلنیوم، کارتنوئیدها اسیدچرب گامالینولنیک عامل دارویی بالقوه¬ای جهت بیماریهای القاء شده به وسیله تنش اکسیداسیونی نظیر سرطان میباشد (12-8). از اینرو در مطالعه حاضر اثر عصاره اسپیرولینا پلاتنسیس بر میزان بیان ژن آپوپتوزی Drp1 و تنظیم مرگ سلولی برنامهریزی شده در رده سلولی آدنوکارسینومای معده انسان (AGS) مورد بررسی قرار گرفت. Drp1 به عنوان یک GTPase در آپوپتوز میتوکندریایی نقش دارد (شکافت میتوکندری). به عبارت دیگر Drp1 بهطور مستقل یا پاییندست BH3-mimetics برای تسهیل آزاد سازی سیتوکروم c و آپوپتوز عمل کند (13).
روش بررسی
این مطالعه بهصورت تجربی از فروردین 1403 تا شهریور 1403 در مراکز تحقیقاتی سلولی- تکوینی، بیوتکنولوژی و گیاهان دارویی مجتمع آزمایشگاهی دانشگاه آزاد اسلامی واحد شهرکرد بهصورت تجربی با مجوز اخلاق در پژوهش به کد IR.IAU.SHK.REC.1403.247 انجام شد. رده سلولی AGS از مرکز ملی ذخایر ژنتیکی و زیستی ایران خریداری شد. در محیط کشت DMEM-F12 (Dulbecco's Modified Eagle's medium) (Gibco, USA) حاوی 10 درصد FBS (Foetal Bovine Serum) (Gibco, USA) و یک درصد Penstrep (Penicillin-Streptomycin) (Gibco, USA) در انکوباتور (Memmert, Germany) با فشار 5 درصد گاز CO2، رطوبت 90 درصد و دمای 37 درجه سانتیگراد، در فلاسک 75 کشت داده شد. محیط کشت هفتهای سه بار تعویض و برای برداشت کردن سلولها از محلول تریپسین/EDTA استفاده شد. اسپیرولینا پلاتنسیس به صورت آماده و به حالت جامد از شرکت دانشپژوهان قشم با نام تجاری اسپیرولینا (سوپر فود) تهیه گردید. برای تهیه عصاره از این ماده در مرکز تحقیقات گیاهان دارویی دانشگاه آزاد اسلامی واحد شهرکرد، پودر اسـپیرولینا درون فـالکون ریختــه شـد و حلال اتانولی به آن اضافه و اقدام به عصارهگیری شد. عمل عصارهگیری سه بار تکرار گردید و تا زمان استفاده در دمای 4 درجه سانتیگراد نگهداری شد.
سنجش وقوع آپوپتوز: القاء آپوپتوز در رده سلولی AGS، از طریق تست Annexin V-FITC/PI، با استفاده از کیت FITC Annexin V Apoptosis Detection kit (BD Pharmingen, USA)، با شماره محصول (556547)، مورد ارزیابی قرار گرفت. به این ترتیب که، تعداد 5×105 سلول در پلیتهای کشت 6 خانه کشت داده شد، و سپس، با غلظتهای 10 (گروه I)، 20 (گروه II) و 40 (گروه III) میکروگرم/ میلیلیتر عصاره اسپیرولینا پلاتنسیس در بازههای زمانی 24 و 48 ساعت تحت تیمار قرار گرفت. پس از اتمام زمان انکوباسیون، محیط رویی تیمار جمع آوری شد. پس از ترپسینه کردن، رسوب سلولی دو بار با محلول PBS (Phosphate-buffered saline)، (SIGMA-ALDRICH, USA)، سرد شستشو گردید. سپس مقدار 300 میکرولیتر بافر به سلولها اضافه شد و سوسپانس سلول و بافر به لولههای مخصوص فلوسیتومتری انتقال یافت. با اضافه کردن 5 میکرولیتر Annexin و PIبه لولهها و به حجم رساندن آنها با بافر به میزان 200 میکرولیتر برای سایر لولهها و 500 میکرولیتر برای لولههای کنترل، لولهها به محیط تاریک و در دمای اتاق ظرف مدت زمان 20 دقیقه انتقال داده شدند (14). پس از گذشت مدت زمان معلوم از دستگاه فلوسیتومتری(BD Facscalibur, USA) جهت خوانش نتایج استفاده گردید.
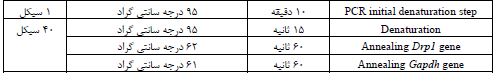
سنجش بیان ژن: به منظور بررسی میزان بیان ژن Drp1، تعداد 105×3 سلول در پلیتهای 6 خانه کشت داده شد، و سپس، با غلظت 40 میکروگرم/ میلیلیتر عصاره اسپیرولینا پلاتنسیس در بازه زمانی 48 ساعت تیمار و انکوبه شدند. پس از گذشت زمان انکوباسیون، سلولها در دو گروه تست شامل غلظت 40 میکروگرم/ میلیلیتر از عصاره اسپیرولینا پلاتنسیس و گروه کنترل، برداشت و پس از شستشو با بافر PBS، Total RNA سلولی با استفاده از معرف RNXTM –PLUS (RNX-Plus Solution for total RNA isolation)، جدا گردید. به منظور انجام مرحله Heat block، نمونههای حاصل از مرحله قبل در دستگاه ترموسایکلر با دمای 60 درجه سانتی گراد به مدت 20 دقیقه قرار داده شدند. در ادامه تمام توالی-های RNA با استفاده از کیت سنتز cDNA (PrimeScriptTM RT Reagent kit (Perfect Real Time))، (Takara)، به cDNA تبدیل و به فریزر 20- درجه سانتیگراد منتقل شدند. سنجش میزان بیان ژن Drp1 با استفاده از دستگاه Real Time PCR مدل (Rotor gene 3000 corbett, Australia) مورد ارزیابی قرار گرفت. برای انجام واکنش، مخلوط واکنشی متشکل از cDNA، به مقدار 1 میکرولیتر، پرایمر رفت و برگشت هرکدام به مقدار 0/5 میکرولیتر، RNase-free water، به مقدار 5/5 میکرولیتر و 12/5 میکرولیتر مسترمیکس (Master Mix RT-PCR) (Ampliqon) تهیه گردید (15). توالی پرایمرهای پیشرو (Forward) و پسرو (Reverse) ژنهای GAPDH و Drp1 با استفاده از نرم افزار Oligo6 طراحی و سپس با Blast نمودن آنها در NBCI از صحیح بودن آنها اطمینان حاصل شد و نهایتا توسط شرکت Macrogen سنتز شدند (جدول 1). از ژن GAPDH، به عنوان کنترل داخلی استفاده شد. سپس مخلوط واکنش پس از آماده سازی با حجم نهایی 20 میکرولیتر تحت تاثیر برنامه¬ی دمایی ذکر شده در جدول 2 قرار گرفت.
تجزیه و تحلیل آماری
بررسی آماری با استفاده از آزمون t از طریق نرمافزارهای SPSS و GraphPad Prism انجام شد. حدود اطمینان برای همه آزمایشات 95% در نظر گرفته شد و 5% < P معنی دار محسوب گردید.
.
جدول1: مشخصات پرایمر مربوط به ژنهای Drp1 و Gapdh

جدول2: شرایط دمایی واکنش Rael Time PCR
نتایج
سلولهای ردهی AGS در غلظت 40 میکروگرم/ میلیلیتر از عصارهی جلبک اسپیرولینا پلاتنسیس برای مدت زمان 48 ساعت کشت داده شدند. تصویر زیر (شکل 1) انکوباسیون سلولهای تحت تیمار با غلظت 40 میکروگرم/ میلیلیتر از عصارهی جلبک اسپیرولینا پلاتنسیس را برای مدت زمان 48 ساعت نشان میدهد که مشاهدات میکروسکوپی حاکی از کاهش تعداد سلولها در گروههای تحت تیمار میباشد. به منظور بررسی میزان القاء آپوپتوز از تست Annexin V-FITS استفاده شد. سلولها برای مدت زمان 48 ساعت تحت تیمار با غلظت 40 میکروگرم/ میلیلیتر از عصاره جلبک اسپیرولینا پلاتنسیس قرار گرفتند (بهعنوان غلظت و زمان تیماری که بقای سلولی را 50 درصد کاهش میدهد). نتایج نشان میدهد که میزان القاء آپوپتوز درگروه تحت تیمار افزایش مییابد. آنالیز آماری نشان داد که درصد مرگ سلولی در رده سلولی AGS افزایش یافته است. همانطور که در نمودار 1 دیده میشود، درصد سلولهای زنده در گروه کنترل 98/44 درصد است که بیشتر از گروه آزمایشی میباشد. درصد سلولهای زنده در گروه آزمایشی نسبت به گروه کنترل کاهش را نشان میدهد که این اختلاف از نظر آماری نسبت به گروه کنترل معنیدار است (P≤0.05). در تیمار 48 ساعته، درصد سلولهایی که در مراحل اولیه آپوپتوز هستند از 2 درصد در گروه کنترل به 4./39 درصد در غلظت 40 میکروگرم/ میلیلیتر رسیده است که این افزایش درصد آپوپتوز نسبت به گروه کنترل اختلاف معنیداری دارد (P<0.001). بهعلاوه درصد سلولهایی که در مراحل انتهایی آپوپتوز هستند افزایش را نشان دادهاند، به گونهای که از 9/ 0درصد در گروه کنترل به 46/01 درصد در غلظت 40 میکروگرم/ میلیلیتر رسیده است که این افزایش درصد آپوپتوز نسبت به گروه کنترل معنیدار است (P<0.0001) (شکل 2) ( نمودار 1). تیمار سلولهای رده AGS با عصاره¬ جلبک اسپیرولینا پلاتنسیس و انکوباسیون آنها برای مدت 48 ساعت افزایش معنیداری را در میزان بیان ژن Drp1 نشان داد. نمودارهای زیر این افزایش بیان را در ژنهای Drp1 براساس CtΔΔ نمایش میدهد.
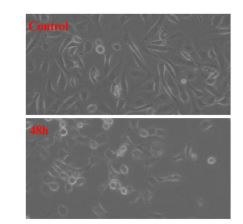
شکل1: تاثیر غلظت 40 میکروگرم/ میلیلیتر از عصاره جلبک اسپیرولینا پلاتنسیس بر رده سلولی AGS برای مدت زمان 48 ساعت; تصویر بالا: سلولهای رده AGS در معرض محیط کشت DMEM+ FBS10% (گروه کنترل)، تصویر پایین: سلولهای رده AGS در غلظت 40 میکروگرم/ میلیلیتر از عصاره جلبک اسپیرولینا پلاتنسیس برای مدت زمان 48 ساعت
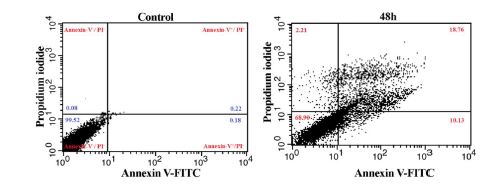
شکل2: تاثیر عصاره جلبک اسپیرولینا پلاتنسیس بر القاء آپوپتوز در رده سلولی AGS.; تصویر چپ: گروه کنترل ، تصویر راست: وقوع آپوپتوز اولیه و انتهایی سلولهای رده AGS تحت تیمار غلظت 40 میکروگرم/ میلیلیتر از عصارهی جلبک اسپیرولینا پلاتنسیس برای مدت زمان 48 ساعت
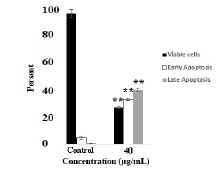
نمودار 1: درصد سلولهای زنده، آپوپتوز اولیه و آپوپتوز انتهایی در سلول¬های AGS تحت تیمار با غلظت 40 میکروگرم/ میلیلیتر به مدت 48 ساعت.P<0.0001** در مقابل گروه کنترل
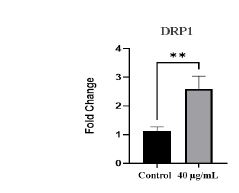
نمودار2: نمودار میزان بیان ژن Drp1 براساس Ct در غلظت 40 میکروگرم/ میلیلیتر و زمان انکوباسیون 48 ساعت.
P<0.001** اختلاف معنیدار در مقابل گروه کنترل
بحث
یکی از معضلات امروزی در جوامع بشری سرطان معده میباشد که به عنوان یک بیماری چند عاملی در نتیجهی تداوم آسیبهای ناشی از مواجهه مداوم با عوامل سرطانزا ایجاد میشود. علی رقم کاهش قابلملاحظه در بروز این نوع بدخیمی در طول دهههای گذشته، در اکثر کشورهای صنعتی هنوز این بیماری دومین علت شایع مرگ و میر افراد در اثر سرطان میباشد که سالیانه باعث مرگ حدود یک میلیون نفر در سرتاسر جهان میشود (16,17). مبتلایان به آدنوکارسینومای معده دارای بقاء 5 ساله هستند و در بیش از 90% موارد درمان تومور معدی با جراحی، تنها شانس درمانی میباشد. اما به دلیل اینکه در حال حاضر تشخیص زود هنگام سرطان معده امکانپذیر نیست و معمولا تشخیص زمانی صورت میگیرد که سرطان بهطور موضعی پیشرفت کرده است و به درون دیواره معده نفوذ نموده، این شانس به کمتر از 30% کاهش مییابد (18). لذا با توجه به افزایش روز افزون تعداد مبتلایان که شمار زیادی از آنها پس از گذراندن مراحل دشوار عملهای جراحی باز هم دچار عود بیماری میشوند و از آنجاییکه مقاومت به مرگ سلولی و عدم وجود تعادل بین تقسیم سلولی و مرگ سلولی منجر به عدم کنترل تکثیر سلولهای توموری میشود، امروزه نیاز به ترکیبات درمانی که قادر به مهار تکثیر سلولهای توموری باشند، به شدت احساس میشود (19). تحقیقات گذشته نشان داده است که سیانوباکترها میتوانند مواد زیست فعّال داخل و خارج سلولی با فعالیتهای ضد باکتری تولید کنند. فعالیت ضد میکروبی اسپیرولینا پلاتنسیس میتواند ناشی از گاما-لینولنیک اسید، اسیدهای چرب فعّال، اثرات سینرژیستی لائوریک اسید و پالمیتولئیک اسید، فایکوسیانین، فایکوسیانوبیلین و الوفایکوسیانین، آمیدها، آلکالوئیدها، هپتادکان، تترادکان، تترامین، اسپرمین و پیپرازین باشد. کلسیم-اسپیرولن یک پلیساکارید سولفاته در اسپیرولینا پلاتنسیس است که شامل رامنوز، ریبوز، مانوز، فروکتوز، گالاکتوز، زایلوز، گلوکز، گلوکورونیک اسید، گالاکتورونیک اسید و سولفات کلسیم است. اسپیرولینا پلاتنسیس منبعی از ترکیبات فنولیک نظیر کافئیک، کلروژنیک، سالیسیلیک، سیناپتیک و ترانس سینامیک اسید است. ترکیبات فنولیک مواد ضد میکروب و آنتیاکسیدان طبیعی هستند که حلقههای بنزنیک آنها توسط یک یا تعداد بیشتر گروه هیدروکسیل جایگزین شده است. عصاره اسپیرولینا دارای فعالیت ضد میکروبی علیه باکتریهای گرم منفی نظیر هلیکوباکتر پیلوری عامل سرطان معده است. مطالعات طی 40 سال گذشته نشان داده است که بیش از 15000 ترکیب جدید از جلبکها استخراج شده است که بسیاری از آنها کارکرد زیست فعال دارند. همچنین، به دلیل اینکه اسپیرولینا پلاتنسیس حاوی زی- سلنیوم، منگنز، ویتامین E و C، گزانتین، بتا-کریپتوگزانتین، گزانتوفیل، میکسوگزانتوفیل، بتا-کاروتن، کلروفیل، ویتامین فایکواریترین و فایکوسیانین است خاصیت آنتیاکسیدانی خوبی دارد. این ترکیبات رادیکالهای آزاد مضر را که در بروز بسیاری از سرطانها نقش دارند جاروب میکنند. اسپیرولینا پرسشنامه منبع ترکیبات فنولی همچون اسید کافئیک، کلروجنیک، سالیسیلیک، سیناپتیک و ترانس- سینامیک است. ترکیبات فنولی آنتیاکسیدان¬های طبیعی هستند که حلقههای بنزونیک با یک یا چند گروه هیدروکسیل جایگزین شده است. اسپیرولینا میتواند تولید آنزیمهای گوناگون آنتیاکسیدانی را تحریک نماید، از جمله آنزیم سوپراکسیددسموتاز که یک آنزیم مهم در از بین بردن رادیکالهای آزاد است. این آنزیم پرسشنامه برای درمان انواع بیماریهای مرتبط با تنش اکسیداتیو و یا به عنوان جزئی از لوسیونهای ضد چروک پوست و ماسکهای صورت با افزایش سن فرد مورد استفاده قرار میگیرد. اسپیرولینا پلاتنسیس همچنین باعث افزایش فعالیت آنزیمهایی از قبیل پراکسی ردوکسین و آسکوربات پراکسیداز میشود. مکانیسمهای آنتیاکسیدانی اسپیرولینا پلاتنسیس شامل افزایش فعالیت آنتیاکسیدانهای آنزیمی شامل سوپراکسید دسموتاز، گلوتاتیون پراکسیداز و کاتالاز و پرسشنامه آنتیاکسیدانهای غیر آنزیمی شامل بتاکاروتن، گلوتاتیون و ویتامین E است (20). بهعلاوه، در تحقیق حاضر نیز توانایی عصاره جلبک سبز- آبی اسپیرولینا پلاتنسیس در مهار رشد و خاصیت ضد تکثیری آن که از طریق القاء مرگ برنامهریزی شدهی سلولی اعمال میگردد، در سلولهای رده آدنوکارسینومای معده انسان (AGS)، مورد بررسی قرار گرفت. در این تحقیق تیمار رده سلولی AGS با غلظتی از عصاره جلبک اسپیرولینا پلاتنسیس (40 میلیگرم/ میلیلیتر) و انکوباسیون سلولها برای مدت زمان 48 ساعت نتایج قابلتوجهی را در میزان وقوع آپوپتوز در رده سلولی AGS نشان داد. وقوع آپوپتوز با استفاده از تست Annexin V-FITC بررسی گردید و آنالیز آماری صورت گرفت. نتایج حاصل نشان داد که درصد سلولهایی که در مرحله انتهایی آپوپتوز هستند، در زمان انکوباسیون 48 ساعت در غلظت 40 میلیگرم/ میلیلیتر به بیشترین مقدار نسبت به گروه کنترل رسیده است. به علاوه در این تحقیق توانایی عصاره جلبک اسپیرولینا پلاتنسیس در تغییر بیان ژن رمزکننده پروتئین پروآپوپتوزی Drp1 دخیل در مسیر مرگ سلولی در سلولهای رده AGS سرطان معده، مورد بررسی قرار گرفت. Drp1 با کنترل نفوذپذیری غشای خارجی میتوکندری در آپوپتوز وابسته به Bax/Bak یا Bnip3 نقش دارد. Drp1 در حین مرگ سلولی در اثر آپوپتوز با Bax در مکانهای شکافت میتوکندری متصل میشود و در پایین دست جابجایی Bax اما در بالادست آزاد سازی سیتوکروم c عمل میکند (13). در این پژوهش تیمار سلولهای AGS سرطان معده، با دوز 40 میلیگرم/ میلیلیتر عصاره جلبک اسپیرولینا پلاتنسیس و انکوباسیون آن برای مدت 48 ساعت، افزایش معنیدار میزان بیان ژن Drp1 (P<0.001) را نشان داد. لذا به طور کلی میتوان از دادهی حاصل شده از دو تست نتیجه گرفت که احتمالا عصاره جلبک سبز- آبی اسپیرولینا پلاتنسیس دارای بیشترین قدرت مهاری بر رشد و تکثیر رده سلولهای آدنوکارسینومای معده انسان (AGS)، در غلظت 40 میلی¬گرم/ میلی¬لیتر و زمان انکوباسیون 48 ساعته میباشد. به علاوه تحقیقات ارائه شده در زیر شواهد محکمی بر اثبات صداقت نتایج حاصل شده از تحقیق حاضر میباشند: پینرو و همکارانش، در پی ارزیابی ساز و کار عملکردی پروتئین فیکوسیانین در عصاره جلبک اسپیرولینا پلاتنسیس، نشان دادند که عملکرد آنتیاکسیدانی عصاره جلبک اسپیرولینا پلاتنسیس به واسطه حضور پروتئین فیکوسیانین اعمال میگردد (21). رناتا و همکارانش ، خواص ضد سرطانی ترکیب شمیایی تترا پیرول موجود در جلبک سبز- آبی اسپیرولینا پلاتنسیس را بر روی سلولهای سرطانی پانکراس مورد بررسی قرار دادند. نتایج حاصل از بررسی نشان داد که این ترکیب باعث کاهش رشد سلولهای سرطانی پانکراس تحت تیمار با اسپیرولینا میشود (22). چینگ هایا و همکارانش، اثر آنتیاکسیدانی، ایمن سازی و ضد التهابی جلبک اسپیرولینا پلاتنسیس را در موش و انسان مورد بررسی قرار دادند. نتایج نشان داد که با مصرف جلبک اسپیرولینا پلاتنسیس به عنوان مکمل غذایی فعالیت آنزیمهای آنتیاکسیدانی سلولی، مهار پراکسیداسیون چربی، فعالیت آنزیم سوپراکسیداز دیسموتاز و آنزیم کاتالاز افزایش مییابد (23). لیو و همکارانش، به بررسی خواص ضد سرطانی ترکیب c-cp مشتق شده از جلبک اسپیرولینا پلاتنسیس پرداختند. نتایج نشان داد که این ترکیب دارای خواص آنتیاکسیدانی، ضد توموری و افزایش ایمنولوژیک دارد (24). از آنجاییکه دخالت سایر ژنهای دخیل در مسیرهای پیامرسان مرگ سلولی ممکن است بر عملکرد Drp1 تاثیر گذار باشند، پیشنهاد می شود مطالعات بیشتری در خصوص شبکههای تنظیم ژنی مرتبط انجام شود.
تیجهگیری
نتایج حاصل از تست فلوسیتومتری و سنجش بیان ژن صورت گرفته در تحقیق حاضر، بیانگر این مسئله می¬باشد که عصاره جلبک اسپیرولینا پلاتنسیس احتمالا قادر است با تاثیرگذاری بر مسیر مرگ برنامهریزی شده سلولی، آپوپتوز را در سلول¬های آدنوکارسینومای معده انسان القاء نماید و از این طریق در درمان سرطان معده مؤثر واقع گردد.
سپاسگزاری
این مقاله حاصل پایاننامه تحت عنوان "بررسی اثر عصاره اسپیرولینا پلاتنسیس بر میزان بیان ژن آپوپتوزی Drp1 و تنظیم مرگ سلولی برنامهریزی شده در رده سلولی آدنوکارسینومای معده انسان (AGS)" در مقطع کارشناسی ارشد در سال 1403 دانشگاه آزاد اسلامی واحد شهرکرد میباشد که با حمایت دانشگاه آزاد اسلامی واحد شهرکرد انجام شده است.
حامی مالی: ندارد.
تعارض در منافع: وجود ندارد.
ملاحظات اخلاقی
پروپوزال این تحقیق توسط دانشگاه آزاد اسلامی واحد شهرکرد تایید شده است (کد اخلاق: IR.IAU.SHK.REC.1403.247).
مشارکت نویسندگان
لیلا روحی در ارائه ایده، لیلا روحی در طراحی مطالعه، فرخنده محمدی در جمعآوری دادهها، لیلا روحی و فرخنده محمدی در تجزیه و تحلیل دادهها مشارکت داشته و همه نویسندگان در تدوین، ویرایش اولیه و نهایی مقاله و پاسخگویی به سوالات مرتبط با مقاله سهیم هستند.
.
سرطان در کشورهای توسعه یافته و در حال توسعه به ترتیب اولین و دومین عامل مرگ میباشد. سرطان معده در جهان به عنوان پنجمین سرطان شایع و چهارمین عامل مرگ بر اثر سرطان شناخته میشود (1). این سرطان از دسته سرطانهایی است که به آرامی و طی سالیان رشد میکند، اما قبل از آنکه به معنای واقعی بروز نماید، تغییراتی در لایههای معده ظاهر میگردد، ولی متاسفانه علائم چندانی را در این مرحله بهدنبال نداشته و به همین دلیل این نوع بدخیمی به سختی در مراحل ابتدایی تشخیص داده میشود. این در حالی است که اگر بدخیمیهای معده در مراحل اولیه کشف و درمان شوند، روند بهبود برای مبتلایان فراهم میگردد (3,2). بروز تدریجی چندین جهش در ژنهای کنترل کننده مسیرهای حیاتی سلول از جمله رشد، نمو و مرگ برنامهریزی شده سلولی باعث تولید تودههای توموری در بافت معده میشود، که از قوانین تکاملی حاکم بر ماهیت پر سلولی یک موجود زنده پیروی نکرده و با کسب ویژگیهایی از جمله عدم توجه به فاکتورهای رشد داخلی و خارجی، توانایی تکثیر خود به خودی، فرار از آپوپتوز و متاستاز سرطان معده را ایجاد میکنند (4,5). در طی سالهای اخیر، دانش و درک ما از فرآیندهای مولکولی که موجب بروز و پیشرفت سرطان میشوند، به میزان قابلتوجهی افزایش یافته است. این امر منجر به توسعه درمانهای هدفمند شده است که این فرآیندهای مولکولی را مختل مینمایند. از جمله این دستاوردهای علمی برای درمان سرطان معده میتوان به جراحی، پرتودرمانی، شیمیدرمانی، ایمنیدرمانی و استفاده از داروها اشاره کرد. اما با توجه به عوارض جانبی داروهای شیمیایی و همچنین اثرات منفی بر سایر بافتها و سلولهای بدن، امروزه استفاده از ترکیبات طبیعی بهعنوان دارو به دنبال دارا بودن اثرات جانبی کمتر در مقایسه با ترکیبات شمیایی، بیشتر مورد توجه قرار گرفته است (6,7). در این میان آبزیان دریائی بهواسطه فراوانی و تنوع بسیار بالای آنها همواره قابلتوجه قرار گرفتهاند. یکی از مهم-ترین این آبزیان که از سوی محققان علوم تغذیه به آن اشاره شده است و کشفیات زیادی در خصوص خواص تغذیهای و دارویی آن موجود میباشد، جلبک سبز- آبی اسپیرولینا پلاتنسیس است. اسپیرولینا یکی از نوید بخشترین ریزجلبکها میباشد که از سوی سازمان بهداشت جهانی بهعنوان بهترین راه حل درمانی برای فردا و پرسشنامه به عنوان غذای برتر اعلام گردیده است. فواید و برتری این ریزجلبک نسبت به سایر منابع غذایی گیاهی و دیگر جلبکها بسیار زیاد و قابلتوجه میباشد. اسپیرولینا پلاتنسیس به صورت بالقوه منبع بزرگی از ترکیباتی بوده که می¬توانند جهت تولید مواد اولیه فرآوردههای غذایی استفاده شوند. کاربرد اسپیرولینا پلاتنسیس و متابولیتهای آن روند جالبی در بهبود ارزش فراوردههای غذایی سالم ایجاد کرده است. اسپیرولینا غنیترین افزودنی به لحاظ پروتئینی، اسیدهای چرب ضروری نظیر گامالینولنیک، ویتامینها خصوصا ویتامین B12 و پیش ساز ویتامین A، مواد معدنی بخصوص آهن و کلسیم و رنگدانههایی از جمله فایکوسیانین و سولفولیپیدها میباشد. نداشتن دیواره سلولی سلولزی باعث جذب راحتتر مواد مغذی آن شده است. کم بودن میزان اسید نوکلئیک (کمتر از 4%) اسپیرولینا، یکی دیگر از برتریهای این ریز جلبک نسبت به سایر منابع پروتئینی مشابه میباشد. اسپیرولینا به دلیل داشتن اجزا و ترکیبات آنتیاکسیدانی مانند فایکوسیانین، سلنیوم، کارتنوئیدها اسیدچرب گامالینولنیک عامل دارویی بالقوه¬ای جهت بیماریهای القاء شده به وسیله تنش اکسیداسیونی نظیر سرطان میباشد (12-8). از اینرو در مطالعه حاضر اثر عصاره اسپیرولینا پلاتنسیس بر میزان بیان ژن آپوپتوزی Drp1 و تنظیم مرگ سلولی برنامهریزی شده در رده سلولی آدنوکارسینومای معده انسان (AGS) مورد بررسی قرار گرفت. Drp1 به عنوان یک GTPase در آپوپتوز میتوکندریایی نقش دارد (شکافت میتوکندری). به عبارت دیگر Drp1 بهطور مستقل یا پاییندست BH3-mimetics برای تسهیل آزاد سازی سیتوکروم c و آپوپتوز عمل کند (13).
روش بررسی
این مطالعه بهصورت تجربی از فروردین 1403 تا شهریور 1403 در مراکز تحقیقاتی سلولی- تکوینی، بیوتکنولوژی و گیاهان دارویی مجتمع آزمایشگاهی دانشگاه آزاد اسلامی واحد شهرکرد بهصورت تجربی با مجوز اخلاق در پژوهش به کد IR.IAU.SHK.REC.1403.247 انجام شد. رده سلولی AGS از مرکز ملی ذخایر ژنتیکی و زیستی ایران خریداری شد. در محیط کشت DMEM-F12 (Dulbecco's Modified Eagle's medium) (Gibco, USA) حاوی 10 درصد FBS (Foetal Bovine Serum) (Gibco, USA) و یک درصد Penstrep (Penicillin-Streptomycin) (Gibco, USA) در انکوباتور (Memmert, Germany) با فشار 5 درصد گاز CO2، رطوبت 90 درصد و دمای 37 درجه سانتیگراد، در فلاسک 75 کشت داده شد. محیط کشت هفتهای سه بار تعویض و برای برداشت کردن سلولها از محلول تریپسین/EDTA استفاده شد. اسپیرولینا پلاتنسیس به صورت آماده و به حالت جامد از شرکت دانشپژوهان قشم با نام تجاری اسپیرولینا (سوپر فود) تهیه گردید. برای تهیه عصاره از این ماده در مرکز تحقیقات گیاهان دارویی دانشگاه آزاد اسلامی واحد شهرکرد، پودر اسـپیرولینا درون فـالکون ریختــه شـد و حلال اتانولی به آن اضافه و اقدام به عصارهگیری شد. عمل عصارهگیری سه بار تکرار گردید و تا زمان استفاده در دمای 4 درجه سانتیگراد نگهداری شد.
سنجش وقوع آپوپتوز: القاء آپوپتوز در رده سلولی AGS، از طریق تست Annexin V-FITC/PI، با استفاده از کیت FITC Annexin V Apoptosis Detection kit (BD Pharmingen, USA)، با شماره محصول (556547)، مورد ارزیابی قرار گرفت. به این ترتیب که، تعداد 5×105 سلول در پلیتهای کشت 6 خانه کشت داده شد، و سپس، با غلظتهای 10 (گروه I)، 20 (گروه II) و 40 (گروه III) میکروگرم/ میلیلیتر عصاره اسپیرولینا پلاتنسیس در بازههای زمانی 24 و 48 ساعت تحت تیمار قرار گرفت. پس از اتمام زمان انکوباسیون، محیط رویی تیمار جمع آوری شد. پس از ترپسینه کردن، رسوب سلولی دو بار با محلول PBS (Phosphate-buffered saline)، (SIGMA-ALDRICH, USA)، سرد شستشو گردید. سپس مقدار 300 میکرولیتر بافر به سلولها اضافه شد و سوسپانس سلول و بافر به لولههای مخصوص فلوسیتومتری انتقال یافت. با اضافه کردن 5 میکرولیتر Annexin و PIبه لولهها و به حجم رساندن آنها با بافر به میزان 200 میکرولیتر برای سایر لولهها و 500 میکرولیتر برای لولههای کنترل، لولهها به محیط تاریک و در دمای اتاق ظرف مدت زمان 20 دقیقه انتقال داده شدند (14). پس از گذشت مدت زمان معلوم از دستگاه فلوسیتومتری(BD Facscalibur, USA) جهت خوانش نتایج استفاده گردید.
سنجش بیان ژن: به منظور بررسی میزان بیان ژن Drp1، تعداد 105×3 سلول در پلیتهای 6 خانه کشت داده شد، و سپس، با غلظت 40 میکروگرم/ میلیلیتر عصاره اسپیرولینا پلاتنسیس در بازه زمانی 48 ساعت تیمار و انکوبه شدند. پس از گذشت زمان انکوباسیون، سلولها در دو گروه تست شامل غلظت 40 میکروگرم/ میلیلیتر از عصاره اسپیرولینا پلاتنسیس و گروه کنترل، برداشت و پس از شستشو با بافر PBS، Total RNA سلولی با استفاده از معرف RNXTM –PLUS (RNX-Plus Solution for total RNA isolation)، جدا گردید. به منظور انجام مرحله Heat block، نمونههای حاصل از مرحله قبل در دستگاه ترموسایکلر با دمای 60 درجه سانتی گراد به مدت 20 دقیقه قرار داده شدند. در ادامه تمام توالی-های RNA با استفاده از کیت سنتز cDNA (PrimeScriptTM RT Reagent kit (Perfect Real Time))، (Takara)، به cDNA تبدیل و به فریزر 20- درجه سانتیگراد منتقل شدند. سنجش میزان بیان ژن Drp1 با استفاده از دستگاه Real Time PCR مدل (Rotor gene 3000 corbett, Australia) مورد ارزیابی قرار گرفت. برای انجام واکنش، مخلوط واکنشی متشکل از cDNA، به مقدار 1 میکرولیتر، پرایمر رفت و برگشت هرکدام به مقدار 0/5 میکرولیتر، RNase-free water، به مقدار 5/5 میکرولیتر و 12/5 میکرولیتر مسترمیکس (Master Mix RT-PCR) (Ampliqon) تهیه گردید (15). توالی پرایمرهای پیشرو (Forward) و پسرو (Reverse) ژنهای GAPDH و Drp1 با استفاده از نرم افزار Oligo6 طراحی و سپس با Blast نمودن آنها در NBCI از صحیح بودن آنها اطمینان حاصل شد و نهایتا توسط شرکت Macrogen سنتز شدند (جدول 1). از ژن GAPDH، به عنوان کنترل داخلی استفاده شد. سپس مخلوط واکنش پس از آماده سازی با حجم نهایی 20 میکرولیتر تحت تاثیر برنامه¬ی دمایی ذکر شده در جدول 2 قرار گرفت.
تجزیه و تحلیل آماری
بررسی آماری با استفاده از آزمون t از طریق نرمافزارهای SPSS و GraphPad Prism انجام شد. حدود اطمینان برای همه آزمایشات 95% در نظر گرفته شد و 5% < P معنی دار محسوب گردید.
.
جدول1: مشخصات پرایمر مربوط به ژنهای Drp1 و Gapdh

جدول2: شرایط دمایی واکنش Rael Time PCR

نتایج
سلولهای ردهی AGS در غلظت 40 میکروگرم/ میلیلیتر از عصارهی جلبک اسپیرولینا پلاتنسیس برای مدت زمان 48 ساعت کشت داده شدند. تصویر زیر (شکل 1) انکوباسیون سلولهای تحت تیمار با غلظت 40 میکروگرم/ میلیلیتر از عصارهی جلبک اسپیرولینا پلاتنسیس را برای مدت زمان 48 ساعت نشان میدهد که مشاهدات میکروسکوپی حاکی از کاهش تعداد سلولها در گروههای تحت تیمار میباشد. به منظور بررسی میزان القاء آپوپتوز از تست Annexin V-FITS استفاده شد. سلولها برای مدت زمان 48 ساعت تحت تیمار با غلظت 40 میکروگرم/ میلیلیتر از عصاره جلبک اسپیرولینا پلاتنسیس قرار گرفتند (بهعنوان غلظت و زمان تیماری که بقای سلولی را 50 درصد کاهش میدهد). نتایج نشان میدهد که میزان القاء آپوپتوز درگروه تحت تیمار افزایش مییابد. آنالیز آماری نشان داد که درصد مرگ سلولی در رده سلولی AGS افزایش یافته است. همانطور که در نمودار 1 دیده میشود، درصد سلولهای زنده در گروه کنترل 98/44 درصد است که بیشتر از گروه آزمایشی میباشد. درصد سلولهای زنده در گروه آزمایشی نسبت به گروه کنترل کاهش را نشان میدهد که این اختلاف از نظر آماری نسبت به گروه کنترل معنیدار است (P≤0.05). در تیمار 48 ساعته، درصد سلولهایی که در مراحل اولیه آپوپتوز هستند از 2 درصد در گروه کنترل به 4./39 درصد در غلظت 40 میکروگرم/ میلیلیتر رسیده است که این افزایش درصد آپوپتوز نسبت به گروه کنترل اختلاف معنیداری دارد (P<0.001). بهعلاوه درصد سلولهایی که در مراحل انتهایی آپوپتوز هستند افزایش را نشان دادهاند، به گونهای که از 9/ 0درصد در گروه کنترل به 46/01 درصد در غلظت 40 میکروگرم/ میلیلیتر رسیده است که این افزایش درصد آپوپتوز نسبت به گروه کنترل معنیدار است (P<0.0001) (شکل 2) ( نمودار 1). تیمار سلولهای رده AGS با عصاره¬ جلبک اسپیرولینا پلاتنسیس و انکوباسیون آنها برای مدت 48 ساعت افزایش معنیداری را در میزان بیان ژن Drp1 نشان داد. نمودارهای زیر این افزایش بیان را در ژنهای Drp1 براساس CtΔΔ نمایش میدهد.

شکل1: تاثیر غلظت 40 میکروگرم/ میلیلیتر از عصاره جلبک اسپیرولینا پلاتنسیس بر رده سلولی AGS برای مدت زمان 48 ساعت; تصویر بالا: سلولهای رده AGS در معرض محیط کشت DMEM+ FBS10% (گروه کنترل)، تصویر پایین: سلولهای رده AGS در غلظت 40 میکروگرم/ میلیلیتر از عصاره جلبک اسپیرولینا پلاتنسیس برای مدت زمان 48 ساعت

شکل2: تاثیر عصاره جلبک اسپیرولینا پلاتنسیس بر القاء آپوپتوز در رده سلولی AGS.; تصویر چپ: گروه کنترل ، تصویر راست: وقوع آپوپتوز اولیه و انتهایی سلولهای رده AGS تحت تیمار غلظت 40 میکروگرم/ میلیلیتر از عصارهی جلبک اسپیرولینا پلاتنسیس برای مدت زمان 48 ساعت

نمودار 1: درصد سلولهای زنده، آپوپتوز اولیه و آپوپتوز انتهایی در سلول¬های AGS تحت تیمار با غلظت 40 میکروگرم/ میلیلیتر به مدت 48 ساعت.P<0.0001** در مقابل گروه کنترل

نمودار2: نمودار میزان بیان ژن Drp1 براساس Ct در غلظت 40 میکروگرم/ میلیلیتر و زمان انکوباسیون 48 ساعت.
P<0.001** اختلاف معنیدار در مقابل گروه کنترل
بحث
یکی از معضلات امروزی در جوامع بشری سرطان معده میباشد که به عنوان یک بیماری چند عاملی در نتیجهی تداوم آسیبهای ناشی از مواجهه مداوم با عوامل سرطانزا ایجاد میشود. علی رقم کاهش قابلملاحظه در بروز این نوع بدخیمی در طول دهههای گذشته، در اکثر کشورهای صنعتی هنوز این بیماری دومین علت شایع مرگ و میر افراد در اثر سرطان میباشد که سالیانه باعث مرگ حدود یک میلیون نفر در سرتاسر جهان میشود (16,17). مبتلایان به آدنوکارسینومای معده دارای بقاء 5 ساله هستند و در بیش از 90% موارد درمان تومور معدی با جراحی، تنها شانس درمانی میباشد. اما به دلیل اینکه در حال حاضر تشخیص زود هنگام سرطان معده امکانپذیر نیست و معمولا تشخیص زمانی صورت میگیرد که سرطان بهطور موضعی پیشرفت کرده است و به درون دیواره معده نفوذ نموده، این شانس به کمتر از 30% کاهش مییابد (18). لذا با توجه به افزایش روز افزون تعداد مبتلایان که شمار زیادی از آنها پس از گذراندن مراحل دشوار عملهای جراحی باز هم دچار عود بیماری میشوند و از آنجاییکه مقاومت به مرگ سلولی و عدم وجود تعادل بین تقسیم سلولی و مرگ سلولی منجر به عدم کنترل تکثیر سلولهای توموری میشود، امروزه نیاز به ترکیبات درمانی که قادر به مهار تکثیر سلولهای توموری باشند، به شدت احساس میشود (19). تحقیقات گذشته نشان داده است که سیانوباکترها میتوانند مواد زیست فعّال داخل و خارج سلولی با فعالیتهای ضد باکتری تولید کنند. فعالیت ضد میکروبی اسپیرولینا پلاتنسیس میتواند ناشی از گاما-لینولنیک اسید، اسیدهای چرب فعّال، اثرات سینرژیستی لائوریک اسید و پالمیتولئیک اسید، فایکوسیانین، فایکوسیانوبیلین و الوفایکوسیانین، آمیدها، آلکالوئیدها، هپتادکان، تترادکان، تترامین، اسپرمین و پیپرازین باشد. کلسیم-اسپیرولن یک پلیساکارید سولفاته در اسپیرولینا پلاتنسیس است که شامل رامنوز، ریبوز، مانوز، فروکتوز، گالاکتوز، زایلوز، گلوکز، گلوکورونیک اسید، گالاکتورونیک اسید و سولفات کلسیم است. اسپیرولینا پلاتنسیس منبعی از ترکیبات فنولیک نظیر کافئیک، کلروژنیک، سالیسیلیک، سیناپتیک و ترانس سینامیک اسید است. ترکیبات فنولیک مواد ضد میکروب و آنتیاکسیدان طبیعی هستند که حلقههای بنزنیک آنها توسط یک یا تعداد بیشتر گروه هیدروکسیل جایگزین شده است. عصاره اسپیرولینا دارای فعالیت ضد میکروبی علیه باکتریهای گرم منفی نظیر هلیکوباکتر پیلوری عامل سرطان معده است. مطالعات طی 40 سال گذشته نشان داده است که بیش از 15000 ترکیب جدید از جلبکها استخراج شده است که بسیاری از آنها کارکرد زیست فعال دارند. همچنین، به دلیل اینکه اسپیرولینا پلاتنسیس حاوی زی- سلنیوم، منگنز، ویتامین E و C، گزانتین، بتا-کریپتوگزانتین، گزانتوفیل، میکسوگزانتوفیل، بتا-کاروتن، کلروفیل، ویتامین فایکواریترین و فایکوسیانین است خاصیت آنتیاکسیدانی خوبی دارد. این ترکیبات رادیکالهای آزاد مضر را که در بروز بسیاری از سرطانها نقش دارند جاروب میکنند. اسپیرولینا پرسشنامه منبع ترکیبات فنولی همچون اسید کافئیک، کلروجنیک، سالیسیلیک، سیناپتیک و ترانس- سینامیک است. ترکیبات فنولی آنتیاکسیدان¬های طبیعی هستند که حلقههای بنزونیک با یک یا چند گروه هیدروکسیل جایگزین شده است. اسپیرولینا میتواند تولید آنزیمهای گوناگون آنتیاکسیدانی را تحریک نماید، از جمله آنزیم سوپراکسیددسموتاز که یک آنزیم مهم در از بین بردن رادیکالهای آزاد است. این آنزیم پرسشنامه برای درمان انواع بیماریهای مرتبط با تنش اکسیداتیو و یا به عنوان جزئی از لوسیونهای ضد چروک پوست و ماسکهای صورت با افزایش سن فرد مورد استفاده قرار میگیرد. اسپیرولینا پلاتنسیس همچنین باعث افزایش فعالیت آنزیمهایی از قبیل پراکسی ردوکسین و آسکوربات پراکسیداز میشود. مکانیسمهای آنتیاکسیدانی اسپیرولینا پلاتنسیس شامل افزایش فعالیت آنتیاکسیدانهای آنزیمی شامل سوپراکسید دسموتاز، گلوتاتیون پراکسیداز و کاتالاز و پرسشنامه آنتیاکسیدانهای غیر آنزیمی شامل بتاکاروتن، گلوتاتیون و ویتامین E است (20). بهعلاوه، در تحقیق حاضر نیز توانایی عصاره جلبک سبز- آبی اسپیرولینا پلاتنسیس در مهار رشد و خاصیت ضد تکثیری آن که از طریق القاء مرگ برنامهریزی شدهی سلولی اعمال میگردد، در سلولهای رده آدنوکارسینومای معده انسان (AGS)، مورد بررسی قرار گرفت. در این تحقیق تیمار رده سلولی AGS با غلظتی از عصاره جلبک اسپیرولینا پلاتنسیس (40 میلیگرم/ میلیلیتر) و انکوباسیون سلولها برای مدت زمان 48 ساعت نتایج قابلتوجهی را در میزان وقوع آپوپتوز در رده سلولی AGS نشان داد. وقوع آپوپتوز با استفاده از تست Annexin V-FITC بررسی گردید و آنالیز آماری صورت گرفت. نتایج حاصل نشان داد که درصد سلولهایی که در مرحله انتهایی آپوپتوز هستند، در زمان انکوباسیون 48 ساعت در غلظت 40 میلیگرم/ میلیلیتر به بیشترین مقدار نسبت به گروه کنترل رسیده است. به علاوه در این تحقیق توانایی عصاره جلبک اسپیرولینا پلاتنسیس در تغییر بیان ژن رمزکننده پروتئین پروآپوپتوزی Drp1 دخیل در مسیر مرگ سلولی در سلولهای رده AGS سرطان معده، مورد بررسی قرار گرفت. Drp1 با کنترل نفوذپذیری غشای خارجی میتوکندری در آپوپتوز وابسته به Bax/Bak یا Bnip3 نقش دارد. Drp1 در حین مرگ سلولی در اثر آپوپتوز با Bax در مکانهای شکافت میتوکندری متصل میشود و در پایین دست جابجایی Bax اما در بالادست آزاد سازی سیتوکروم c عمل میکند (13). در این پژوهش تیمار سلولهای AGS سرطان معده، با دوز 40 میلیگرم/ میلیلیتر عصاره جلبک اسپیرولینا پلاتنسیس و انکوباسیون آن برای مدت 48 ساعت، افزایش معنیدار میزان بیان ژن Drp1 (P<0.001) را نشان داد. لذا به طور کلی میتوان از دادهی حاصل شده از دو تست نتیجه گرفت که احتمالا عصاره جلبک سبز- آبی اسپیرولینا پلاتنسیس دارای بیشترین قدرت مهاری بر رشد و تکثیر رده سلولهای آدنوکارسینومای معده انسان (AGS)، در غلظت 40 میلی¬گرم/ میلی¬لیتر و زمان انکوباسیون 48 ساعته میباشد. به علاوه تحقیقات ارائه شده در زیر شواهد محکمی بر اثبات صداقت نتایج حاصل شده از تحقیق حاضر میباشند: پینرو و همکارانش، در پی ارزیابی ساز و کار عملکردی پروتئین فیکوسیانین در عصاره جلبک اسپیرولینا پلاتنسیس، نشان دادند که عملکرد آنتیاکسیدانی عصاره جلبک اسپیرولینا پلاتنسیس به واسطه حضور پروتئین فیکوسیانین اعمال میگردد (21). رناتا و همکارانش ، خواص ضد سرطانی ترکیب شمیایی تترا پیرول موجود در جلبک سبز- آبی اسپیرولینا پلاتنسیس را بر روی سلولهای سرطانی پانکراس مورد بررسی قرار دادند. نتایج حاصل از بررسی نشان داد که این ترکیب باعث کاهش رشد سلولهای سرطانی پانکراس تحت تیمار با اسپیرولینا میشود (22). چینگ هایا و همکارانش، اثر آنتیاکسیدانی، ایمن سازی و ضد التهابی جلبک اسپیرولینا پلاتنسیس را در موش و انسان مورد بررسی قرار دادند. نتایج نشان داد که با مصرف جلبک اسپیرولینا پلاتنسیس به عنوان مکمل غذایی فعالیت آنزیمهای آنتیاکسیدانی سلولی، مهار پراکسیداسیون چربی، فعالیت آنزیم سوپراکسیداز دیسموتاز و آنزیم کاتالاز افزایش مییابد (23). لیو و همکارانش، به بررسی خواص ضد سرطانی ترکیب c-cp مشتق شده از جلبک اسپیرولینا پلاتنسیس پرداختند. نتایج نشان داد که این ترکیب دارای خواص آنتیاکسیدانی، ضد توموری و افزایش ایمنولوژیک دارد (24). از آنجاییکه دخالت سایر ژنهای دخیل در مسیرهای پیامرسان مرگ سلولی ممکن است بر عملکرد Drp1 تاثیر گذار باشند، پیشنهاد می شود مطالعات بیشتری در خصوص شبکههای تنظیم ژنی مرتبط انجام شود.
تیجهگیری
نتایج حاصل از تست فلوسیتومتری و سنجش بیان ژن صورت گرفته در تحقیق حاضر، بیانگر این مسئله می¬باشد که عصاره جلبک اسپیرولینا پلاتنسیس احتمالا قادر است با تاثیرگذاری بر مسیر مرگ برنامهریزی شده سلولی، آپوپتوز را در سلول¬های آدنوکارسینومای معده انسان القاء نماید و از این طریق در درمان سرطان معده مؤثر واقع گردد.
سپاسگزاری
این مقاله حاصل پایاننامه تحت عنوان "بررسی اثر عصاره اسپیرولینا پلاتنسیس بر میزان بیان ژن آپوپتوزی Drp1 و تنظیم مرگ سلولی برنامهریزی شده در رده سلولی آدنوکارسینومای معده انسان (AGS)" در مقطع کارشناسی ارشد در سال 1403 دانشگاه آزاد اسلامی واحد شهرکرد میباشد که با حمایت دانشگاه آزاد اسلامی واحد شهرکرد انجام شده است.
حامی مالی: ندارد.
تعارض در منافع: وجود ندارد.
ملاحظات اخلاقی
پروپوزال این تحقیق توسط دانشگاه آزاد اسلامی واحد شهرکرد تایید شده است (کد اخلاق: IR.IAU.SHK.REC.1403.247).
مشارکت نویسندگان
لیلا روحی در ارائه ایده، لیلا روحی در طراحی مطالعه، فرخنده محمدی در جمعآوری دادهها، لیلا روحی و فرخنده محمدی در تجزیه و تحلیل دادهها مشارکت داشته و همه نویسندگان در تدوین، ویرایش اولیه و نهایی مقاله و پاسخگویی به سوالات مرتبط با مقاله سهیم هستند.
.
References:
1- Sung H, Ferlay J, Siegel RL, Laversanne M, Soerjomataram I, Jemal A, et al. Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries. CA Cancer J Clin 2021; 71(3): 209-49.
2- Sotoudeh M, Mirsamadi MM, Sedghi M. Comparisonof the Type of Intera Cellular Mucin in Patients with Pylori Gastritis and Normal Population. Tehran Uni Med J 2002; 29: 245. [Persian]
3- Roshnaei G, Kazemnejad A, Sedighi S. Survival Estimating Following Recurrence in Gastric Cancer Patients and Its Relative Factors. Koomesh 2024; 12(3): 223-28.
4- Kitano H. Cancer as a Robust System: Implicationsfor Anticancer Therapy. Nat Rev Cancer 2004; 4: 227-37.
5- McCormick F. Cancer Gene Therapy: Fringe Orcutting Edge? Nat Rev Cancer 2001; 1(2): 130-41.
6- Backwith D MG. Inequalities in Health and Community-Oriented Social Work Lessons from Cuba. Inte social work 2009; 59: 499-511.
7- Cassileth BR. Complementary and Alternativetherapies for Cancer. The oncologist 2004; 9: 80-9.
8- Konícková R, Vanková K, Vaníková J, Vánová K, Muchová L, Subhanová I, et al. Anti-Cancer Effects of Blue-Green Alga Spirulina Platensis, A Natural Source of Bilirubin-Like Tetrapyrrolic Compounds. Ann Hepatol 2014; 13(2): 273-83
9- Maryati M, Saifudin A, Wahyuni S, Rahmawati J, Arrum A, Priyunita O, et al. Cytotoxic Effect of Spirulina Platensis Extract and Ulva Compressa Linn on Cancer Cell Lines. Food Res 2020; 4(4): 1018-23.
10- Czerwonka A, Kaławaj K, Sławińska-Brych A, Lemieszek MK, Bartnik M, Wojtanowski KK, et al. Anticancer Effect of the Water Extract of a Commercial Spirulina (Arthrospira Platensis) Product on the Human Lung Cancer A549 Cell Line. Biomed Pharmacother 2018; 106: 292-302.
11- Wang Z, Zhang X. Inhibitory Effects of Small Molecular Peptides from Spirulina (Arthrospira) Platensis on Cancer Cell Growth. Food Funct. 2016; 7(2): 781-8.
12- Fayyad RJ, Ali ANM, Dwaish AS, Al-Abboodi AKA. Anticancer Activity of Spirulina Platensis Methanolic Extracts Against L20B and MCF7 Human Cancer Cell Lines. Plant Arch 2019; 19(1): 1419-26.
13- Milani M, Beckett AJ, Al-Zebeeby A, Luo X, Prior IA, Cohen GM, Varadarajan S. DRP-1 Functions Independently of Mitochondrial Structural Perturbations to Facilitate BH3 Mimetic-Mediated Apoptosis. Cell Death Discov 2019; 5: 117.
14- Malaki MS, Rouhi L, Khashei Varnamkhasti K. Apoptotic Induction in Human Colorectal Adenocarcinoma Cell Line and Growth Inhibition of Some Gastrointestinal Pathogenic Species by Lactobacillus Sakei Metabolites. Payavard Salamat 2021; 14(6): 476-83.
15- Varnamkhasti KK, Tavakoli P, Rouhi L, Raisi S. Cytotoxicity, Apoptosis Induction and Change of P53, PARP, P21 and Bcl-2 Genes Expression in the Human Anaplastic Thyroid Carcinoma Cells Line (SW-1736) with Curcumin. Genetics & Applications 2021; 5(1): 10-7.
16- Rafter J. Lactic Acid Bacteria and Cancer: Mechanistic Perspective. Br J Nutr 2008; 88 (1): 89-94.
17- Caldas C, Carneiro F. Familial Gastric Cancer: Overview and Guidelines for Management. J Med Genet 1999; 36(12): 873-80.
18- Whelan SL, Parkin DM. Trends in Cancer Incidence and Mortality. IARC Sci Publ 1993; 102.
19- Azizi F, Hatami H. Epidemiology and control of common Diseases in Iran. Tehran: Eshtiagh Publication 2000; 602-16. [Persian]
20- Broecker-Preuss M, Viehof J, Jastrow H. Cell Death Induction by the BH3 Mimetic GX15-070 in Thyroid Carcinoma Cells. J Exp Clin Cancer Res 2015; 34(1): 69.
21- Mohseni R, Mohseni R, Zamani Sedehi A, Arab Sadeghabadi Z, Safaei M, Heiat M. Dietary Supplement Based on Microalgae, as a New Therapeutic Approach in the Future. NCMBJ 2021; 11(42): 31-54. [Persian]
22- Estrada JP, Bescós PB, Villar del Fresno AM. Antioxidant Activity of Different Fractions of Spirulina Platensis Protean Extract. Farmaco 2001; 56(5): 497-500.
23- Wu Q, Liu L. The Antioxidant, Immunomodulatory, and Anti-Inflammatory Activities of Spirulina: an Overview. Arch Toxicol 2016; 90(8): 1817-40.
24- Liu Q, Huang Y. Medical Application of Spirulina Platensis Derived C-Phycocyanin. Evid Based Complement Alternat Med 2016; 2016: 7803846.
1- Sung H, Ferlay J, Siegel RL, Laversanne M, Soerjomataram I, Jemal A, et al. Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries. CA Cancer J Clin 2021; 71(3): 209-49.
2- Sotoudeh M, Mirsamadi MM, Sedghi M. Comparisonof the Type of Intera Cellular Mucin in Patients with Pylori Gastritis and Normal Population. Tehran Uni Med J 2002; 29: 245. [Persian]
3- Roshnaei G, Kazemnejad A, Sedighi S. Survival Estimating Following Recurrence in Gastric Cancer Patients and Its Relative Factors. Koomesh 2024; 12(3): 223-28.
4- Kitano H. Cancer as a Robust System: Implicationsfor Anticancer Therapy. Nat Rev Cancer 2004; 4: 227-37.
5- McCormick F. Cancer Gene Therapy: Fringe Orcutting Edge? Nat Rev Cancer 2001; 1(2): 130-41.
6- Backwith D MG. Inequalities in Health and Community-Oriented Social Work Lessons from Cuba. Inte social work 2009; 59: 499-511.
7- Cassileth BR. Complementary and Alternativetherapies for Cancer. The oncologist 2004; 9: 80-9.
8- Konícková R, Vanková K, Vaníková J, Vánová K, Muchová L, Subhanová I, et al. Anti-Cancer Effects of Blue-Green Alga Spirulina Platensis, A Natural Source of Bilirubin-Like Tetrapyrrolic Compounds. Ann Hepatol 2014; 13(2): 273-83
9- Maryati M, Saifudin A, Wahyuni S, Rahmawati J, Arrum A, Priyunita O, et al. Cytotoxic Effect of Spirulina Platensis Extract and Ulva Compressa Linn on Cancer Cell Lines. Food Res 2020; 4(4): 1018-23.
10- Czerwonka A, Kaławaj K, Sławińska-Brych A, Lemieszek MK, Bartnik M, Wojtanowski KK, et al. Anticancer Effect of the Water Extract of a Commercial Spirulina (Arthrospira Platensis) Product on the Human Lung Cancer A549 Cell Line. Biomed Pharmacother 2018; 106: 292-302.
11- Wang Z, Zhang X. Inhibitory Effects of Small Molecular Peptides from Spirulina (Arthrospira) Platensis on Cancer Cell Growth. Food Funct. 2016; 7(2): 781-8.
12- Fayyad RJ, Ali ANM, Dwaish AS, Al-Abboodi AKA. Anticancer Activity of Spirulina Platensis Methanolic Extracts Against L20B and MCF7 Human Cancer Cell Lines. Plant Arch 2019; 19(1): 1419-26.
13- Milani M, Beckett AJ, Al-Zebeeby A, Luo X, Prior IA, Cohen GM, Varadarajan S. DRP-1 Functions Independently of Mitochondrial Structural Perturbations to Facilitate BH3 Mimetic-Mediated Apoptosis. Cell Death Discov 2019; 5: 117.
14- Malaki MS, Rouhi L, Khashei Varnamkhasti K. Apoptotic Induction in Human Colorectal Adenocarcinoma Cell Line and Growth Inhibition of Some Gastrointestinal Pathogenic Species by Lactobacillus Sakei Metabolites. Payavard Salamat 2021; 14(6): 476-83.
15- Varnamkhasti KK, Tavakoli P, Rouhi L, Raisi S. Cytotoxicity, Apoptosis Induction and Change of P53, PARP, P21 and Bcl-2 Genes Expression in the Human Anaplastic Thyroid Carcinoma Cells Line (SW-1736) with Curcumin. Genetics & Applications 2021; 5(1): 10-7.
16- Rafter J. Lactic Acid Bacteria and Cancer: Mechanistic Perspective. Br J Nutr 2008; 88 (1): 89-94.
17- Caldas C, Carneiro F. Familial Gastric Cancer: Overview and Guidelines for Management. J Med Genet 1999; 36(12): 873-80.
18- Whelan SL, Parkin DM. Trends in Cancer Incidence and Mortality. IARC Sci Publ 1993; 102.
19- Azizi F, Hatami H. Epidemiology and control of common Diseases in Iran. Tehran: Eshtiagh Publication 2000; 602-16. [Persian]
20- Broecker-Preuss M, Viehof J, Jastrow H. Cell Death Induction by the BH3 Mimetic GX15-070 in Thyroid Carcinoma Cells. J Exp Clin Cancer Res 2015; 34(1): 69.
21- Mohseni R, Mohseni R, Zamani Sedehi A, Arab Sadeghabadi Z, Safaei M, Heiat M. Dietary Supplement Based on Microalgae, as a New Therapeutic Approach in the Future. NCMBJ 2021; 11(42): 31-54. [Persian]
22- Estrada JP, Bescós PB, Villar del Fresno AM. Antioxidant Activity of Different Fractions of Spirulina Platensis Protean Extract. Farmaco 2001; 56(5): 497-500.
23- Wu Q, Liu L. The Antioxidant, Immunomodulatory, and Anti-Inflammatory Activities of Spirulina: an Overview. Arch Toxicol 2016; 90(8): 1817-40.
24- Liu Q, Huang Y. Medical Application of Spirulina Platensis Derived C-Phycocyanin. Evid Based Complement Alternat Med 2016; 2016: 7803846.
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |







