دوره 32، شماره 6 - ( شهریور 1403 )
جلد 32 شماره 6 صفحات 7962-7951 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Kargarian-Marvasti S, Hasannezhad M, Abolghasemi J. Survival Analysis of Patients with Covid-19 Using Parametric Models in the Presence of Frailty Variable: A Prospective Cohort Study. JSSU 2024; 32 (6) :7951-7962
URL: http://jssu.ssu.ac.ir/article-1-6146-fa.html
URL: http://jssu.ssu.ac.ir/article-1-6146-fa.html
کارگریان مروستی صادق، حسننژاد ملیحه، ابوالقاسمی جمیله. آنالیز زمان بقای بیماران مبتلا به کووید-19 با مدلهای پارامتری با استفاده از مدل شکنندگی: مطالعۀ کوهورت آیندهنگر. مجله علمي پژوهشي دانشگاه علوم پزشكي شهید صدوقی يزد. 1403; 32 (6) :7951-7962
متن کامل [PDF 880 kb]
(445 دریافت)
| چکیده (HTML) (1298 مشاهده)
References:
1- Gralinski Le, Menachery Vd. Return of the Coronavirus: 2019-Ncov. Viruses 2020; 12(2): 135.
2- Who. Novel Coronavirus (2019-Ncov). Available at: https://www.who.int/docs/default-source/coronaviruse/situation-reports/20200211-sitrep-22-ncov.pdf, Page:7. Accessed: Aug 21, 2024.
3- Zhao S, Musa Ss, Lin Q, Ran J, Yang G, Wang W, et al. Estimating the Unreported Number of Novel Coronavirus (2019-Ncov) Cases in China in the First Half of January 2020: A Data-Driven Modelling Analysis of the Early Outbreak. J Clin Med 2020; 9(2): 388.
4- Wang M, Cao R, Zhang L, Yang X, Liu J, Xu M, et al. Remdesivir and Chloroquine Effectively Inhibit the Recently Emerged Novel Coronavirus (2019-Ncov) in Vitro. Cell Research 2020; 30(3): 269-71.
5- Wang M, Zhou Y, Zong Z, Liang Z, Cao Y, Tang H, et al. A Precision Medicine Approach to Managing 2019 Novel Coronavirus Pneumonia. Precis Clin Med 2020; 3(1): 14-21.
6- Liu J, Zheng X, Tong Q, Li W, Wang B, Sutter K, et al. Overlapping and Discrete Aspects of the Pathology and Pathogenesis of the Emerging Human Pathogenic Coronaviruses Sars‐Cov, Mers‐Cov, and 2019‐Ncov. J Med Virol 2020; 92(5): 491-4.
7- Daszak P, Olival Kj, Li H. A Strategy to Prevent Future Epidemics Similar to the 2019-Ncov Outbreak. Biosaf Health 2020; 2(1): 6-8.
8- Tavakoli A, Karbalaie Niya Mh, Keshavarz M, Safarnezhad Tameshke F, Monavari Sh. Middle East Respiratory Syndrome Coronavirus (Mers-Cov). Iran J Med Microbiol 2017; 11(1): 1-8.
9- Momattin H, Al-Ali Ay, Al-Tawfiq Ja. A Systematic Review of Therapeutic Agents for the Treatment of the Middle East Respiratory Syndrome Coronavirus (Mers-Cov). Travel Med Infect Dis 2019; 30: 9-18.
10- Vahdat K, Amini A, Najafi A, Haerinejad Mj. A Review of Novel Coronavirus, Cause of Middle East Respiratory Syndrome. ISMJ 2014; 16(6): 486-92.
11- L Zhang L, Lin D, Kusov Y, Nian Y, Ma Q, Wang J, et al. Α-Ketoamides as Broad-Spectrum Inhibitors of Coronavirus and Enterovirus Replication: Structure-Based Design, Synthesis, and Activity Assessment. Journal of Medicinal Chemistry 2020; 63(9): 4562-78.
12- N Zhu N, Zhang D, Wang W, Li X, Yang B, Song J, et al. A Novel Coronavirus from Patients with Pneumonia in China, 2019. New England Journal of Medicine 2020; 382(8): 727-33.
13- Lai CC, Shih TP, Ko WC, Tang HJ, Hsueh PR. Severe Acute Respiratory Syndrome Coronavirus 2 (SARS-Cov-2) and Coronavirus Disease-2019 (COVID-19): The Epidemic and the Challenges. International Journal of Antimicrobial Agents 2020; 55(3): 105924.
14- Cui J, Li F, Shi ZL. Origin and Evolution of Pathogenic Coronaviruses. Nature Reviews Microbiology 2019; 17(3): 181-92.
15- Bonilla-Aldana Dk, Quintero-Rada K, Montoya-Posada Jp, Ramírez-Ocampo S, Paniz-Mondolfi A, Rabaan Aa, et al. Sars-Cov, Mers-Cov and Now the 2019-Novel Cov: Have We Investigated Enough about Coronaviruses?–A Bibliometric Analysis. Travel Medicine and Infectious Disease 2020; 33: 101566.
16- Hougaard P. Frailty Models For Survival Data. Lifetime Data Anal 1995; 1(3): 255-73.
17- Hougaard P. A Class of Multivanate Failure Time Distributions. Biometrika 1986; 73(3): 671-8.
18- Mcgilchrist C, Aisbett C. Regression with Frailty in Survival Analysis. Biometrics 1991; 47: 461-6.
19- Ripatti S, Larsen K, Palmgren J. Maximum Likelihood Inference for Multivariate Frailty Models Using an Automated Monte Carlo Em Algorithm. Lifetime Data Anal 2002; 8(4): 349-60.
20- Hougaard P. Frailty Models for Survival Data. Lifetime Data Analysis 1995; 1(3): 255-73.
21- Oakes D. Bivariate Survival Models Induced by Frailties. Journal of the American Statistical Association 1989; 84(406): 487-93.
22- Bjarnason H, Hougaard P. Fisher Information for Two Gamma Frailty Bivariate Weibull Models. Lifetime Data Anal 2000; 6(1): 59-71.
23- Bolstad Wm, Manda So. Investigating Child Mortality in Malawi Using Family and Community Random Effects: A Bayesian Analysis. Journal of the American Statistical Association 2001; 96(453): 12-9.
24- Gohari Mr, Mahmoudi M, Mohammed K, Pasha E, Khodabakhshi R. Recurrence in Breast Cancer. Analysis with Frailty Model. Saudi Med J 2006; 27(8): 1187-93.
25- Rajaeefard A, Dehkordi B, Tabatabaee H, Zeighami B. Applying Parametric Models for Survival Analysis of Gastric Cancer. Feyz Med Sci J 2009; 13(2): 83-8. [Persian]
26- Cox Dr. Regression Models and Life-Tables. Journal of the Royal Statistical Society. 1972; 34(2): 187-220.
27- Nardi A, Schemper M. Comparing Cox and Parametric Models in Clinical Studies. Stat Med 2003; 22(23): 3597-610.
28- Who .Available At: https:// data.who.int/ dashboards/covid19/deaths. Accessed: Aug 21, 2024.
29- Zandkarimi E, Moradi G, Mohsenpour B. The Prognostic Factors Affecting the Survival of Kurdistan Province Covid-19 Patients: A Cross-Sectional Study from February to May 2020. Int J Health Policy Manag 2020; 11(4): 453-58.
30- Naeini Mb, Sahebi M, Nikbakht F, Jamshidi Z, Ahmadimanesh M, Hashemi M, et al. A Meta-Meta-Analysis: Evaluation of Meta-Analyses Published in the Effectiveness of Cardiovascular Comorbidities on The Severity of Covid-19. Obesity Medicine 2021; 22: 100323.
31- Shahid Z, Kalayanamitra R, Mcclafferty B, Kepko D, Ramgobin D, Patel R, et al. Covid-19 and Older Adults: What We Know. J Am Geriat Society 2020; 68(5): 926-9.
32- Altonen Bl, Arreglado Tm, Leroux O, Murray-Ramcharan M, Engdahl R. Characteristics, Comorbidities and Survival Analysis of Young Adults Hospitalized with Covid-19 in New York City. Plos One 2020; 15(12): E0243343.
33- Bansal M. Cardiovascular Disease and Covid-19. Diabetes & Metabolic Syndrome 2020; 14(3): 247-50.
34- Esenwa Cc, Elkind Ms. Inflammatory Risk Factors, Biomarkers and Associated Therapy in Ischaemic Stroke. Nat Rev Neurol 2016; 12(10): 594-604.
35- Lindsberg PJ, Grau AJ. Inflammation and Infections as Risk Factors for Ischemic Stroke. Stroke 2003; 34(10): 2518-32.
36- Soares Rcm, Mattos Lr, Raposo Lm. Risk Factors for Hospitalization and Mortality Due to Covid-19 in Espírito Santo State, Brazil. Am J Trop Med Hyg 2020; 103(3): 1184-90.
37- Drake Tm, Docherty Ab, Harrison Em, Quint Jk, Adamali H, Agnew S, et al. Outcome of Hospitalization for Covid-19 in Patients with Interstitial Lung Disease. An International Multicenter Study. Am J Respir Crit Care Med 2020; 202(12): 1656-65.
38- Zhang Jj, Cao Yy, Tan G, Dong X, Wang Bc, Lin J, et al. Clinical, Radiological, and Laboratory Characteristics and Risk Factors for Severity and Mortality of 289 Hospitalized Covid-19 Patients. Allergy 2021; 76(2): 533-50.
39- Salinas-Escudero G, Carrillo-Vega Mf, Granados-García V, Martínez-Valverde S, Toledano-Toledano F, Garduño-Espinosa J. A Survival Analysis of Covid-19 in the Mexican Population. Bmc Public Health 2020; 20(1): 1616.
40- Tian R, Wu W, Wang C, Pang H, Zhang Z, Xu H, et al. Clinical Characteristics and Survival Analysis in Critical and Non-Critical Patients with Covid-19 in Wuhan, China: A Single-Center Retrospective Case Control Study. Sci Rep 2020;10(1):17524.
41- Zhang Xm, Jiao J, Cao J, Huo Xp, Zhu C, Wu Xj, et al. Frailty as a Predictor of Mortality among Patients with Covid-19: A Systematic Review and Meta-Analysis. BMC Geriatrics 2021; 21(1): 186.
42- Saragih Id, Advani S, Saragih Is, Suarilah I, Susanto I, Lin Cj. Frailty as a Mortality Predictor in Older Adults with Covid-19: A Systematic Review and Meta-Analysis of Cohort Studies. Geriatric Nurs 2021; 42(5): 983-92.
متن کامل: (498 مشاهده)
مقدمه
بیماریهای ناشی از کروناویروس (Coronavirus)، از بیماریهای مشترک بین انسان و حیوان (Zoonosis) و عامل طیف وسیعی از بیماریهای ویروسی بوده که از سرماخوردگی خفیف تا بیماریهای شدیدتر مانند کروناویروس سندرم تنفسی خاورمیانه (MERS-CoV) و سندرم حاد تنفسی سارس (SARS-CoV) را ایجاد میکنند (2, 1). کروناویروسها مراقبت جدی در زمینه حدّت (Virulence)، بیماریزایی(Pathogenesis) و آسیبشناسی (pathology) بینالمللی را به خود معطوف داشته (5-3) و تهدیدی برای سلامت عمومی میباشند (7, 6).
کروناویروسها اولین بار با شیوع بیماری SARS خبرساز شدند. MERS-CoV بهعنوان عامل ایجاد عفونت شدید دستگاه تنفسی تحتانی در انسان، نرخ مرگ و میری بیشتر از SARS-CoV را به خود اختصاص داد (10-8). در سال 2002، سارس باعث ابتلای بیش از 8000 نفر و مرگ حدود 10% از مبتلایان شد. برای بار دوم و در سال 2012، کروناویروس MERS باعث ابتلای 2500 نفر و مرگ 35% از مبتلایان گردید (12, 11).
کروناویروس جدید (nCoV-2019) در ماه دسامبر سال 2019 و با مشاهدۀ مواردی از بیماری تنفسی در شهر ووهان چین توسط سازمان بهداشت جهانی (World Health Organization) شناسایی شد (4, 3, 1). در ژانویه 2020، سازمان بهداشت جهانی، ویروسِ عامل بیماری را کروناویروس جدید 2019 نامگذاری و همهگیری ناشی از آن را یک فوریت بهداشت عمومی تلقی نمود. در ماه فوریه، WHO این بیماری را یک سندرم تنفسی حاد شدید (Severe Acute Respiratory Syndrome) و تحت عنوان COVID-19 نامگذاری نمود. ویروس کووید-19 سومین ویروس بیماریزای زئونوز پس از SARS و MERS (سندرم تنفسی خاورمیانه) است (13). در حال حاضر، کووید-۱۹ خطرناکترین ویروس خانوادهCoronaviridae محسوب شده (14) که علاوه بر بروز عفونتهای شدید تنفسی و رودهای در حیوانات و انسانها (15) با میزان مرگ و میر مورد (CFR: Case Fatality Rate) 2/2 درصد در جهان و 3/6 درصد در ایران همراه است.
در بسیاری از مطالعات، جامعه موردنظر، همگن (Homogeneous) فرض میشود؛ به این معنی که خطر وقوع رخداد برای تمام افراد مورد مطالعه یکسان میباشد اما به دلیل وجود متغیرهایی نظیر خصوصیات فردی و ژنتیکی، وضعیت اقتصادی و اجتماعی، سبک زندگی و بسیاری از عوامل دیگر که قابلمشاهده و اندازهگیری نمیباشند، همگنی بین افراد وجود ندارد و باعث ایجاد ناهمگنی (Heterogeneity) در جامعه میگردد، اینگونه متغیرها را باید به کمک متغیرهای کمی، محاسبه و در مطالعه لحاظ کرد زیرا با حذف کردن و درنظرنگرفتن آنها، هنگام برآورد پارامترها به مشکل اریبی برمیخوریم. این متغیرها تحت عنوان شکنندگی (Frailty) نام دارند و میتوانند بهصورت تک متغیره و یا چند متغیره در مدل ظاهر گردند (16). روش دقیق و مشخصی جهت انتخاب توزیع متغیر شکنندگی در نظر گرفته نشده اما با توجه به اینکه تابع خطر مثبت است، لازم است توزیع متغیر شکنندگی نیز مثبت در نظر گرفته شود. در عمل به دلیل انعطافپذیری و کاربردهای مختلف توزیع گاما، میتوان این توزیع را برای متغیر شکنندگی انتخاب کرد. توزیع¬های دیگری از جمله توزیع مانای مثبت (Positive Stable)، لگ نرمال (Log-Normal)، معکوس گاوسین (Inverse Gaussian) و توزیع واریانس توانی (Power Variance) را میتوان برای متغیر شکنندگی در نظر گرفت (23-17).
در مطالعۀ اصغری و همکاران، پس از تشکیل تابع درستنمایی، برآورد پارامترها را با لحاظ کردن شکنندگی گاما محاسبه نمودند. بنابراین مدلهای شکنندگی به دلیل تصحیح قابلملاحظهای که در برآورد پارامترها اعمال میکنند و باعث کاهش اریبی در برآوردها میشوند، مدل مخاطرههای رقیب و برآوردهای مزبور را از این نظر بهبود میبخشند. گوهری و همکاران، با استفاده از مدل شکنندگی به تعیین ارزش فاکتورهای پیشآگهی شناخته شده در متاستاز سرطان سینه پرداختند. این مطالعه، نشان داد عوامل خطر شناخته شده در توصیف خطر متاستاز تا حدودی اهمیت داشته، درحالیکه عوامل ناشناخته مانند ژنتیک یا عوامل محیطی در توصیف خطر متاستاز در سرطان سینه بسیار مهم بودند (24).
با توجه به همهگیری جهانی کووید-19 و نوپدید بودن بیماری و متفاوت بودن عوامل اعلامشده در شدت بیماری در مطالعات مختلف، این مطالعه با هدف تحلیل بقای بیماران مبتلا به کووید-19 با استفاده از مدلهای پارامتری در حضور متغیر شکنندگی انجام گردید. با استفاده از مدل شکنندگی میتوان عوامل مؤثر بر بقای بیماران کووید-19 را – که با مدلهای معمولی بقا قابل تشخیص نمیباشند - شناسایی نموده؛ باعث افزایش بقای این بیماران شد.
روش بررسی
دادههای این پژوهش متعلق به یک مطالعه کوهورت آیندهنگر (تحلیل دادههای بقا) از کلیه بیماران مبتلا به کووید-19 در شهرستان فریدونشهر (واقع در غرب استان اصفهان) است. بدین ترتیب 880 بیمار مبتلا به کووید-19، شناساییشده از ابتدای اسفند سال 1398 تا ابتدای آذر سال 1399 با روش سرشماری وارد مطالعه شدند. وضعیت حیاتی بیماران (مرگ/ زندهبودن) حداقل به مدت 4 ماه مورد پیگیری قرار گرفت. پیشامد موردنظر (شکست) در این مطالعه، مرگ بیماران به علت کووید-19 بوده و متغیر پاسخ، زمان شروع علائم تا زمان مرگ یا سانسور شدگی در پایان مطالعه بود. موارد سانسور شده شامل بیمارانی بود که تا پایان مطالعه زنده ماندند. این بیماران با انجام آزمایش PCR (Polymerase Chain Reaction) بر 2269 فرد مشکوک به بیماری کووید-19 (بستری و سرپایی) که به بیمارستان حضرت رسول اکرم (ص) و مرکز منتخب نمونهگیری کووید-19 در مرکز بهداشت شهرستان فریدونشهر ارجاع گردیده بودند، شناسایی و اطلاعات آنها از پرونده الکترونیکی آنها بدون درج نام استخراج گردید. جهت تشخیص کووید-19 از آزمایش PCR توسط آزمایشگاه رفرنس مرکز بهداشت استان اصفهان استفاده گردید. طبق پروتکل کشوری از کلیۀ موارد مشکوک سرپایی و یا بستری دارای علائم بیماری تنفسی، نمونهگیری PCR با دو روش Nasopharyngeal swab - Oropharyngeal swab انجام و آزمایش SARS coronavirus 2 RNA-RT PCR بر روی نمونۀ تمامی بیماران انجام و جهت تأیید نتیجه، از متد توالی ژنی (Genes/Sequence(s)) استفاده شد. آنالیز بقا یکی از روشهای آماری است که برای مطالعه زمان تا وقوع یک پیشامد بهکار میرود (25). هدف اصلی مطالعات بقا تعیین اثر فاکتورهای مهم بیماری در مدت زمان وقوع یک پیشامد مانند عود بیماری، مرگ بیمار و غیره میباشد. مدلسازی در این نوع مطالعات، ابزاری است که به دنبال پاسخگویی به سئوالات مذکور میباشد. روشهای آماری جهت تحلیل دادههای بقا میتواند دربرگیرنده روشهای ناپارامتری، نیمهپارامتری و پارامتری باشد. دو رویکرد ناپارامتری شامل جداول طول عمر (Life table) و روش کاپلان-مایر، در حل مسائل بقا بسیار رایج بوده و کاربرد فراوانی دارند. مدل نیمه¬پارامتری خطرات متناسب کاکس نیز به دلایل مختلف از جمله پشتیبانی اکثر نرمافزارهای آماری و داشتن پیشفرضهای کمتر، کاربردیترین ابزار مدلسازی در مطالعات بقا بوده و محبوبیت ویژهای در بین محققین دارد. مدلهای دیگری که در آنها متغیر زمان بقا دارای یک توزیع احتمال مشخص مانند نمایی، وایبل، لگ لجستیک و غیره میباشد، وجود دارد. این مدلها به دلیل مشخص بودن توزیع زمان بقا به مدلهای پارامتری معروف هستند. این مدلها دارای پیشفرضهای بیشتری نسبت به مدل خطرات متناسب کاکس میباشند (27, 26). با استفاده از اطلاعات درجشده در پرونده بیماران و پیگیریهای انجامشده، متغیرهایی از قبیل؛ سن، جنس، وضعیت تأهل، تحصیلات، وضعیت بستری یا سرپایی بودن بیمار، نوع درمان تجویزشده (درمان تخصصی با داروهای ضدویروسی، درمان علامتی، عدم دریافت دارو)، تاریخ شروع علائم، تاریخ نمونهبرداری، تاریخ مرگ، فاصله زمانی بین شروع علائم تا مراجعه به پزشک و یا مرگ، فشارخون سیستولیک و دیاستولیک، قد، وزن و BMI (Body Mass Index)، قومیت بیمار (گرجی، لر، فارس، ترک)، سابقۀ تماس با دام، سابقۀ مسافرت در یک ماه اخیر، راه انتقال بیماری، شغل بیمار، درآمد، بارداری، محل سکونت (شهری، روستایی)، سابقۀ ابتلا به بیماری زمینهای (فشارخون بالا، دیابت، بیماری قلبی، بیماری تنفسی ریوی، بدخیمی، بیماری سیستم عصبی و بیماری کلیوی و کبدی) و زمان دسترسی به خدمات بیمارستانی (کمتر یا بیشتر از 1 ساعت) جمعآوری گردید. در این مطالعه، مقیاس اندازهگیری شدت بیماری، نوع درمان تجویزشده توسط پزشک متخصص بوده است (1. عدم دریافت دارو: در بیماران بدون علامت یا علائم بسیار خفیف 2. درمان علامتی: در بیماران با علائم متوسط ولی بدون نیاز به بستری 3. درمان تخصصی با داروهای ضدویروسی: در بیماران دارای علائم شدید و نیاز فوری به بستری)
تجزیه و تحلیل آماری
پس از جمع آوری دادهها و ورود آنها به نرمافزار version16 SPSS و پالایش دادهها، با استفاده از نرمافزار R (نسخه 4.3.2) مدلهای بقای پارامتری نمایی، وایبل، لگ-لجستیک و لگ- نرمال با و بدون متغیر شکنندگی ( با در نظر گرفتن توزیع گاما برای متغیر شکنندگی) برازش گردید.
نتایج
با انجام آزمایش PCR بر 2269 فرد مشکوک به بیماری کووید-19، 880 بیمار قطعی مبتلا به کووید-19 شناسایی شدند. 445 نفر از بیماران، مَرد (50/6%) و 435 نفر زن (49/4%) بودند. انحراف معیار± میانگین سنی کل بیماران؛ 21/23±48/9 سال، میانه سنی کل 48 سال و دامنۀ سنی 103 سال بود. انحراف معیار± میانگین سنی بیماران سرپایی، بیماران بستری و بیماران فوتشده به ترتیب 19/56±44/9، 19/61±65/6 و 15/06±75/1 محاسبه گردید. میانۀ فاصلۀ زمانی از شروع اولین علائم بالینی تا مراجعه به پزشک 3/0 روز و میانه فاصلۀ زمانی از شروع اولین علائم بالینی تا زمان مرگ 11 روز محاسبه گردید. در پایان مطالعه، 7% از بیماران (62 نفر) به علت کووید-19 فوت شدند (میزان بروز تجمعی). جدول 1، اطلاعات دموگرافیک شرکتکنندگان در مطالعه را نشان میدهد. انحرافمعیار± میانگین فشارخون سیستول و دیاستول بیماران به ترتیب 16/05±117/1 و 9/93±73/1 میلیمتر جیوه و انحرافمعیار± میانگین قد، وزن و شاخص توده بدنی به ترتیب 14/47±163/1 سانتیمتر، 15/81±69/9 کیلوگرم و 4/89±26/1 بود. طبق اطلاعات جدول 2، در مدل چند متغیره پارامتری، متغیر سن بالا و وضعیت بستری بیمار در هر 4 مدل و متغیر پیک بیماری در مدل نمایی به عنوان متغیرهای مؤثر بر زمان بروز مرگ شناخته شدند (0/05>P). در مطالعه حاضر، توزیع گاما به متغیر شکنندگی و توزیعهای نمایی، وایبل، لگنرمال و لگ-لجستیک به زمان بقای دادهها برازش داده شد و با استفاده ازشاخص آکائیکه به مقایسه مدلها پرداخته شد. با توجه به مقدار آکائیکه میتوان دریافت مدل شکنندگی گاما با توزیع لگ نرمال، انتخاب مناسبتری جهت برازش به دادههای کووید-19 در مطالعه حاضر میباشد زیرا مقدار آماره آکائیکه آن از سایر مدلها کمتر بهدست آمده است. در این مطالعه، کمترین مقدار تابع درستنمایی و ملاک AIC مربوط به مدل لگ نرمال بود. همچنین مدل شکنندگی در مقایسه با مدلهای معمولی بقا، انحراف معیار کوچکتری در بر داشت. در این بررسی، با ورود ترم شکنندگی (متغیر تصادفی Random effect) به مدل با توزیع گاما، ضریب تتا نشان دهنده معنیدار بودن مدل شکنندگی بود. در مدل نهایی لگ نرمال (بدون ورود ترم شکنندگی) دو متغیر سن و وضعیت بیمار به عنوان عوامل اثرگذار بر بقای بیماران مبتلا به کووید-19 شناخته شدند. در حالیکه در مدل شکنندگی، علاوه بر دو متغیر فوق، متغیر ابتلا به بیماری زمینهای (قلبی عروقی) نیز به عنوان یک فاکتور بسیار مهم شناخته گردید. به عبارت دیگر، این بیماری زمینهای است که باعث میشود افراد زودتر بمیرند. به عبارت دیگر، مدل دارای 2 متغیر سن و وضعیت بیمار (بستری / سرپایی) به تنهایی کارآیی لازم را نداشته و هنگامیکه 2 متغیر فوق به همراه متغیر شکنندگی وارد مدل گردید، متغیر تأثیرگذار دیگری به نام ابتلا به بیماری قلبی عروقی نیز وارد مدل شکنندگی شد. در نتیجه میتوان گفت بیماران کووید-19 که سابقۀ ابتلا به بیماری قلبی عروقی دارند در مقایسه با بیماران فاقد ابتلا به بیماری قلبی، بقای کمتری دارند (جدول 3).
بر اساس تجزیه و تحلیل رگرسیون چندگانه در جمعیت مورد بررسی، خطر مرگ در بیماران دارای سابقه بیماری قلبی 4/9 برابر افراد فاقد بیماری قلبی (HR=4.9 , 95% CI for HR: 2.21-10.98) و در بیمارانیکه نیاز به بستری داشتند 4/2 برابر موارد سرپایی بود (HR=4.2 , 95% CI for HR: 1.74-10.24). همچنین افزایش سن ابتلا با نرخ مرگ و میر رابطه مستقیم و معنیدار نشان داد (HR=1.05 , 95% CI for HR: 1.02-1.08). نمودار شمارۀ 1، مقایسۀ توابع بقا در مدل نهایی را به تفکیک ابتلا (یا عدم ابتلا) به بیماریهای قلبی عروقی نشان میدهد.
جدول 1: مشخصات دموگرافیک بیماران شرکت کننده در مطالعه*
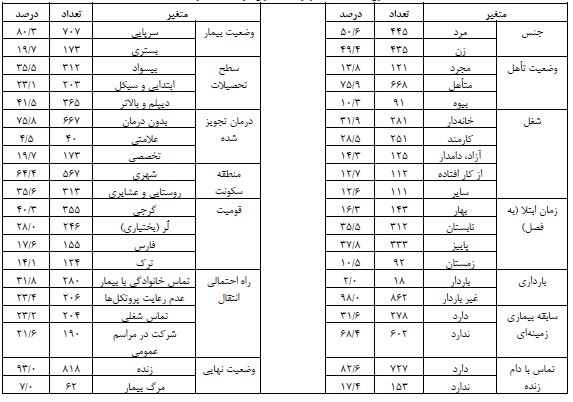
* جمع کلیه متغیرها 880 نفر میباشد.
جدول 2: مقایسه نتایج نهایی برازش شده مدلهای پارامتری در آنالیز چندمتغیره زمان مرگ در بیماران کووید (سطح خطای 0/05)
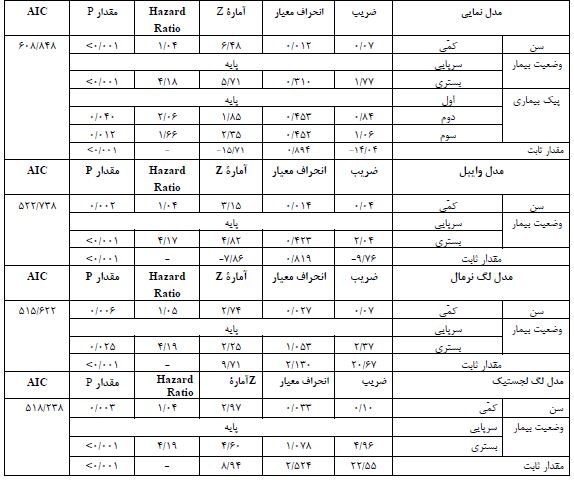
جدول 3: نتایج نهایی برازش شده مدل لگ لجستیک در حضور متغیر شکنندگی در آنالیز چندمتغیره زمان مرگ بیماران کووید (سطح خطای 0/05)
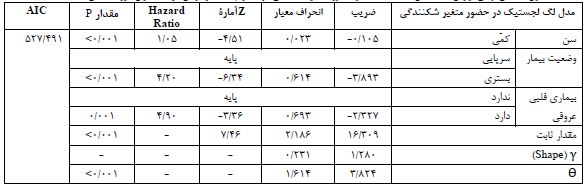
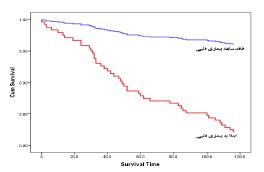
نمودار 1 : مقایسۀ توابع بقا در مدل نهایی بر اساس ابتلا به بیماری قلبی (سطح خطای 0/05)
بحث
در این مطالعه، میزان بروز کووید-19 در شهرستان فریدونشهر در طی یک سال، 244 در 10.000 برآورد گردید که از نرخ کشوری و جهانی بالاتر است. میزان بروز بیماری طبق آمارهای رسمی در ایران و جهان به ترتیب 206 و 154 در 10.000 است متوسط میزان کشندگی مورد (CFR: Case Fatality Rate) در شهرستان فریدونشهر 7% بوده که از میزان جهانی (2/2) و کشوری (3/5) بالاتر است (28). بر اساس تجزیه و تحلیل رگرسیون چندگانه در جمعیت مورد بررسی، خطر مرگ در بیماران دارای سابقه بیماری قلبی 9/4 برابر افراد فاقد بیماری قلبی بود که این تفاوت ازلحاظ آماری معنیدار بوده است (95% CI for HR=2.21-10.98، 4.9=HR). نتایج آنالیز بقای انجام شده در یک بررسی صورت گرفته در ایران، و همچنین نتایج یک «متا-آنالیز» در ایران، حاکی از اهمیت نقش بیماریهای قلبی عروقی بر بقای بیماران مبتلا به کووید-19 بود (31-29). مطالعات متعددی بر نقش بیماریهای قلبی در شدت وخامت بیماری کووید-19 و بقای بیماران تأکید داشتهاند (33, 32). اگرچه ریهها ارگانهای اصلی درگیر در سندرم دیسترس تنفسی حاد ناشی از عفونت کووید-19 هستند ولی عفونت میتواند مکانیسمهای التهابی و ایمنی ایجاد کند. در مقایسه با افراد سالم، بیماران مبتلا به بیماریهای قلبی عمدتاً افراد سالخورده هستند که به نسبت، بیشتر به بیماریهای مزمنی نظیر فشارخون بالا، چربی بالا، کاهش عملکرد سیستم ایمنی و دیابت مبتلا هستند. بنابراین این افراد بیشتر مستعد ابتلا به عفونت میباشند. برخی از عفونتهای مزمن طولانیمدت میتوانند خطر سکته را افزایش دهند. همچنین عفونتهای حاد و شدید نظیر کووید-19 میتوانند با افزایش لخته شدن خون منجر به تصلب شرایین شوند (35, 34). در مطالعۀ حاضر، انحراف معیار± میانگین سن در بیماران کووید مبتلا به بیماری قلبی و غیر مبتلا به بیماری قلبی به ترتیب 15/15±66/7 و 20/98±47/4 سال بوده که از نظر آماری، معنیدار میباشد (P<0.001).
افزایش شدت بیماری، میتواند منجر به بستری بیمار و افزایش میزان مرگ و میر بیمارستانی گردد. خطر مرگ در بیمارانیکه نیاز به بستری داشتند 4/2 برابر موارد سرپایی است (HR=4.2 ,95% CI for HR=1.74-10.24). در یک بررسی مبتنی بر جمعیت در برزیل، افزایش مرگ و میر در بیماران بستری با سن این بیماران ارتباط معنیدار داشت (36). در یک مطالعۀ چندمرکزی بینالمللی در اروپا، بقای بیماران بستری با علائم ریوی کاهش قابلتوجهی در مقایسه با سایر بیماران نشان میداد (37). همچنین در این مطالعه طبق آزمون ANOVA مشاهده گردید که زمان مراجعه به پزشک بر مرگ بیماران تأثیر داشته و نسبت مرگ در بیمارانی که در کمتر از 3 روز پس از شروع علائم بالینی به مراکز درمانی مراجعه کردهاند، بیش از سایر بیماران بوده است (0.008=P). این امر میتواند به دلیل افزایش شدت و وخامت بیماری باشد که بیمار را در روزهای اول مجبور به مراجعۀ سریعتر به دریافت خدمات درمانی و درنهایت بستری بیمار مینماید. در این مطالعه، افزایش سن ابتلا با نرخ مرگ و میر رابطۀ مستقیم و معنیدار نشان داد (95% CI for HR=1.02-1.08، 1.05=HR). در طبقهبندی سنی در این بررسی میانگین سنی بیماران فوتشده در مطالعۀ حاضر 75 سال بود که 30 سال از متوسط سن بیماران سرپایی بالاتر است. نتایج اکثر مطالعات داخلی و خارجی نشان میدهد خطر مرگ با بالا رفتن سن بیمار، افزایش مییابد (40-38، 35، 34، 31، 29). در این بررسی جهت برازش مدلهای پارامتری به دادههای زمان تشخیص مرگ همانند ابتدا در آنالیز تک متغیره، متغیرهای موثر بر زمان مرگ مشخص گردیده، سپس این متغیرها در مدلهای چند متغیره پارامتری برای آنالیز نتایج وارد شدند. در تمامی مدلهای برازش شده، متغیرهای سن، وضعیت تأهل، سطح تحصیلات، شغل، وضعیت بیمار، نوع درمان، ابتلا به بیماری زمینهای، فاصله تا مرکز بهداشتی درمانی، وضعیت مالی بیمار و پیک (موج) بیماری در شهرستان معنیدار بودند (P<0.20). متغیرهای فوق به مدلهای رگرسیونی چندگانه وارد شدند. در مدل چند متغیرۀ پارامتری، متغیر سن بالا و وضعیت بستری بیمار در هر 4 مدل و متغیر پیک بیماری در مدل نمایی به عنوان متغیرهای مؤثر بر زمان بروز مرگ شناخته شدند (0/05>P). در مرحلۀ بعد، متغیر شکنندگی در مدل وارد و توزیع گاما به متغیر شکنندگی و توزیعهای نمایی، وایبل، لگنرمال و لگلجستیک به زمان بقای دادهها برازش داده شد و با استفاده ازشاخص آکائیکه به مقایسه مدلها پرداخته شد. با توجه به مقدار آکائیکه، مدل شکنندگی گاما با توزیع لگ نرمال با کمترین مقدار AIC به عنوان انتخاب مناسبتری جهت برازش به دادههای کووید-19 شناسایی گردید. با توجه به ویژگی مهم مدل لگنرمال یعنی افزایش رخداد در شروع پیگیری و در ادامه کاهش رخداد، برازش مناسب مدل لگنرمال گویای مرگ و میر مبتلایان به کووید-19 در روزها و هفتههای نخست پس از ابتلا و میرایی در روزها و هفتههای پایانی کمتر نشان داده شد. در این مطالعه، مدل شکنندگی در مقایسه با مدلهای معمولی بقا (نیمه پارامتری و پارامتری) انحراف معیار کوچکتری در بر داشت. در مدل شکنندگی، علاوه بر دو متغیر سن و وضعیت بیماری، متغیر ابتلا به بیماری زمینهای (قلبی عروقی) به عنوان فاکتور بسیار مهم بر بقای بیماران مبتلا به کووید-19 شناخته شد. به عبارت دیگر، بیماران مبتلا به کووید-19 که سابقه ابتلا به بیماری قلبی عروقی دارند در مقایسه با بیماران بدون سابقۀ ابتلا به بیماری قلبی، بقای کمتری دارند (جدول 2). در دو متا آنالیز انجام شده در سال 2021 توسط Zhang (41) و Saragih (42)، متغیر شکنندگی به عنوان یک متغیر پیشبینی کننده در مرگ و میر بیماران مبتلا به کووید-19 معرفی شده است. نتایج حاصل از متا آنالیز انجام شده بر 22 مطالعه توسط Saragih که بر روی بیش از 924000 بیمار مبتلا به کووید انجام گردید، متغیر سن به عنوان یک فاکتور پیشبینی کننده در مرگ و میر بیماران مبتلا به کووید-19 تشخیص داده شد (OR=5.76) (42).
نتیجهگیری
بیماران مسن و بیمارانی که نیاز به بستری دارند بهویژه افرادیکه سابقۀ ابتلا به بیماری قلبی دارند نسبت به سایر گروهها در معرض خطر بالای مرگ قرار دارند. این بیماران علاوه بر غربالگری منظم، نیاز به نظارت فعال بهویژه در زمان بستری خواهند داشت. با ورود متغیر شکنندگی به مدل، متغیر ابتلا به بیماری زمینهای (قلبی عروقی) به عنوان یک فاکتور بسیار مهم در بقای بیماران شناخته شد؛ در حالی¬که بدون متغیر شکنندگی، این متغیر نادیده گرفته میشد. همچنین از خصوصیات مدل لگ نرمال، افزایش رخداد در شروع پیگیری و کاهش آن در ادامه پیگیری میباشد که با روند مرگ و میر در بیماری کووید-19 سازگار میباشد.
سپاسگزاری
بدینوسیله از کارکنان محترم واحد کروناویروس آزمایشگاه مرکز بهداشت استان اصفهان تشکر و سپاسگزاری میشود. این مطالعه قسمتی از پایاننامۀ مصوب معاونت پژوهشی دانشگاه علوم پزشکی ایران با کد پژوهشی 20259 جهت اخذ مقطع MPH عمومی است.
حامی مالی: ندارد.
تعارض در منافع: وجود ندارد.
ملاحظات اخلاقی
این پژوهش، پس از طرح در شورای برنامهریزی دانشکدۀ بهداشت دانشگاه علوم پزشکی ایران با کد پژوهشی 20259 و کد مصوبه اخلاق IR.IUMS.REC.1399.1426 تصویب گردید. با توجه به اینکه آنالیز آماری فقط بر روی دادههای جمعی بیماران انجام و بهجای نام بیماران از سیستم کددهی استفاده شد، این مطالعه فاقد مشکل اخلاقی است. با توجه به پیگیریهای انجامشده توسط واحد مبارزه با بیماریهای مرکز بهداشت شهرستان فریدونشهر، تعداد و درصد دادههای ازدسترفته، صفر است. از محدودیتهای مطالعه میتوان به عدم استفاده از متغیرهای بیوشیمیایی و فاکتورهای آزمایشگاهی نمونهها اشاره کرد.
مشارکت نویسندگان
جمیله ابوالقاسمی در ارائه ایده، صادق کارگریان/ جمیله ابوالقاسمی/ ملیحه حسننژاد در طراحی مطالعه، صادق کارگریان در جمعآوری دادهها، جمیله ابوالقاسمی/ صادق کارگریان در تجزیه و تحلیل دادهها مشارکت داشته و همه نویسندگان در تدوین، ویرایش اولیه و نهایی مقاله و پاسخگویی به سوالات مرتبط با مقاله سهیم هستند.
بیماریهای ناشی از کروناویروس (Coronavirus)، از بیماریهای مشترک بین انسان و حیوان (Zoonosis) و عامل طیف وسیعی از بیماریهای ویروسی بوده که از سرماخوردگی خفیف تا بیماریهای شدیدتر مانند کروناویروس سندرم تنفسی خاورمیانه (MERS-CoV) و سندرم حاد تنفسی سارس (SARS-CoV) را ایجاد میکنند (2, 1). کروناویروسها مراقبت جدی در زمینه حدّت (Virulence)، بیماریزایی(Pathogenesis) و آسیبشناسی (pathology) بینالمللی را به خود معطوف داشته (5-3) و تهدیدی برای سلامت عمومی میباشند (7, 6).
کروناویروسها اولین بار با شیوع بیماری SARS خبرساز شدند. MERS-CoV بهعنوان عامل ایجاد عفونت شدید دستگاه تنفسی تحتانی در انسان، نرخ مرگ و میری بیشتر از SARS-CoV را به خود اختصاص داد (10-8). در سال 2002، سارس باعث ابتلای بیش از 8000 نفر و مرگ حدود 10% از مبتلایان شد. برای بار دوم و در سال 2012، کروناویروس MERS باعث ابتلای 2500 نفر و مرگ 35% از مبتلایان گردید (12, 11).
کروناویروس جدید (nCoV-2019) در ماه دسامبر سال 2019 و با مشاهدۀ مواردی از بیماری تنفسی در شهر ووهان چین توسط سازمان بهداشت جهانی (World Health Organization) شناسایی شد (4, 3, 1). در ژانویه 2020، سازمان بهداشت جهانی، ویروسِ عامل بیماری را کروناویروس جدید 2019 نامگذاری و همهگیری ناشی از آن را یک فوریت بهداشت عمومی تلقی نمود. در ماه فوریه، WHO این بیماری را یک سندرم تنفسی حاد شدید (Severe Acute Respiratory Syndrome) و تحت عنوان COVID-19 نامگذاری نمود. ویروس کووید-19 سومین ویروس بیماریزای زئونوز پس از SARS و MERS (سندرم تنفسی خاورمیانه) است (13). در حال حاضر، کووید-۱۹ خطرناکترین ویروس خانوادهCoronaviridae محسوب شده (14) که علاوه بر بروز عفونتهای شدید تنفسی و رودهای در حیوانات و انسانها (15) با میزان مرگ و میر مورد (CFR: Case Fatality Rate) 2/2 درصد در جهان و 3/6 درصد در ایران همراه است.
در بسیاری از مطالعات، جامعه موردنظر، همگن (Homogeneous) فرض میشود؛ به این معنی که خطر وقوع رخداد برای تمام افراد مورد مطالعه یکسان میباشد اما به دلیل وجود متغیرهایی نظیر خصوصیات فردی و ژنتیکی، وضعیت اقتصادی و اجتماعی، سبک زندگی و بسیاری از عوامل دیگر که قابلمشاهده و اندازهگیری نمیباشند، همگنی بین افراد وجود ندارد و باعث ایجاد ناهمگنی (Heterogeneity) در جامعه میگردد، اینگونه متغیرها را باید به کمک متغیرهای کمی، محاسبه و در مطالعه لحاظ کرد زیرا با حذف کردن و درنظرنگرفتن آنها، هنگام برآورد پارامترها به مشکل اریبی برمیخوریم. این متغیرها تحت عنوان شکنندگی (Frailty) نام دارند و میتوانند بهصورت تک متغیره و یا چند متغیره در مدل ظاهر گردند (16). روش دقیق و مشخصی جهت انتخاب توزیع متغیر شکنندگی در نظر گرفته نشده اما با توجه به اینکه تابع خطر مثبت است، لازم است توزیع متغیر شکنندگی نیز مثبت در نظر گرفته شود. در عمل به دلیل انعطافپذیری و کاربردهای مختلف توزیع گاما، میتوان این توزیع را برای متغیر شکنندگی انتخاب کرد. توزیع¬های دیگری از جمله توزیع مانای مثبت (Positive Stable)، لگ نرمال (Log-Normal)، معکوس گاوسین (Inverse Gaussian) و توزیع واریانس توانی (Power Variance) را میتوان برای متغیر شکنندگی در نظر گرفت (23-17).
در مطالعۀ اصغری و همکاران، پس از تشکیل تابع درستنمایی، برآورد پارامترها را با لحاظ کردن شکنندگی گاما محاسبه نمودند. بنابراین مدلهای شکنندگی به دلیل تصحیح قابلملاحظهای که در برآورد پارامترها اعمال میکنند و باعث کاهش اریبی در برآوردها میشوند، مدل مخاطرههای رقیب و برآوردهای مزبور را از این نظر بهبود میبخشند. گوهری و همکاران، با استفاده از مدل شکنندگی به تعیین ارزش فاکتورهای پیشآگهی شناخته شده در متاستاز سرطان سینه پرداختند. این مطالعه، نشان داد عوامل خطر شناخته شده در توصیف خطر متاستاز تا حدودی اهمیت داشته، درحالیکه عوامل ناشناخته مانند ژنتیک یا عوامل محیطی در توصیف خطر متاستاز در سرطان سینه بسیار مهم بودند (24).
با توجه به همهگیری جهانی کووید-19 و نوپدید بودن بیماری و متفاوت بودن عوامل اعلامشده در شدت بیماری در مطالعات مختلف، این مطالعه با هدف تحلیل بقای بیماران مبتلا به کووید-19 با استفاده از مدلهای پارامتری در حضور متغیر شکنندگی انجام گردید. با استفاده از مدل شکنندگی میتوان عوامل مؤثر بر بقای بیماران کووید-19 را – که با مدلهای معمولی بقا قابل تشخیص نمیباشند - شناسایی نموده؛ باعث افزایش بقای این بیماران شد.
روش بررسی
دادههای این پژوهش متعلق به یک مطالعه کوهورت آیندهنگر (تحلیل دادههای بقا) از کلیه بیماران مبتلا به کووید-19 در شهرستان فریدونشهر (واقع در غرب استان اصفهان) است. بدین ترتیب 880 بیمار مبتلا به کووید-19، شناساییشده از ابتدای اسفند سال 1398 تا ابتدای آذر سال 1399 با روش سرشماری وارد مطالعه شدند. وضعیت حیاتی بیماران (مرگ/ زندهبودن) حداقل به مدت 4 ماه مورد پیگیری قرار گرفت. پیشامد موردنظر (شکست) در این مطالعه، مرگ بیماران به علت کووید-19 بوده و متغیر پاسخ، زمان شروع علائم تا زمان مرگ یا سانسور شدگی در پایان مطالعه بود. موارد سانسور شده شامل بیمارانی بود که تا پایان مطالعه زنده ماندند. این بیماران با انجام آزمایش PCR (Polymerase Chain Reaction) بر 2269 فرد مشکوک به بیماری کووید-19 (بستری و سرپایی) که به بیمارستان حضرت رسول اکرم (ص) و مرکز منتخب نمونهگیری کووید-19 در مرکز بهداشت شهرستان فریدونشهر ارجاع گردیده بودند، شناسایی و اطلاعات آنها از پرونده الکترونیکی آنها بدون درج نام استخراج گردید. جهت تشخیص کووید-19 از آزمایش PCR توسط آزمایشگاه رفرنس مرکز بهداشت استان اصفهان استفاده گردید. طبق پروتکل کشوری از کلیۀ موارد مشکوک سرپایی و یا بستری دارای علائم بیماری تنفسی، نمونهگیری PCR با دو روش Nasopharyngeal swab - Oropharyngeal swab انجام و آزمایش SARS coronavirus 2 RNA-RT PCR بر روی نمونۀ تمامی بیماران انجام و جهت تأیید نتیجه، از متد توالی ژنی (Genes/Sequence(s)) استفاده شد. آنالیز بقا یکی از روشهای آماری است که برای مطالعه زمان تا وقوع یک پیشامد بهکار میرود (25). هدف اصلی مطالعات بقا تعیین اثر فاکتورهای مهم بیماری در مدت زمان وقوع یک پیشامد مانند عود بیماری، مرگ بیمار و غیره میباشد. مدلسازی در این نوع مطالعات، ابزاری است که به دنبال پاسخگویی به سئوالات مذکور میباشد. روشهای آماری جهت تحلیل دادههای بقا میتواند دربرگیرنده روشهای ناپارامتری، نیمهپارامتری و پارامتری باشد. دو رویکرد ناپارامتری شامل جداول طول عمر (Life table) و روش کاپلان-مایر، در حل مسائل بقا بسیار رایج بوده و کاربرد فراوانی دارند. مدل نیمه¬پارامتری خطرات متناسب کاکس نیز به دلایل مختلف از جمله پشتیبانی اکثر نرمافزارهای آماری و داشتن پیشفرضهای کمتر، کاربردیترین ابزار مدلسازی در مطالعات بقا بوده و محبوبیت ویژهای در بین محققین دارد. مدلهای دیگری که در آنها متغیر زمان بقا دارای یک توزیع احتمال مشخص مانند نمایی، وایبل، لگ لجستیک و غیره میباشد، وجود دارد. این مدلها به دلیل مشخص بودن توزیع زمان بقا به مدلهای پارامتری معروف هستند. این مدلها دارای پیشفرضهای بیشتری نسبت به مدل خطرات متناسب کاکس میباشند (27, 26). با استفاده از اطلاعات درجشده در پرونده بیماران و پیگیریهای انجامشده، متغیرهایی از قبیل؛ سن، جنس، وضعیت تأهل، تحصیلات، وضعیت بستری یا سرپایی بودن بیمار، نوع درمان تجویزشده (درمان تخصصی با داروهای ضدویروسی، درمان علامتی، عدم دریافت دارو)، تاریخ شروع علائم، تاریخ نمونهبرداری، تاریخ مرگ، فاصله زمانی بین شروع علائم تا مراجعه به پزشک و یا مرگ، فشارخون سیستولیک و دیاستولیک، قد، وزن و BMI (Body Mass Index)، قومیت بیمار (گرجی، لر، فارس، ترک)، سابقۀ تماس با دام، سابقۀ مسافرت در یک ماه اخیر، راه انتقال بیماری، شغل بیمار، درآمد، بارداری، محل سکونت (شهری، روستایی)، سابقۀ ابتلا به بیماری زمینهای (فشارخون بالا، دیابت، بیماری قلبی، بیماری تنفسی ریوی، بدخیمی، بیماری سیستم عصبی و بیماری کلیوی و کبدی) و زمان دسترسی به خدمات بیمارستانی (کمتر یا بیشتر از 1 ساعت) جمعآوری گردید. در این مطالعه، مقیاس اندازهگیری شدت بیماری، نوع درمان تجویزشده توسط پزشک متخصص بوده است (1. عدم دریافت دارو: در بیماران بدون علامت یا علائم بسیار خفیف 2. درمان علامتی: در بیماران با علائم متوسط ولی بدون نیاز به بستری 3. درمان تخصصی با داروهای ضدویروسی: در بیماران دارای علائم شدید و نیاز فوری به بستری)
تجزیه و تحلیل آماری
پس از جمع آوری دادهها و ورود آنها به نرمافزار version16 SPSS و پالایش دادهها، با استفاده از نرمافزار R (نسخه 4.3.2) مدلهای بقای پارامتری نمایی، وایبل، لگ-لجستیک و لگ- نرمال با و بدون متغیر شکنندگی ( با در نظر گرفتن توزیع گاما برای متغیر شکنندگی) برازش گردید.
نتایج
با انجام آزمایش PCR بر 2269 فرد مشکوک به بیماری کووید-19، 880 بیمار قطعی مبتلا به کووید-19 شناسایی شدند. 445 نفر از بیماران، مَرد (50/6%) و 435 نفر زن (49/4%) بودند. انحراف معیار± میانگین سنی کل بیماران؛ 21/23±48/9 سال، میانه سنی کل 48 سال و دامنۀ سنی 103 سال بود. انحراف معیار± میانگین سنی بیماران سرپایی، بیماران بستری و بیماران فوتشده به ترتیب 19/56±44/9، 19/61±65/6 و 15/06±75/1 محاسبه گردید. میانۀ فاصلۀ زمانی از شروع اولین علائم بالینی تا مراجعه به پزشک 3/0 روز و میانه فاصلۀ زمانی از شروع اولین علائم بالینی تا زمان مرگ 11 روز محاسبه گردید. در پایان مطالعه، 7% از بیماران (62 نفر) به علت کووید-19 فوت شدند (میزان بروز تجمعی). جدول 1، اطلاعات دموگرافیک شرکتکنندگان در مطالعه را نشان میدهد. انحرافمعیار± میانگین فشارخون سیستول و دیاستول بیماران به ترتیب 16/05±117/1 و 9/93±73/1 میلیمتر جیوه و انحرافمعیار± میانگین قد، وزن و شاخص توده بدنی به ترتیب 14/47±163/1 سانتیمتر، 15/81±69/9 کیلوگرم و 4/89±26/1 بود. طبق اطلاعات جدول 2، در مدل چند متغیره پارامتری، متغیر سن بالا و وضعیت بستری بیمار در هر 4 مدل و متغیر پیک بیماری در مدل نمایی به عنوان متغیرهای مؤثر بر زمان بروز مرگ شناخته شدند (0/05>P). در مطالعه حاضر، توزیع گاما به متغیر شکنندگی و توزیعهای نمایی، وایبل، لگنرمال و لگ-لجستیک به زمان بقای دادهها برازش داده شد و با استفاده ازشاخص آکائیکه به مقایسه مدلها پرداخته شد. با توجه به مقدار آکائیکه میتوان دریافت مدل شکنندگی گاما با توزیع لگ نرمال، انتخاب مناسبتری جهت برازش به دادههای کووید-19 در مطالعه حاضر میباشد زیرا مقدار آماره آکائیکه آن از سایر مدلها کمتر بهدست آمده است. در این مطالعه، کمترین مقدار تابع درستنمایی و ملاک AIC مربوط به مدل لگ نرمال بود. همچنین مدل شکنندگی در مقایسه با مدلهای معمولی بقا، انحراف معیار کوچکتری در بر داشت. در این بررسی، با ورود ترم شکنندگی (متغیر تصادفی Random effect) به مدل با توزیع گاما، ضریب تتا نشان دهنده معنیدار بودن مدل شکنندگی بود. در مدل نهایی لگ نرمال (بدون ورود ترم شکنندگی) دو متغیر سن و وضعیت بیمار به عنوان عوامل اثرگذار بر بقای بیماران مبتلا به کووید-19 شناخته شدند. در حالیکه در مدل شکنندگی، علاوه بر دو متغیر فوق، متغیر ابتلا به بیماری زمینهای (قلبی عروقی) نیز به عنوان یک فاکتور بسیار مهم شناخته گردید. به عبارت دیگر، این بیماری زمینهای است که باعث میشود افراد زودتر بمیرند. به عبارت دیگر، مدل دارای 2 متغیر سن و وضعیت بیمار (بستری / سرپایی) به تنهایی کارآیی لازم را نداشته و هنگامیکه 2 متغیر فوق به همراه متغیر شکنندگی وارد مدل گردید، متغیر تأثیرگذار دیگری به نام ابتلا به بیماری قلبی عروقی نیز وارد مدل شکنندگی شد. در نتیجه میتوان گفت بیماران کووید-19 که سابقۀ ابتلا به بیماری قلبی عروقی دارند در مقایسه با بیماران فاقد ابتلا به بیماری قلبی، بقای کمتری دارند (جدول 3).
بر اساس تجزیه و تحلیل رگرسیون چندگانه در جمعیت مورد بررسی، خطر مرگ در بیماران دارای سابقه بیماری قلبی 4/9 برابر افراد فاقد بیماری قلبی (HR=4.9 , 95% CI for HR: 2.21-10.98) و در بیمارانیکه نیاز به بستری داشتند 4/2 برابر موارد سرپایی بود (HR=4.2 , 95% CI for HR: 1.74-10.24). همچنین افزایش سن ابتلا با نرخ مرگ و میر رابطه مستقیم و معنیدار نشان داد (HR=1.05 , 95% CI for HR: 1.02-1.08). نمودار شمارۀ 1، مقایسۀ توابع بقا در مدل نهایی را به تفکیک ابتلا (یا عدم ابتلا) به بیماریهای قلبی عروقی نشان میدهد.
جدول 1: مشخصات دموگرافیک بیماران شرکت کننده در مطالعه*

* جمع کلیه متغیرها 880 نفر میباشد.
جدول 2: مقایسه نتایج نهایی برازش شده مدلهای پارامتری در آنالیز چندمتغیره زمان مرگ در بیماران کووید (سطح خطای 0/05)

جدول 3: نتایج نهایی برازش شده مدل لگ لجستیک در حضور متغیر شکنندگی در آنالیز چندمتغیره زمان مرگ بیماران کووید (سطح خطای 0/05)


نمودار 1 : مقایسۀ توابع بقا در مدل نهایی بر اساس ابتلا به بیماری قلبی (سطح خطای 0/05)
بحث
در این مطالعه، میزان بروز کووید-19 در شهرستان فریدونشهر در طی یک سال، 244 در 10.000 برآورد گردید که از نرخ کشوری و جهانی بالاتر است. میزان بروز بیماری طبق آمارهای رسمی در ایران و جهان به ترتیب 206 و 154 در 10.000 است متوسط میزان کشندگی مورد (CFR: Case Fatality Rate) در شهرستان فریدونشهر 7% بوده که از میزان جهانی (2/2) و کشوری (3/5) بالاتر است (28). بر اساس تجزیه و تحلیل رگرسیون چندگانه در جمعیت مورد بررسی، خطر مرگ در بیماران دارای سابقه بیماری قلبی 9/4 برابر افراد فاقد بیماری قلبی بود که این تفاوت ازلحاظ آماری معنیدار بوده است (95% CI for HR=2.21-10.98، 4.9=HR). نتایج آنالیز بقای انجام شده در یک بررسی صورت گرفته در ایران، و همچنین نتایج یک «متا-آنالیز» در ایران، حاکی از اهمیت نقش بیماریهای قلبی عروقی بر بقای بیماران مبتلا به کووید-19 بود (31-29). مطالعات متعددی بر نقش بیماریهای قلبی در شدت وخامت بیماری کووید-19 و بقای بیماران تأکید داشتهاند (33, 32). اگرچه ریهها ارگانهای اصلی درگیر در سندرم دیسترس تنفسی حاد ناشی از عفونت کووید-19 هستند ولی عفونت میتواند مکانیسمهای التهابی و ایمنی ایجاد کند. در مقایسه با افراد سالم، بیماران مبتلا به بیماریهای قلبی عمدتاً افراد سالخورده هستند که به نسبت، بیشتر به بیماریهای مزمنی نظیر فشارخون بالا، چربی بالا، کاهش عملکرد سیستم ایمنی و دیابت مبتلا هستند. بنابراین این افراد بیشتر مستعد ابتلا به عفونت میباشند. برخی از عفونتهای مزمن طولانیمدت میتوانند خطر سکته را افزایش دهند. همچنین عفونتهای حاد و شدید نظیر کووید-19 میتوانند با افزایش لخته شدن خون منجر به تصلب شرایین شوند (35, 34). در مطالعۀ حاضر، انحراف معیار± میانگین سن در بیماران کووید مبتلا به بیماری قلبی و غیر مبتلا به بیماری قلبی به ترتیب 15/15±66/7 و 20/98±47/4 سال بوده که از نظر آماری، معنیدار میباشد (P<0.001).
افزایش شدت بیماری، میتواند منجر به بستری بیمار و افزایش میزان مرگ و میر بیمارستانی گردد. خطر مرگ در بیمارانیکه نیاز به بستری داشتند 4/2 برابر موارد سرپایی است (HR=4.2 ,95% CI for HR=1.74-10.24). در یک بررسی مبتنی بر جمعیت در برزیل، افزایش مرگ و میر در بیماران بستری با سن این بیماران ارتباط معنیدار داشت (36). در یک مطالعۀ چندمرکزی بینالمللی در اروپا، بقای بیماران بستری با علائم ریوی کاهش قابلتوجهی در مقایسه با سایر بیماران نشان میداد (37). همچنین در این مطالعه طبق آزمون ANOVA مشاهده گردید که زمان مراجعه به پزشک بر مرگ بیماران تأثیر داشته و نسبت مرگ در بیمارانی که در کمتر از 3 روز پس از شروع علائم بالینی به مراکز درمانی مراجعه کردهاند، بیش از سایر بیماران بوده است (0.008=P). این امر میتواند به دلیل افزایش شدت و وخامت بیماری باشد که بیمار را در روزهای اول مجبور به مراجعۀ سریعتر به دریافت خدمات درمانی و درنهایت بستری بیمار مینماید. در این مطالعه، افزایش سن ابتلا با نرخ مرگ و میر رابطۀ مستقیم و معنیدار نشان داد (95% CI for HR=1.02-1.08، 1.05=HR). در طبقهبندی سنی در این بررسی میانگین سنی بیماران فوتشده در مطالعۀ حاضر 75 سال بود که 30 سال از متوسط سن بیماران سرپایی بالاتر است. نتایج اکثر مطالعات داخلی و خارجی نشان میدهد خطر مرگ با بالا رفتن سن بیمار، افزایش مییابد (40-38، 35، 34، 31، 29). در این بررسی جهت برازش مدلهای پارامتری به دادههای زمان تشخیص مرگ همانند ابتدا در آنالیز تک متغیره، متغیرهای موثر بر زمان مرگ مشخص گردیده، سپس این متغیرها در مدلهای چند متغیره پارامتری برای آنالیز نتایج وارد شدند. در تمامی مدلهای برازش شده، متغیرهای سن، وضعیت تأهل، سطح تحصیلات، شغل، وضعیت بیمار، نوع درمان، ابتلا به بیماری زمینهای، فاصله تا مرکز بهداشتی درمانی، وضعیت مالی بیمار و پیک (موج) بیماری در شهرستان معنیدار بودند (P<0.20). متغیرهای فوق به مدلهای رگرسیونی چندگانه وارد شدند. در مدل چند متغیرۀ پارامتری، متغیر سن بالا و وضعیت بستری بیمار در هر 4 مدل و متغیر پیک بیماری در مدل نمایی به عنوان متغیرهای مؤثر بر زمان بروز مرگ شناخته شدند (0/05>P). در مرحلۀ بعد، متغیر شکنندگی در مدل وارد و توزیع گاما به متغیر شکنندگی و توزیعهای نمایی، وایبل، لگنرمال و لگلجستیک به زمان بقای دادهها برازش داده شد و با استفاده ازشاخص آکائیکه به مقایسه مدلها پرداخته شد. با توجه به مقدار آکائیکه، مدل شکنندگی گاما با توزیع لگ نرمال با کمترین مقدار AIC به عنوان انتخاب مناسبتری جهت برازش به دادههای کووید-19 شناسایی گردید. با توجه به ویژگی مهم مدل لگنرمال یعنی افزایش رخداد در شروع پیگیری و در ادامه کاهش رخداد، برازش مناسب مدل لگنرمال گویای مرگ و میر مبتلایان به کووید-19 در روزها و هفتههای نخست پس از ابتلا و میرایی در روزها و هفتههای پایانی کمتر نشان داده شد. در این مطالعه، مدل شکنندگی در مقایسه با مدلهای معمولی بقا (نیمه پارامتری و پارامتری) انحراف معیار کوچکتری در بر داشت. در مدل شکنندگی، علاوه بر دو متغیر سن و وضعیت بیماری، متغیر ابتلا به بیماری زمینهای (قلبی عروقی) به عنوان فاکتور بسیار مهم بر بقای بیماران مبتلا به کووید-19 شناخته شد. به عبارت دیگر، بیماران مبتلا به کووید-19 که سابقه ابتلا به بیماری قلبی عروقی دارند در مقایسه با بیماران بدون سابقۀ ابتلا به بیماری قلبی، بقای کمتری دارند (جدول 2). در دو متا آنالیز انجام شده در سال 2021 توسط Zhang (41) و Saragih (42)، متغیر شکنندگی به عنوان یک متغیر پیشبینی کننده در مرگ و میر بیماران مبتلا به کووید-19 معرفی شده است. نتایج حاصل از متا آنالیز انجام شده بر 22 مطالعه توسط Saragih که بر روی بیش از 924000 بیمار مبتلا به کووید انجام گردید، متغیر سن به عنوان یک فاکتور پیشبینی کننده در مرگ و میر بیماران مبتلا به کووید-19 تشخیص داده شد (OR=5.76) (42).
نتیجهگیری
بیماران مسن و بیمارانی که نیاز به بستری دارند بهویژه افرادیکه سابقۀ ابتلا به بیماری قلبی دارند نسبت به سایر گروهها در معرض خطر بالای مرگ قرار دارند. این بیماران علاوه بر غربالگری منظم، نیاز به نظارت فعال بهویژه در زمان بستری خواهند داشت. با ورود متغیر شکنندگی به مدل، متغیر ابتلا به بیماری زمینهای (قلبی عروقی) به عنوان یک فاکتور بسیار مهم در بقای بیماران شناخته شد؛ در حالی¬که بدون متغیر شکنندگی، این متغیر نادیده گرفته میشد. همچنین از خصوصیات مدل لگ نرمال، افزایش رخداد در شروع پیگیری و کاهش آن در ادامه پیگیری میباشد که با روند مرگ و میر در بیماری کووید-19 سازگار میباشد.
سپاسگزاری
بدینوسیله از کارکنان محترم واحد کروناویروس آزمایشگاه مرکز بهداشت استان اصفهان تشکر و سپاسگزاری میشود. این مطالعه قسمتی از پایاننامۀ مصوب معاونت پژوهشی دانشگاه علوم پزشکی ایران با کد پژوهشی 20259 جهت اخذ مقطع MPH عمومی است.
حامی مالی: ندارد.
تعارض در منافع: وجود ندارد.
ملاحظات اخلاقی
این پژوهش، پس از طرح در شورای برنامهریزی دانشکدۀ بهداشت دانشگاه علوم پزشکی ایران با کد پژوهشی 20259 و کد مصوبه اخلاق IR.IUMS.REC.1399.1426 تصویب گردید. با توجه به اینکه آنالیز آماری فقط بر روی دادههای جمعی بیماران انجام و بهجای نام بیماران از سیستم کددهی استفاده شد، این مطالعه فاقد مشکل اخلاقی است. با توجه به پیگیریهای انجامشده توسط واحد مبارزه با بیماریهای مرکز بهداشت شهرستان فریدونشهر، تعداد و درصد دادههای ازدسترفته، صفر است. از محدودیتهای مطالعه میتوان به عدم استفاده از متغیرهای بیوشیمیایی و فاکتورهای آزمایشگاهی نمونهها اشاره کرد.
مشارکت نویسندگان
جمیله ابوالقاسمی در ارائه ایده، صادق کارگریان/ جمیله ابوالقاسمی/ ملیحه حسننژاد در طراحی مطالعه، صادق کارگریان در جمعآوری دادهها، جمیله ابوالقاسمی/ صادق کارگریان در تجزیه و تحلیل دادهها مشارکت داشته و همه نویسندگان در تدوین، ویرایش اولیه و نهایی مقاله و پاسخگویی به سوالات مرتبط با مقاله سهیم هستند.
References:
1- Gralinski Le, Menachery Vd. Return of the Coronavirus: 2019-Ncov. Viruses 2020; 12(2): 135.
2- Who. Novel Coronavirus (2019-Ncov). Available at: https://www.who.int/docs/default-source/coronaviruse/situation-reports/20200211-sitrep-22-ncov.pdf, Page:7. Accessed: Aug 21, 2024.
3- Zhao S, Musa Ss, Lin Q, Ran J, Yang G, Wang W, et al. Estimating the Unreported Number of Novel Coronavirus (2019-Ncov) Cases in China in the First Half of January 2020: A Data-Driven Modelling Analysis of the Early Outbreak. J Clin Med 2020; 9(2): 388.
4- Wang M, Cao R, Zhang L, Yang X, Liu J, Xu M, et al. Remdesivir and Chloroquine Effectively Inhibit the Recently Emerged Novel Coronavirus (2019-Ncov) in Vitro. Cell Research 2020; 30(3): 269-71.
5- Wang M, Zhou Y, Zong Z, Liang Z, Cao Y, Tang H, et al. A Precision Medicine Approach to Managing 2019 Novel Coronavirus Pneumonia. Precis Clin Med 2020; 3(1): 14-21.
6- Liu J, Zheng X, Tong Q, Li W, Wang B, Sutter K, et al. Overlapping and Discrete Aspects of the Pathology and Pathogenesis of the Emerging Human Pathogenic Coronaviruses Sars‐Cov, Mers‐Cov, and 2019‐Ncov. J Med Virol 2020; 92(5): 491-4.
7- Daszak P, Olival Kj, Li H. A Strategy to Prevent Future Epidemics Similar to the 2019-Ncov Outbreak. Biosaf Health 2020; 2(1): 6-8.
8- Tavakoli A, Karbalaie Niya Mh, Keshavarz M, Safarnezhad Tameshke F, Monavari Sh. Middle East Respiratory Syndrome Coronavirus (Mers-Cov). Iran J Med Microbiol 2017; 11(1): 1-8.
9- Momattin H, Al-Ali Ay, Al-Tawfiq Ja. A Systematic Review of Therapeutic Agents for the Treatment of the Middle East Respiratory Syndrome Coronavirus (Mers-Cov). Travel Med Infect Dis 2019; 30: 9-18.
10- Vahdat K, Amini A, Najafi A, Haerinejad Mj. A Review of Novel Coronavirus, Cause of Middle East Respiratory Syndrome. ISMJ 2014; 16(6): 486-92.
11- L Zhang L, Lin D, Kusov Y, Nian Y, Ma Q, Wang J, et al. Α-Ketoamides as Broad-Spectrum Inhibitors of Coronavirus and Enterovirus Replication: Structure-Based Design, Synthesis, and Activity Assessment. Journal of Medicinal Chemistry 2020; 63(9): 4562-78.
12- N Zhu N, Zhang D, Wang W, Li X, Yang B, Song J, et al. A Novel Coronavirus from Patients with Pneumonia in China, 2019. New England Journal of Medicine 2020; 382(8): 727-33.
13- Lai CC, Shih TP, Ko WC, Tang HJ, Hsueh PR. Severe Acute Respiratory Syndrome Coronavirus 2 (SARS-Cov-2) and Coronavirus Disease-2019 (COVID-19): The Epidemic and the Challenges. International Journal of Antimicrobial Agents 2020; 55(3): 105924.
14- Cui J, Li F, Shi ZL. Origin and Evolution of Pathogenic Coronaviruses. Nature Reviews Microbiology 2019; 17(3): 181-92.
15- Bonilla-Aldana Dk, Quintero-Rada K, Montoya-Posada Jp, Ramírez-Ocampo S, Paniz-Mondolfi A, Rabaan Aa, et al. Sars-Cov, Mers-Cov and Now the 2019-Novel Cov: Have We Investigated Enough about Coronaviruses?–A Bibliometric Analysis. Travel Medicine and Infectious Disease 2020; 33: 101566.
16- Hougaard P. Frailty Models For Survival Data. Lifetime Data Anal 1995; 1(3): 255-73.
17- Hougaard P. A Class of Multivanate Failure Time Distributions. Biometrika 1986; 73(3): 671-8.
18- Mcgilchrist C, Aisbett C. Regression with Frailty in Survival Analysis. Biometrics 1991; 47: 461-6.
19- Ripatti S, Larsen K, Palmgren J. Maximum Likelihood Inference for Multivariate Frailty Models Using an Automated Monte Carlo Em Algorithm. Lifetime Data Anal 2002; 8(4): 349-60.
20- Hougaard P. Frailty Models for Survival Data. Lifetime Data Analysis 1995; 1(3): 255-73.
21- Oakes D. Bivariate Survival Models Induced by Frailties. Journal of the American Statistical Association 1989; 84(406): 487-93.
22- Bjarnason H, Hougaard P. Fisher Information for Two Gamma Frailty Bivariate Weibull Models. Lifetime Data Anal 2000; 6(1): 59-71.
23- Bolstad Wm, Manda So. Investigating Child Mortality in Malawi Using Family and Community Random Effects: A Bayesian Analysis. Journal of the American Statistical Association 2001; 96(453): 12-9.
24- Gohari Mr, Mahmoudi M, Mohammed K, Pasha E, Khodabakhshi R. Recurrence in Breast Cancer. Analysis with Frailty Model. Saudi Med J 2006; 27(8): 1187-93.
25- Rajaeefard A, Dehkordi B, Tabatabaee H, Zeighami B. Applying Parametric Models for Survival Analysis of Gastric Cancer. Feyz Med Sci J 2009; 13(2): 83-8. [Persian]
26- Cox Dr. Regression Models and Life-Tables. Journal of the Royal Statistical Society. 1972; 34(2): 187-220.
27- Nardi A, Schemper M. Comparing Cox and Parametric Models in Clinical Studies. Stat Med 2003; 22(23): 3597-610.
28- Who .Available At: https:// data.who.int/ dashboards/covid19/deaths. Accessed: Aug 21, 2024.
29- Zandkarimi E, Moradi G, Mohsenpour B. The Prognostic Factors Affecting the Survival of Kurdistan Province Covid-19 Patients: A Cross-Sectional Study from February to May 2020. Int J Health Policy Manag 2020; 11(4): 453-58.
30- Naeini Mb, Sahebi M, Nikbakht F, Jamshidi Z, Ahmadimanesh M, Hashemi M, et al. A Meta-Meta-Analysis: Evaluation of Meta-Analyses Published in the Effectiveness of Cardiovascular Comorbidities on The Severity of Covid-19. Obesity Medicine 2021; 22: 100323.
31- Shahid Z, Kalayanamitra R, Mcclafferty B, Kepko D, Ramgobin D, Patel R, et al. Covid-19 and Older Adults: What We Know. J Am Geriat Society 2020; 68(5): 926-9.
32- Altonen Bl, Arreglado Tm, Leroux O, Murray-Ramcharan M, Engdahl R. Characteristics, Comorbidities and Survival Analysis of Young Adults Hospitalized with Covid-19 in New York City. Plos One 2020; 15(12): E0243343.
33- Bansal M. Cardiovascular Disease and Covid-19. Diabetes & Metabolic Syndrome 2020; 14(3): 247-50.
34- Esenwa Cc, Elkind Ms. Inflammatory Risk Factors, Biomarkers and Associated Therapy in Ischaemic Stroke. Nat Rev Neurol 2016; 12(10): 594-604.
35- Lindsberg PJ, Grau AJ. Inflammation and Infections as Risk Factors for Ischemic Stroke. Stroke 2003; 34(10): 2518-32.
36- Soares Rcm, Mattos Lr, Raposo Lm. Risk Factors for Hospitalization and Mortality Due to Covid-19 in Espírito Santo State, Brazil. Am J Trop Med Hyg 2020; 103(3): 1184-90.
37- Drake Tm, Docherty Ab, Harrison Em, Quint Jk, Adamali H, Agnew S, et al. Outcome of Hospitalization for Covid-19 in Patients with Interstitial Lung Disease. An International Multicenter Study. Am J Respir Crit Care Med 2020; 202(12): 1656-65.
38- Zhang Jj, Cao Yy, Tan G, Dong X, Wang Bc, Lin J, et al. Clinical, Radiological, and Laboratory Characteristics and Risk Factors for Severity and Mortality of 289 Hospitalized Covid-19 Patients. Allergy 2021; 76(2): 533-50.
39- Salinas-Escudero G, Carrillo-Vega Mf, Granados-García V, Martínez-Valverde S, Toledano-Toledano F, Garduño-Espinosa J. A Survival Analysis of Covid-19 in the Mexican Population. Bmc Public Health 2020; 20(1): 1616.
40- Tian R, Wu W, Wang C, Pang H, Zhang Z, Xu H, et al. Clinical Characteristics and Survival Analysis in Critical and Non-Critical Patients with Covid-19 in Wuhan, China: A Single-Center Retrospective Case Control Study. Sci Rep 2020;10(1):17524.
41- Zhang Xm, Jiao J, Cao J, Huo Xp, Zhu C, Wu Xj, et al. Frailty as a Predictor of Mortality among Patients with Covid-19: A Systematic Review and Meta-Analysis. BMC Geriatrics 2021; 21(1): 186.
42- Saragih Id, Advani S, Saragih Is, Suarilah I, Susanto I, Lin Cj. Frailty as a Mortality Predictor in Older Adults with Covid-19: A Systematic Review and Meta-Analysis of Cohort Studies. Geriatric Nurs 2021; 42(5): 983-92.
نوع مطالعه: پژوهشي |
موضوع مقاله:
اپیدمیولوژی
دریافت: 1402/9/28 | پذیرش: 1403/2/9 | انتشار: 1403/6/15
دریافت: 1402/9/28 | پذیرش: 1403/2/9 | انتشار: 1403/6/15
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |







