دوره 31، شماره 1 - ( فروردین 1402 )
جلد 31 شماره 1 صفحات 6338-6327 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Rahmatinejad P, Past N, Mozafari M, Shahi Sadrabadi F. Efficacy of Transcranial Direct Current Stimulation in Reducing Symptoms in Patients with Major Depressive Disorder: A Randomized Controlled Trial. JSSU 2023; 31 (1) :6327-6338
URL: http://jssu.ssu.ac.ir/article-1-5607-fa.html
URL: http://jssu.ssu.ac.ir/article-1-5607-fa.html
رحمتینژاد پروین، پاست نگین، مظفری محمدرضا، شاهی صدرآبادی فاطمه. اثربخشی تحریک الکتریکی مستقیم مغز در کاهش نشانههای بیماران مبتلا به اختلال افسردگی اساسی: یک کارآزمایی تصادفی کنترل شده. مجله علمي پژوهشي دانشگاه علوم پزشكي شهید صدوقی يزد. 1402; 31 (1) :6327-6338
واژههای کلیدی: اثربخشی، تحریک الکتریکی مستقیم مغز، اختلال افسردگی اساسی، کارآزمایی تصادفی کنترل شده با گروه شم.
متن کامل [PDF 999 kb]
(739 دریافت)
| چکیده (HTML) (1602 مشاهده)
References:
1- De Graaf R, Radovanovic M, Van Laar M, Fairman B, Degenhardt L, Aguilar-Gaxiola S, et al. J Early Cannabis Use and Estimated Risk of Later Onset of Depression Spells: Epidemiologic Evidence from the Population-Based World Health Organization World Mental Health Survey Initiative. Am J Epidemiol 2010; 172(2): 149-59.
2- Rush AJ, Trivedi MH, Wisniewski SR, Nierenberg AA, Stewart JW, Warden D, et al. Acute and Longer-Term Outcomes in Depressed Outpatients Requiring One or Several Treatment Steps: A STAR*D Report. Am J Psychiatry 2006; 163(11): 1905-17.
3- Rush AJ, Warden D, Wisniewski SR, Fava M, Trivedi MH, Gaynes BN, et al. STAR*D: Revising Conventional Wisdom. CNS Drugs 2009; 23(8): 627-47.
4- Culpepper L. Functional Impairment and Improvement in Depression. J Clin Psychiatry 2016; 77(1): e35.
5- Stagg CJ, Nitsche MA. Physiological Basis of Transcranial Direct Current Stimulation. Neuroscientist 2011; 17: 37-53.
6- Nitsche M, Nitsche MS, Klein CC, Tergau F, Rothwell JC, and Paulus W. Level of Action of Cathodal DC Polarisation Induced Inhibition of the Human Motor Cortex. Clin Neurophysiol 2003; 114(4): 600-4.
7- Filmer HL, Dux PE, Mattingley JB. Applications of Transcranial Direct Current Stimulation for Understanding Brain Function. Trends Neurosci 2014; 37(12): 742-53.
8- Coffman BA, Clark VP, Parasuraman R. Battery Powered Thought: Enhancement of Attention, Learning, and Memory in Healthy Adults Using Transcranial Direct Current Stimulation. NeuroImage 2014, 85(3): 895-908.
9- Parasuraman R, McKinley RA. Using Noninvasive Brain Stimulation to Accelerate Learning and Enhance Human Performance. Hum Factors 2014; 56(5): 816-24.
10- Reis J, Schambra HM, Cohen LG, Buch ER, Fritsch B, et al. Noninvasive Cortical Stimulation Enhances Motor Skill Acquisition Over Multiple Days Through an Effect on Consolidation. Proc Natl Acad Sci USA 2009; 106(5): 1590-5.
11- Arul-Anandam AP, Loo C. Transcranial Direct Current Stimulation: A New Tool for the Treatment of Depression? J Affect Disord 2009; 117(3): 137-45.
12- Nitsche MA, Cohen LG, Wassermann EM, Priori A, Lang N, Antal A, et al. Transcranial Direct Current Stimulation: State of the Art. Brain Stimul 2008; 1(3): 206-23.
13- Agarwal SM, Shivakumar V, Bose A, Subramaniam A, Nawani H, Chhabra H, et al. Transcranial Direct Current Stimulation in Schizophrenia. Clin Psychopharmacol Neurosci 2013; 11(3): 118-25.
14- Schneider HD, Hopp J. The Use of the Bilingual Aphasia Test for Assessment and Transcranial Direct Current Stimulation to Modulate Language Acquisition in Minimally Verbal Children with Autism. Clin Linguist Phon 2011; 25(6-7): 640-54.
15- Khedr EM, El Gamal NF, EL Fetoh NA, Khalifa H, Ahmad EM, Ali AM. A Double-Blind Randomized Clinical Trial on the Efficacy of Cortical Direct Current Stimulation for the Treatment of Alzheimer’s disease. Front Aging Neurosci 2014; 6: 275.
16- Razza LB, De Smet S, Moffa A, Sudbrack-Oliveira, P, Vanderhasselt MA, Brunoni AR. Follow-Up Effects of Transcranial Direct Current Stimulation (Tdcs) for the Major Depressive Episode: A Systematic Review and Meta-Analysis. Psychiatry Res 2021; 302: 114024.
17- Hamilton JP, Siemer M, Gottlib IH. Amygdala Volume in Major Depressive Disorder: A Meta-Analysis of Magnetic Resonance Imaging Studies. Mol Psychiatry 2008; 13: 993-1000.
18- Koenigs M, Grafman J. The Functional Neuroanatomy of Depression: Distinct Roles for Ventromedial and Dorsolateral Prefrontal Cortex. Behav Brain Res 2009; 201(2): 239-43.
19- Brunoni AR, Moffa AH, Fregni F, Palm U, Padberg F, Blumberger DM, et al. Transcranial Direct Current Stimulation for Acute Major Depressive Episodes: Meta-Analysis of Individual Patient Data. Br J Psychiatry 2016; 208(6): 522-31.
20- Brunoni A, Teng CT, Imamura M, Brasil-Neto JP, Boechat R, Caramelli P, et al. Neuromodulation Approaches for the Treatment of Major Depression: Challenges and Recommendations from a Working Group Meeting. Arq Neuropsiquiatr 2010; 68(3): 433-51.
21- Brunoni AR, Valiengo L, Baccaro A, Zanao TA, De oliveira JF , Goulart A, et al. The Sertraline Vs Electrical Current Therapy for Treating Depression Clinical Study Result from a Factorial, Randomized, Controlled Trial. JAMA Psychiatry 2013; 70(4): 383-91.
22- Fregni F, Boggio PS, Nitsche MA, Marcolin MA, Rigonatti SP, Pascual-Leone A. Treatment of Major Depression with Transcranial Direct Current Stimulation. Bipolar Disord 2006; 8(2): 203-4.
23- Boggio PS, Rigontti SP, Ribeiro RB, Myczkowski ML, Nitsche MA, Pascual-Leone A, et al. A Randomized, Double-Blind Clinical Trial on the Efficacy of Cortical Direct Current Stimulation for the Treatment of Major Depression. Int J Neuropsychopharmacol 2008; 11(2): 249-54.
24- Brunoni AR, Moffa AH, Sampaio-Junior B, Borrione L, Moreno ML, Fernandes, RA and et al. Trial of Electrical Direct-Current Therapy versus Escitalopram for Depression. N Engl J Med 2017; 376(26): 2523-33.
25- Aparicio LVM, Guarienti F, Razza LB, Carvalho AF, Fregni F, Brunoni AR. A Systematic Review on the Acceptability and Tolerability of Transcranial Direct Current Stimulation Treatment in Neuropsychiatry Trials. Brain Stimul 2016; 9(5): 571-681.
26- Mutz J, Vipulananthan V, Carter B, Hurlemann R, Fu CHY, Young AH. Comparative Efficacy and Acceptability of Non-Surgical Brain Stimulation for the Acute Treatment of Major Depressive Episodes in Adults: Systematic Review and Network Meta-analysis. BMJ 2019; 364: l1079.
27- Ebrahimi A, Neshatdoost HT, Mousavi SG, Asadollahi GA, Nasiri H. Controlled Randomized Clinical Trial of Spirituality Integrated Psychotherapy (SIPT), Cognitive-Behavioral Therapy (CBT) and Medication Intervention on Depressive Symptoms and Dysfunctional Attitudes in Patients with Dysthymic Disorder. Adv Biomed Res 2013; 2: 53.
28- Beck AT, Steer RA, Garbin MG. Psychometric Properties of the Beck Depression Inventory Twenty-Five Years of Evaluation. Clinical psychology review 1998, 8(1); 77-100.
29- Fata L. Established Structures of Meaning and Emotional States of Cognitive Processing of Emotional Information: A Comparison of Two Conceptual Frameworks [Dissertation]. Tehran: Iran University of Medical Sciences; 2003. [Persian]
30- Fitzgerald PB, Daskalakis ZJ. A Practical Guide to the Use of Repetitive Transcranial Magnetic Stimulation in the Treatment of Depression. Brain Stimul 2012; 5(3): 287-96.
31- Murray EA, Wise SP, Drevets WC. Localization of Dysfunction in Major Depressive Disorder: Prefrontal Cortex and Amygdala. Biol Psychiatry 2011; 69(12): 43-54.
32- Martin DM, Teng JZ, Lo TY, Alonzo A, Goh T, Iacoviello BM, et al. Clinical Pilot Study of Transcranial Direct Current Stimulation Combined with Cognitive Emotional Training for Medication Resistant Depression. J Affect Disord 2018; 232: 89-95.
33- Brunoni AR, Tortella G, Benseñor IM, Lotufo PA, Carvalho AF, Fregni F. Cognitive Effects of Transcranial Direct Current Stimulation in Depression: Results from the SELECT-TDCS Trial and Insights for Further Clinical Trials. J Affect Disord 2016; 202: 46-52.
34- Philip NS, Barredo J, van’t Wout-Frank M, Tyrka AR, Price LH, Carpenter LL. Network Mechanisms of Clinical Response to Transcranial Magnetic Stimulation in Posttraumatic Stress Disorder and Major Depressive Disorder. Biol psychiatry 2018; 83(3): 263-72.
35- Hamilton JP, Furman DJ, Chang C, Thomason ME, Dennis E, Gotlib IH. Default-Mode and Task-Positive Network Activity in Major Depressive Disorder: Implications for Adaptive and Maladaptive Rumination. Biol psychiatry 2011; 70(4): 327-33.
36- Vanderhasselt MA, De Raedt R, Brunoni AR, Campanhã C, Baeken C, Remue J, et al. Tdcs Over the Left Prefrontal Cortex Enhances Cognitive Control for Positive Affective Stimuli. PloS one 2013; 8(5): e62219.
37- Mutz J, Edgcumbe DR, Brunoni AR, Fu CHY. Efficacy and Acceptability of Non-Invasive Brain Stimulation for the Treatment of Adult Unipolar and Bipolar Depression: A Systematic Review and Meta-Analysis of Randomised Sham-Controlled Trials. Neurosci Biobehav Rev 2018; 92: 291-303.
متن کامل: (2502 مشاهده)
مقدمه
براساس آمار سازمان بهداشت جهانی اختلال افسردگی اساسی (Major Depressive Disorder (MDD))یکی از شایعترین اختلالات روانشناختی و وضعیت ناتوان کنندهای است که هزینههای فردی، اجتماعی، اقتصادی زیادی را بر فرد و جامعه تحمیل کرده و میزان بالایی از مرگ و میر و ناتوانی عمده را به همراه دارد (1). پاسخ ضعیف به داروهای ضدافسردگی و افسردگی مقاوم به درمان یکی از چالشهای عمده در محیطهای بالینی است. تنها یک چهارم بیماران مبتلا به MDD بعد از دریافت اولین دوره داروهای ضدافسردگی بهبود مییابند و حدود 70% از این بیماران نیاز به حداقل چهار دوره درمانی دیگر تا کسب بهبودی دارند (2). عدم پاسخ به درمانهای دارویی و غیردارویی، خطر مزمن شدن بیماری، رفتارهای خودکشی (3) کاهش کیفیت زندگی افراد مبتلا به دلیل اختلالات عملکردی (4) باعث شده تا رویکردهای درمانی دیگر از جمله تکنیکهای تحریک غیرتهاجمی مغز (Non-invasive brain stimulation) (NIBS) برای درمان این اختلال مورد توجه محققان و درمانگران قرار گیرد. تحریک الکتریکی مستقیم مغز (Transcranial Direct Current Stimulation) (tDCS) یک روش درمانی غیرتهاجمی است که باعث تعدیل عصبی برگشتپذیر در فعالیت نواحی مخصوصی از مغز میشود. در واقع تغییرات پتانسیل غشا عصبی و افزایش برانگیختگی قشر مغز از مهمترین مکانیسمهای بیولوژیکی tDCS به حساب میآید (5). علاوه بر تغییرات بالقوه زودگذر و ناگهانی در غشا که میتواند تا یک ساعت ادامه داشته باشدtDCS با تغییرات طولانیمدت سیناپسی همراه است (6). این روش یک فناوری ارزشمند برای سازماندهی ارتباطات مغز-رفتار از طریق حوزههای مختلف حرکتی، شناختی، اجتماعی و هیجانی است (7). در جمعیت افراد سالم یافتهها موید آن است که tDCS باعث تغییر موقت رفتار، سرعت بخشیدن به فرآیند یادگیری و افزایش کارایی در تکالیف میشود (9،8). تعداد زیادی از مطالعات روزافزون انسانی گزارش دادهاند کهtDCS منجر به تقویت عملکرد مغز از جمله یادگیری حرکتی و حافظه میشود (6،10). در حال حاضر اثراتtDCS بر روی قابلیت تحریک عصبی در مطالعات تصویربرداریهای عصبی و روانشناختی مورد تایید قرار گرفته و پایههای عصبی-زیستی برای کاربرد آن جهت تعدیل عصبی در جمعیت بیماران فراهم کرده است (11،12). در این راستا نتایج برخی مطالعات نیز سودمندی این مداخله درمانی، در کاهش توهم بیماران مبتلا به اسکیزوفرنی (13)، بهبود تاخیر در اکتساب زبانی بیماران مبتلا به اختلالات طیف اتیسم (14) و بهبود کارکرد شناختی در بیماران مبتلا به آلزایمر (15) مورد تایید قرار داده است. هر چند این تکنیک در مقایسه با سایر تکنیکهای NIBSمانند تحریک الکتریکی فراجمجمهای (TMS) (Transcranial magnetic stimulation) کمتر مورد مطالعه قرار گرفته و هنوز به تایید سازمان غذا و داروی آمریکا نیز نرسیده اما بهطور گستردهای از لحاظ ایمنی، تحملپذیری (Tolerability) و کارایی بهویژه در MDD مورد توجه محققان بوده و بهصورت موفقیتآمیزی در کاهش علائم MDD بهکار رفته است (12). موسسه ملی تعالی مراقبتهای بهداشتی و درمانی انگلستان در سال 2015 دستورالعمل روش مداخلهای برای تحریک الکتریکی مستقیم مغز در درمان افسردگی را منتشر کرد. این راهنما مبتنی بر اطلاعات بهدست آمده از بررسی بیش از 2000 بیمار در تحقیقات فراتحلیل (شامل 7 مطالعه آزمایشی کنترل شده) یک مطالعه سیستماتیک و یک مطالعه پیگیرانه برچسبباز و مطالعات موردی بود (16). دلایل استفاده از tDCS در اختلال افسردگی اساسی به نتایج مثبت کسب شده از مطالعاتی مربوط میشود که از تحریک الکتریکی فراجمجمهای (TMS) برای درمان بیماران مبتلا به افسردگی اساسی استفاده کردند. شواهد بهدست آمده موید آن است که بیماران مبتلا به MDD تغییرات کارکردی و ساختاری در چندین ناحیه کورتکس از جمله قشر دورسولاترال و شکمی-میانی چپ، آمیگدال و هیپوکامپ نشان میدهند (18،17) به گفته محققان اثرات tDCS در بهبودی افسردگی مربوط به تحریک کانونی (DLPFC) چپ است که با برخی از علائم افسردگی ملانکولیک از جمله علائم روانی-حرکتی ضعیف ارتباط دارد (20،19). بهنظر می¬رسد که اثرات درمانی tDCS در اختلال افسردگی همانند داروهای ضد افسردگی است که منجر به برانگیختگی DLPFC در بیماران و در نهایت تعدیل فعالیت پیش پیشانی راست و چپ متعاقب کاهش علائم افسردگی میشود (21). در مورد اثربخشی tDCS برای درمان افسردگی، دو آزمایش کنترل شده نتایج دلگرم کنندهای را گزارش کردهاند. از نظر فرگنی و همکاران (10= n mA 1، 20 دقیقه در هر جلسه، 5 جلسه در روزهای متناوب) و بوگیو و همکاران (40=n، mA2، 20 دقیقه در هر جلسه، 10 جلسه در روزهای متوالی هفته) tDCS موثرتر از دارونما بود (23،22). در یک تحقیق که روی 245 بیمار مبتلا به MDD انجام شد، یافتهها نشان دادtDCS در مقایسه با سیتالوپرام mg 20 روزانه اثربخشی کمتری دارد. اما نسبت به پلاسبو برتری دارد (24). در یک مطالعه دیگر که روی بیماران افسرده صورت گرفت، پیگیری نشان داد تقریباً 25 درصد از بیمارانی که دو بار در هفته تحت درمانtDCS قرار داشتند، بعد از 6 ماه بیماریشان عود کرد (25). موتز و همکاران در یک فراتحلیل؛ نتایج بهدست آمده از اثربخشی TMS،tDCS و ECT (Electro Convulsive Therapy) در 113 مطالعه آزمایشی که روی مجموعاً 6750 بیمار صورت گرفته بود را مورد بررسی قرار دادند. در این مطالعه ECT با بالاترین نسبت شانس پاسخ ارتباط داشت (26). با توجه به آنچه گفته شد، نتایج در ارتباط با اثرگذاری روش درمانی tDCS متناقض بوده و این در حالی است که بیماری افسردگی هزینه زیادی برای جامعه و رنج بسیاری برای فرد مبتلا دارد که شناسایی اثربخشترین روشهای درمانی به ویژه برای بیماران مقاوم و کم پاسخ ده به درمان دارویی از اهمیت دوچندانی برخوردار میشود. بنابراین هدف از پژوهش حاضر، تعیین اثربخشی tDCS بر کاهش نشانههای افسردگی افراد مبتلا به اختلال افسردگی اساسی است. این پژوهش در صدد پاسخگویی به این پرسشهاست که آیا tDCS موجب کاهش نشانههای افسردگی شرکتکنندگان گروه آزمایش نسبت به گروه کنترل میگردد و آیا نتایج بهدست آمده از این پژوهش در پیگیری یک ماهه نیز پایدار خواهد بود؟
روش بررسی
این پژوهش از نوع کارآزمایی بالینی بوده است. جامعه آماری پژوهش حاضر کلیه افراد مراجعه کننده به یک کلینیک خصوصی خدمات روانشناختی شهر تهران بودند که توسط روانپزشک تشخیص اختلال افسردگی اساسی دریافت کردند. این افراد از هر دو جنس زن و مرد و در بازه سنی ۲۰ تا ۶۰ سال بودند. سطح تحصیلات آنها نیز از ابتدایی تا دکتری متغیر بود. با استفاده از روش نمونهگیری هدفمند تعداد 20 نفر افراد مبتلا که نمرات آنها در پرسشنامه افسردگی بک بالاتر از 18 و در پرسشنامه همیلتون نیز بالاتر از ۱۳ بود، انتخاب شده و با استفاده از روش بلوکبندی تصادفی و با اندازه بلوک برابر 4 به دو گروه مداخله (10 نفر) و کنترل (10 نفر) تقسیم شدند. به دلیل این که مطالعه از نوع تجربی و آزمایشی بود تعداد 10 برای گروه مداخله و کنترل انتخاب شد. هر دو گروه کنترل و مداخله در متغیرهایی نظیر جنس، سن، وضعیت تاهل، نوع داروی مصرفی، تعداد شوک¬های دریافتی در پروتکلهای درمانی پیشین و شدت افسردگی (که با استفاده از هر دو مقیاس درجهبندی هملیتون و بک سنجیده میشد) همتا شدند. معیارهای ورود شامل تشخیص اختلال افسردگی اساسی، سن بالای 18 سال و نداشتن اختلالات بالینی همایند دیگر بود. معیارهای خروج نیز شامل همبودی با سایر اختلالات محورI وII ، سابقه تشنج و صرع، سوءمصرف مواد، اختلالات نورولوژیکی، سابقه بیماری قلبی، شکست در درمان با شوک الکتریکی برای دوره فعلی افسردگی، بارداری، درمان دارویی همزمان با بنزودیازپینها و ضدتشنجها بود. ابزار گردآوری دادهها در این پژوهش شامل مقیاس درجهبندی افسردگی همیلتون (Hamilton Depression Rating Scale) و پرسشنامه افسردگی بک ویرایش دوم (Beck Depression Inventory-II) بود. مقیاس درجهبندی افسردگی همیلتون: در پژوهش حاضر برای ارزیابی شدت افسردگی در طول درمان از این ابزار استفاده گردید. این مقیاس توسط مصاحبهگر اجرا میشود و 8 علامت مربوط به شکایات جسمانی، 5 علامت مربوط به مشکلات رفتاری، 2 علامت مربوط شکایات شناختی و در نهایت 2 علامت هم مربوط به تغییرات هیجانی بیماران افسرده را مورد ارزیابی قرار میدهد. هر پرسش از 0 تا 4 نمرهگذاری میگردد، به صورتیکه 4 بالاترین شدت ممکن را در مورد هر قسمت نشان میدهد (طبیعی= < 7، خفیف= 13-8، متوسط= 18-14). روایی فرم فارسی این ابزار با استفاده از سنجش همبستگی با مقیاس افسردگی بک 0/55 بهدست آمده است. همچنین پایایی بین ارزیابها نیز 0/95 گزارش شده است (27). پرسشنامه افسردگی بک - ویرایش دوم: این ابزار شامل 21 سوال است که نشانه¬های تعریف شده افسردگی از جمله غمگینی، احساس گناه، از دست دادن علاقه، کنارهگیری اجتماعی و افکار خودکشی را طی دو هفته قبل مورد ارزیابی قرار می¬دهد. آیتم¬ها شامل چهار گزینه هستند که روی یک مقیاس 0 تا 3 نمره گذاری میشوند. بدین ترتیب مجموع امتیازها میتواند بین 0 تا 63 تغییر کند که نمرات بالا نشانه شدت بیشتر افسردگی است. تقسیمبندی ارائه شده توسط Beck & Steer برای شدت افسردگی در این پرسشنامه به این قرار است: بدون علامت (۹-۰)، افسردگی خفیف (1۸-1۰)، افسردگی متوسط (۲9-۱۹) و افسردگی شدید (۶۳-۳۰) (28). در مطالعات مربوط به بررسی ویژگیهای روانسنجی فرم فارسی این پرسشنامه ضریب آلفای کرونباخ 0/91 و اعتبار بازآزمایی یک هفتهای 0/96 گزارش شده است (29). روش اجرا به این صورت بود، بیمارانی که توسط روانپزشک حاضر در کلینیک، تشخیص اختلال افسردگی اساسی دریافت میکردند، برای اجرای آزمون به پژوهشگر ارجاع داده میشدند. با بررسیهای روانپزشکی و روانشناسی، مطالعه پرونده و مطابقت با معیارهای ورود و خروج، بیماران وارد طرح پژوهشی میشدند. بعد از ارائه توضیحات لازم در مورد اهداف پژوهش و قبل از اجرای آزمون از بیماران شرکتکننده درخواست میشد تا فرم رضایت آگاهانه را پرکنند. قبل از شروع درمان خط پایه شدت و علایم افسردگی به وسیله پرسشنامه¬های افسردگی بک و همیلتون ارزیابی میشدند. بلافاصله بعد از پایان هرجلسه، بعد از جلسه 5 و جلسه 10 آزمون افسردگی بک برای سنجش شدت افسردگی آزمودنی ها اجرا میگردید. برای ارزیابی دوام و پایداری اثرات درمانی تحریک الکتریکی مستقیم مغز در طول 4 هفته، پس از آخرین جلسه درمان، مقیاس افسردگی بک دوباره اجرا گردیده و نتایج آن در پروفایل آزمودنیها ثبت گردید. هر دو گروه کنترل و آزمایش تحت درمآنهای دارویی ضدافسردگی (بنزودیازپینها) قرار داشتند و گروه آزمایش علاوه بر دارو درمانی، تحت درمان تحریک الکتریکی مستقیم مغز نیز قرار گرفت. به دلایل اخلاقی و برای کنترل متغیرهای مزاحم دوز داروهای ضدافسردگی در طول درمان ثابت نگه داشته شد. جهت رعایت اصول اخلاقی، افراد گروه کنترل وارد لیست انتظار شدند تا در صورت اثربخشی آزمایش، آنها نیز همانند گروه آزمایش مورد مداخله قرار گیرند.
نحوه مداخله درمانی با تحریک الکتریکی مستقیم مغز: تحریک الکتریکی مستقیم مغز به وسیله روانشناس بالینی آموزش دیده برای کار با دستگاه اجرا میشد. تحریک از طریق دستگاه آلمانی NeuroConn با دو الکترود بود. قطب مثبت در کرتکس دورسولترال پره فرونتال که در سیستم 10/20 الکتروانسفالوگرافی با PF3 مشخص میشود جایگذاری میشد و قطب منفی در سوپراوربیتال مخالف قرار داده میشد. الکترودهای لاستیکی (cm 35)که بهوسلیه اسفنجی نمدار پوشیده شده بود بهوسلیه هدبندهایی بر دورسر نگه داشته میشد. تحریک فعالی که برای گروه آزمایشی انجام میشد 2میلیآمپر (mA 2) برای 20 دقیقه بود. شوکها در 10 جلسه و بهصورت فاصله زمانی ۲۴ ساعته انجام میشد. برای تحریک ساختگی در گروه کنترل، تحریک الکتریکی مستقیم مغز بعد از چند ثانیه تحریک خاموش میگردید. برای مقایسه ویژگیهای بالینی و جمعیت شناختی بین دو گروه از آزمون-های x2 و t- test استفاده شد. برای بررسی اثربخشی مداخله، روش Mixed ANOVA و برای در نظر گرفتن اثرات زمان در دو گروه از آزمون تحلیل واریاس اندازهگیری مکرر در سطح معنیداری 0/05 استفاده گردید. نمرات مقیاس همیلتون به عنوان متغیر وابسته،گروهها در دو سطح گروه مداخله و گروه کنترل به عنوان متغیرهای مستقل بین گروهی و زمان در سه سطح 5 روز (بعد از 5 جلسه مداخله)10 روز (10 جلسه بعد از مداخله) و 30 روز (4هفته بعد از پایان درمان) به عنوان متغیرهای مستقل درونگروهی در نظر گرفته شدند.
تجزیه و تحلیل آماری
به منظور تفاوت بین گروهها در هر نقطه از زمان از t.test مستقل و برای آزمون تغییرات درون گروهها در طول زمان ازt.test وابسته استفاده شد. تمامی محاسبات آماری دادهها نیز توسط نرمافزارSPSS version 16 صورت گرفت.
ملاحظات اخلاقی
پروپوزال این تحقیق توسط دانشگاه علوم پزشکی قم تایید شده است (کد اخلاقIR.MUQ.REC.021). شرکتکنندگان با تکمیل فرم رضایت آگاهانه در پژوهش حاضر شرکت کردند و حضور آنها کاملاً داوطلبانه بود. لازم به ذکر است، بیماران به تشخیص روانپزشک نیازمند شوک الکتریکی و درمان فیزیولوژیکی دیگری تشخیص داده نشدند و در نتیجه از نظر اخلاقی شرکت در پژوهش منجر به تاخیر در درمان برای آنها نبود.
نتایج
ویژگیهای بالینی و اطلاعات جمعیت شناختی گروهها در جدول 1 نشان داده شده است. نتایج آزمون تحلیل واریانس مکرر برای نمرات افسردگی همیلتون(F=43/5 و P=0/017) و بک (F=125/12 و P=0/022) نشان دهنده معناداری اثر تعاملی زمان (چهار مرحله اندازهگیری) و عضویت گروهی (آزمایش و کنترل) بود (0/05 >P) که در جدول ۳ نمایش داده شده است. همانطور که جدول ۳ نشان میدهد بین دو گروه آزمایش و کنترل در هر دو متغیر وابسته حداقل در یکی از مراحل مداخله و پیگیری تفاوت معناداری وجود دارد. اثرات درون گروهی مطابق با جدول ۳ نیز بیانگر این است که حتی با اصلاح درجه آزادی بین زمان و عضویت گروهی در متغیرهای وابسته تعامل معنادار وجود دارد (0/05>P). برای بررسی اینکه تفاوت بین گروهها در متغیرهای وابسته در کدام یک از مراحل آزمون (بعد از 5 جلسه، بعد از 10 جلسه و 4هفته بعد از خاتمه درمان) وجود دارد از آزمون t مستقل استفاده شد که نتایج آن در جدول ۴ گزارش شده است. مطابق با این جدول نمرات افسردگی در هر دو مقیاس در گروه آزمایش در مراحل مداخله (در مقیاس همیلتون P=0/019 و در مقیاس بک (P=0/01) و پیگیری (در مقیاس همیلتون P=0/019 و در مقیاس بک 0۳/0P =) نسبت به گروه کنترل بهطور معناداری کاهش یافته است.
جدول 1: تفاوت گروههای آزمایش و کنترل بر حسب ویژگیهای بالینی و اطلاعات جمعیت شناختی قبل از شروع درمان بر اساس نتایج آزمون x2 و t.test
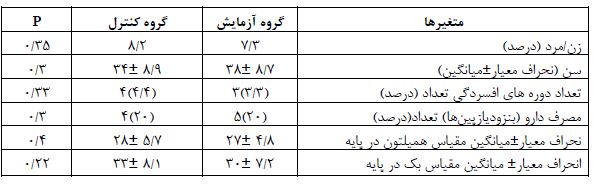
بر اساس نتایج آزمون x2 برای متغیرهای جنسیت و مصرف دارو و t.test برای متغیرهای سن، تعداد دورههای افسردگی و میانگین نمرات افسردگی پایه در مقیاسهای همیلتون و بک در بین گروه مداخله و کنترل تفاوت معنی داری مشاهده نشد.
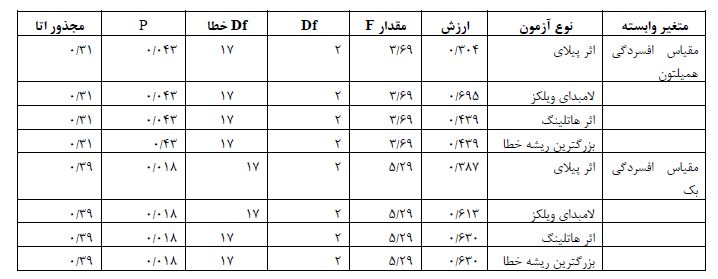
جدول ۲: نتایج آزمونهای چندگانه تحلیل واریانس مکرر برای متغیرهای افسردگی همیلتون و بک
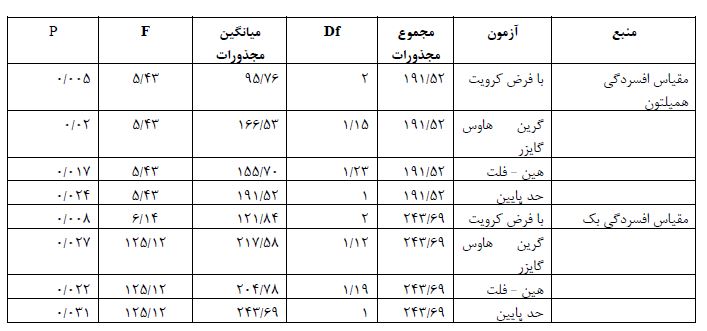
جدول ۳: نتایج آزمون تحلیل واریانس مکرر برای مقایسه نمرات هر دو مقیاس در گروه آزمایش و کنترل
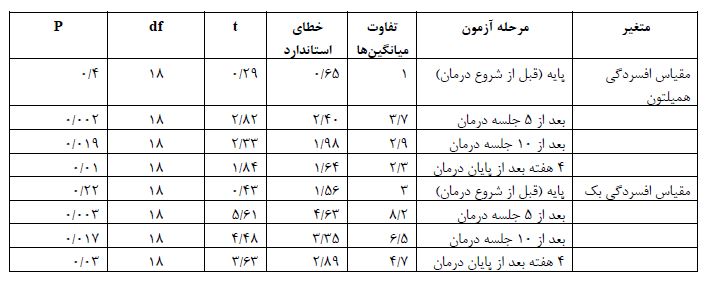
جدول 4: مقایسه میانگینهای نمرات افسردگی بک و همیلتون در چهار مرحله در گروه آزمایش و کنترل
بحث
هدف اساسی این پژوهش تعیین اثربخشی تحریک الکتریکی مستقیم مغز در کاهش نشانههای افسردگی بیماران مبتلا به افسردگی اساسی بود. نتایج این مطالعه نشان داد، تحریک الکتریکی مستقیم مغز بعد از مداخله و در طول زمان در کاهش نشانههای افسردگی اساسی گروه مداخله برتری نسبی به گروه کنترل داشته است. این نتایج با یافتههای سایر پژوهشها (22،12) همخوانی دارد که نشان دادند تحریک الکتریکی مستقیم مغز در بهبودی علائم افسردگی اثربخش است. همچنین، با توجه به نتایج آزمون، مرحله پیگیری نیز تاییدی بر پایداری ثبات و اثربخشی تحریک الکتریکی مستقیم مغز بر کاهش نشانههای افسردگی این بیماران است. این یافتهها با نتایج بهدست آمده از مطالعات پیشین از قبیل مطالعه Boggio ,et al که این روش را فقط موثرتر از دارونما میدانند ناهمخوان است (23). با این همه تفاوت حجم نمونه و نیز تفاوت در زمانبندی اجرای مداخله (روزهای متوالی یا متناوب در هفته) در تحقیق پیشرو و مطالعه مذکور یکی از دلایل احتمالی این ناهمخوانی در نتایج است. از سوی دیگر تشخیص اینکه چه مقدار از میزان بهبودی مشاهده شده در گروه کنترل مربوط به اثرات شرایط پلاسبو است دشوار میباشد و برای اثبات آن نیاز به کارآزماییهای بالینی دقیقتر با گروه کنترل بزرگتری است. در راستای تفسیر یافتههای پژوهش این فرضیه مطرح میشود که تحریک الکتریکی مستقیم مغز ابزاری است که احتمالاً توانمندی مغز را در پردازش اطلاعات ورودی بهبود میبخشد؛ این ویژگی اثربخشی سایر درمانها را افزایش میولی فرد را از آنها بی نیاز نمیکند (30). در راستای تایید این فرضیه میتوان به نتایج تحقیقاتی اشاره کرد که نشان دادند تحریک الکتریکی مستقیم مغز بر روی کرتکس دورسولاترال پیش پیشانی چپ یک اثر وابسته-دوز دارد (19) و منجر به بهبودی بالینی بیشتر در ترکیب با یک داروی ضد افسردگی نظیر مهارکنندههای انتخابی جذب مجدد سروتونین میشود (21). از سوی دیگر با توجه به اینکه افسردگی علاوه بر کاهش فعالیت کورتکس دورسولاترال پیش پیشانی چپ با بدکارکردی ناحیه تحت قشری لیمبیک همراه است (31) محققان فرض میکنند که تحریک الکتریکی مستقیم مغز عمدتا منجر به فعالسازی قشری میگردد در حالیکه داروهای بازدارنده جذب مجدد سروتونین اغلب منجر به کاهش فعالیت بیش از حد سیستم لیمبیک میشوند (21). نکته دیگری که باید به آن توجه داشت این است که به نظر میرسد مدت زمان و تعداد جلسات روزانه درمان نیز در اثربخشی آن نقش داشته باشد. برای مثال نتایج مطالعات صورت گرفته حاکی از آن است نرخ کارایی در مداخلات برچسب بازی که تحریک الکتریکی مستقیم مغز بهصورت دوبار در روز به مدت 5 روز متوالی ادامه داشته باشد بالاتر از مداخلاتی است که بهصورت به مدت 10 روز، بهصورت روزانه و مدت زمان 20 دقیقه انجام میشود (32). علاوه بر این در روش درمانی تحریک الکتریکی مستقیم مغز تحریک کاتودال (بازداری) ناحیه پیشپیشانی پشتی جانبی راست باعث کاهش پردازشهای هیجانی منفی و تحریک آنودال (افزایش فعالیت) ناحیه پیشپیشانی پشتی جانبی چپ باعث افزایش پردازش هیجانهای مثبت میشود. زیرا نیمکره راست بیشتر مسئول پردازش هیجانی منفی و نیمکره چپ نیز پردازشکننده هیجانهای مثبت است (33). علاوه بر این تحریک ناحیه پیشپیشانی پشتی جانبی باعث کاهش ارتباطهای بین قشر سینگلوت قدامی، شبکه پیشفرض مغز، اینسولا و همچنین کاهش ارتباط بین هیپوکامپ و شبکه برجستگی میشود که در نهایتا باعث عملکرد بهتر افراد افسرده و کاهش نشانههای افسردگی در آنها میشود (34). همچنین باید گفت یکی از علایم اصلی در اختلال افسردگی اساسی نشخوار فکری است. ناحیه پیشپیشانی پشتیجانبی که در درمان تحریک الکتریکی مستقیم مغز درگیر است ارتباط بسیار نزدیکی با نشخوار فکری دارد. در نشخوار فکری در شبکه اجرایی مرکزی و شبکه حالت پیش فرض مغز درگیری دارند که سطوح بالای فعالیت شبکه حالت پیش فرض با میزان بالای نشخوار فکری افسردهساز همراه است و میزان پایین فعالیت آن نیز با سبکهای فکری انطباقی رابطه دارد. همزمان با افزایش شبکه حالت پیش فرض، شبکه اجرایی مرکزی فعالیت خود را افزایش میدهد. بنابراین این درمان نقش مهمی در ایجاد تعادل بین دو شبکه و بهبود فکری فرد افسرده دارد (35). این تحریک در نیمکره راست با تعدیل پردازش شناختی و اطلاعات هیجانی منفی و همچنین در نیمکره چپ با افزایش کنترل شناختی بر محرک عاطفی مثبت بر نشخوار فکری اثرگذار است (36). همچنین شواهد تحقیقاتی موید این نکته است که اگر چه کیفیت روشهای تحریک مغناطیسی فراجمجمهای مکرر (Repetitive transcranial magnetic stimulation) مانند تحریک مغناطیسی مکرر مغزی دوطرفه با فرکانس بالا، تحریک مغناطیسی مکرر مغزی با فرکانس پایین و تحریک تتا (Theta burst stimulation) از لحاظ عددی در مقایسه با تحریک الکتریکی مستقیم مغز اثربخشی بیشتری داشتند فاصله اطمینان تکنیکهای تحریک مغناطیسی فراجمجمهای مکرر و تحریک الکتریکی مستقیم مغز با یکدیگر همپوشانی دارد لذا این موضوع هنوز بهصورت لاینحل باقی مانده است که کدام یک از مداخلات تحریک غیرتهاجمی مغز و تا چه اندازه بر دیگر تکنیکها برتری دارد. در این راستا Mutz, et al نشان دادند تحریک الکتریکی مستقیم مغز نسبت به درمان ساختگی برتری داشته است و در طیف مشابه تحریک مغناطیسی مکرر مغزی دوطرفه با فرکانس بالا نیز نسبت به درمان ساختگی برتری نشان داده است (37). در حقیقت حتی اگر تحریک مغناطیسی مکرر مغزی دوطرفه با فرکانس بالا واقعا 20 الی 30 درصد نسبت به تحریک الکتریکی مستقیم مغز اثربخشی بیشتری داشته باشد هزینههای بالای تحریک مغناطیسی مکرر در مقایسه با تحریک مغناطیسی مکرر، باعث میشود تا تحریک الکتریکی مستقیم مغز به عنوان خط اول درمان و تعدیل عصبی در راستای هزینه اثربخشی در نظر گرفته شود، زیرا که اغلب دستگاههای تحریک الکتریکی مستقیم مغز 50 بار ارزانتر از دستگاههای تحریک مغناطیسی مکرر هستند و هزینه¬های اجرایی آن نیز کمتر است. در هر صورت نتایج اغلب تحقیقات در مورد میزان اثربخشی یا کارایی انواع مختلف روشهای تحریک مغزی ضدو نقیض است و باید کارآزمایی¬های بالینی بیشتری برای کشف نحوه کار و میزان اثربخشی این رویکردهای جدید درمانی بهویژه تحریک مغناطیسی مکرر در برنامههای تحقیقاتی گنجانده شود. کوتاه بودن مدت زمان پیگیری، عدم کنترل متغیرهای مزاحمی مانند مصرف داروهای ضدافسردگی و حجم نمونه ناکافی را میتوان از محدودیتهای پژوهش حاضر دانست.
نتیجهگیری
بر اساس نتایج بهدست آمده از این پژوهش تحریک الکتریکی مستقیم مغز به عنوان یک مداخله درمانی در کاهش علائم بیماران مبتلا به اختلال افسردگی موثر میباشد. بهنظر میرسد تحریک الکتریکی مستقیم مغز میتواند بهعنوان یک مداخله درمانی بهتنهایی یا بهعنوان یک راهکار مکمل در پروتکل درمانی بیمارانی که از افسردگی متوسط مقاوم به درمان رنج میبرند مورد استفاده قرار بگیرد. در این پژوهش حجم نمونه محدود بوده و تنها با درمان دارویی مورد مقایسه قرار گرفته و دوره پیگیری نیز یک ماهه بوده است. بر این اساس برای دستیابی به نتایج کاربردی لازم است، آزمایشات بالینی کنترل شده بیشتری، اثرات درمانی طولانیمدت تحریک الکتریکی مستقیم مغز را در همراهی یا بدون همراهی با سایر درمآنها از قبیل رواندرمانی مورد ارزیابی قرار دهند. همچنین اثربخشی این روش درمانی برای تعیین پارامترهای بهینه تحریک به منظور بهبودی حداکثری خلق به مطالعات بیشتری نیاز دارد.
سپاسگزاری
این پژوهش حاصل طرح تحقیقاتی است که در دانشگاه علوم پزشکی قم به تصویب رسیده است. بدین وسیله محققان از دانشگاه علوم پزشکی قم که با تامین مالی امکانات لازم برای اجرای طرح را در اختیار محققان قرار دادند و از تمامی افراد شرکتکننده در این پژوهش تشکر و قدردانی به عمل می-آورند.
حامی مالی: دانشگاه علوم پزشکی قم
تعارض در منافع: وجود ندارد.
براساس آمار سازمان بهداشت جهانی اختلال افسردگی اساسی (Major Depressive Disorder (MDD))یکی از شایعترین اختلالات روانشناختی و وضعیت ناتوان کنندهای است که هزینههای فردی، اجتماعی، اقتصادی زیادی را بر فرد و جامعه تحمیل کرده و میزان بالایی از مرگ و میر و ناتوانی عمده را به همراه دارد (1). پاسخ ضعیف به داروهای ضدافسردگی و افسردگی مقاوم به درمان یکی از چالشهای عمده در محیطهای بالینی است. تنها یک چهارم بیماران مبتلا به MDD بعد از دریافت اولین دوره داروهای ضدافسردگی بهبود مییابند و حدود 70% از این بیماران نیاز به حداقل چهار دوره درمانی دیگر تا کسب بهبودی دارند (2). عدم پاسخ به درمانهای دارویی و غیردارویی، خطر مزمن شدن بیماری، رفتارهای خودکشی (3) کاهش کیفیت زندگی افراد مبتلا به دلیل اختلالات عملکردی (4) باعث شده تا رویکردهای درمانی دیگر از جمله تکنیکهای تحریک غیرتهاجمی مغز (Non-invasive brain stimulation) (NIBS) برای درمان این اختلال مورد توجه محققان و درمانگران قرار گیرد. تحریک الکتریکی مستقیم مغز (Transcranial Direct Current Stimulation) (tDCS) یک روش درمانی غیرتهاجمی است که باعث تعدیل عصبی برگشتپذیر در فعالیت نواحی مخصوصی از مغز میشود. در واقع تغییرات پتانسیل غشا عصبی و افزایش برانگیختگی قشر مغز از مهمترین مکانیسمهای بیولوژیکی tDCS به حساب میآید (5). علاوه بر تغییرات بالقوه زودگذر و ناگهانی در غشا که میتواند تا یک ساعت ادامه داشته باشدtDCS با تغییرات طولانیمدت سیناپسی همراه است (6). این روش یک فناوری ارزشمند برای سازماندهی ارتباطات مغز-رفتار از طریق حوزههای مختلف حرکتی، شناختی، اجتماعی و هیجانی است (7). در جمعیت افراد سالم یافتهها موید آن است که tDCS باعث تغییر موقت رفتار، سرعت بخشیدن به فرآیند یادگیری و افزایش کارایی در تکالیف میشود (9،8). تعداد زیادی از مطالعات روزافزون انسانی گزارش دادهاند کهtDCS منجر به تقویت عملکرد مغز از جمله یادگیری حرکتی و حافظه میشود (6،10). در حال حاضر اثراتtDCS بر روی قابلیت تحریک عصبی در مطالعات تصویربرداریهای عصبی و روانشناختی مورد تایید قرار گرفته و پایههای عصبی-زیستی برای کاربرد آن جهت تعدیل عصبی در جمعیت بیماران فراهم کرده است (11،12). در این راستا نتایج برخی مطالعات نیز سودمندی این مداخله درمانی، در کاهش توهم بیماران مبتلا به اسکیزوفرنی (13)، بهبود تاخیر در اکتساب زبانی بیماران مبتلا به اختلالات طیف اتیسم (14) و بهبود کارکرد شناختی در بیماران مبتلا به آلزایمر (15) مورد تایید قرار داده است. هر چند این تکنیک در مقایسه با سایر تکنیکهای NIBSمانند تحریک الکتریکی فراجمجمهای (TMS) (Transcranial magnetic stimulation) کمتر مورد مطالعه قرار گرفته و هنوز به تایید سازمان غذا و داروی آمریکا نیز نرسیده اما بهطور گستردهای از لحاظ ایمنی، تحملپذیری (Tolerability) و کارایی بهویژه در MDD مورد توجه محققان بوده و بهصورت موفقیتآمیزی در کاهش علائم MDD بهکار رفته است (12). موسسه ملی تعالی مراقبتهای بهداشتی و درمانی انگلستان در سال 2015 دستورالعمل روش مداخلهای برای تحریک الکتریکی مستقیم مغز در درمان افسردگی را منتشر کرد. این راهنما مبتنی بر اطلاعات بهدست آمده از بررسی بیش از 2000 بیمار در تحقیقات فراتحلیل (شامل 7 مطالعه آزمایشی کنترل شده) یک مطالعه سیستماتیک و یک مطالعه پیگیرانه برچسبباز و مطالعات موردی بود (16). دلایل استفاده از tDCS در اختلال افسردگی اساسی به نتایج مثبت کسب شده از مطالعاتی مربوط میشود که از تحریک الکتریکی فراجمجمهای (TMS) برای درمان بیماران مبتلا به افسردگی اساسی استفاده کردند. شواهد بهدست آمده موید آن است که بیماران مبتلا به MDD تغییرات کارکردی و ساختاری در چندین ناحیه کورتکس از جمله قشر دورسولاترال و شکمی-میانی چپ، آمیگدال و هیپوکامپ نشان میدهند (18،17) به گفته محققان اثرات tDCS در بهبودی افسردگی مربوط به تحریک کانونی (DLPFC) چپ است که با برخی از علائم افسردگی ملانکولیک از جمله علائم روانی-حرکتی ضعیف ارتباط دارد (20،19). بهنظر می¬رسد که اثرات درمانی tDCS در اختلال افسردگی همانند داروهای ضد افسردگی است که منجر به برانگیختگی DLPFC در بیماران و در نهایت تعدیل فعالیت پیش پیشانی راست و چپ متعاقب کاهش علائم افسردگی میشود (21). در مورد اثربخشی tDCS برای درمان افسردگی، دو آزمایش کنترل شده نتایج دلگرم کنندهای را گزارش کردهاند. از نظر فرگنی و همکاران (10= n mA 1، 20 دقیقه در هر جلسه، 5 جلسه در روزهای متناوب) و بوگیو و همکاران (40=n، mA2، 20 دقیقه در هر جلسه، 10 جلسه در روزهای متوالی هفته) tDCS موثرتر از دارونما بود (23،22). در یک تحقیق که روی 245 بیمار مبتلا به MDD انجام شد، یافتهها نشان دادtDCS در مقایسه با سیتالوپرام mg 20 روزانه اثربخشی کمتری دارد. اما نسبت به پلاسبو برتری دارد (24). در یک مطالعه دیگر که روی بیماران افسرده صورت گرفت، پیگیری نشان داد تقریباً 25 درصد از بیمارانی که دو بار در هفته تحت درمانtDCS قرار داشتند، بعد از 6 ماه بیماریشان عود کرد (25). موتز و همکاران در یک فراتحلیل؛ نتایج بهدست آمده از اثربخشی TMS،tDCS و ECT (Electro Convulsive Therapy) در 113 مطالعه آزمایشی که روی مجموعاً 6750 بیمار صورت گرفته بود را مورد بررسی قرار دادند. در این مطالعه ECT با بالاترین نسبت شانس پاسخ ارتباط داشت (26). با توجه به آنچه گفته شد، نتایج در ارتباط با اثرگذاری روش درمانی tDCS متناقض بوده و این در حالی است که بیماری افسردگی هزینه زیادی برای جامعه و رنج بسیاری برای فرد مبتلا دارد که شناسایی اثربخشترین روشهای درمانی به ویژه برای بیماران مقاوم و کم پاسخ ده به درمان دارویی از اهمیت دوچندانی برخوردار میشود. بنابراین هدف از پژوهش حاضر، تعیین اثربخشی tDCS بر کاهش نشانههای افسردگی افراد مبتلا به اختلال افسردگی اساسی است. این پژوهش در صدد پاسخگویی به این پرسشهاست که آیا tDCS موجب کاهش نشانههای افسردگی شرکتکنندگان گروه آزمایش نسبت به گروه کنترل میگردد و آیا نتایج بهدست آمده از این پژوهش در پیگیری یک ماهه نیز پایدار خواهد بود؟
روش بررسی
این پژوهش از نوع کارآزمایی بالینی بوده است. جامعه آماری پژوهش حاضر کلیه افراد مراجعه کننده به یک کلینیک خصوصی خدمات روانشناختی شهر تهران بودند که توسط روانپزشک تشخیص اختلال افسردگی اساسی دریافت کردند. این افراد از هر دو جنس زن و مرد و در بازه سنی ۲۰ تا ۶۰ سال بودند. سطح تحصیلات آنها نیز از ابتدایی تا دکتری متغیر بود. با استفاده از روش نمونهگیری هدفمند تعداد 20 نفر افراد مبتلا که نمرات آنها در پرسشنامه افسردگی بک بالاتر از 18 و در پرسشنامه همیلتون نیز بالاتر از ۱۳ بود، انتخاب شده و با استفاده از روش بلوکبندی تصادفی و با اندازه بلوک برابر 4 به دو گروه مداخله (10 نفر) و کنترل (10 نفر) تقسیم شدند. به دلیل این که مطالعه از نوع تجربی و آزمایشی بود تعداد 10 برای گروه مداخله و کنترل انتخاب شد. هر دو گروه کنترل و مداخله در متغیرهایی نظیر جنس، سن، وضعیت تاهل، نوع داروی مصرفی، تعداد شوک¬های دریافتی در پروتکلهای درمانی پیشین و شدت افسردگی (که با استفاده از هر دو مقیاس درجهبندی هملیتون و بک سنجیده میشد) همتا شدند. معیارهای ورود شامل تشخیص اختلال افسردگی اساسی، سن بالای 18 سال و نداشتن اختلالات بالینی همایند دیگر بود. معیارهای خروج نیز شامل همبودی با سایر اختلالات محورI وII ، سابقه تشنج و صرع، سوءمصرف مواد، اختلالات نورولوژیکی، سابقه بیماری قلبی، شکست در درمان با شوک الکتریکی برای دوره فعلی افسردگی، بارداری، درمان دارویی همزمان با بنزودیازپینها و ضدتشنجها بود. ابزار گردآوری دادهها در این پژوهش شامل مقیاس درجهبندی افسردگی همیلتون (Hamilton Depression Rating Scale) و پرسشنامه افسردگی بک ویرایش دوم (Beck Depression Inventory-II) بود. مقیاس درجهبندی افسردگی همیلتون: در پژوهش حاضر برای ارزیابی شدت افسردگی در طول درمان از این ابزار استفاده گردید. این مقیاس توسط مصاحبهگر اجرا میشود و 8 علامت مربوط به شکایات جسمانی، 5 علامت مربوط به مشکلات رفتاری، 2 علامت مربوط شکایات شناختی و در نهایت 2 علامت هم مربوط به تغییرات هیجانی بیماران افسرده را مورد ارزیابی قرار میدهد. هر پرسش از 0 تا 4 نمرهگذاری میگردد، به صورتیکه 4 بالاترین شدت ممکن را در مورد هر قسمت نشان میدهد (طبیعی= < 7، خفیف= 13-8، متوسط= 18-14). روایی فرم فارسی این ابزار با استفاده از سنجش همبستگی با مقیاس افسردگی بک 0/55 بهدست آمده است. همچنین پایایی بین ارزیابها نیز 0/95 گزارش شده است (27). پرسشنامه افسردگی بک - ویرایش دوم: این ابزار شامل 21 سوال است که نشانه¬های تعریف شده افسردگی از جمله غمگینی، احساس گناه، از دست دادن علاقه، کنارهگیری اجتماعی و افکار خودکشی را طی دو هفته قبل مورد ارزیابی قرار می¬دهد. آیتم¬ها شامل چهار گزینه هستند که روی یک مقیاس 0 تا 3 نمره گذاری میشوند. بدین ترتیب مجموع امتیازها میتواند بین 0 تا 63 تغییر کند که نمرات بالا نشانه شدت بیشتر افسردگی است. تقسیمبندی ارائه شده توسط Beck & Steer برای شدت افسردگی در این پرسشنامه به این قرار است: بدون علامت (۹-۰)، افسردگی خفیف (1۸-1۰)، افسردگی متوسط (۲9-۱۹) و افسردگی شدید (۶۳-۳۰) (28). در مطالعات مربوط به بررسی ویژگیهای روانسنجی فرم فارسی این پرسشنامه ضریب آلفای کرونباخ 0/91 و اعتبار بازآزمایی یک هفتهای 0/96 گزارش شده است (29). روش اجرا به این صورت بود، بیمارانی که توسط روانپزشک حاضر در کلینیک، تشخیص اختلال افسردگی اساسی دریافت میکردند، برای اجرای آزمون به پژوهشگر ارجاع داده میشدند. با بررسیهای روانپزشکی و روانشناسی، مطالعه پرونده و مطابقت با معیارهای ورود و خروج، بیماران وارد طرح پژوهشی میشدند. بعد از ارائه توضیحات لازم در مورد اهداف پژوهش و قبل از اجرای آزمون از بیماران شرکتکننده درخواست میشد تا فرم رضایت آگاهانه را پرکنند. قبل از شروع درمان خط پایه شدت و علایم افسردگی به وسیله پرسشنامه¬های افسردگی بک و همیلتون ارزیابی میشدند. بلافاصله بعد از پایان هرجلسه، بعد از جلسه 5 و جلسه 10 آزمون افسردگی بک برای سنجش شدت افسردگی آزمودنی ها اجرا میگردید. برای ارزیابی دوام و پایداری اثرات درمانی تحریک الکتریکی مستقیم مغز در طول 4 هفته، پس از آخرین جلسه درمان، مقیاس افسردگی بک دوباره اجرا گردیده و نتایج آن در پروفایل آزمودنیها ثبت گردید. هر دو گروه کنترل و آزمایش تحت درمآنهای دارویی ضدافسردگی (بنزودیازپینها) قرار داشتند و گروه آزمایش علاوه بر دارو درمانی، تحت درمان تحریک الکتریکی مستقیم مغز نیز قرار گرفت. به دلایل اخلاقی و برای کنترل متغیرهای مزاحم دوز داروهای ضدافسردگی در طول درمان ثابت نگه داشته شد. جهت رعایت اصول اخلاقی، افراد گروه کنترل وارد لیست انتظار شدند تا در صورت اثربخشی آزمایش، آنها نیز همانند گروه آزمایش مورد مداخله قرار گیرند.
نحوه مداخله درمانی با تحریک الکتریکی مستقیم مغز: تحریک الکتریکی مستقیم مغز به وسیله روانشناس بالینی آموزش دیده برای کار با دستگاه اجرا میشد. تحریک از طریق دستگاه آلمانی NeuroConn با دو الکترود بود. قطب مثبت در کرتکس دورسولترال پره فرونتال که در سیستم 10/20 الکتروانسفالوگرافی با PF3 مشخص میشود جایگذاری میشد و قطب منفی در سوپراوربیتال مخالف قرار داده میشد. الکترودهای لاستیکی (cm 35)که بهوسلیه اسفنجی نمدار پوشیده شده بود بهوسلیه هدبندهایی بر دورسر نگه داشته میشد. تحریک فعالی که برای گروه آزمایشی انجام میشد 2میلیآمپر (mA 2) برای 20 دقیقه بود. شوکها در 10 جلسه و بهصورت فاصله زمانی ۲۴ ساعته انجام میشد. برای تحریک ساختگی در گروه کنترل، تحریک الکتریکی مستقیم مغز بعد از چند ثانیه تحریک خاموش میگردید. برای مقایسه ویژگیهای بالینی و جمعیت شناختی بین دو گروه از آزمون-های x2 و t- test استفاده شد. برای بررسی اثربخشی مداخله، روش Mixed ANOVA و برای در نظر گرفتن اثرات زمان در دو گروه از آزمون تحلیل واریاس اندازهگیری مکرر در سطح معنیداری 0/05 استفاده گردید. نمرات مقیاس همیلتون به عنوان متغیر وابسته،گروهها در دو سطح گروه مداخله و گروه کنترل به عنوان متغیرهای مستقل بین گروهی و زمان در سه سطح 5 روز (بعد از 5 جلسه مداخله)10 روز (10 جلسه بعد از مداخله) و 30 روز (4هفته بعد از پایان درمان) به عنوان متغیرهای مستقل درونگروهی در نظر گرفته شدند.
تجزیه و تحلیل آماری
به منظور تفاوت بین گروهها در هر نقطه از زمان از t.test مستقل و برای آزمون تغییرات درون گروهها در طول زمان ازt.test وابسته استفاده شد. تمامی محاسبات آماری دادهها نیز توسط نرمافزارSPSS version 16 صورت گرفت.
ملاحظات اخلاقی
پروپوزال این تحقیق توسط دانشگاه علوم پزشکی قم تایید شده است (کد اخلاقIR.MUQ.REC.021). شرکتکنندگان با تکمیل فرم رضایت آگاهانه در پژوهش حاضر شرکت کردند و حضور آنها کاملاً داوطلبانه بود. لازم به ذکر است، بیماران به تشخیص روانپزشک نیازمند شوک الکتریکی و درمان فیزیولوژیکی دیگری تشخیص داده نشدند و در نتیجه از نظر اخلاقی شرکت در پژوهش منجر به تاخیر در درمان برای آنها نبود.
نتایج
ویژگیهای بالینی و اطلاعات جمعیت شناختی گروهها در جدول 1 نشان داده شده است. نتایج آزمون تحلیل واریانس مکرر برای نمرات افسردگی همیلتون(F=43/5 و P=0/017) و بک (F=125/12 و P=0/022) نشان دهنده معناداری اثر تعاملی زمان (چهار مرحله اندازهگیری) و عضویت گروهی (آزمایش و کنترل) بود (0/05 >P) که در جدول ۳ نمایش داده شده است. همانطور که جدول ۳ نشان میدهد بین دو گروه آزمایش و کنترل در هر دو متغیر وابسته حداقل در یکی از مراحل مداخله و پیگیری تفاوت معناداری وجود دارد. اثرات درون گروهی مطابق با جدول ۳ نیز بیانگر این است که حتی با اصلاح درجه آزادی بین زمان و عضویت گروهی در متغیرهای وابسته تعامل معنادار وجود دارد (0/05>P). برای بررسی اینکه تفاوت بین گروهها در متغیرهای وابسته در کدام یک از مراحل آزمون (بعد از 5 جلسه، بعد از 10 جلسه و 4هفته بعد از خاتمه درمان) وجود دارد از آزمون t مستقل استفاده شد که نتایج آن در جدول ۴ گزارش شده است. مطابق با این جدول نمرات افسردگی در هر دو مقیاس در گروه آزمایش در مراحل مداخله (در مقیاس همیلتون P=0/019 و در مقیاس بک (P=0/01) و پیگیری (در مقیاس همیلتون P=0/019 و در مقیاس بک 0۳/0P =) نسبت به گروه کنترل بهطور معناداری کاهش یافته است.
جدول 1: تفاوت گروههای آزمایش و کنترل بر حسب ویژگیهای بالینی و اطلاعات جمعیت شناختی قبل از شروع درمان بر اساس نتایج آزمون x2 و t.test

بر اساس نتایج آزمون x2 برای متغیرهای جنسیت و مصرف دارو و t.test برای متغیرهای سن، تعداد دورههای افسردگی و میانگین نمرات افسردگی پایه در مقیاسهای همیلتون و بک در بین گروه مداخله و کنترل تفاوت معنی داری مشاهده نشد.
جدول ۲: نتایج آزمونهای چندگانه تحلیل واریانس مکرر برای متغیرهای افسردگی همیلتون و بک

جدول ۳: نتایج آزمون تحلیل واریانس مکرر برای مقایسه نمرات هر دو مقیاس در گروه آزمایش و کنترل

جدول 4: مقایسه میانگینهای نمرات افسردگی بک و همیلتون در چهار مرحله در گروه آزمایش و کنترل

بحث
هدف اساسی این پژوهش تعیین اثربخشی تحریک الکتریکی مستقیم مغز در کاهش نشانههای افسردگی بیماران مبتلا به افسردگی اساسی بود. نتایج این مطالعه نشان داد، تحریک الکتریکی مستقیم مغز بعد از مداخله و در طول زمان در کاهش نشانههای افسردگی اساسی گروه مداخله برتری نسبی به گروه کنترل داشته است. این نتایج با یافتههای سایر پژوهشها (22،12) همخوانی دارد که نشان دادند تحریک الکتریکی مستقیم مغز در بهبودی علائم افسردگی اثربخش است. همچنین، با توجه به نتایج آزمون، مرحله پیگیری نیز تاییدی بر پایداری ثبات و اثربخشی تحریک الکتریکی مستقیم مغز بر کاهش نشانههای افسردگی این بیماران است. این یافتهها با نتایج بهدست آمده از مطالعات پیشین از قبیل مطالعه Boggio ,et al که این روش را فقط موثرتر از دارونما میدانند ناهمخوان است (23). با این همه تفاوت حجم نمونه و نیز تفاوت در زمانبندی اجرای مداخله (روزهای متوالی یا متناوب در هفته) در تحقیق پیشرو و مطالعه مذکور یکی از دلایل احتمالی این ناهمخوانی در نتایج است. از سوی دیگر تشخیص اینکه چه مقدار از میزان بهبودی مشاهده شده در گروه کنترل مربوط به اثرات شرایط پلاسبو است دشوار میباشد و برای اثبات آن نیاز به کارآزماییهای بالینی دقیقتر با گروه کنترل بزرگتری است. در راستای تفسیر یافتههای پژوهش این فرضیه مطرح میشود که تحریک الکتریکی مستقیم مغز ابزاری است که احتمالاً توانمندی مغز را در پردازش اطلاعات ورودی بهبود میبخشد؛ این ویژگی اثربخشی سایر درمانها را افزایش میولی فرد را از آنها بی نیاز نمیکند (30). در راستای تایید این فرضیه میتوان به نتایج تحقیقاتی اشاره کرد که نشان دادند تحریک الکتریکی مستقیم مغز بر روی کرتکس دورسولاترال پیش پیشانی چپ یک اثر وابسته-دوز دارد (19) و منجر به بهبودی بالینی بیشتر در ترکیب با یک داروی ضد افسردگی نظیر مهارکنندههای انتخابی جذب مجدد سروتونین میشود (21). از سوی دیگر با توجه به اینکه افسردگی علاوه بر کاهش فعالیت کورتکس دورسولاترال پیش پیشانی چپ با بدکارکردی ناحیه تحت قشری لیمبیک همراه است (31) محققان فرض میکنند که تحریک الکتریکی مستقیم مغز عمدتا منجر به فعالسازی قشری میگردد در حالیکه داروهای بازدارنده جذب مجدد سروتونین اغلب منجر به کاهش فعالیت بیش از حد سیستم لیمبیک میشوند (21). نکته دیگری که باید به آن توجه داشت این است که به نظر میرسد مدت زمان و تعداد جلسات روزانه درمان نیز در اثربخشی آن نقش داشته باشد. برای مثال نتایج مطالعات صورت گرفته حاکی از آن است نرخ کارایی در مداخلات برچسب بازی که تحریک الکتریکی مستقیم مغز بهصورت دوبار در روز به مدت 5 روز متوالی ادامه داشته باشد بالاتر از مداخلاتی است که بهصورت به مدت 10 روز، بهصورت روزانه و مدت زمان 20 دقیقه انجام میشود (32). علاوه بر این در روش درمانی تحریک الکتریکی مستقیم مغز تحریک کاتودال (بازداری) ناحیه پیشپیشانی پشتی جانبی راست باعث کاهش پردازشهای هیجانی منفی و تحریک آنودال (افزایش فعالیت) ناحیه پیشپیشانی پشتی جانبی چپ باعث افزایش پردازش هیجانهای مثبت میشود. زیرا نیمکره راست بیشتر مسئول پردازش هیجانی منفی و نیمکره چپ نیز پردازشکننده هیجانهای مثبت است (33). علاوه بر این تحریک ناحیه پیشپیشانی پشتی جانبی باعث کاهش ارتباطهای بین قشر سینگلوت قدامی، شبکه پیشفرض مغز، اینسولا و همچنین کاهش ارتباط بین هیپوکامپ و شبکه برجستگی میشود که در نهایتا باعث عملکرد بهتر افراد افسرده و کاهش نشانههای افسردگی در آنها میشود (34). همچنین باید گفت یکی از علایم اصلی در اختلال افسردگی اساسی نشخوار فکری است. ناحیه پیشپیشانی پشتیجانبی که در درمان تحریک الکتریکی مستقیم مغز درگیر است ارتباط بسیار نزدیکی با نشخوار فکری دارد. در نشخوار فکری در شبکه اجرایی مرکزی و شبکه حالت پیش فرض مغز درگیری دارند که سطوح بالای فعالیت شبکه حالت پیش فرض با میزان بالای نشخوار فکری افسردهساز همراه است و میزان پایین فعالیت آن نیز با سبکهای فکری انطباقی رابطه دارد. همزمان با افزایش شبکه حالت پیش فرض، شبکه اجرایی مرکزی فعالیت خود را افزایش میدهد. بنابراین این درمان نقش مهمی در ایجاد تعادل بین دو شبکه و بهبود فکری فرد افسرده دارد (35). این تحریک در نیمکره راست با تعدیل پردازش شناختی و اطلاعات هیجانی منفی و همچنین در نیمکره چپ با افزایش کنترل شناختی بر محرک عاطفی مثبت بر نشخوار فکری اثرگذار است (36). همچنین شواهد تحقیقاتی موید این نکته است که اگر چه کیفیت روشهای تحریک مغناطیسی فراجمجمهای مکرر (Repetitive transcranial magnetic stimulation) مانند تحریک مغناطیسی مکرر مغزی دوطرفه با فرکانس بالا، تحریک مغناطیسی مکرر مغزی با فرکانس پایین و تحریک تتا (Theta burst stimulation) از لحاظ عددی در مقایسه با تحریک الکتریکی مستقیم مغز اثربخشی بیشتری داشتند فاصله اطمینان تکنیکهای تحریک مغناطیسی فراجمجمهای مکرر و تحریک الکتریکی مستقیم مغز با یکدیگر همپوشانی دارد لذا این موضوع هنوز بهصورت لاینحل باقی مانده است که کدام یک از مداخلات تحریک غیرتهاجمی مغز و تا چه اندازه بر دیگر تکنیکها برتری دارد. در این راستا Mutz, et al نشان دادند تحریک الکتریکی مستقیم مغز نسبت به درمان ساختگی برتری داشته است و در طیف مشابه تحریک مغناطیسی مکرر مغزی دوطرفه با فرکانس بالا نیز نسبت به درمان ساختگی برتری نشان داده است (37). در حقیقت حتی اگر تحریک مغناطیسی مکرر مغزی دوطرفه با فرکانس بالا واقعا 20 الی 30 درصد نسبت به تحریک الکتریکی مستقیم مغز اثربخشی بیشتری داشته باشد هزینههای بالای تحریک مغناطیسی مکرر در مقایسه با تحریک مغناطیسی مکرر، باعث میشود تا تحریک الکتریکی مستقیم مغز به عنوان خط اول درمان و تعدیل عصبی در راستای هزینه اثربخشی در نظر گرفته شود، زیرا که اغلب دستگاههای تحریک الکتریکی مستقیم مغز 50 بار ارزانتر از دستگاههای تحریک مغناطیسی مکرر هستند و هزینه¬های اجرایی آن نیز کمتر است. در هر صورت نتایج اغلب تحقیقات در مورد میزان اثربخشی یا کارایی انواع مختلف روشهای تحریک مغزی ضدو نقیض است و باید کارآزمایی¬های بالینی بیشتری برای کشف نحوه کار و میزان اثربخشی این رویکردهای جدید درمانی بهویژه تحریک مغناطیسی مکرر در برنامههای تحقیقاتی گنجانده شود. کوتاه بودن مدت زمان پیگیری، عدم کنترل متغیرهای مزاحمی مانند مصرف داروهای ضدافسردگی و حجم نمونه ناکافی را میتوان از محدودیتهای پژوهش حاضر دانست.
نتیجهگیری
بر اساس نتایج بهدست آمده از این پژوهش تحریک الکتریکی مستقیم مغز به عنوان یک مداخله درمانی در کاهش علائم بیماران مبتلا به اختلال افسردگی موثر میباشد. بهنظر میرسد تحریک الکتریکی مستقیم مغز میتواند بهعنوان یک مداخله درمانی بهتنهایی یا بهعنوان یک راهکار مکمل در پروتکل درمانی بیمارانی که از افسردگی متوسط مقاوم به درمان رنج میبرند مورد استفاده قرار بگیرد. در این پژوهش حجم نمونه محدود بوده و تنها با درمان دارویی مورد مقایسه قرار گرفته و دوره پیگیری نیز یک ماهه بوده است. بر این اساس برای دستیابی به نتایج کاربردی لازم است، آزمایشات بالینی کنترل شده بیشتری، اثرات درمانی طولانیمدت تحریک الکتریکی مستقیم مغز را در همراهی یا بدون همراهی با سایر درمآنها از قبیل رواندرمانی مورد ارزیابی قرار دهند. همچنین اثربخشی این روش درمانی برای تعیین پارامترهای بهینه تحریک به منظور بهبودی حداکثری خلق به مطالعات بیشتری نیاز دارد.
سپاسگزاری
این پژوهش حاصل طرح تحقیقاتی است که در دانشگاه علوم پزشکی قم به تصویب رسیده است. بدین وسیله محققان از دانشگاه علوم پزشکی قم که با تامین مالی امکانات لازم برای اجرای طرح را در اختیار محققان قرار دادند و از تمامی افراد شرکتکننده در این پژوهش تشکر و قدردانی به عمل می-آورند.
حامی مالی: دانشگاه علوم پزشکی قم
تعارض در منافع: وجود ندارد.
References:
1- De Graaf R, Radovanovic M, Van Laar M, Fairman B, Degenhardt L, Aguilar-Gaxiola S, et al. J Early Cannabis Use and Estimated Risk of Later Onset of Depression Spells: Epidemiologic Evidence from the Population-Based World Health Organization World Mental Health Survey Initiative. Am J Epidemiol 2010; 172(2): 149-59.
2- Rush AJ, Trivedi MH, Wisniewski SR, Nierenberg AA, Stewart JW, Warden D, et al. Acute and Longer-Term Outcomes in Depressed Outpatients Requiring One or Several Treatment Steps: A STAR*D Report. Am J Psychiatry 2006; 163(11): 1905-17.
3- Rush AJ, Warden D, Wisniewski SR, Fava M, Trivedi MH, Gaynes BN, et al. STAR*D: Revising Conventional Wisdom. CNS Drugs 2009; 23(8): 627-47.
4- Culpepper L. Functional Impairment and Improvement in Depression. J Clin Psychiatry 2016; 77(1): e35.
5- Stagg CJ, Nitsche MA. Physiological Basis of Transcranial Direct Current Stimulation. Neuroscientist 2011; 17: 37-53.
6- Nitsche M, Nitsche MS, Klein CC, Tergau F, Rothwell JC, and Paulus W. Level of Action of Cathodal DC Polarisation Induced Inhibition of the Human Motor Cortex. Clin Neurophysiol 2003; 114(4): 600-4.
7- Filmer HL, Dux PE, Mattingley JB. Applications of Transcranial Direct Current Stimulation for Understanding Brain Function. Trends Neurosci 2014; 37(12): 742-53.
8- Coffman BA, Clark VP, Parasuraman R. Battery Powered Thought: Enhancement of Attention, Learning, and Memory in Healthy Adults Using Transcranial Direct Current Stimulation. NeuroImage 2014, 85(3): 895-908.
9- Parasuraman R, McKinley RA. Using Noninvasive Brain Stimulation to Accelerate Learning and Enhance Human Performance. Hum Factors 2014; 56(5): 816-24.
10- Reis J, Schambra HM, Cohen LG, Buch ER, Fritsch B, et al. Noninvasive Cortical Stimulation Enhances Motor Skill Acquisition Over Multiple Days Through an Effect on Consolidation. Proc Natl Acad Sci USA 2009; 106(5): 1590-5.
11- Arul-Anandam AP, Loo C. Transcranial Direct Current Stimulation: A New Tool for the Treatment of Depression? J Affect Disord 2009; 117(3): 137-45.
12- Nitsche MA, Cohen LG, Wassermann EM, Priori A, Lang N, Antal A, et al. Transcranial Direct Current Stimulation: State of the Art. Brain Stimul 2008; 1(3): 206-23.
13- Agarwal SM, Shivakumar V, Bose A, Subramaniam A, Nawani H, Chhabra H, et al. Transcranial Direct Current Stimulation in Schizophrenia. Clin Psychopharmacol Neurosci 2013; 11(3): 118-25.
14- Schneider HD, Hopp J. The Use of the Bilingual Aphasia Test for Assessment and Transcranial Direct Current Stimulation to Modulate Language Acquisition in Minimally Verbal Children with Autism. Clin Linguist Phon 2011; 25(6-7): 640-54.
15- Khedr EM, El Gamal NF, EL Fetoh NA, Khalifa H, Ahmad EM, Ali AM. A Double-Blind Randomized Clinical Trial on the Efficacy of Cortical Direct Current Stimulation for the Treatment of Alzheimer’s disease. Front Aging Neurosci 2014; 6: 275.
16- Razza LB, De Smet S, Moffa A, Sudbrack-Oliveira, P, Vanderhasselt MA, Brunoni AR. Follow-Up Effects of Transcranial Direct Current Stimulation (Tdcs) for the Major Depressive Episode: A Systematic Review and Meta-Analysis. Psychiatry Res 2021; 302: 114024.
17- Hamilton JP, Siemer M, Gottlib IH. Amygdala Volume in Major Depressive Disorder: A Meta-Analysis of Magnetic Resonance Imaging Studies. Mol Psychiatry 2008; 13: 993-1000.
18- Koenigs M, Grafman J. The Functional Neuroanatomy of Depression: Distinct Roles for Ventromedial and Dorsolateral Prefrontal Cortex. Behav Brain Res 2009; 201(2): 239-43.
19- Brunoni AR, Moffa AH, Fregni F, Palm U, Padberg F, Blumberger DM, et al. Transcranial Direct Current Stimulation for Acute Major Depressive Episodes: Meta-Analysis of Individual Patient Data. Br J Psychiatry 2016; 208(6): 522-31.
20- Brunoni A, Teng CT, Imamura M, Brasil-Neto JP, Boechat R, Caramelli P, et al. Neuromodulation Approaches for the Treatment of Major Depression: Challenges and Recommendations from a Working Group Meeting. Arq Neuropsiquiatr 2010; 68(3): 433-51.
21- Brunoni AR, Valiengo L, Baccaro A, Zanao TA, De oliveira JF , Goulart A, et al. The Sertraline Vs Electrical Current Therapy for Treating Depression Clinical Study Result from a Factorial, Randomized, Controlled Trial. JAMA Psychiatry 2013; 70(4): 383-91.
22- Fregni F, Boggio PS, Nitsche MA, Marcolin MA, Rigonatti SP, Pascual-Leone A. Treatment of Major Depression with Transcranial Direct Current Stimulation. Bipolar Disord 2006; 8(2): 203-4.
23- Boggio PS, Rigontti SP, Ribeiro RB, Myczkowski ML, Nitsche MA, Pascual-Leone A, et al. A Randomized, Double-Blind Clinical Trial on the Efficacy of Cortical Direct Current Stimulation for the Treatment of Major Depression. Int J Neuropsychopharmacol 2008; 11(2): 249-54.
24- Brunoni AR, Moffa AH, Sampaio-Junior B, Borrione L, Moreno ML, Fernandes, RA and et al. Trial of Electrical Direct-Current Therapy versus Escitalopram for Depression. N Engl J Med 2017; 376(26): 2523-33.
25- Aparicio LVM, Guarienti F, Razza LB, Carvalho AF, Fregni F, Brunoni AR. A Systematic Review on the Acceptability and Tolerability of Transcranial Direct Current Stimulation Treatment in Neuropsychiatry Trials. Brain Stimul 2016; 9(5): 571-681.
26- Mutz J, Vipulananthan V, Carter B, Hurlemann R, Fu CHY, Young AH. Comparative Efficacy and Acceptability of Non-Surgical Brain Stimulation for the Acute Treatment of Major Depressive Episodes in Adults: Systematic Review and Network Meta-analysis. BMJ 2019; 364: l1079.
27- Ebrahimi A, Neshatdoost HT, Mousavi SG, Asadollahi GA, Nasiri H. Controlled Randomized Clinical Trial of Spirituality Integrated Psychotherapy (SIPT), Cognitive-Behavioral Therapy (CBT) and Medication Intervention on Depressive Symptoms and Dysfunctional Attitudes in Patients with Dysthymic Disorder. Adv Biomed Res 2013; 2: 53.
28- Beck AT, Steer RA, Garbin MG. Psychometric Properties of the Beck Depression Inventory Twenty-Five Years of Evaluation. Clinical psychology review 1998, 8(1); 77-100.
29- Fata L. Established Structures of Meaning and Emotional States of Cognitive Processing of Emotional Information: A Comparison of Two Conceptual Frameworks [Dissertation]. Tehran: Iran University of Medical Sciences; 2003. [Persian]
30- Fitzgerald PB, Daskalakis ZJ. A Practical Guide to the Use of Repetitive Transcranial Magnetic Stimulation in the Treatment of Depression. Brain Stimul 2012; 5(3): 287-96.
31- Murray EA, Wise SP, Drevets WC. Localization of Dysfunction in Major Depressive Disorder: Prefrontal Cortex and Amygdala. Biol Psychiatry 2011; 69(12): 43-54.
32- Martin DM, Teng JZ, Lo TY, Alonzo A, Goh T, Iacoviello BM, et al. Clinical Pilot Study of Transcranial Direct Current Stimulation Combined with Cognitive Emotional Training for Medication Resistant Depression. J Affect Disord 2018; 232: 89-95.
33- Brunoni AR, Tortella G, Benseñor IM, Lotufo PA, Carvalho AF, Fregni F. Cognitive Effects of Transcranial Direct Current Stimulation in Depression: Results from the SELECT-TDCS Trial and Insights for Further Clinical Trials. J Affect Disord 2016; 202: 46-52.
34- Philip NS, Barredo J, van’t Wout-Frank M, Tyrka AR, Price LH, Carpenter LL. Network Mechanisms of Clinical Response to Transcranial Magnetic Stimulation in Posttraumatic Stress Disorder and Major Depressive Disorder. Biol psychiatry 2018; 83(3): 263-72.
35- Hamilton JP, Furman DJ, Chang C, Thomason ME, Dennis E, Gotlib IH. Default-Mode and Task-Positive Network Activity in Major Depressive Disorder: Implications for Adaptive and Maladaptive Rumination. Biol psychiatry 2011; 70(4): 327-33.
36- Vanderhasselt MA, De Raedt R, Brunoni AR, Campanhã C, Baeken C, Remue J, et al. Tdcs Over the Left Prefrontal Cortex Enhances Cognitive Control for Positive Affective Stimuli. PloS one 2013; 8(5): e62219.
37- Mutz J, Edgcumbe DR, Brunoni AR, Fu CHY. Efficacy and Acceptability of Non-Invasive Brain Stimulation for the Treatment of Adult Unipolar and Bipolar Depression: A Systematic Review and Meta-Analysis of Randomised Sham-Controlled Trials. Neurosci Biobehav Rev 2018; 92: 291-303.
نوع مطالعه: پژوهشي |
موضوع مقاله:
روانشناسی
دریافت: 1400/8/26 | پذیرش: 1400/11/3 | انتشار: 1402/1/15
دریافت: 1400/8/26 | پذیرش: 1400/11/3 | انتشار: 1402/1/15
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |







