دوره 28، شماره 9 - ( آذر 1399 )
جلد 28 شماره 9 صفحات 3055-3044 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Hosseinzade F, Tabesh H, Farzaneh F. Fabrication of a Reservoir Ring for Sustained and Prolonged Release of Levonorgestrel for Vaginal Administration. JSSU 2020; 28 (9) :3044-3055
URL: http://jssu.ssu.ac.ir/article-1-4995-fa.html
URL: http://jssu.ssu.ac.ir/article-1-4995-fa.html
حسینزاده فاطمه، تابش هادی، فرزانه فرح. ساخت حلقه مخزنی با قابلیت رهایش پیوسته و طولانیمدت داروی لوونورژسترل جهت کاربردهای واژینال. مجله علمي پژوهشي دانشگاه علوم پزشكي شهید صدوقی يزد. 1399; 28 (9) :3044-3055
متن کامل [PDF 1005 kb]
(425 دریافت)
| چکیده (HTML) (1420 مشاهده)
متن کامل: (796 مشاهده)
مقدمه
خونریزی غیرطبیعی رحمی (Abnormal Uterine Bleeding (AUB)) توصیف کننده اختلالات چرخه قاعدگی شامل تکرر، بینظمی، تغییرات طول دوره و حجم خونریزی است. بیش از یک سوم زنان در طول زندگی خود خونریزی غیرطبیعی رحمی را تجربه میکنند. چرخه طبیعی قاعدگی هر 24 تا 38 روز یکبار اتفاق میافتد، بین 7 تا 9 روز طول میکشد و حجم خونریزی بین 5 تا 80 میلیلیتر است، حال تغییر در هریک از این پارامترها، نشاندهنده AUB است (1). فدراسیون بینالمللی زنان و مامایی (International Federation of Gynecology and Obstetrics (FIGO)) دلایل خونریزیهای غیرطبیعی رحمی را در دو دسته دلایل ساختاری (Structural) و غیرساختاری (non-Structural) قرار داده است. دلایل ساختاری شامل پولیپ (Polyp)، آدنومیوزیز (Adenomyosis)، لیومیوم (Leiomyoma) و بدخیمی (Malignancy) و دلایل غیرساختاری شامل اختلال انعقاد خون (Coagulopathy)، مشکلات تخمدانی (Ovulatory disorders)، اندومتریال (Endometrial)، مسائل یاتروژنیک (Iatrogenic) و مشکلات دستهبندی نشده (Not classified) است. بسته به سببشناسی انجام شده برای AUB نوع درمان انتخاب میشود که از درمانهای موجود میتوان بهریسکشن، اعمال جراحی، هورمونهای پروژسترونی و اصلاح سبک زندگی مثل کاهش وزن اشاره کرد. محصولات هورمونی در فرم قرص (Tablet)، دستگاههای درون رحمی (Intra Uterine Device) و پچهای پوستی (Transdermal patch) در کنترل چرخه قاعدگی، خونریزیهای نامنظم و همچنین کاهش خونریزی قاعدگی مؤثر عمل کردهاند (2-5). اما همه این روشهای درمانی با مشکلاتی همراه هستند برای مثال قرصهای هورمونی موجب نوسان سطوح هورمون در پلاسمای خون میشوند (6)، دستگاههای درون رحمی باید تحتنظر پزشک متخصص استعمال شوند و عوارضی همچون درد هنگام کارگذاری و خطر خارج شدن از رحم را ایجاد میکنند (7)، برای مثال میرنا (Mirena) نوعی سیستم درون رحمی حاوی 52 میلیگرم لوونورژسترل است (Levonorgestrel intrauterine system (LNG-IUS)) که در بازه زمانی 5 سال روزانه 20 میکروگرم هورمون را رهایش میدهد و برای درمان AUB مورد استفاده است (8). همچنین پچهای پوستی مشکلاتی نظیر خارش شدید، عدم چسبندگی کامل و قابل رویت بودن (9) دارند. حلقههای واژینال (Vaginal rings (VRs)) نوعی سیستم دارورسانی هستند که از مواد پلیمری ساخته میشوند و حاوی مواد فعال دارویی مثل هورمونها هستند. این حلقهها بهآسانی داخل واژن کار گذاشته میشوند و مواد فعال درزمان مشخص و با الگویی کنترل شده در آن محیط رهایش مییابند. رهایش کنترلشده دارو، عدم مصرف یا استعمال روزانه، بکارگیری دوزهای پایین دارو، امکان بارگذاری همزمان چندین دارو در یک حلقه و تحت کنترل کاربر بودن ازجمله مزایای استفاده از حلقههای واژینال هستند (11, 10). اولین کارآزماییهای بالینی مربوط به حلقه واژینال در دهه 1970 انجام گرفته است که آن حلقه واژینال بهمنظور پیشگیری از بارداری توسعه یافته بوده و حاوی مدروکسی پروژسترون استات (Medroxyprogesterone Acetate) بوده است (12). نواک (Novak) و همکارانش میزان مقبولیت حلقه واژینال پیشگیری کننده از بارداری ترکیبی نوارینگ را طی انجام دو کارآزمایی در آمریکای شمالی و اروپا بررسی کردند. در پایان کارآزمایی 97 درصد از افراد شرکتکننده از شفافیت دستورالعمل حلقه رضایت داشتند، 85 درصد زنان و 71 درصد از همسران (شریکان جنسی) هرگز یا بهندرت حضور حلقه را درطول مقاربت جنسی حس کردند و بهطور کلی 96 درصد کاربران از حلقه راضی بودند (13). بارنتسن (Barentsen) و همکارانش مطالعهای را درجهت تعیین کارایی حلقه واژینال دارای رهایش پیوسته استرادیول با دوز پایین در مقایسه با کرم واژینال حاوی استریول برای بهبود خشکی واژن انجام دادهاند. در هر دو گروه تسکین علائم خشکی واژن و آتروفی واژینال گزارش شده است و استفاده از استرینگ درمقایسه با سیناپاز بین افراد بیشتر ترجیح داده شده است (14). در مطالعهای جهت درمان بیماری اندومتریوزیس از نوعی حلقه واژینال مخزنی سیلیکونی حاوی داروی آناستروزول استفاده گردیده است که طبق نتایج حاصله غلظت آناستروزول در پلاسمای خون در یک بازه زمانی 21 روزه رضایت بخش توصیف شده و همبستگی قابل قبولی بین نتایج در دوحالت برونتنی و درونتنی مشاهده شده است (15). همچنین در پژوهش دیگری از آناستروزول بهعنوان نوعی مهارکننده آروماتاز و لوونورژسترل جهت کاربرد کانتراسپتیو استفاده شده است (16). علاوه بر این در مطالعات مختلفی از هورمون لوونورژسترل بههمراه استروژن برای هورموندرمانی جایگزین استفاده شده است (19-17). در سالهای اخیر حلقههای واژینال برای رسانش داروهای پیشگیری کننده از ابتلا به ویروس نقص سیستم ایمنی انسانی (HumanImmunodeficiency Virus (HIV)) بسیار بهکار رفته است. داروهای MK-2048 و ویکریویروک (20)، تنوفوویر دیزوپروکسیل فومارات (21)، داپیویرین و ماراویروک (22) طی مطالعات مختلف درون حلقههای واژینال بارگذاری شده و حلقهها از نظر رهایش برونتنی و درونتنی دارو، پایداری دارویی، خواص مکانیکی و سایر عوامل مورد ارزیابی قرار گرفتهاند. حلقههای واژینال طراحیهای مختلفی دارند که از رایجترین آنها میتوان بهطراحی ماتریکسی (Matrix) و مخزنی (Reservoir) اشاره کرد (24, 23, 10). هریک از حلقههای واژینال تجاریسازی شده نوارینگ (Nuvaring®)، استرینگ (Estring®) و فمرینگ (Femring®) دارای طراحی مخزنی هستند (25-23). سیلیکون، پلییورتان و اتیلنوینیلاستات در طراحی و ساخت حلقههای واژینال بسیار مورد استفاده قرار گرفتهاند. از دلایل استفاده از سیلیکون در کاربردهای زیستپزشکی میتوان بهسمیت پایین، پایداری دمایی و اکسیداتیو مناسب، نفوذپذیری آسان داروهای آبدوست با وزن مولکولی پایین از آن، خون سازگاری بالا، خنثی بودن ازنظر بیولوژیکی و مدول الاستیتسیته پایین اشاره کرد. استرینگ و فمرینگ ازجمله حلقههای واژینال تجاری شدهای هستند که از سیلیکون ساخته شدهاند (26, 10). اتیلن وینیل استاتها کوپلیمرهای اتیلن و وینیل استات هستند و قدمتی طولانی در کاربردهای دارورسانی دارند (27). نوارینگ که حلقه پیشگیری کننده از بارداری تجاری شده حاوی اتونوژسترل و اتینیلاسترادیول است از اتیلنوینیلاستات ساخته شده است (25). پلییورتانهای ترموپلاستیک زیستسازگار نیز برای ساخت حلقههای واژینال مورد ارزیابی قرار گرفتهاند (23). در این راستا میتوان حلقه واژینال چندمنظوره طراحی شده با استفاده از دو نوع پلییورتان برای رهایش داروی آنتی HIV تنوفوویر (Tenofovir) و لوونورژسترل بهعنوان عامل کانتراسپتیو را نام برد. رهایش داروها در بازه زمانی 90 روزه اندازهگیری شدهاست و از روز 2 تا روز 90 تنوفوویر و لوونورژسترل به ترتیب با نرخ تقریباً ثابت 0/1 ± 7/5 میلیگرم در روز و 2 ± 21 میکروگرم در روز رهایش یافتهاند (29). راهکار پیشنهادی ما برای درمان AUB بکارگیری VR جهت رهایش پیوسته و طولانی مدت داروی لوونورژسترل است. با استفاده از VR میتوان هورمون لوونورژسترل را در مدتزمان طولانی با دوز مشخص روزانه در محیط واژینال رهایش داد. طبق بررسیهای انجام شده هدف پژوهشهای قبلی، استفاده از لوونورژسترل برای پیشگیری از بارداری یا هورمون درمانی جایگزین با یک نرخ معین رهایش روزانه دارو بوده است و در هیچیک از منابع علمی، تحقیقی در خصوص بهکارگیری لوونورژسترل برای درمان AUB انجام نشده است. هدف اصلی در این پژوهش، طراحی یک سامانه دارورسانی بهشکل یک حلقه واژینال حاوی لوونورژسترل با قابلیت کنترل میزان رهایش روزانه آن است که برای این منظور، طراحی حلقه بهصورت مخزنی (Reservoir Solution Core (RSC)) انجام گرفته است. حلقه مخزنی از فایبرهای سیلیکونی ساخته شده و هسته حلقه شامل محلول لوونورژسترل و پارافین مایع است.
روش بررسی
طراحی و ساخت حلقههای واژینال حاوی لوونورژسترل
در مطالعه تجربی حاضر، برای ساخت حلقه واژینال مدنظر از فایبرهای سیلیکونی مورد استفاده در دارورسانی استفاده شد، به این صورت که فایبرهای سیلیکونی با ابعاد 6*4 میلی متر (قطر داخلی 4 میلیمتر و قطر خارجی 6 میلیمتر) از شرکت Deutsch-Neumann کشور آلمان تهیه شد. این فایبرها زیستسازگار بوده، تخریب نمیشوند، مواد سمی از خود آزاد نمیکنند، مورد تأیید سازمان غذا و داروی آمریکا (United States Food and Drug Administration (USFDA)) هستند و نسبت به برخی مواد و داروها نفوذپذیرند که برای ساخت سامانه رهایش دارو قابل استفادهاند (شکل1).

شکل1: (1) فایبرهای سیلیکونی 6*4 (2) کلاهکهای یک و دوطرفه (3) حلقه RSC
برای مسدود کردن دو انتهای فایبرها، یک کلاهک (Cap) توسط نرمافزار سالیدورک (SolidWorks 2014) طراحی شد و کلاهکها بهوسیله دستگاه پرینتر سهبعدی کوانتوم (Quantum 2035) ساخته شدند. این کلاهکها از جنس پلیمر اکریلونیتریل بوتادین استایرن (Acrylonitrile butadiene styrene (ABS)) زیستسازگار هستند (29). برای اینکه بتوان غلظت معینی از دارو را در فایبرها بارگذاری کرد نیاز به یک حامل دارو وجود دارد که بتواند دارو را بهصورت همگن در خود حل کند و بایستی بهصورت مایع یا ژل باشد تا در فایبرها بارگذاری شود اما خودش از فایبر نفوذ نکند. حامل پیشنهادی ما در این طرح پارافین مایع بود که خواص موردنظر را داشت. پس از اینکه امکانسنجی رهایش دارو از فایبرها انجام پذیرفت، اولین نمونه بهصورت حلقه توسط فایبرها ساخته شد. برای ساخت این حلقه 17/5 سانتیمتر از فایبرها انتخاب شد، ازآنجاییکه 0/5 سانتیمتر از فایبر از هر طرف با کلاهک پوشیده میشود، طول مؤثر حلقه 16/5 سانتیمتر خواهد بود که معادل حجم داخلی 2 میلیلیتر جهت بارگذاری دارو و حامل آن خواهد بود. حال یک سر آن توسط یک کلاهک دوطرفه کاملاً مسدود میشود. با درنظر گرفتن چگالی پارافین مایع (0/8گرم بر میلیلیتر)، 1/6 گرم پارافین معادل 2 میلیلیتر حجم خواهد داشت. برای ساخت ترکیب دارو و پارافین با غلظت 0/2 درصد وزنی لوونورژسترل، مقدار 3/2 میلیگرم لوونورژسترل با 2 میلیلیتر پارافین ترکیب و توسط همزن مکانیکی کاملا مخلوط میشود و بهنحوی که هیچ حبابی وارد آن نشود داخل حلقه بارگذاری میشود. در نهایت بهکمک سر دیگر کلاهک دوطرفه فایبر کاملا مسدود میشود و به شکل یک حلقه کامل با قطر خارجی 5/5 سانتیمتر در میآید (شکل 1). برای بررسی اثر غلظت داروی بارگذاری شده روی میزان رهایش دارو از فایبرها، سه نوع پروتوتایپ (RSC1 ، RSC2 و RSC3) با مقدار داروی بارگذاری شده 0/1، 0/2 و 0/4 درصد وزنی طراحی گردیدند و مشخصات این پروتوتایپها در جدول 1 آمده است.
جدول 1: سه سری حلقه مخزنی با درصدهای بارگذاری متفاوت لوونورژسترل

طراحی آزمایش رهایش داروی لوونورژسترل
برای بررسی میزان رهایش داروی لوونورژسترل، از هر پروتوتایپ سه نمونه ساخته شده و سپس نمونهها در 100 میلیلیتر از محیط رهایش (بافر سدیم استات 25 میلیمولار با 4/5= pH) و در شیکر انکوباتور با دمای 37 درجه سانتیگراد و rpm 80 قرار میگیرند. پس از 24 ساعت نمونهگیری انجام میشود و توسط دستگاه اسپکتروفتومتر مدلNanoDrop 2000/2000c ساخت شرکت ترمو ساینتیفیک (Thermo Scientific) آمریکا جذب نوری آن در طول موج 247 نانومتر بررسی میشود. میتوان بهکمک نمودار استاندارد، غلظت داروی لوونورژسترل در محیط رهایش را بهدست آورد. نمونهگیری بهصورت روزانه و بهمدت 30 روز و هربار با سه تکرار انجام میگیرد. محیط رهایش بهصورت روزانه تعویض میشود.
تجزیه و تحلیل آماری
بررسی آماری رهایش برون تنی لوونورژسترل از سه پروتوتایپ با آزمون تحلیل واریانس یک طرفه (one-way ANOVA) و آنالیز تعقیبی توکی-کرامر انجام گرفته است. آنالیزها با نرمافزارversion 16 SPSS انجام شده و مقادیر P کمتر از 0/05 (P<0/05) بهعنوان سطح معناداری درنظرگرفته شده است.
ملاحظات اخلاقی
پروپوزال این تحقیق توسط دانشگاه علوم پزشکی شهید بهشتی تایید شده است (کد اخلاق IR.SBMU.RETECH.REC.1395.21).
نتایج
آزمایش رهایش دارو از حلقههای RSC1، RSC2 و RSC3 انجام گرفته است. بهاینصورت که از هر پروتوتایپ سه نمونه تهیه کردیم و هر آزمایش رهایش را سه بار تکرار کردیم.
رهایش دارو در 24 ساعت ابتدایی
برای بهدست آوردن میزان رهایش تجمعی لوونورژسترل در 24 ساعت ابتدایی در ساعتهای اول تا هفتم و همچنین نوزده تا بیست و چهار مقدار رهایش دارو را اندازهگیری کردیم و عددهای نمایش داده شده بصورت Mean ± SD است (شکل (2)). همانطور که در شکل (3) مشاهده میشود در روز اول رهایش انفجاری و نسبتا زیاد از حلقهها اتفاق میافتد که باتوجه به میزان بارگذاری متغیر است. مقدار رهایش انفجاری روز اول حلقه RSC1 1/1 ± 132/74 میکروگرم، حلقه RSC2 0/77 ± 184/45 میکروگرم و حلقه RSC3 1/07 ± 236/15 میکروگرم در 100 میلیلیتر محیط رهایش است. اعداد گزارش شده بهصورت Mean ± SD هستند.
رهایش طولانی مدت 30 روزه
شکل (3) نمودار رهایش روزانه لوونورژسترل از حلقههای مخزنی با درصدهای بارگذاری مختلف را نشان میدهد.
شکل 4) نمودار رهایش تجمعی لوونورژسترل از حلقههای مخزنی با درصدهای بارگذاری متفاوت را نشان میدهد. طبق شکل (4) در یک بازه زمانی 30 روزه مقدار رهایش تجمعی نمونه RSC1 950 میکروگرم، نمونه RSC2 1465 میکروگرم و نمونه RSC3 2665 میکروگرم در 100 میلیلیتر محیط رهایش است. نمودار رهایش تجمعی دارو برحسب زمان اثر میزان لود دارو بر رهایش را نشان میدهد. با افزایش لود دارو در پروتوتایپها، نرخ رهایش دارو بهطور معناداری افزایش مییابد (P<0/01). میزان بارگذاری اولیه لوونورژسترل روی درصد تجمعی داروی آزاد شده اثر معکوس دارد بهنحوی که در نمونه RSC3 41/64درصد و در نمونه RSC2 45/78 درصد از لوونورژسترل بارگذاری شده آزاد شده است، درصورتیکه این مقدار در نمونه RSC1 به 59/38 درصد افزایش یافته است. برای بهدست آوردن درصد داروی رهایش یافته نسبت به کل داروی بارگذاری شده از رابطه (1) استفاده میکنیم که در آن مقدار بارگذاری اولیه دارو در حلقه و مقدار رهایش تجمعی دارو در طول 30 روز است.
= [(Ci-Cf)/Ci]*100 (1)درصد داروی باقیمانده در نمونه
همانطور که در شکل 4 مشخص است، در روز اول شیب هر سه نمودار کمی انحنا دارد ولی بعد شیب ثابت میشود. در درصدهای بارگذاری بالاتر میزان رهایش تجمعی بیشتر است و این تفاوت مشهود در میزان داروی آزادشده را میتوان با توجه به قانون فیک، به گرادیان غلظت موجود بین حلقه و محیط رهایش نسبت داد. با افزایش غلظت لوونورژسترل در حلقه، گرادیان غلظت نیز زیاد میشود، لذا شار انتقال جرم نیز متعاقباً افزایش پیدا میکند. نتایج حاصل نیز این فرضیه را تأیید میکند.

شکل2: نمودار رهایش تجمعی لوونورژسترل از حلقههای مخزنی با درصدهای بارگذاری متفاوت طی 24 ساعت ابتدایی
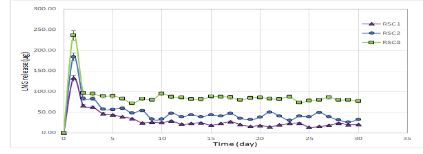
شکل 3: نمودار رهایش روزانه لوونورژسترل از حلقههای مخزنی با درصدهای بارگذاری متفاوت

شکل 4 نمودار رهایش تجمعی لوونورژسترل از حلقه های مخزنی با درصدهای بارگذاری متفاوت
بحث
در این پژوهش سه حلقه واژینال مخزنی حاوی مقادیر متفاوت هورمون لوونورژسترل طراحی شده است و رهایش روزانه و تجمعی آنها باهم مقایسه شده است. همانطور که در شکل 2 دیده میشود و طبق جدول 2 برای نمونه RSC3 میزان رهایش در ساعت اول با شیب بیشتری نسبت به ساعتهای دیگر رخ داده و در واقع بخش عمده رهایش انفجاری این نمونه در ساعت اول رخ داده است. برای نمونههای RSC1 و RSC2 بهترتیب شیب نمودار در ساعت ششم و پنجم بیشتر است و در این ساعت ها میزان رهایش بالاتری از هورمون را داریم. حال دلیل این موضوع ممکن است به ضریب نفوذ هورمون، لایه تماسی سیلیکون و مایع محیط رهایش و یا غلظت دارویی که باید به سطح سیلیکون برسد و رهایش یابد برگردد که برای درک این قضیه نیاز به آزمایشهای بیشتری است. در پایان 24 ساعت اول مقدار رهایش سه پروتوتایپ RSC1، RSC2 و RSC3 بهترتیب 1/1 ± 132/74، 0/77 ± 184/45 و 1/07 ± 236/15 میکروگرم در 100 میلیلیتر محیط رهایش است. این میزان رهایش بهترتیب 8/3، 5/76 و 3/69 درصد از میزان بارگذاری اولیه است. مقدار بارگذاری هورمون در هر مرحله دو برابر شده است اما میزان رهایش در هر مرحله دو برابر نشده است، بهعبارت دیگر رهایش افزایش یافته است اما با میزان بارگذاری اولیه رابطه خطی ندارد. همانطور که در شکل 3 دیده میشود و در جدول 3 هم آورده شده است، یک رهایش انفجاری اولیه در روز اول داریم، در پروتوتایپهای RSC1 و RSC2 در روز دو و سه هم رهایش بالایی داریم و همچنان درحالت پس از انفجار هستیم و میتوانیم نتیجه بگیریم که برای این دو پروتوتایپ از روز 4 به بعد نوسانات کم میشود و رهایش بهحالت پایدار میرسد، اما برای پروتوتایپ RSC3 از روز 2 به حالت پایدار میسیم و این موضوع را میتوان طبق جدول4 باتوجه به میانگین رهایش روزانه در بازههای زمانی مختلف دریافت. رهایش انفجاری در روز اول میتواند ناشی از نفوذ دارو در دیواره حلقه قبل از اینکه شرایط به حالت تعادل برسد باشد. ازطرفی میتوان این مقدار داروی آزاد شده در روز اول را به میزان داروی نفوذ کرده در پلیمر در بازه ذخیرهسازی یا انبارش (Storage) حلقه قبل از استفاده و مطالعه نسبت داد (30). بهطور منطقی انتظار میرود، هرچه حلالیت دارو در پلیمر بیشتر باشد، میزان رهایش انفجاری اولیه نیز بیشتر شود. میزان داروی نفوذ کرده در پلیمر در زمان انبارش را میتوان با محاسبه میزان آزاد شده بهصورت انفجاری در روز اول بهدست آورد زیرا ضریب نفوذ با غلظت داروی بارگذاری شده نسبتی ندارد.
جدول 2: مقادیر شیب نمودار رهایش تجمعی در 24 ساعت ابتدایی
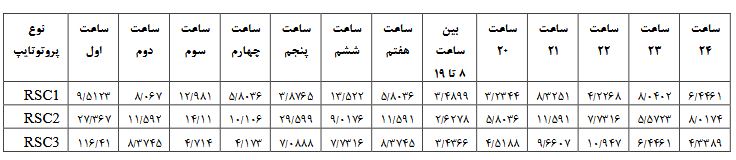
جدول 3: مقادیر حداقل و حداکثر رهایش، رهایش انفجاری روز اول و درصد رهایش تجمعی

جدول 4: میانگین رهایش روزانه در بازههای زمانی مختلف برای سه پروتوتایپ
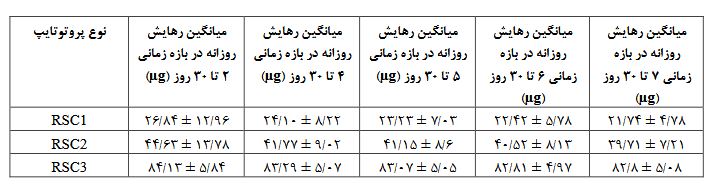
در شکل (5) میانگین رهایش روزانه لوونورژسترل برحسب میکروگرم از سه پروتوتایپ نشان داده شده است. باتوجه بهشکل 5 اگر برای کل زمانی که پایدار هستیم (از روز دوم برای RSC3 و از روز چهارم برای RSC1 و RSC2) نمودار میانگین رهایش روزانه سه پروتوتایپ را برحسب میزان بارگذاری اولیه هورمون رسم کنیم درمییابیم رابطه بین میزان بارگذاری و رهایش رابطهای خطی است و با دوبرابر شدن بارگذاری میانگین رهایش نیز دوبرابر میشود. باتوجه به رابطه L+ 2/92 R = 201/77میتوان برای پروتوتایپهای با میزان بارگذاری مختلف دارو میانگین رهایش روزانه را بدست آورد. همچنین طبق رابطه L= 0/00496 R-0/0145 اگر مقدار میانگین رهایش روزانه خاصی مدنظر داشته باشیم میتوانیم باتوجه به این رابطه مقدار بارگذاری دارو را تنظیم کنیم.
در شکل (6) نمودار مقدار رهایش لوونورژسترل برحسب میکروگرم از سه پروتوتایپ در فاز انفجاری رسم شده است. همانطور که در شکل (6) دیده میشود، مقدار رهایش لوونورژسترل در فاز انفجاری با میزان بارگذاری اولیه رابطه غیرخطی دارد. باتوجه به رابطه B = 953 L2 + 822/4 L + 58/56 میتوان با تغییر بارگذاری اولیه دارو میزان رهایش انفجاری را پیشبینی کرد. مقایسه سه پروتوتایپ طراحی شده با LNG-IUS نشان میدهد حلقه RSC1 با مقادیر رهایش روزانه حدود 20 میکروگرم، نزدیکترین پروتوتایپ به دستگاه تجاریسازی شده میرنا برای درمان AUB است با این تفاوت که با استفاده از حلقههای واژینال عوارض ناشی از LNG-IUS که پیشتر توضیح داده شد برطرف میگردد.

شکل 5: میانگین رهایش روزانه لوونورژسترل (میکروگرم) از سه پروتوتایپ
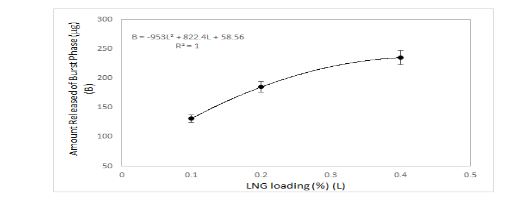
شکل 6: مقدار رهایش لوونورژسترل (میکروگرم) در فاز انفجاری از سه پروتوتایپ
نتیجهگیری
حلقههای واژینال ازجمله سیستمهای دارورسانی هستند که قابلیت رهایش کنترلشده و پیوسته دارو در محیط واژن را دارا هستند. طی دارورسانی واژینال، داروی جذب شده از واژن ازطریق عروق ایلیاک داخلی وارد گردش خون سیستمیک میشود و با حذف متابولیسم عبور اول کبدی، دارورسانی مؤثرتری انجام میشود (16). حلقههای واژینال طراحیهای مختلفی دارند که دو نوع مخزنی و ماتریکسی جزء رایجترین طراحیها محسوب میشوند و طراحی حلقههای تجاریسازی شده نیز براساس همین دو نوع استوار بوده است (23). تاکنون از حلقههای واژینال برای کاربردهای دارورسانی مختلف بهره برده شده است. هورمونهای استروژنی و پروژسترونی جهت پیشگیری از بارداری و هورمون درمانی جایگزین (HRT)، مهارکنندههای آروماتاز برای درمان اندومتریوزیس و داروهای پیشگیری کننده از ابتلا به HIV ازجمله رایجترین مواد مؤثره بکارگرفته شده در حلقههای واژینال هستند. در این تحقیق با طراحی نوعی سیستم مخزنی سیلیکونی، رهایش پیوسته و طولانیمدت هورمون لوونورژسترل در مدت مورد نیاز 30 روز جهت درمان خونریزی غیرطبیعی رحمی بررسی شد و نتایج تحقیق نشان داد که حلقهها میتوانند جایگزین مناسبی برای قرصهای هورمونی باشند و از عوارض جانبی این قرصها بکاهند. البته امکان رهایش بیشتر از 30 روز نیز وجود دارد که نیاز به تستهای تکمیلیتر دارد. دراین حلقهها، باتوجه به میزان بارگذاری اولیه دارو تقریبا از روز دوم یا چهارم (با توجه به نوع پروتوتایپ) به یک نرخ رهایش ثابت میرسیم و تا روز سیام این نرخ رهایش همچنان ادامه دارد. مقایسه نتایج این تحقیق با پژوهشهای انجام گرفته نشاندهنده این است که میانگین رهایش روزانه پروتوتایپ RSC1 در محدوده 20 میکروگرم در روز تطابق قابل قبولی با سایر مطالعاتی دارد که از لوونورژسترل بهعنوان عامل کانتراسپتیو استفاده کردهاند (28, 16). علاوه بر این میانگین رهایش روزنه این پروتوتایپ با نتیجه مطالعهای مروری که در آن اثر استفاده از سیستمهای درونرحمی رهایشدهنده لوونورژسترل (LNG-IUS) به میزان 20 میکروگرم در روز در طول استروژن درمانی زنان یائسه، بر کاهش خطر هایپرپلازی آندومتر و سرطان بررسی شده همسو بوده و اثرگذاری سیستم به اثبات رسیده است (19). این پژوهش مشخص نمود که با تغییر میزان بارگذاری اولیه دارو میتوان مقدار رهایش روزانه دارو را با دقت بالایی (0/99= R2) تخمین زد و بنابراین با طراحی انجام شده حلقههای متعدد با میزان رهایش مختلف دارو را تولید نمود که با درنظر گرفتن شرایط بیمار و با توجه به نظر پزشک میتوان از هرکدام از آنها در درمان AUB استفاده نمود. از آنجاییکه مطالعه انجام شده رهایش لوونورژسترل را درحالت برونتنی مورد ارزیابی قرار میدهد، دستیابی به میزان رهایش درونتنی دارو در محیط واژینال تنها از طریق نمونهگیری خون و بهدست آوردن سطح دارو در پلاسمای خون افراد تحت بررسی امکانپذیر است.
سپاسگزاری
محققین این پژوهش مراتب تشکر و قدردانی خود را از حمایتهای مادی و معنوی مرکز تحقیقات پیشگیری از بیماریهای زنان دانشگاه علوم پزشکی شهید بهشتی و دانشکده علوم و فنون نوین دانشگاه تهران اعلام میدارد. این مقاله در راستای پروژه تحقیقاتی با عنوان "سیستم نوین رهایش کنترل شده داروی Levonorgestrel بهمنظور کاربرد همزمان در کنترل AUB و بارداری ناخواسته" مصوب مرکز تحقیقات پیشگیری از بیماریهای زنان دانشگاه علوم پزشکی شهید بهشتی، نگارش شده است.
حامی مالی: این تحقیق با حمایت مالی مرکز تحقیقات پیشگیری از بیماریهای زنان دانشگاه علوم پزشکی شهید بهشتی طی قرارداد شماره 103/ز/95 به انجام رسیده است.
تعارض در منافع: وجود ندارد.
خونریزی غیرطبیعی رحمی (Abnormal Uterine Bleeding (AUB)) توصیف کننده اختلالات چرخه قاعدگی شامل تکرر، بینظمی، تغییرات طول دوره و حجم خونریزی است. بیش از یک سوم زنان در طول زندگی خود خونریزی غیرطبیعی رحمی را تجربه میکنند. چرخه طبیعی قاعدگی هر 24 تا 38 روز یکبار اتفاق میافتد، بین 7 تا 9 روز طول میکشد و حجم خونریزی بین 5 تا 80 میلیلیتر است، حال تغییر در هریک از این پارامترها، نشاندهنده AUB است (1). فدراسیون بینالمللی زنان و مامایی (International Federation of Gynecology and Obstetrics (FIGO)) دلایل خونریزیهای غیرطبیعی رحمی را در دو دسته دلایل ساختاری (Structural) و غیرساختاری (non-Structural) قرار داده است. دلایل ساختاری شامل پولیپ (Polyp)، آدنومیوزیز (Adenomyosis)، لیومیوم (Leiomyoma) و بدخیمی (Malignancy) و دلایل غیرساختاری شامل اختلال انعقاد خون (Coagulopathy)، مشکلات تخمدانی (Ovulatory disorders)، اندومتریال (Endometrial)، مسائل یاتروژنیک (Iatrogenic) و مشکلات دستهبندی نشده (Not classified) است. بسته به سببشناسی انجام شده برای AUB نوع درمان انتخاب میشود که از درمانهای موجود میتوان بهریسکشن، اعمال جراحی، هورمونهای پروژسترونی و اصلاح سبک زندگی مثل کاهش وزن اشاره کرد. محصولات هورمونی در فرم قرص (Tablet)، دستگاههای درون رحمی (Intra Uterine Device) و پچهای پوستی (Transdermal patch) در کنترل چرخه قاعدگی، خونریزیهای نامنظم و همچنین کاهش خونریزی قاعدگی مؤثر عمل کردهاند (2-5). اما همه این روشهای درمانی با مشکلاتی همراه هستند برای مثال قرصهای هورمونی موجب نوسان سطوح هورمون در پلاسمای خون میشوند (6)، دستگاههای درون رحمی باید تحتنظر پزشک متخصص استعمال شوند و عوارضی همچون درد هنگام کارگذاری و خطر خارج شدن از رحم را ایجاد میکنند (7)، برای مثال میرنا (Mirena) نوعی سیستم درون رحمی حاوی 52 میلیگرم لوونورژسترل است (Levonorgestrel intrauterine system (LNG-IUS)) که در بازه زمانی 5 سال روزانه 20 میکروگرم هورمون را رهایش میدهد و برای درمان AUB مورد استفاده است (8). همچنین پچهای پوستی مشکلاتی نظیر خارش شدید، عدم چسبندگی کامل و قابل رویت بودن (9) دارند. حلقههای واژینال (Vaginal rings (VRs)) نوعی سیستم دارورسانی هستند که از مواد پلیمری ساخته میشوند و حاوی مواد فعال دارویی مثل هورمونها هستند. این حلقهها بهآسانی داخل واژن کار گذاشته میشوند و مواد فعال درزمان مشخص و با الگویی کنترل شده در آن محیط رهایش مییابند. رهایش کنترلشده دارو، عدم مصرف یا استعمال روزانه، بکارگیری دوزهای پایین دارو، امکان بارگذاری همزمان چندین دارو در یک حلقه و تحت کنترل کاربر بودن ازجمله مزایای استفاده از حلقههای واژینال هستند (11, 10). اولین کارآزماییهای بالینی مربوط به حلقه واژینال در دهه 1970 انجام گرفته است که آن حلقه واژینال بهمنظور پیشگیری از بارداری توسعه یافته بوده و حاوی مدروکسی پروژسترون استات (Medroxyprogesterone Acetate) بوده است (12). نواک (Novak) و همکارانش میزان مقبولیت حلقه واژینال پیشگیری کننده از بارداری ترکیبی نوارینگ را طی انجام دو کارآزمایی در آمریکای شمالی و اروپا بررسی کردند. در پایان کارآزمایی 97 درصد از افراد شرکتکننده از شفافیت دستورالعمل حلقه رضایت داشتند، 85 درصد زنان و 71 درصد از همسران (شریکان جنسی) هرگز یا بهندرت حضور حلقه را درطول مقاربت جنسی حس کردند و بهطور کلی 96 درصد کاربران از حلقه راضی بودند (13). بارنتسن (Barentsen) و همکارانش مطالعهای را درجهت تعیین کارایی حلقه واژینال دارای رهایش پیوسته استرادیول با دوز پایین در مقایسه با کرم واژینال حاوی استریول برای بهبود خشکی واژن انجام دادهاند. در هر دو گروه تسکین علائم خشکی واژن و آتروفی واژینال گزارش شده است و استفاده از استرینگ درمقایسه با سیناپاز بین افراد بیشتر ترجیح داده شده است (14). در مطالعهای جهت درمان بیماری اندومتریوزیس از نوعی حلقه واژینال مخزنی سیلیکونی حاوی داروی آناستروزول استفاده گردیده است که طبق نتایج حاصله غلظت آناستروزول در پلاسمای خون در یک بازه زمانی 21 روزه رضایت بخش توصیف شده و همبستگی قابل قبولی بین نتایج در دوحالت برونتنی و درونتنی مشاهده شده است (15). همچنین در پژوهش دیگری از آناستروزول بهعنوان نوعی مهارکننده آروماتاز و لوونورژسترل جهت کاربرد کانتراسپتیو استفاده شده است (16). علاوه بر این در مطالعات مختلفی از هورمون لوونورژسترل بههمراه استروژن برای هورموندرمانی جایگزین استفاده شده است (19-17). در سالهای اخیر حلقههای واژینال برای رسانش داروهای پیشگیری کننده از ابتلا به ویروس نقص سیستم ایمنی انسانی (HumanImmunodeficiency Virus (HIV)) بسیار بهکار رفته است. داروهای MK-2048 و ویکریویروک (20)، تنوفوویر دیزوپروکسیل فومارات (21)، داپیویرین و ماراویروک (22) طی مطالعات مختلف درون حلقههای واژینال بارگذاری شده و حلقهها از نظر رهایش برونتنی و درونتنی دارو، پایداری دارویی، خواص مکانیکی و سایر عوامل مورد ارزیابی قرار گرفتهاند. حلقههای واژینال طراحیهای مختلفی دارند که از رایجترین آنها میتوان بهطراحی ماتریکسی (Matrix) و مخزنی (Reservoir) اشاره کرد (24, 23, 10). هریک از حلقههای واژینال تجاریسازی شده نوارینگ (Nuvaring®)، استرینگ (Estring®) و فمرینگ (Femring®) دارای طراحی مخزنی هستند (25-23). سیلیکون، پلییورتان و اتیلنوینیلاستات در طراحی و ساخت حلقههای واژینال بسیار مورد استفاده قرار گرفتهاند. از دلایل استفاده از سیلیکون در کاربردهای زیستپزشکی میتوان بهسمیت پایین، پایداری دمایی و اکسیداتیو مناسب، نفوذپذیری آسان داروهای آبدوست با وزن مولکولی پایین از آن، خون سازگاری بالا، خنثی بودن ازنظر بیولوژیکی و مدول الاستیتسیته پایین اشاره کرد. استرینگ و فمرینگ ازجمله حلقههای واژینال تجاری شدهای هستند که از سیلیکون ساخته شدهاند (26, 10). اتیلن وینیل استاتها کوپلیمرهای اتیلن و وینیل استات هستند و قدمتی طولانی در کاربردهای دارورسانی دارند (27). نوارینگ که حلقه پیشگیری کننده از بارداری تجاری شده حاوی اتونوژسترل و اتینیلاسترادیول است از اتیلنوینیلاستات ساخته شده است (25). پلییورتانهای ترموپلاستیک زیستسازگار نیز برای ساخت حلقههای واژینال مورد ارزیابی قرار گرفتهاند (23). در این راستا میتوان حلقه واژینال چندمنظوره طراحی شده با استفاده از دو نوع پلییورتان برای رهایش داروی آنتی HIV تنوفوویر (Tenofovir) و لوونورژسترل بهعنوان عامل کانتراسپتیو را نام برد. رهایش داروها در بازه زمانی 90 روزه اندازهگیری شدهاست و از روز 2 تا روز 90 تنوفوویر و لوونورژسترل به ترتیب با نرخ تقریباً ثابت 0/1 ± 7/5 میلیگرم در روز و 2 ± 21 میکروگرم در روز رهایش یافتهاند (29). راهکار پیشنهادی ما برای درمان AUB بکارگیری VR جهت رهایش پیوسته و طولانی مدت داروی لوونورژسترل است. با استفاده از VR میتوان هورمون لوونورژسترل را در مدتزمان طولانی با دوز مشخص روزانه در محیط واژینال رهایش داد. طبق بررسیهای انجام شده هدف پژوهشهای قبلی، استفاده از لوونورژسترل برای پیشگیری از بارداری یا هورمون درمانی جایگزین با یک نرخ معین رهایش روزانه دارو بوده است و در هیچیک از منابع علمی، تحقیقی در خصوص بهکارگیری لوونورژسترل برای درمان AUB انجام نشده است. هدف اصلی در این پژوهش، طراحی یک سامانه دارورسانی بهشکل یک حلقه واژینال حاوی لوونورژسترل با قابلیت کنترل میزان رهایش روزانه آن است که برای این منظور، طراحی حلقه بهصورت مخزنی (Reservoir Solution Core (RSC)) انجام گرفته است. حلقه مخزنی از فایبرهای سیلیکونی ساخته شده و هسته حلقه شامل محلول لوونورژسترل و پارافین مایع است.
روش بررسی
طراحی و ساخت حلقههای واژینال حاوی لوونورژسترل
در مطالعه تجربی حاضر، برای ساخت حلقه واژینال مدنظر از فایبرهای سیلیکونی مورد استفاده در دارورسانی استفاده شد، به این صورت که فایبرهای سیلیکونی با ابعاد 6*4 میلی متر (قطر داخلی 4 میلیمتر و قطر خارجی 6 میلیمتر) از شرکت Deutsch-Neumann کشور آلمان تهیه شد. این فایبرها زیستسازگار بوده، تخریب نمیشوند، مواد سمی از خود آزاد نمیکنند، مورد تأیید سازمان غذا و داروی آمریکا (United States Food and Drug Administration (USFDA)) هستند و نسبت به برخی مواد و داروها نفوذپذیرند که برای ساخت سامانه رهایش دارو قابل استفادهاند (شکل1).

شکل1: (1) فایبرهای سیلیکونی 6*4 (2) کلاهکهای یک و دوطرفه (3) حلقه RSC
برای مسدود کردن دو انتهای فایبرها، یک کلاهک (Cap) توسط نرمافزار سالیدورک (SolidWorks 2014) طراحی شد و کلاهکها بهوسیله دستگاه پرینتر سهبعدی کوانتوم (Quantum 2035) ساخته شدند. این کلاهکها از جنس پلیمر اکریلونیتریل بوتادین استایرن (Acrylonitrile butadiene styrene (ABS)) زیستسازگار هستند (29). برای اینکه بتوان غلظت معینی از دارو را در فایبرها بارگذاری کرد نیاز به یک حامل دارو وجود دارد که بتواند دارو را بهصورت همگن در خود حل کند و بایستی بهصورت مایع یا ژل باشد تا در فایبرها بارگذاری شود اما خودش از فایبر نفوذ نکند. حامل پیشنهادی ما در این طرح پارافین مایع بود که خواص موردنظر را داشت. پس از اینکه امکانسنجی رهایش دارو از فایبرها انجام پذیرفت، اولین نمونه بهصورت حلقه توسط فایبرها ساخته شد. برای ساخت این حلقه 17/5 سانتیمتر از فایبرها انتخاب شد، ازآنجاییکه 0/5 سانتیمتر از فایبر از هر طرف با کلاهک پوشیده میشود، طول مؤثر حلقه 16/5 سانتیمتر خواهد بود که معادل حجم داخلی 2 میلیلیتر جهت بارگذاری دارو و حامل آن خواهد بود. حال یک سر آن توسط یک کلاهک دوطرفه کاملاً مسدود میشود. با درنظر گرفتن چگالی پارافین مایع (0/8گرم بر میلیلیتر)، 1/6 گرم پارافین معادل 2 میلیلیتر حجم خواهد داشت. برای ساخت ترکیب دارو و پارافین با غلظت 0/2 درصد وزنی لوونورژسترل، مقدار 3/2 میلیگرم لوونورژسترل با 2 میلیلیتر پارافین ترکیب و توسط همزن مکانیکی کاملا مخلوط میشود و بهنحوی که هیچ حبابی وارد آن نشود داخل حلقه بارگذاری میشود. در نهایت بهکمک سر دیگر کلاهک دوطرفه فایبر کاملا مسدود میشود و به شکل یک حلقه کامل با قطر خارجی 5/5 سانتیمتر در میآید (شکل 1). برای بررسی اثر غلظت داروی بارگذاری شده روی میزان رهایش دارو از فایبرها، سه نوع پروتوتایپ (RSC1 ، RSC2 و RSC3) با مقدار داروی بارگذاری شده 0/1، 0/2 و 0/4 درصد وزنی طراحی گردیدند و مشخصات این پروتوتایپها در جدول 1 آمده است.
جدول 1: سه سری حلقه مخزنی با درصدهای بارگذاری متفاوت لوونورژسترل

طراحی آزمایش رهایش داروی لوونورژسترل
برای بررسی میزان رهایش داروی لوونورژسترل، از هر پروتوتایپ سه نمونه ساخته شده و سپس نمونهها در 100 میلیلیتر از محیط رهایش (بافر سدیم استات 25 میلیمولار با 4/5= pH) و در شیکر انکوباتور با دمای 37 درجه سانتیگراد و rpm 80 قرار میگیرند. پس از 24 ساعت نمونهگیری انجام میشود و توسط دستگاه اسپکتروفتومتر مدلNanoDrop 2000/2000c ساخت شرکت ترمو ساینتیفیک (Thermo Scientific) آمریکا جذب نوری آن در طول موج 247 نانومتر بررسی میشود. میتوان بهکمک نمودار استاندارد، غلظت داروی لوونورژسترل در محیط رهایش را بهدست آورد. نمونهگیری بهصورت روزانه و بهمدت 30 روز و هربار با سه تکرار انجام میگیرد. محیط رهایش بهصورت روزانه تعویض میشود.
تجزیه و تحلیل آماری
بررسی آماری رهایش برون تنی لوونورژسترل از سه پروتوتایپ با آزمون تحلیل واریانس یک طرفه (one-way ANOVA) و آنالیز تعقیبی توکی-کرامر انجام گرفته است. آنالیزها با نرمافزارversion 16 SPSS انجام شده و مقادیر P کمتر از 0/05 (P<0/05) بهعنوان سطح معناداری درنظرگرفته شده است.
ملاحظات اخلاقی
پروپوزال این تحقیق توسط دانشگاه علوم پزشکی شهید بهشتی تایید شده است (کد اخلاق IR.SBMU.RETECH.REC.1395.21).
نتایج
آزمایش رهایش دارو از حلقههای RSC1، RSC2 و RSC3 انجام گرفته است. بهاینصورت که از هر پروتوتایپ سه نمونه تهیه کردیم و هر آزمایش رهایش را سه بار تکرار کردیم.
رهایش دارو در 24 ساعت ابتدایی
برای بهدست آوردن میزان رهایش تجمعی لوونورژسترل در 24 ساعت ابتدایی در ساعتهای اول تا هفتم و همچنین نوزده تا بیست و چهار مقدار رهایش دارو را اندازهگیری کردیم و عددهای نمایش داده شده بصورت Mean ± SD است (شکل (2)). همانطور که در شکل (3) مشاهده میشود در روز اول رهایش انفجاری و نسبتا زیاد از حلقهها اتفاق میافتد که باتوجه به میزان بارگذاری متغیر است. مقدار رهایش انفجاری روز اول حلقه RSC1 1/1 ± 132/74 میکروگرم، حلقه RSC2 0/77 ± 184/45 میکروگرم و حلقه RSC3 1/07 ± 236/15 میکروگرم در 100 میلیلیتر محیط رهایش است. اعداد گزارش شده بهصورت Mean ± SD هستند.
رهایش طولانی مدت 30 روزه
شکل (3) نمودار رهایش روزانه لوونورژسترل از حلقههای مخزنی با درصدهای بارگذاری مختلف را نشان میدهد.
شکل 4) نمودار رهایش تجمعی لوونورژسترل از حلقههای مخزنی با درصدهای بارگذاری متفاوت را نشان میدهد. طبق شکل (4) در یک بازه زمانی 30 روزه مقدار رهایش تجمعی نمونه RSC1 950 میکروگرم، نمونه RSC2 1465 میکروگرم و نمونه RSC3 2665 میکروگرم در 100 میلیلیتر محیط رهایش است. نمودار رهایش تجمعی دارو برحسب زمان اثر میزان لود دارو بر رهایش را نشان میدهد. با افزایش لود دارو در پروتوتایپها، نرخ رهایش دارو بهطور معناداری افزایش مییابد (P<0/01). میزان بارگذاری اولیه لوونورژسترل روی درصد تجمعی داروی آزاد شده اثر معکوس دارد بهنحوی که در نمونه RSC3 41/64درصد و در نمونه RSC2 45/78 درصد از لوونورژسترل بارگذاری شده آزاد شده است، درصورتیکه این مقدار در نمونه RSC1 به 59/38 درصد افزایش یافته است. برای بهدست آوردن درصد داروی رهایش یافته نسبت به کل داروی بارگذاری شده از رابطه (1) استفاده میکنیم که در آن مقدار بارگذاری اولیه دارو در حلقه و مقدار رهایش تجمعی دارو در طول 30 روز است.
= [(Ci-Cf)/Ci]*100 (1)درصد داروی باقیمانده در نمونه
همانطور که در شکل 4 مشخص است، در روز اول شیب هر سه نمودار کمی انحنا دارد ولی بعد شیب ثابت میشود. در درصدهای بارگذاری بالاتر میزان رهایش تجمعی بیشتر است و این تفاوت مشهود در میزان داروی آزادشده را میتوان با توجه به قانون فیک، به گرادیان غلظت موجود بین حلقه و محیط رهایش نسبت داد. با افزایش غلظت لوونورژسترل در حلقه، گرادیان غلظت نیز زیاد میشود، لذا شار انتقال جرم نیز متعاقباً افزایش پیدا میکند. نتایج حاصل نیز این فرضیه را تأیید میکند.

شکل2: نمودار رهایش تجمعی لوونورژسترل از حلقههای مخزنی با درصدهای بارگذاری متفاوت طی 24 ساعت ابتدایی

شکل 3: نمودار رهایش روزانه لوونورژسترل از حلقههای مخزنی با درصدهای بارگذاری متفاوت

شکل 4 نمودار رهایش تجمعی لوونورژسترل از حلقه های مخزنی با درصدهای بارگذاری متفاوت
بحث
در این پژوهش سه حلقه واژینال مخزنی حاوی مقادیر متفاوت هورمون لوونورژسترل طراحی شده است و رهایش روزانه و تجمعی آنها باهم مقایسه شده است. همانطور که در شکل 2 دیده میشود و طبق جدول 2 برای نمونه RSC3 میزان رهایش در ساعت اول با شیب بیشتری نسبت به ساعتهای دیگر رخ داده و در واقع بخش عمده رهایش انفجاری این نمونه در ساعت اول رخ داده است. برای نمونههای RSC1 و RSC2 بهترتیب شیب نمودار در ساعت ششم و پنجم بیشتر است و در این ساعت ها میزان رهایش بالاتری از هورمون را داریم. حال دلیل این موضوع ممکن است به ضریب نفوذ هورمون، لایه تماسی سیلیکون و مایع محیط رهایش و یا غلظت دارویی که باید به سطح سیلیکون برسد و رهایش یابد برگردد که برای درک این قضیه نیاز به آزمایشهای بیشتری است. در پایان 24 ساعت اول مقدار رهایش سه پروتوتایپ RSC1، RSC2 و RSC3 بهترتیب 1/1 ± 132/74، 0/77 ± 184/45 و 1/07 ± 236/15 میکروگرم در 100 میلیلیتر محیط رهایش است. این میزان رهایش بهترتیب 8/3، 5/76 و 3/69 درصد از میزان بارگذاری اولیه است. مقدار بارگذاری هورمون در هر مرحله دو برابر شده است اما میزان رهایش در هر مرحله دو برابر نشده است، بهعبارت دیگر رهایش افزایش یافته است اما با میزان بارگذاری اولیه رابطه خطی ندارد. همانطور که در شکل 3 دیده میشود و در جدول 3 هم آورده شده است، یک رهایش انفجاری اولیه در روز اول داریم، در پروتوتایپهای RSC1 و RSC2 در روز دو و سه هم رهایش بالایی داریم و همچنان درحالت پس از انفجار هستیم و میتوانیم نتیجه بگیریم که برای این دو پروتوتایپ از روز 4 به بعد نوسانات کم میشود و رهایش بهحالت پایدار میرسد، اما برای پروتوتایپ RSC3 از روز 2 به حالت پایدار میسیم و این موضوع را میتوان طبق جدول4 باتوجه به میانگین رهایش روزانه در بازههای زمانی مختلف دریافت. رهایش انفجاری در روز اول میتواند ناشی از نفوذ دارو در دیواره حلقه قبل از اینکه شرایط به حالت تعادل برسد باشد. ازطرفی میتوان این مقدار داروی آزاد شده در روز اول را به میزان داروی نفوذ کرده در پلیمر در بازه ذخیرهسازی یا انبارش (Storage) حلقه قبل از استفاده و مطالعه نسبت داد (30). بهطور منطقی انتظار میرود، هرچه حلالیت دارو در پلیمر بیشتر باشد، میزان رهایش انفجاری اولیه نیز بیشتر شود. میزان داروی نفوذ کرده در پلیمر در زمان انبارش را میتوان با محاسبه میزان آزاد شده بهصورت انفجاری در روز اول بهدست آورد زیرا ضریب نفوذ با غلظت داروی بارگذاری شده نسبتی ندارد.
جدول 2: مقادیر شیب نمودار رهایش تجمعی در 24 ساعت ابتدایی

جدول 3: مقادیر حداقل و حداکثر رهایش، رهایش انفجاری روز اول و درصد رهایش تجمعی

جدول 4: میانگین رهایش روزانه در بازههای زمانی مختلف برای سه پروتوتایپ

در شکل (5) میانگین رهایش روزانه لوونورژسترل برحسب میکروگرم از سه پروتوتایپ نشان داده شده است. باتوجه بهشکل 5 اگر برای کل زمانی که پایدار هستیم (از روز دوم برای RSC3 و از روز چهارم برای RSC1 و RSC2) نمودار میانگین رهایش روزانه سه پروتوتایپ را برحسب میزان بارگذاری اولیه هورمون رسم کنیم درمییابیم رابطه بین میزان بارگذاری و رهایش رابطهای خطی است و با دوبرابر شدن بارگذاری میانگین رهایش نیز دوبرابر میشود. باتوجه به رابطه L+ 2/92 R = 201/77میتوان برای پروتوتایپهای با میزان بارگذاری مختلف دارو میانگین رهایش روزانه را بدست آورد. همچنین طبق رابطه L= 0/00496 R-0/0145 اگر مقدار میانگین رهایش روزانه خاصی مدنظر داشته باشیم میتوانیم باتوجه به این رابطه مقدار بارگذاری دارو را تنظیم کنیم.
در شکل (6) نمودار مقدار رهایش لوونورژسترل برحسب میکروگرم از سه پروتوتایپ در فاز انفجاری رسم شده است. همانطور که در شکل (6) دیده میشود، مقدار رهایش لوونورژسترل در فاز انفجاری با میزان بارگذاری اولیه رابطه غیرخطی دارد. باتوجه به رابطه B = 953 L2 + 822/4 L + 58/56 میتوان با تغییر بارگذاری اولیه دارو میزان رهایش انفجاری را پیشبینی کرد. مقایسه سه پروتوتایپ طراحی شده با LNG-IUS نشان میدهد حلقه RSC1 با مقادیر رهایش روزانه حدود 20 میکروگرم، نزدیکترین پروتوتایپ به دستگاه تجاریسازی شده میرنا برای درمان AUB است با این تفاوت که با استفاده از حلقههای واژینال عوارض ناشی از LNG-IUS که پیشتر توضیح داده شد برطرف میگردد.

شکل 5: میانگین رهایش روزانه لوونورژسترل (میکروگرم) از سه پروتوتایپ

شکل 6: مقدار رهایش لوونورژسترل (میکروگرم) در فاز انفجاری از سه پروتوتایپ
نتیجهگیری
حلقههای واژینال ازجمله سیستمهای دارورسانی هستند که قابلیت رهایش کنترلشده و پیوسته دارو در محیط واژن را دارا هستند. طی دارورسانی واژینال، داروی جذب شده از واژن ازطریق عروق ایلیاک داخلی وارد گردش خون سیستمیک میشود و با حذف متابولیسم عبور اول کبدی، دارورسانی مؤثرتری انجام میشود (16). حلقههای واژینال طراحیهای مختلفی دارند که دو نوع مخزنی و ماتریکسی جزء رایجترین طراحیها محسوب میشوند و طراحی حلقههای تجاریسازی شده نیز براساس همین دو نوع استوار بوده است (23). تاکنون از حلقههای واژینال برای کاربردهای دارورسانی مختلف بهره برده شده است. هورمونهای استروژنی و پروژسترونی جهت پیشگیری از بارداری و هورمون درمانی جایگزین (HRT)، مهارکنندههای آروماتاز برای درمان اندومتریوزیس و داروهای پیشگیری کننده از ابتلا به HIV ازجمله رایجترین مواد مؤثره بکارگرفته شده در حلقههای واژینال هستند. در این تحقیق با طراحی نوعی سیستم مخزنی سیلیکونی، رهایش پیوسته و طولانیمدت هورمون لوونورژسترل در مدت مورد نیاز 30 روز جهت درمان خونریزی غیرطبیعی رحمی بررسی شد و نتایج تحقیق نشان داد که حلقهها میتوانند جایگزین مناسبی برای قرصهای هورمونی باشند و از عوارض جانبی این قرصها بکاهند. البته امکان رهایش بیشتر از 30 روز نیز وجود دارد که نیاز به تستهای تکمیلیتر دارد. دراین حلقهها، باتوجه به میزان بارگذاری اولیه دارو تقریبا از روز دوم یا چهارم (با توجه به نوع پروتوتایپ) به یک نرخ رهایش ثابت میرسیم و تا روز سیام این نرخ رهایش همچنان ادامه دارد. مقایسه نتایج این تحقیق با پژوهشهای انجام گرفته نشاندهنده این است که میانگین رهایش روزانه پروتوتایپ RSC1 در محدوده 20 میکروگرم در روز تطابق قابل قبولی با سایر مطالعاتی دارد که از لوونورژسترل بهعنوان عامل کانتراسپتیو استفاده کردهاند (28, 16). علاوه بر این میانگین رهایش روزنه این پروتوتایپ با نتیجه مطالعهای مروری که در آن اثر استفاده از سیستمهای درونرحمی رهایشدهنده لوونورژسترل (LNG-IUS) به میزان 20 میکروگرم در روز در طول استروژن درمانی زنان یائسه، بر کاهش خطر هایپرپلازی آندومتر و سرطان بررسی شده همسو بوده و اثرگذاری سیستم به اثبات رسیده است (19). این پژوهش مشخص نمود که با تغییر میزان بارگذاری اولیه دارو میتوان مقدار رهایش روزانه دارو را با دقت بالایی (0/99= R2) تخمین زد و بنابراین با طراحی انجام شده حلقههای متعدد با میزان رهایش مختلف دارو را تولید نمود که با درنظر گرفتن شرایط بیمار و با توجه به نظر پزشک میتوان از هرکدام از آنها در درمان AUB استفاده نمود. از آنجاییکه مطالعه انجام شده رهایش لوونورژسترل را درحالت برونتنی مورد ارزیابی قرار میدهد، دستیابی به میزان رهایش درونتنی دارو در محیط واژینال تنها از طریق نمونهگیری خون و بهدست آوردن سطح دارو در پلاسمای خون افراد تحت بررسی امکانپذیر است.
سپاسگزاری
محققین این پژوهش مراتب تشکر و قدردانی خود را از حمایتهای مادی و معنوی مرکز تحقیقات پیشگیری از بیماریهای زنان دانشگاه علوم پزشکی شهید بهشتی و دانشکده علوم و فنون نوین دانشگاه تهران اعلام میدارد. این مقاله در راستای پروژه تحقیقاتی با عنوان "سیستم نوین رهایش کنترل شده داروی Levonorgestrel بهمنظور کاربرد همزمان در کنترل AUB و بارداری ناخواسته" مصوب مرکز تحقیقات پیشگیری از بیماریهای زنان دانشگاه علوم پزشکی شهید بهشتی، نگارش شده است.
حامی مالی: این تحقیق با حمایت مالی مرکز تحقیقات پیشگیری از بیماریهای زنان دانشگاه علوم پزشکی شهید بهشتی طی قرارداد شماره 103/ز/95 به انجام رسیده است.
تعارض در منافع: وجود ندارد.
References:
1-Fraser IS, Critchley HO, Munro MG, Broder M. Can We Achieve International Agreement on Terminologies and Definitions Used to Describe Abnormalities of Menstrual Bleeding?. Human Reproduction 2007; 22(3): 635-43.
2-Whitaker L, Critchley HO. Abnormal Uterine Bleeding. Best Practice & Research Clinical Obstetrics & Gynaecology 2016; 34: 54-65.
3-Bradley LD, Gueye NA. The Medical Management of Abnormal Uterine Bleeding in Reproductive-Aged Women. American J Obstetrics and Gynecology 2016; 214(1): 31-44.
4-Cheong Y, Cameron IT, Critchley HO. Abnormal Uterine Bleeding. British Medical Bulletin 2017; 123(1): 103-14.
5-Allen C, Kolehmainen C. Intrauterine Devices and other forms of Contraception: Thinking Outside The Pack. Medical Clinics 2015; 99(3): 505-20.
6-Bjarnadóttir RI, Tuppurainen M, Killick SR. Comparison of Cycle Control with a Combined Contraceptive Vaginal Ring and Oral Levonorgestrel/Ethinyl Estradiol. Am J Obstet Gynecol 2002; 186(3): 389-95.
7-Polis RL, Hertweck S. Treatment Options for the Adolescent Patient Experiencing Abnormal Uterine Bleeding. Current Treatment Options in Pediatrics 2016; 2(3): 184-95.
8-Dhamangaonkar C, Anuradha K, Saxena A. Levonorgestrel Intrauterine System (Mirena): An Emerging Tool for Conservative Treatment of Abnormal Uterine Bleeding. J Mid-Life Health 2015; 6(1): 26-30.
9-Graziottin A, Safety. Efficacy and Patient Acceptability of the Combined Estrogen and Progestin Transdermal Contraceptive Patch: A Review. Patient Prefer Adherence 2008; 2: 357-67.
10-Helbling IM, Ibarra JC, Luna JA. The Optimization of an Intravaginal Ring Releasing Progesterone Using a Mathematical Model. Pharm Res 2014; 31(3): 795-808.
11-Brache V, Faundes A. Contraceptive Vaginal Rings: A Review. Contraception 2010; 82(5): 418-27.
12-Mishell Jr DR, Talas M, Parlow AF, Moyer DL. Contraception by Means of a Silastic Vaginal Ring Impregnated with Medroxyprogesterone Acetate. Am J Obstet Gynecol 1970; 107(1): 100-7.
13-Novak A, De la Loge C, Abetz L, Van der Meulen EA. The Combined Contraceptive Vaginal Ring, Nuvaring®: An International Study of User Acceptability. Contraception 2003; 67(3): 187-94.
14-Barentsen R, Van De Weijer PH, Schram JH. Continuous Low Dose Estradiol Released from a Vaginal Ring Versus Estriol Vaginal Cream for Urogenital Atrophy. Eur J Obstet Gynecol Reprod Biol 1997; 71(1): 73-80.
15-Xia L, Qiu S, Liu Z, Ning M. Preparation and in Vitro/In Vivo Evaluation of Anastrozole Reservoir‐Type Intravaginal Ring. Biomed Chromatogr 2019; 33(4): E4459.
16-Nave R. Development of an Intravaginal Ring Delivering Simultaneously Anastrozole and Levonorgestrel: A Pharmacokinetic Perspective. Drug Delivery 2019; 26(1): 586-94.
17-Suvanto-Luukkonen E, KauppilaA. The Levonorgestrel Intrauterine System in Menopausal Hormone Replacement Therapy: Five-Year Experience. Fertility and Sterility 1999; 72(1): 161-63.
18-Suhonen S, HO Allonen, Lähteenmäki. Sustained-Release Estradiol Implants and a Levonorgestrel-Releasing Intrauterine Device in Hormone Replacement Therapy. American J Obstetrics and Gynecology 1995; 172(2): 562-7.
19-Depypere H, Inki P. The Levonorgestrel-Releasing Intrauterine System for Endometrial Protection During Estrogen Replacement Therapy: A Clinical Review. Climacteric 2015; 18(4): 470-82.
20-Liu AY, Zhang J, Anderson PL, Wagner T, Pan Z, Peda M, Gomez K, Beamer M, Jacobson C, Strizki J, Dezzutti CS. Phase 1 Pharmacokinetic Trial of 2 Intravaginal Rings Containing Different Dose Strengths of Vicriviroc (MK-4176) and MK-2048. Clin Infect Dis 2019; 68(7): 1129-35.
21-Keller MJ, Wood L, Billingsley JM, Ray LL, Goymer J, Sinclair S, et al. Tenofovir Disoproxil Fumarate Intravaginal Ring for HIV Pre-Exposure Prophylaxis in Sexually Active Women: A Phase 1, Single-Blind, Randomised, Controlled Trial. Lancet HIV 2019; 6(8): e498-508.
22-Fetherston SM, Boyd P, McCoy CF, McBride MC, Edwards KL, Ampofo S, Malcolm RK. A Silicone Elastomer Vaginal Ring for HIV Prevention Containing two Microbicides with Different Mechanisms of Action. Eur J Pharm Sci 2013; 48(3): 406-15.
23-Malcolm RK, Boyd PJ, Mccoy CF, Murphy DJ. Microbicide Vaginal Rings: Technological Challenges and Clinical Development. Adv Drug Deliv Rev 2016; 103: 33-56.
24-Externbrink A, Eggenreich K, Eder S, Mohr S, Nickisch K, Klein S. Development and Evaluation of Accelerated Drug Release Testing Methods for a Matrix-Type Intravaginal Ring. Eur J Pharm Biopharm 2017; 110: 1-2.
25-Roumen FJ, Apter D, Mulders TM, Dieben TO. Efficacy, Tolerability and Acceptability of a Novel Contraceptive Vaginal Ring Releasing Etonogestrel and Ethinyl Oestradiol. Hum Reprod 2001; 16(3): 469-75.
26-Malcolm RK, Edwards KL, Kiser P, Romano J, Smith TJ. Advances in Microbicide Vaginal Rings. Antiviral Res 2010; 88: S30-9.
27-Schneider C, Langer R, Loveday D, Hair D. Applications of Ethylene Vinyl Acetate Copolymers (EVA) in Drug Delivery Systems. J Control Release 2017; 262: 284-95.
28-Clark JT, Clark MR, Shelke NB, Johnson TJ, Smith EM, Andreasen AK, et al. Engineering a Segmented Dual-Reservoir Polyurethane Intravaginal Ring for Simultaneous Prevention of HIV Transmission and Unwanted Pregnancy. Plos One 2014; 9(3): e88509.
29-Ziąbka M, Dziadek M, Menaszek E. Biocompatibility of Poly (Acrylonitrile-Butadiene-Styrene) Nanocomposites Modified with Silver Nanoparticles. Polymers 2018; 10(11): 1257.
30-Laarhoven JAH, Kruft MA, Vromans H. In Vitro Release Properties of Etonogestrel and Ethinyl Estradiol from a Contraceptive Vaginal Ring. Int J Pharm 2002; 232(1-2): 163-73.
1-Fraser IS, Critchley HO, Munro MG, Broder M. Can We Achieve International Agreement on Terminologies and Definitions Used to Describe Abnormalities of Menstrual Bleeding?. Human Reproduction 2007; 22(3): 635-43.
2-Whitaker L, Critchley HO. Abnormal Uterine Bleeding. Best Practice & Research Clinical Obstetrics & Gynaecology 2016; 34: 54-65.
3-Bradley LD, Gueye NA. The Medical Management of Abnormal Uterine Bleeding in Reproductive-Aged Women. American J Obstetrics and Gynecology 2016; 214(1): 31-44.
4-Cheong Y, Cameron IT, Critchley HO. Abnormal Uterine Bleeding. British Medical Bulletin 2017; 123(1): 103-14.
5-Allen C, Kolehmainen C. Intrauterine Devices and other forms of Contraception: Thinking Outside The Pack. Medical Clinics 2015; 99(3): 505-20.
6-Bjarnadóttir RI, Tuppurainen M, Killick SR. Comparison of Cycle Control with a Combined Contraceptive Vaginal Ring and Oral Levonorgestrel/Ethinyl Estradiol. Am J Obstet Gynecol 2002; 186(3): 389-95.
7-Polis RL, Hertweck S. Treatment Options for the Adolescent Patient Experiencing Abnormal Uterine Bleeding. Current Treatment Options in Pediatrics 2016; 2(3): 184-95.
8-Dhamangaonkar C, Anuradha K, Saxena A. Levonorgestrel Intrauterine System (Mirena): An Emerging Tool for Conservative Treatment of Abnormal Uterine Bleeding. J Mid-Life Health 2015; 6(1): 26-30.
9-Graziottin A, Safety. Efficacy and Patient Acceptability of the Combined Estrogen and Progestin Transdermal Contraceptive Patch: A Review. Patient Prefer Adherence 2008; 2: 357-67.
10-Helbling IM, Ibarra JC, Luna JA. The Optimization of an Intravaginal Ring Releasing Progesterone Using a Mathematical Model. Pharm Res 2014; 31(3): 795-808.
11-Brache V, Faundes A. Contraceptive Vaginal Rings: A Review. Contraception 2010; 82(5): 418-27.
12-Mishell Jr DR, Talas M, Parlow AF, Moyer DL. Contraception by Means of a Silastic Vaginal Ring Impregnated with Medroxyprogesterone Acetate. Am J Obstet Gynecol 1970; 107(1): 100-7.
13-Novak A, De la Loge C, Abetz L, Van der Meulen EA. The Combined Contraceptive Vaginal Ring, Nuvaring®: An International Study of User Acceptability. Contraception 2003; 67(3): 187-94.
14-Barentsen R, Van De Weijer PH, Schram JH. Continuous Low Dose Estradiol Released from a Vaginal Ring Versus Estriol Vaginal Cream for Urogenital Atrophy. Eur J Obstet Gynecol Reprod Biol 1997; 71(1): 73-80.
15-Xia L, Qiu S, Liu Z, Ning M. Preparation and in Vitro/In Vivo Evaluation of Anastrozole Reservoir‐Type Intravaginal Ring. Biomed Chromatogr 2019; 33(4): E4459.
16-Nave R. Development of an Intravaginal Ring Delivering Simultaneously Anastrozole and Levonorgestrel: A Pharmacokinetic Perspective. Drug Delivery 2019; 26(1): 586-94.
17-Suvanto-Luukkonen E, KauppilaA. The Levonorgestrel Intrauterine System in Menopausal Hormone Replacement Therapy: Five-Year Experience. Fertility and Sterility 1999; 72(1): 161-63.
18-Suhonen S, HO Allonen, Lähteenmäki. Sustained-Release Estradiol Implants and a Levonorgestrel-Releasing Intrauterine Device in Hormone Replacement Therapy. American J Obstetrics and Gynecology 1995; 172(2): 562-7.
19-Depypere H, Inki P. The Levonorgestrel-Releasing Intrauterine System for Endometrial Protection During Estrogen Replacement Therapy: A Clinical Review. Climacteric 2015; 18(4): 470-82.
20-Liu AY, Zhang J, Anderson PL, Wagner T, Pan Z, Peda M, Gomez K, Beamer M, Jacobson C, Strizki J, Dezzutti CS. Phase 1 Pharmacokinetic Trial of 2 Intravaginal Rings Containing Different Dose Strengths of Vicriviroc (MK-4176) and MK-2048. Clin Infect Dis 2019; 68(7): 1129-35.
21-Keller MJ, Wood L, Billingsley JM, Ray LL, Goymer J, Sinclair S, et al. Tenofovir Disoproxil Fumarate Intravaginal Ring for HIV Pre-Exposure Prophylaxis in Sexually Active Women: A Phase 1, Single-Blind, Randomised, Controlled Trial. Lancet HIV 2019; 6(8): e498-508.
22-Fetherston SM, Boyd P, McCoy CF, McBride MC, Edwards KL, Ampofo S, Malcolm RK. A Silicone Elastomer Vaginal Ring for HIV Prevention Containing two Microbicides with Different Mechanisms of Action. Eur J Pharm Sci 2013; 48(3): 406-15.
23-Malcolm RK, Boyd PJ, Mccoy CF, Murphy DJ. Microbicide Vaginal Rings: Technological Challenges and Clinical Development. Adv Drug Deliv Rev 2016; 103: 33-56.
24-Externbrink A, Eggenreich K, Eder S, Mohr S, Nickisch K, Klein S. Development and Evaluation of Accelerated Drug Release Testing Methods for a Matrix-Type Intravaginal Ring. Eur J Pharm Biopharm 2017; 110: 1-2.
25-Roumen FJ, Apter D, Mulders TM, Dieben TO. Efficacy, Tolerability and Acceptability of a Novel Contraceptive Vaginal Ring Releasing Etonogestrel and Ethinyl Oestradiol. Hum Reprod 2001; 16(3): 469-75.
26-Malcolm RK, Edwards KL, Kiser P, Romano J, Smith TJ. Advances in Microbicide Vaginal Rings. Antiviral Res 2010; 88: S30-9.
27-Schneider C, Langer R, Loveday D, Hair D. Applications of Ethylene Vinyl Acetate Copolymers (EVA) in Drug Delivery Systems. J Control Release 2017; 262: 284-95.
28-Clark JT, Clark MR, Shelke NB, Johnson TJ, Smith EM, Andreasen AK, et al. Engineering a Segmented Dual-Reservoir Polyurethane Intravaginal Ring for Simultaneous Prevention of HIV Transmission and Unwanted Pregnancy. Plos One 2014; 9(3): e88509.
29-Ziąbka M, Dziadek M, Menaszek E. Biocompatibility of Poly (Acrylonitrile-Butadiene-Styrene) Nanocomposites Modified with Silver Nanoparticles. Polymers 2018; 10(11): 1257.
30-Laarhoven JAH, Kruft MA, Vromans H. In Vitro Release Properties of Etonogestrel and Ethinyl Estradiol from a Contraceptive Vaginal Ring. Int J Pharm 2002; 232(1-2): 163-73.
نوع مطالعه: پژوهشي |
موضوع مقاله:
زنان و زایمان
دریافت: 1398/7/23 | پذیرش: 1399/9/10 | انتشار: 1399/9/10
دریافت: 1398/7/23 | پذیرش: 1399/9/10 | انتشار: 1399/9/10
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |







