دوره 33، شماره 12 - ( اسفند 1404 )
جلد 33 شماره 12 صفحات 9383-9671 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Mesripour A, Satari S, Meamar R, Akbari V, karimi R. Evaluating the Impact of Vitamins C and E Treatment on Paraquat-Induced Acute Toxicity in Animal: A Systematic Review and Meta-Analysis. JSSU 2026; 33 (12) :9671-9383
URL: http://jssu.ssu.ac.ir/article-1-6470-fa.html
URL: http://jssu.ssu.ac.ir/article-1-6470-fa.html
مصری پور آزاده، ستاری سبا، معمار رخساره، اکبری وجیهه، کریمی راهله. بررسی تأثیر مصرف ویتامین C و E بر مسمومیت حاد ناشی از پاراکوات در حیوان: یک مطالعه مروری نظاممند و متاآنالیز. مجله علمي پژوهشي دانشگاه علوم پزشكي شهید صدوقی يزد. 1404; 33 (12) :9671-9383
متن کامل [PDF 813 kb]
(7 دریافت)
| چکیده (HTML) (10 مشاهده)
References:
1- Gil HW, Hong JR, Jang SH, Hong SY. Diagnostic and Therapeutic Approach for Acute Paraquat Intoxication. J Korean Med Sci 2014; 29(11): 1441-9.
2- Bidaki R, Mostafavi N, Al-Saeed S, Zarch M, Karimoddini M, Dehghani F, et al. Oral Ulcers Following Suicide Attempt by Paraquat Herbicide. Hosp Pract Res 2020; 5(3): 117-9.
3- Sabzghabaee A, Eizadi-Mood N, Montazeri K, Yaraghi A, Golabi M. Fatality in Paraquat Poisoning. Singapore Med J 2010; 51(6): 496-500.
4- Delirrad M, Majidi M, Boushehri B. Clinical Features and Prognosis of Paraquat Poisoning: A Review of 41 Cases. Int J Clin Exp Med 2015; 8(5): 8122-8.
5- Dinis-Oliveira R, Duarte J, Sánchez-Navarro A, Remião F, Bastos M, Carvalho F. Paraquat Poisonings: Mechanisms of Lung Toxicity, Clinical Features, and Treatment. Crit Rev Toxicol 2008; 38(1): 13-71.
6- Chatterjee A, Ansar M, Chandra A, Chakraborty U, Dasgupta S. An Overview of Paraquat Poisoning: A Review. Bengal Phys J 2024; 11(1): 24-9.
7- Gawarammana IB, Buckley NA. Medical Management of Paraquat Ingestion. Br J Clin Pharmacol 2011; 72(5): 745-57.
8- Eizadi-Mood N, Sabzghabaee AM, Yaraghi A, Montazeri K, Golabi M, Sharifian A, Badri S. Effect of Antioxidants on the Outcome of Therapy in Paraquat-Intoxicated Patients. Trop J Pharm Res 2011; 10(1): 27-31.
9- Okolonkwo BN. The Effect of Combined Vitamin Treatment on Paraquat-Inflicted Liver Damage. Asian J Biochem Genet Mol Biol 2022; 12(4): 132-8.
10- O'Connor D, Green S, Higgins JPT, editors. Cochrane handbook for systematic reviews of interventions. New Delhi: The Cochrane Collaboration and John Wiley & Sons Ltd; 2011. p. 81–94.
11- Kilkenny C, Browne WJ, Cuthill IC, Emerson M, Altman DG. The ARRIVE Guidelines Checklist: Animal Research Reporting In Vivo Experiments. Plos Biol 2010; 8(6): 1-5.
12- Higgins JP, Thompson SG. Quantifying Heterogeneity in a Meta-Analysis. Suku Stat Med 2002; 21(11): 1539-58
13- Okolonkwo BN, Nyenke CU, Ajibo DN, Ibitoroko GM, Odiabara KK. Chronic Paraquat Exposure on Kidney and Vitamin E and C Treatment Benefits. J Biomed Biosens 2023; 3(3): 3-10.
14- Okolonkwo BN, Brisibe N, Ibitoroko GM. Vitamin E and C Long-Term Treatment Effect on Paraquat Poisoned Liver in Rat. J Appl Health Sci Med 2023; 3(2): 1-8.
15- Okolonkwo BN, Brisibe N, Maureen I. Antidotal Effect of Vitamin E and C in the Management of Paraquat Intoxication in Rat. Health Stud 2023; 1(1): 24-9.
16- Okolonkwo BN, Adjekuko JN, Collins O, Jumbo I. Hematological Recovery by Vitamin E and C on Paraquat Inflicted Hematological Insult in Rattus Norvegicus. Curr J Appl Sci Technol 2022; 41(15): 16-22.
17- Divya VS. Studies on the Ameliorative Effects of Vitamin E on Paraquat Toxicity in Rats [dissertation]. Mannuthy, Kerala, India: College of Veterinary and Animal Sciences, Centre of Excellence in Pathology; 2010.
18- Okolonkwo BN, Adjekuko JN, Collins O, Jumbo I. Ameliorative Effect of Vitamin E on Paraquat Induced Hematological Disorder in Male Albino Rats. Biotechnol J Int 2022; 26(2): 9-17.
19- Okolonkwo BN, Brisibe N, Ibitoroko GM. Evaluating The Impact of Vitamin E Treatment on Paraquat Induced Toxicity in Liver. Curr Res Interdiscip Stud 2023; 2(2): 6-11.
20- Okolonkwo BN, Brisibe N, Ibitoroko GM. Ameliorative Effect of Vitamin E on Paraquat Induced Nephrotoxicity in Rat. Curr Res Interdiscip Stud 2023; 2(2): 1-5.
21- Okolonkwo BN, Ikpeama AR. The Antioxidant Effects of Vitamin C on Liver Enzyme (SGPT) Activity in Rats Under Paraquat Toxicity. Ann Food Sci Technol 2012; 13(1): 100-3.
22- Akinloye OA, Adamson I, Ademuyiwa O, Arowolo TA. Supplementation of Vitamins C, E And its Combination on Paraquat-Intoxicated Rats: Effects on Some Biochemical and Markers of Oxidative Stress Parameters. J Appl Pharm Sci 2011; 1(6): 85-91.
23- Shalaby MA, Emam SR, Soliman AM. Protective Effect of Vitamin E Against Herbicide Paraquat-Induced Enzymatic Leakage and Oxidative Damage in The Liver of Rats. Adv Anim Vet Sci 2020; 8(6): 639-46.
24- Harada N, Saito S, Minakata K. Effects of Vitamin E on Toxicity by Minute Amounts of Paraquat Fed Continuously to Rats. J Nutr Sci Vitaminol 1991; 37(1): 1-13.
25- Rodrigues da Silva M, Schapochnik A, Peres Leal M, Esteves J, Bichels Hebeda C, Sandri S, et al. Beneficial Effects of Ascorbic Acid to Treat Lung Fibrosis Induced by Paraquat. Plos One 2018; 13(11): 1-14.
26- Carr AC, Maggini S. Vitamin C and Immune Function. Nutrients 2017; 9(11): 1211.
27- Okolonkwo BN, Amadi CF, Chikwubike UO, Nyenke CU. The Comparative Effects of Vitamin E+ C on the Chronic Toxicity of Paraquat. Eur J Med Plants 2022; 33(6): 7-13.
متن کامل: (8 مشاهده)
مقدمه
پاراکوات ،]′1-1دی متیل،۴-۴ ′بی پیریدینیوم دی کلراید [، یک ترکیب بی پیریدیل سمیاست. خواص علفکشـی آن در سال ۱۹۵۵ کشف و در سـال ۱۹۶۲ در بـیش از ۱۲۰ کشور بهعنوان یک علفکش قوی و کارآمد معرفی شد و راه خود را در کشاورزی پیدا کرد. این علفکش غیرانتخابی مایع عمدتاً برای کنترل علفهای هرز بهطور گسترده در کشاورزی مورد استفاده قرار میگیرد. این علفکش به دلیل سمیت بالای آن، سلامت انسان را تهدید میکند. مصرف حداقل ۱۰ تا ۲۰ میلی لیتر پاراکوات ۲۰ درصد (در حدود یک قاشق غذاخوری) کشنده است. مصرف تصادفی یا عمدی محصولات حاوی پاراکوات میتواند منجر به مسمومیت شدید شود که اغلب با وجود مداخلات پزشکی منجر به پیامدهای کشنده میشود (1،2). این علفکش در بازار با نام تجاری گراماکسون (Gramaxon 20%) وجود دارد.پاراکوات بهصورت فرمولاسیون محلول قابل حل در آب (20%) بوده که در تماس با خاک به سرعت بیاثر و غیر فعال میشود. مطالعات اندکی در مورد مسمومیت با پاراکوات در ایران انجام شده است. سبزقبایی و همکاران، در یک دوره ۵ ساله (۱۳۸۶-۱۳۸۱) در اصفهان ۲۹ مورد مسمومیت با پاراکوات با میزان مرگ و میر ۲/۵۵ درصد گزارش کردند (3). دلیراد و همکاران در مطالعهای در شهر ارومیه طی یک دوره ۷ ساله (۱۳۹۲-۱۳۸۶) نرخ مرگ و میر ناشی از پاراکوات را ۴/۴۶ درصد گزارش کردند (4). پاراکوات عموماً در پوست و مخاط سالم جذب ضعیفی دارد. جذب دستگاه گوارش نیز کم (۵ تا ۱۰ درصد دوز مصرفی) اما سریع است و غلظت پلاسما در عرض ۲ ساعت پس از مصرف به حداکثر میرسد و بهصورت گسترده در بافتهای بدن انسان توزیع میشود، حجم توزیع تا ۷۵/۲ لیتر به ازای کیلوگرم تخمین زده میشود (5). پاراکوات نسبتاً سریع از بدن دفع میشود بهطوریکه حدود ۸۰ درصد دوز مصرفی طی ۲۴ ساعت از طریق ادرار حذف میشود. با اینحال، دوز باقی مانده و مقدار توزیع شده در بافتها به دلیل کاهش سریع عملکرد کلیه ناشی از سمیت آن بر این ارگان، بسیار آهسته حذف میشوند. بنابراین، در حالیکه نیمهعمر حذف اولیه حدود ۶ ساعت است، نیمهعمر نهایی میتواند تا ۱۲۰ ساعت و بیشتر باشد (5). از آنجاییکه هیچ پادزهر خاصی وجود ندارد، درمانها عمدتاً حمایتی است. درمان فوری عامل بسیار مهمی برای بقا در بیماران مسموم با پاراکوات است. بنابراین، هر بیمار در معرض پاراکوات باید با فوریت پزشکی درمان شود (6،7). پس از پذیرش بیمار در بیمارستان، ارزیابی اولیه و رسیدگی به عوارض تهدید کننده زندگی (راه هوایی، تنفس و قلب و عروق) مطابق با دستورالعملهای موجود، در اولویت قرار گیرد (7). مطالعات نشان داده است که آنتیاکسیدانها باعث کاهش مرگ و میر بیماران دچار مسمومیت با پاراکوات میگردند. مکانیسم اثر این است که آنتی اکسیدانها نظیر ویتامینE و C میتواند الکترونها را به رادیکالهای آزاد اهدا کنند و در نتیجه آنها را خنثی کنند و آسیبهای کبدی و کلیوی را کاهش دهند (8). نتایج مطالعات مختلف نشان میدهد که درمان با ویتامین E و/یاC ممکن است در بیماران مبتلا به سمّیت ناشی از پاراکوات مفید باشد و بهطور بالقوه آسیب کبد و کلیه را کاهش دهد (8،9). با اینحال، شواهد موجود غیرقطعی است و یک ارزیابی سیستماتیک از اثربخشی این ویتامینها در مسمومیت ناشی از پاراکوات را میطلبد. بنابراین، در مطالعه پیش رو قصد داریم شواهد موجود از تاثیر تجویز ویتامینهای C و E در مدیریت عوارض ناشی از سم پاراکوات در مطالعات حیوانی را استخراج کرده و با انجام متاآنالیز بر روی نتایج، بتوانیم در صورت امکان به شواهد قویتری در خصوص اثربخشی این فراوردهها دست یابیم.
روش بررسی
این مطالعه یک مرور نظاممند (Systematic review) به همراه متاآنالیز (فراتحلیل) بود که بر اساس دستورالعمل PRISMA (Preferred Reporting Items for Systematic Reviews and Meta-Analyses) در مورد تأثیر ویتامینهای C و E در بهبود علائم سمّیت ناشی از پاراکوات در حیوان، انجام گرفت. کد اخلاق این تحقیق IR.MUI.PHANUT.REC.1402.052 و تاریخ تصویب 2/10/1402 میباشد. این مطالعه از الگوی PICO(T) (10) پیروی میکند که عبارتند از: ,Pجمعیت Population)) شامل رتهای بالغ مسموم شده با پاراکوات بود. ,I مداخله (Intervention) شامل تجویز ویتامین C و/یا E میباشد. C، مقایسه (Comparison) عبارت از تغییرات قبل و بعد از مداخله میباشد. O، پیامدOutcome) ) مورد بررسی که شامل فاکتورهای نشان دهنده سمیّت کلیوی و کبدی میباشد. T، زمانی Time)) که لازم است تا مداخله انجام گرفته منجر به بروز پیامد مورد نظر گردد، که حداقل چهار هفته میباشد.
روش جستجوی منابع الکترونیکی: ابتدا پایگاههای «Cochrane Database of Systematic Reviews»، «Database of Abstracts of Reviews of Effects (DARE) » و « NIHR Centre for Reviews and Dissemination» جهت جستجوی مقالات مروری مرتبط مورد بررسی قرار گرفتند. پایگاههای الکترونیکی شاملPubMed/Medline, Google scholar ,ISI Web of Science ,Embase, Scopus تا پایان دسامبر ۲۰۲۴ برای مقالات حیوانی با استفاده از برخی لغات انتخابی MeSH (Medical Subject Headings) و سایر لغات مرتبط با موضوع مطالعه، جستجو شدند. لغات اصلی مورد جستجو شامل “Paraquat”)،“Vitamin C ”) (“Vitamin E” AND/OR بود که با واژه AND همزمان با سایر لغات “Toxicity”، “Efficacy”، “Liver enzyme”، “Mortality”،“ALT” ، “AST”، “Creatinine”، “Urea”، و با واژه OR همزمان با سایر لغات“Kidney disease” ،“Renal Failure”، “Hepatic Failure” و به کار بردن فیلتر (Animal) در پایگاههای مذکور مورد جستجو قرار گرفت. مطالعات با زبان انگلیسی و فارسی درنظر گرفته شدند. مقالاتی که در چند پایگاه ایندکس شده بودند، تنها یکبار در آنالیز نهایی وارد شدند.
معیارهای ورود مقالات به مطالعه: نتایج جستجوی اولیه بر اساس عنوان و خلاصه مقاله بررسی شده و مقالات متناسب با موضوع شناسایی شدند. مقالات حیوانی که در این مطالعه مورد بررسی قرار گرفتند، دارای شرایط زیر بودند: جمعیت موشهای صحرایی آزمایشگاهی بالغ با وزن تقریبی ۲۰۰ گرم که پاراکوات را بهصورت خوراکی و یا داخل صفاقی دریافت کرده باشند و ویتامینهای C یا E به منظور بهبود وضعیتشان تجویز شده باشد. نوع مداخله شامل، تجویز ویتامینهای C یا E با دوزهای تقریباً مشابه در گروه ها، به مدت حداقل چهار هفته. پیامدهای مورد بررسی در این مطالعات فاکتورهای نشاندهنده سمیّت کلیوی (سطح اوره و کراتینین)، فاکتورهای نشاندهنده سمیّت کبدی (سطح آنزیمهای کبدی)، و میزان مرگ و میر بود.
خروج مقالات از مطالعه: معیارهای خروج شامل مطالعات فاقد معیارهای نتیجه مرتبط، چکیده کنفرانسها و مطالعاتی بود که در قالب متن کامل در دسترس نبودند. گزارشات موردی(Case reports) ، مقالات مروری و سرمقالهها نیز حذف شدند، ولی رفرانسهای این مقالات جهت دستیابی به سایر مطالعات مرتبط، مورد بررسی قرار گرفت. غربالگری و انتخاب نهایی مقالات از مجموع مقالات اولیه، توسط دو محقق بهصورت مستقل و بر اساس معیارهای فوقالذکر، صورت گرفت. ارزیابی کیفی مطالعات حیوانی: ارزیابی کیفیت مطالعات حیوانی، با استفاده از ابزارهای سنجش کیفیت مقالات ARRIVE (پیوست) متناسب با طراحی مطالعه، کیفیت روش اجرا و و شیوه گزارش نتایج در مقالات، انجام شد. مواردی که در این ارزیابی مورد بررسی قرار گرفت، عبارتند از رعایت ملاحظات اخلاقی، پروسه آزمایشگاهی، شرایط نگهداری حیوانات آزمایشگاهی، تخصیص حیوان به هر گروه، و گزارش پیامدهای مطالعه (11).
استخراج اطلاعات از مقالات: استخراج دادهها بهطور مستقل توسط دو پژوهشگر با استفاده از یک فرم استاندارد استخراج داده، انجام شد. دادههای استخراجشده شامل ویژگیهای مطالعه (مانند طراحی مطالعه، حجم نمونه)، ویژگیهای شرکتکننده (مانند گونه، سن، جنس)، جزئیات (مانند دوز، مسیر تجویز)، نتایج مورد نظر و یافتههای کلیدی بود. تمام محاسبات عددی و دادههای استخراج شده از جداول، اشکال، و نمودارها، توسط متخصص آمار مورد تأیید قرار گرفت. اطلاعات استخراج شده از مقالات که در چکلیستهای از پیش طراحی شده وارد شدند، عبارت بودند از: نام نویسندگان، سال انتشار مقاله، شهر یا کشور محل انجام مطالعه، معیارهای ورود جمعیت به مطالعه، معیارهای خروج جمعیت از مطالعه.
متاآنالیز: دادههای کمّی استخراج شده از مقالات در مورد هر متغیر (پیامد) وارد نرمافزارComprehensive Meta-analysis (CAM-9.1.1) شده و مورد آنالیز قرار گرفت. متاآنالیز تجمعی در صورتی انجام شد که دادههای مرتبط با یک پیامد خاص در بیش از یک مطالعه گزارش شده باشد. به منظور بررسی اثر درمان بر روی متغیرهای کمّی پیوسته، از میانگین/ انحراف معیار هر متغیر استفاده شد. اثر درمان با ویتامینهای C ، E و یا ترکیب این ویتامین ها بر روی هر متغیر در صورتی معنیدار تلقی گردید که P value کوچکتر از ۰۵/۰ باشد. در صورت وجود تعداد مطالعات کافی در زیر گروه ها بر اساس دوز سم و یا زمان بررسی غلظت پارامترها در طول زمان، از تحلیلهای زیر گروهی استفاده شده است. ناهمگونی بین مطالعات با استفاده از تست آماری Chi2 (Cochrane-Q) و آمارهیI2 مورد ارزیابی قرار گرفت تا قدرت شواهدی که بیانگر واقعی بودن ناهمگونی هستند، را تعیین سازد. مقادیر I2 کمتر از ۲۵%، ۲۵-۷۵% و بیشتر از ۷۵% به ترتیب معادل با میزان ناهمگونی کم، متوسط و زیاد در نظر گرفته شد (12). بر این اساس، ناهمگونی بین مطالعات در صورتی معنیدار تلقی گردید که P value حاصل از تست Chi2 کوچکتر از 05/0 باشد. در مورد هر متغیر، در صورتیکه شواهدی از ناهمگونی وجود نداشت (۲۵% I2< )، از مدلFixed effects و در شرایطی که ناهمگونی معنیدار بین مطالعات وجود داشت (۷۵% I2 >)، از رویکرد فراتحلیل به روش اثرات تصادفی (Random effects) استفاده گردید.
نتایج
جمعیت مورد مطالعه: جمعیت نهایی وارد شده به متاآنالیز (از مجموع ۹ مطالعه حیوانی) شامل ۸۵۲ رت بود، که تعداد آن ها از ۳۶ تا ۲۰۰ رت بین مطالعات مختلف، متغیر بود. تمام مطالعات بر روی حیوانات آزمایشگاهی مسموم شده با پاراکوات انجام شده است (شکل 1).
نوع مداخله: از مجموع ۹ مطالعهای که وارد متاآنالیز شدند، ۴ مطالعه در مورد بررسی تأثیر درمان ترکیبی با ویتامینهای C و E (13-16)، ۴ مطالعه در مورد تأثیر ویتامین E (17-20) و یک مطالعه در مورد تأثیر ویتامین C میباشد (21).
پیامدهای مورد بررسی: از مجموع مقالاتی که تحت متاآنالیز قرار گرفتند (۹ مقاله)، عمدتاً پارامترهای مرتبط با آسیب کبدی و کلیوی بررسی شده بودند. همچنین از ۱۳ مطالعه حیوانی مورد بررسی، ۹ مطالعه وارد ارزیابی کیفی و سپس آنالیز کمّی (متاآنالیز) شدند (21-13)؛ و ۴ مطالعه به دلیل تفاوت در پیامدهای مورد بررسی و همچنین طول درمان، فقط مورد ارزیابی کیفی قرار گرفتند و در نهایت وارد متاآنالیز نشدند (25-22)(جدول 1).
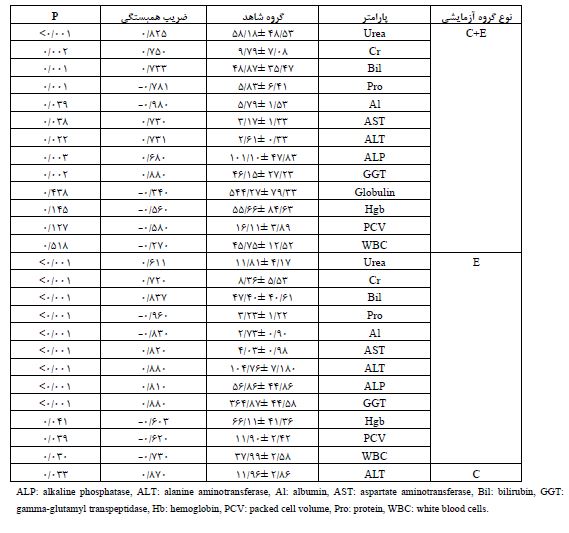
تأثیر پاراکوات و درمان با ویتامینهای C وE بر روی پیامدهای اصلی: از مجموع دادههای گزارش شده در مقالات، تأثیر تجویز ویتامینهای C و E (با دوز و مدت درمانی تقریباً مشابه) بر روی پارامترهای مرتبط با آسیب کبدی و کلیوی به عنوان پیامدهای اصلی مورد ارزیابی قرار گرفت. نتایج (جدول2) نشان داد که بدون توجه به دوز سم و یا زمان پیگیری برای اندازهگیری پارامترها، با وجود آن که پس از دریافت پاراکوات در پارامترهای مختلف روند کاهشی و یا افزایشی وجود داشته است، اما به دلیل کم بودن حجم نمونه مورد بررسی، این اختلاف در هیچیک از آیتمهای مورد بررسی معنادار نبوده است. نتایج (جدول 3) نشان داد که بین میزان پاراکوات تجویز شده و افرایش یا کاهش پارامترها در گروههای مختلف ارتباط معنادار وجود داشت. در صورت مثبت بودن ضریب همبستگی، با افزایش غلظت سم، میزان پارامتر نیز در گروه مربوطه افزایش داشته و در صورت منفی بودن آن، مقدار غلظت پارامتر آزمایشگاهی با افزایش دوز سم کاهش یافت.
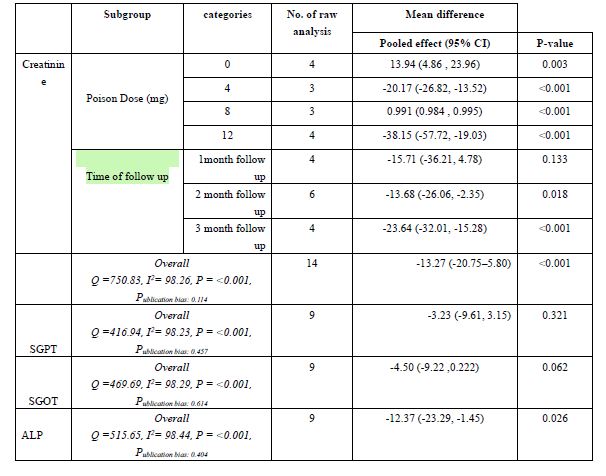
نتایج متاآنالیز: به دلیل وجود مطالعات ناکافی (کمتر از سه مطالعه) بر روی انواع پارامترها، متاآنالیز تنها بر روی پارامترهای Creatinine، SGOT ، SGPT و ALP در مطالعات حیوانی در گروه آزمایشی ویتامین E انجام شد (جدول 4). نتایج نهایی فراتحلیل در مورد پارامترهای مورد بررسی نشان داد، که افزایش کراتینین بهصورت کلی و در اندازهگیریهای پس از دو ماه و سه ماه و در کلیه دوزهای مورد بررسی از پاراکوات، در گروه مداخله نسبت به گروه کنترل معنادار بود. این نتایج در مورد پارامترهای SGPT و SGOT معنادار نبودند. اما در مورد پارامتر ALP به افزایش معنادار دست یافتیم. لازم به ذکر است به دلیل وجود ناهمسانی بین مطالعات، با استفاده از تست آماری Chi2 (Cochrane-Q) و آماره ی I2، کلیه نتایج بر اساس مدل با اثر تصادفی(Random effects) گزارش شد. خطای انتشار در هیچ یک ازحالات با استفاده از آزمون Egger مشاهده نشد.
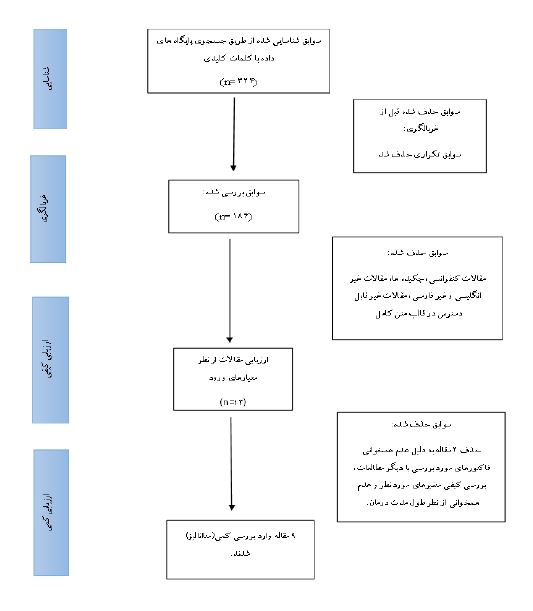
شکل1: فلوچارت انتخاب مطالعات حیوانی
جدول1: مشخصات مطالعات حیوانی
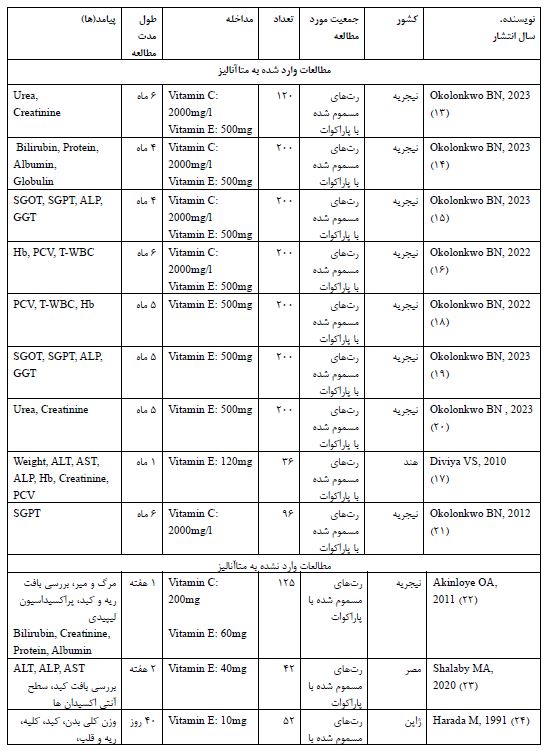
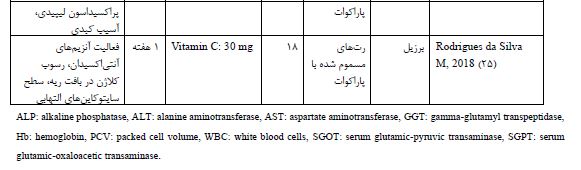
جدول 2: مقایسه غلظت پارامترها به تفکیک گروه مورد و شاهد بدون توجه به دوز پاراکوات در پروتکلهای مختلف مداخله درمطالعات حیوانی.
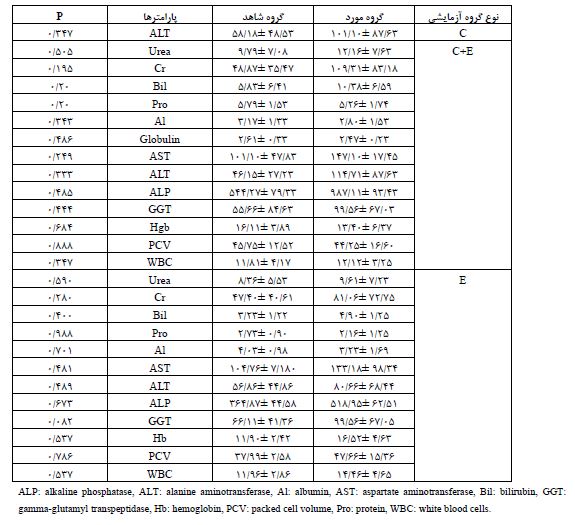
جدول 3: ارتباط میان تغییرات غلظت پارامترها با دوز سمیت بر اساس نوع گروه آزمایشی در مطالعات حیوانی
جدول4: نتایج فراتحلیل برخی پارامترها در مطالعات حیوانی در گروه ویتامین E
بحث
مطالعه حاضر با هدف بررسی تاثیر ویتامینهای C و E بر مسمومیت حاد ناشی از پاراکوات از طریق مرور نظاممند و متاآنالیز انجام شد. یافتههای این تحقیق نشان داد که این ویتامینها میتوانند اثرات حفاظتی قابلتوجهی در برابر آسیبهای ناشی از پاراکوات داشته باشند. این تاثیرات عمدتا از طریق مکانیسمهای کاهش استرس اکسیداتیو، مهار فرآیندهای التهابی و بهبود عملکرد کبد و کلیه اعمال میشوند (21-13). از مجموع ۱۳ مطالعهای که بر روی جمعیت رتها انجام شده بود، ۴ مطالعه فقط مورد بررسی کیفی قرار گرفتند (25-22). این مطالعات به بررسی آسیبهای کبدی، کلیوی، ریوی، میزان بقاء و تغییرات پارامترهای خونی پرداخته اند،که نتایج مشابهی را در پی داشتند و ۹ مطالعه دیگر وارد بررسی کمی شدند (13-21). نتایج مطالعات حیوانی نشان داد که مصرف ویتامینهای C و E میتواند منجر به کاهش نشانگرهای التهابی و بهبود عملکرد ارگانهای حیاتی شود (25-13). ویتامین C با کاهش التهاب و پراکسیداسیون لیپیدی، تنظیم فعالیت آنتیاکسیدانی و مهار مسیرهای اکسیداتیو تأثیر خود را اعمال میکند، همچنین فعالیت آنزیمهای آنتیاکسیدانی (کاتارز) را افزایش میدهد (26). ویتامین C یک پاک کننده قوی رادیکالهای آزاد است و تصور میشود که غلظت مولکولهای التهابی و پیش فیبروتیک مانند IL-6، IL-17 و TGF-β را در بافتهای ریه کاهش میدهد. این ویتامین به دلیل خاصیت آنتی اکسیدانی خود قادر است گونههای اکسیژن فعال (ROS) را خنثی کند و از آسیب سلولی ناشی از استرس اکسیداتیو جلوگیری نماید. در برخی از مطالعات حیوانی استفاده از دوزهای بالای ویتامین C با بهبود عملکرد کلیوی و کاهش سطح کراتینین سرم همراه بوده است (25). از سوی دیگر ویتامین E، بهعنوان یک آنتیاکسیدان محلول در چربی، از طریق کاهش لیپید پراکسیداسیون، افزایش آنتیاکسیدانهای آنزیمی و بهبود هیستوپاتولوژی عمل میکند (17،22). رتهایی که پس از تجویز پاراکوات، ویتامین E دریافت کرده بودند نسبت به گروه کنترل، بیشترین میزان بقا را داشتند (19). درمان ترکیبی با ویتامینهای C وE، تأثیر قابلتوجهی در کاهش پراکسیداسیون لیپیدی و افزایش گلوتاتیون در ریه داشته است (16-13). تغییرات هیستوپاتولوژیکی در گروههای مصرفکننده ویتامینها کاهش یافت، اما شدت آسیب در گروه پاراکوت به تنهایی بالا بود. همچنین کراتینین و اوره پلاسما کاهش یافت و تغییرات هیستوپاتولوژیکی در کلیه کمتر بود. آنزیمهای کبدی کاهش یافته و میزان بهبودی در گروههای پس از درمان بهتر از پیشدرمانی بود (16-13). در مطالعه ای دیگر نشان داده شد که درمان ترکیبی با ویتامینهای C وE، هفتگی برای یک ماه در مسمومست ناشی از پاراکوات در رت باعث بهبود سمیت کبدی گردید (27).
نتیجهگیری
نتایج این مطالعه مرور نظاممند و متاآنالیز نشان داد که مصرف ویتامینهای C و E میتواند تاثیرات مثبتی در کاهش عوارض ناشی از مسمومیت با پاراکوات داشته باشد. بررسیهای انجام شده نشان داد که این ویتامینها بهعنوان آنتیاکسیدانهای قوی، باعث تغییرات قابلتوجه در سطح کراتینین و آنزیمهای کبدی و در نتیجه بهبود عملکرد کبد و کلیه میباشند. با اینحال، نتایج حاصل از این بررسی نشان میدهد که هنوز برخی محدودیتها و چالشها در ارزیابی قطعی اثربخشی این ویتامینها وجود دارد. تنوع در دوز مصرفی، تفاوت در روشهای تجویز، و محدودیتهای مربوط به تعداد مطالعات انسانی، از جمله عواملی هستند که نیاز به پژوهشهای بیشتر را برجسته میکنند. با این0.02حال، برای دستیابی به نتایج قطعیتر و ارائه توصیههای بالینی دقیقتر، انجام کارآزماییهای بالینی گستردهتر با طراحیهای استاندارد و نمونههای بزرگتر توصیه میشود.
حامی مالی: طرح پژوهشی مرکز تحقیقات علوم دارویی (شماره 2402205)، دانشکده داروسازی و علوم دارویی، دانشگاه علوم پزشکی اصفهان.
تعارض در منافع: وجود ندارند.
مشارکت نویسندگان
در ایده، نگارش و ویرایش مقاله کلیه نویسندگان مشارکت داشتند.
پاراکوات ،]′1-1دی متیل،۴-۴ ′بی پیریدینیوم دی کلراید [، یک ترکیب بی پیریدیل سمیاست. خواص علفکشـی آن در سال ۱۹۵۵ کشف و در سـال ۱۹۶۲ در بـیش از ۱۲۰ کشور بهعنوان یک علفکش قوی و کارآمد معرفی شد و راه خود را در کشاورزی پیدا کرد. این علفکش غیرانتخابی مایع عمدتاً برای کنترل علفهای هرز بهطور گسترده در کشاورزی مورد استفاده قرار میگیرد. این علفکش به دلیل سمیت بالای آن، سلامت انسان را تهدید میکند. مصرف حداقل ۱۰ تا ۲۰ میلی لیتر پاراکوات ۲۰ درصد (در حدود یک قاشق غذاخوری) کشنده است. مصرف تصادفی یا عمدی محصولات حاوی پاراکوات میتواند منجر به مسمومیت شدید شود که اغلب با وجود مداخلات پزشکی منجر به پیامدهای کشنده میشود (1،2). این علفکش در بازار با نام تجاری گراماکسون (Gramaxon 20%) وجود دارد.پاراکوات بهصورت فرمولاسیون محلول قابل حل در آب (20%) بوده که در تماس با خاک به سرعت بیاثر و غیر فعال میشود. مطالعات اندکی در مورد مسمومیت با پاراکوات در ایران انجام شده است. سبزقبایی و همکاران، در یک دوره ۵ ساله (۱۳۸۶-۱۳۸۱) در اصفهان ۲۹ مورد مسمومیت با پاراکوات با میزان مرگ و میر ۲/۵۵ درصد گزارش کردند (3). دلیراد و همکاران در مطالعهای در شهر ارومیه طی یک دوره ۷ ساله (۱۳۹۲-۱۳۸۶) نرخ مرگ و میر ناشی از پاراکوات را ۴/۴۶ درصد گزارش کردند (4). پاراکوات عموماً در پوست و مخاط سالم جذب ضعیفی دارد. جذب دستگاه گوارش نیز کم (۵ تا ۱۰ درصد دوز مصرفی) اما سریع است و غلظت پلاسما در عرض ۲ ساعت پس از مصرف به حداکثر میرسد و بهصورت گسترده در بافتهای بدن انسان توزیع میشود، حجم توزیع تا ۷۵/۲ لیتر به ازای کیلوگرم تخمین زده میشود (5). پاراکوات نسبتاً سریع از بدن دفع میشود بهطوریکه حدود ۸۰ درصد دوز مصرفی طی ۲۴ ساعت از طریق ادرار حذف میشود. با اینحال، دوز باقی مانده و مقدار توزیع شده در بافتها به دلیل کاهش سریع عملکرد کلیه ناشی از سمیت آن بر این ارگان، بسیار آهسته حذف میشوند. بنابراین، در حالیکه نیمهعمر حذف اولیه حدود ۶ ساعت است، نیمهعمر نهایی میتواند تا ۱۲۰ ساعت و بیشتر باشد (5). از آنجاییکه هیچ پادزهر خاصی وجود ندارد، درمانها عمدتاً حمایتی است. درمان فوری عامل بسیار مهمی برای بقا در بیماران مسموم با پاراکوات است. بنابراین، هر بیمار در معرض پاراکوات باید با فوریت پزشکی درمان شود (6،7). پس از پذیرش بیمار در بیمارستان، ارزیابی اولیه و رسیدگی به عوارض تهدید کننده زندگی (راه هوایی، تنفس و قلب و عروق) مطابق با دستورالعملهای موجود، در اولویت قرار گیرد (7). مطالعات نشان داده است که آنتیاکسیدانها باعث کاهش مرگ و میر بیماران دچار مسمومیت با پاراکوات میگردند. مکانیسم اثر این است که آنتی اکسیدانها نظیر ویتامینE و C میتواند الکترونها را به رادیکالهای آزاد اهدا کنند و در نتیجه آنها را خنثی کنند و آسیبهای کبدی و کلیوی را کاهش دهند (8). نتایج مطالعات مختلف نشان میدهد که درمان با ویتامین E و/یاC ممکن است در بیماران مبتلا به سمّیت ناشی از پاراکوات مفید باشد و بهطور بالقوه آسیب کبد و کلیه را کاهش دهد (8،9). با اینحال، شواهد موجود غیرقطعی است و یک ارزیابی سیستماتیک از اثربخشی این ویتامینها در مسمومیت ناشی از پاراکوات را میطلبد. بنابراین، در مطالعه پیش رو قصد داریم شواهد موجود از تاثیر تجویز ویتامینهای C و E در مدیریت عوارض ناشی از سم پاراکوات در مطالعات حیوانی را استخراج کرده و با انجام متاآنالیز بر روی نتایج، بتوانیم در صورت امکان به شواهد قویتری در خصوص اثربخشی این فراوردهها دست یابیم.
روش بررسی
این مطالعه یک مرور نظاممند (Systematic review) به همراه متاآنالیز (فراتحلیل) بود که بر اساس دستورالعمل PRISMA (Preferred Reporting Items for Systematic Reviews and Meta-Analyses) در مورد تأثیر ویتامینهای C و E در بهبود علائم سمّیت ناشی از پاراکوات در حیوان، انجام گرفت. کد اخلاق این تحقیق IR.MUI.PHANUT.REC.1402.052 و تاریخ تصویب 2/10/1402 میباشد. این مطالعه از الگوی PICO(T) (10) پیروی میکند که عبارتند از: ,Pجمعیت Population)) شامل رتهای بالغ مسموم شده با پاراکوات بود. ,I مداخله (Intervention) شامل تجویز ویتامین C و/یا E میباشد. C، مقایسه (Comparison) عبارت از تغییرات قبل و بعد از مداخله میباشد. O، پیامدOutcome) ) مورد بررسی که شامل فاکتورهای نشان دهنده سمیّت کلیوی و کبدی میباشد. T، زمانی Time)) که لازم است تا مداخله انجام گرفته منجر به بروز پیامد مورد نظر گردد، که حداقل چهار هفته میباشد.
روش جستجوی منابع الکترونیکی: ابتدا پایگاههای «Cochrane Database of Systematic Reviews»، «Database of Abstracts of Reviews of Effects (DARE) » و « NIHR Centre for Reviews and Dissemination» جهت جستجوی مقالات مروری مرتبط مورد بررسی قرار گرفتند. پایگاههای الکترونیکی شاملPubMed/Medline, Google scholar ,ISI Web of Science ,Embase, Scopus تا پایان دسامبر ۲۰۲۴ برای مقالات حیوانی با استفاده از برخی لغات انتخابی MeSH (Medical Subject Headings) و سایر لغات مرتبط با موضوع مطالعه، جستجو شدند. لغات اصلی مورد جستجو شامل “Paraquat”)،“Vitamin C ”) (“Vitamin E” AND/OR بود که با واژه AND همزمان با سایر لغات “Toxicity”، “Efficacy”، “Liver enzyme”، “Mortality”،“ALT” ، “AST”، “Creatinine”، “Urea”، و با واژه OR همزمان با سایر لغات“Kidney disease” ،“Renal Failure”، “Hepatic Failure” و به کار بردن فیلتر (Animal) در پایگاههای مذکور مورد جستجو قرار گرفت. مطالعات با زبان انگلیسی و فارسی درنظر گرفته شدند. مقالاتی که در چند پایگاه ایندکس شده بودند، تنها یکبار در آنالیز نهایی وارد شدند.
معیارهای ورود مقالات به مطالعه: نتایج جستجوی اولیه بر اساس عنوان و خلاصه مقاله بررسی شده و مقالات متناسب با موضوع شناسایی شدند. مقالات حیوانی که در این مطالعه مورد بررسی قرار گرفتند، دارای شرایط زیر بودند: جمعیت موشهای صحرایی آزمایشگاهی بالغ با وزن تقریبی ۲۰۰ گرم که پاراکوات را بهصورت خوراکی و یا داخل صفاقی دریافت کرده باشند و ویتامینهای C یا E به منظور بهبود وضعیتشان تجویز شده باشد. نوع مداخله شامل، تجویز ویتامینهای C یا E با دوزهای تقریباً مشابه در گروه ها، به مدت حداقل چهار هفته. پیامدهای مورد بررسی در این مطالعات فاکتورهای نشاندهنده سمیّت کلیوی (سطح اوره و کراتینین)، فاکتورهای نشاندهنده سمیّت کبدی (سطح آنزیمهای کبدی)، و میزان مرگ و میر بود.
خروج مقالات از مطالعه: معیارهای خروج شامل مطالعات فاقد معیارهای نتیجه مرتبط، چکیده کنفرانسها و مطالعاتی بود که در قالب متن کامل در دسترس نبودند. گزارشات موردی(Case reports) ، مقالات مروری و سرمقالهها نیز حذف شدند، ولی رفرانسهای این مقالات جهت دستیابی به سایر مطالعات مرتبط، مورد بررسی قرار گرفت. غربالگری و انتخاب نهایی مقالات از مجموع مقالات اولیه، توسط دو محقق بهصورت مستقل و بر اساس معیارهای فوقالذکر، صورت گرفت. ارزیابی کیفی مطالعات حیوانی: ارزیابی کیفیت مطالعات حیوانی، با استفاده از ابزارهای سنجش کیفیت مقالات ARRIVE (پیوست) متناسب با طراحی مطالعه، کیفیت روش اجرا و و شیوه گزارش نتایج در مقالات، انجام شد. مواردی که در این ارزیابی مورد بررسی قرار گرفت، عبارتند از رعایت ملاحظات اخلاقی، پروسه آزمایشگاهی، شرایط نگهداری حیوانات آزمایشگاهی، تخصیص حیوان به هر گروه، و گزارش پیامدهای مطالعه (11).
استخراج اطلاعات از مقالات: استخراج دادهها بهطور مستقل توسط دو پژوهشگر با استفاده از یک فرم استاندارد استخراج داده، انجام شد. دادههای استخراجشده شامل ویژگیهای مطالعه (مانند طراحی مطالعه، حجم نمونه)، ویژگیهای شرکتکننده (مانند گونه، سن، جنس)، جزئیات (مانند دوز، مسیر تجویز)، نتایج مورد نظر و یافتههای کلیدی بود. تمام محاسبات عددی و دادههای استخراج شده از جداول، اشکال، و نمودارها، توسط متخصص آمار مورد تأیید قرار گرفت. اطلاعات استخراج شده از مقالات که در چکلیستهای از پیش طراحی شده وارد شدند، عبارت بودند از: نام نویسندگان، سال انتشار مقاله، شهر یا کشور محل انجام مطالعه، معیارهای ورود جمعیت به مطالعه، معیارهای خروج جمعیت از مطالعه.
متاآنالیز: دادههای کمّی استخراج شده از مقالات در مورد هر متغیر (پیامد) وارد نرمافزارComprehensive Meta-analysis (CAM-9.1.1) شده و مورد آنالیز قرار گرفت. متاآنالیز تجمعی در صورتی انجام شد که دادههای مرتبط با یک پیامد خاص در بیش از یک مطالعه گزارش شده باشد. به منظور بررسی اثر درمان بر روی متغیرهای کمّی پیوسته، از میانگین/ انحراف معیار هر متغیر استفاده شد. اثر درمان با ویتامینهای C ، E و یا ترکیب این ویتامین ها بر روی هر متغیر در صورتی معنیدار تلقی گردید که P value کوچکتر از ۰۵/۰ باشد. در صورت وجود تعداد مطالعات کافی در زیر گروه ها بر اساس دوز سم و یا زمان بررسی غلظت پارامترها در طول زمان، از تحلیلهای زیر گروهی استفاده شده است. ناهمگونی بین مطالعات با استفاده از تست آماری Chi2 (Cochrane-Q) و آمارهیI2 مورد ارزیابی قرار گرفت تا قدرت شواهدی که بیانگر واقعی بودن ناهمگونی هستند، را تعیین سازد. مقادیر I2 کمتر از ۲۵%، ۲۵-۷۵% و بیشتر از ۷۵% به ترتیب معادل با میزان ناهمگونی کم، متوسط و زیاد در نظر گرفته شد (12). بر این اساس، ناهمگونی بین مطالعات در صورتی معنیدار تلقی گردید که P value حاصل از تست Chi2 کوچکتر از 05/0 باشد. در مورد هر متغیر، در صورتیکه شواهدی از ناهمگونی وجود نداشت (۲۵% I2< )، از مدلFixed effects و در شرایطی که ناهمگونی معنیدار بین مطالعات وجود داشت (۷۵% I2 >)، از رویکرد فراتحلیل به روش اثرات تصادفی (Random effects) استفاده گردید.
نتایج
جمعیت مورد مطالعه: جمعیت نهایی وارد شده به متاآنالیز (از مجموع ۹ مطالعه حیوانی) شامل ۸۵۲ رت بود، که تعداد آن ها از ۳۶ تا ۲۰۰ رت بین مطالعات مختلف، متغیر بود. تمام مطالعات بر روی حیوانات آزمایشگاهی مسموم شده با پاراکوات انجام شده است (شکل 1).
نوع مداخله: از مجموع ۹ مطالعهای که وارد متاآنالیز شدند، ۴ مطالعه در مورد بررسی تأثیر درمان ترکیبی با ویتامینهای C و E (13-16)، ۴ مطالعه در مورد تأثیر ویتامین E (17-20) و یک مطالعه در مورد تأثیر ویتامین C میباشد (21).
پیامدهای مورد بررسی: از مجموع مقالاتی که تحت متاآنالیز قرار گرفتند (۹ مقاله)، عمدتاً پارامترهای مرتبط با آسیب کبدی و کلیوی بررسی شده بودند. همچنین از ۱۳ مطالعه حیوانی مورد بررسی، ۹ مطالعه وارد ارزیابی کیفی و سپس آنالیز کمّی (متاآنالیز) شدند (21-13)؛ و ۴ مطالعه به دلیل تفاوت در پیامدهای مورد بررسی و همچنین طول درمان، فقط مورد ارزیابی کیفی قرار گرفتند و در نهایت وارد متاآنالیز نشدند (25-22)(جدول 1).
تأثیر پاراکوات و درمان با ویتامینهای C وE بر روی پیامدهای اصلی: از مجموع دادههای گزارش شده در مقالات، تأثیر تجویز ویتامینهای C و E (با دوز و مدت درمانی تقریباً مشابه) بر روی پارامترهای مرتبط با آسیب کبدی و کلیوی به عنوان پیامدهای اصلی مورد ارزیابی قرار گرفت. نتایج (جدول2) نشان داد که بدون توجه به دوز سم و یا زمان پیگیری برای اندازهگیری پارامترها، با وجود آن که پس از دریافت پاراکوات در پارامترهای مختلف روند کاهشی و یا افزایشی وجود داشته است، اما به دلیل کم بودن حجم نمونه مورد بررسی، این اختلاف در هیچیک از آیتمهای مورد بررسی معنادار نبوده است. نتایج (جدول 3) نشان داد که بین میزان پاراکوات تجویز شده و افرایش یا کاهش پارامترها در گروههای مختلف ارتباط معنادار وجود داشت. در صورت مثبت بودن ضریب همبستگی، با افزایش غلظت سم، میزان پارامتر نیز در گروه مربوطه افزایش داشته و در صورت منفی بودن آن، مقدار غلظت پارامتر آزمایشگاهی با افزایش دوز سم کاهش یافت.
نتایج متاآنالیز: به دلیل وجود مطالعات ناکافی (کمتر از سه مطالعه) بر روی انواع پارامترها، متاآنالیز تنها بر روی پارامترهای Creatinine، SGOT ، SGPT و ALP در مطالعات حیوانی در گروه آزمایشی ویتامین E انجام شد (جدول 4). نتایج نهایی فراتحلیل در مورد پارامترهای مورد بررسی نشان داد، که افزایش کراتینین بهصورت کلی و در اندازهگیریهای پس از دو ماه و سه ماه و در کلیه دوزهای مورد بررسی از پاراکوات، در گروه مداخله نسبت به گروه کنترل معنادار بود. این نتایج در مورد پارامترهای SGPT و SGOT معنادار نبودند. اما در مورد پارامتر ALP به افزایش معنادار دست یافتیم. لازم به ذکر است به دلیل وجود ناهمسانی بین مطالعات، با استفاده از تست آماری Chi2 (Cochrane-Q) و آماره ی I2، کلیه نتایج بر اساس مدل با اثر تصادفی(Random effects) گزارش شد. خطای انتشار در هیچ یک ازحالات با استفاده از آزمون Egger مشاهده نشد.

شکل1: فلوچارت انتخاب مطالعات حیوانی
جدول1: مشخصات مطالعات حیوانی


جدول 2: مقایسه غلظت پارامترها به تفکیک گروه مورد و شاهد بدون توجه به دوز پاراکوات در پروتکلهای مختلف مداخله درمطالعات حیوانی.

جدول 3: ارتباط میان تغییرات غلظت پارامترها با دوز سمیت بر اساس نوع گروه آزمایشی در مطالعات حیوانی

جدول4: نتایج فراتحلیل برخی پارامترها در مطالعات حیوانی در گروه ویتامین E

بحث
مطالعه حاضر با هدف بررسی تاثیر ویتامینهای C و E بر مسمومیت حاد ناشی از پاراکوات از طریق مرور نظاممند و متاآنالیز انجام شد. یافتههای این تحقیق نشان داد که این ویتامینها میتوانند اثرات حفاظتی قابلتوجهی در برابر آسیبهای ناشی از پاراکوات داشته باشند. این تاثیرات عمدتا از طریق مکانیسمهای کاهش استرس اکسیداتیو، مهار فرآیندهای التهابی و بهبود عملکرد کبد و کلیه اعمال میشوند (21-13). از مجموع ۱۳ مطالعهای که بر روی جمعیت رتها انجام شده بود، ۴ مطالعه فقط مورد بررسی کیفی قرار گرفتند (25-22). این مطالعات به بررسی آسیبهای کبدی، کلیوی، ریوی، میزان بقاء و تغییرات پارامترهای خونی پرداخته اند،که نتایج مشابهی را در پی داشتند و ۹ مطالعه دیگر وارد بررسی کمی شدند (13-21). نتایج مطالعات حیوانی نشان داد که مصرف ویتامینهای C و E میتواند منجر به کاهش نشانگرهای التهابی و بهبود عملکرد ارگانهای حیاتی شود (25-13). ویتامین C با کاهش التهاب و پراکسیداسیون لیپیدی، تنظیم فعالیت آنتیاکسیدانی و مهار مسیرهای اکسیداتیو تأثیر خود را اعمال میکند، همچنین فعالیت آنزیمهای آنتیاکسیدانی (کاتارز) را افزایش میدهد (26). ویتامین C یک پاک کننده قوی رادیکالهای آزاد است و تصور میشود که غلظت مولکولهای التهابی و پیش فیبروتیک مانند IL-6، IL-17 و TGF-β را در بافتهای ریه کاهش میدهد. این ویتامین به دلیل خاصیت آنتی اکسیدانی خود قادر است گونههای اکسیژن فعال (ROS) را خنثی کند و از آسیب سلولی ناشی از استرس اکسیداتیو جلوگیری نماید. در برخی از مطالعات حیوانی استفاده از دوزهای بالای ویتامین C با بهبود عملکرد کلیوی و کاهش سطح کراتینین سرم همراه بوده است (25). از سوی دیگر ویتامین E، بهعنوان یک آنتیاکسیدان محلول در چربی، از طریق کاهش لیپید پراکسیداسیون، افزایش آنتیاکسیدانهای آنزیمی و بهبود هیستوپاتولوژی عمل میکند (17،22). رتهایی که پس از تجویز پاراکوات، ویتامین E دریافت کرده بودند نسبت به گروه کنترل، بیشترین میزان بقا را داشتند (19). درمان ترکیبی با ویتامینهای C وE، تأثیر قابلتوجهی در کاهش پراکسیداسیون لیپیدی و افزایش گلوتاتیون در ریه داشته است (16-13). تغییرات هیستوپاتولوژیکی در گروههای مصرفکننده ویتامینها کاهش یافت، اما شدت آسیب در گروه پاراکوت به تنهایی بالا بود. همچنین کراتینین و اوره پلاسما کاهش یافت و تغییرات هیستوپاتولوژیکی در کلیه کمتر بود. آنزیمهای کبدی کاهش یافته و میزان بهبودی در گروههای پس از درمان بهتر از پیشدرمانی بود (16-13). در مطالعه ای دیگر نشان داده شد که درمان ترکیبی با ویتامینهای C وE، هفتگی برای یک ماه در مسمومست ناشی از پاراکوات در رت باعث بهبود سمیت کبدی گردید (27).
نتیجهگیری
نتایج این مطالعه مرور نظاممند و متاآنالیز نشان داد که مصرف ویتامینهای C و E میتواند تاثیرات مثبتی در کاهش عوارض ناشی از مسمومیت با پاراکوات داشته باشد. بررسیهای انجام شده نشان داد که این ویتامینها بهعنوان آنتیاکسیدانهای قوی، باعث تغییرات قابلتوجه در سطح کراتینین و آنزیمهای کبدی و در نتیجه بهبود عملکرد کبد و کلیه میباشند. با اینحال، نتایج حاصل از این بررسی نشان میدهد که هنوز برخی محدودیتها و چالشها در ارزیابی قطعی اثربخشی این ویتامینها وجود دارد. تنوع در دوز مصرفی، تفاوت در روشهای تجویز، و محدودیتهای مربوط به تعداد مطالعات انسانی، از جمله عواملی هستند که نیاز به پژوهشهای بیشتر را برجسته میکنند. با این0.02حال، برای دستیابی به نتایج قطعیتر و ارائه توصیههای بالینی دقیقتر، انجام کارآزماییهای بالینی گستردهتر با طراحیهای استاندارد و نمونههای بزرگتر توصیه میشود.
حامی مالی: طرح پژوهشی مرکز تحقیقات علوم دارویی (شماره 2402205)، دانشکده داروسازی و علوم دارویی، دانشگاه علوم پزشکی اصفهان.
تعارض در منافع: وجود ندارند.
مشارکت نویسندگان
در ایده، نگارش و ویرایش مقاله کلیه نویسندگان مشارکت داشتند.
References:
1- Gil HW, Hong JR, Jang SH, Hong SY. Diagnostic and Therapeutic Approach for Acute Paraquat Intoxication. J Korean Med Sci 2014; 29(11): 1441-9.
2- Bidaki R, Mostafavi N, Al-Saeed S, Zarch M, Karimoddini M, Dehghani F, et al. Oral Ulcers Following Suicide Attempt by Paraquat Herbicide. Hosp Pract Res 2020; 5(3): 117-9.
3- Sabzghabaee A, Eizadi-Mood N, Montazeri K, Yaraghi A, Golabi M. Fatality in Paraquat Poisoning. Singapore Med J 2010; 51(6): 496-500.
4- Delirrad M, Majidi M, Boushehri B. Clinical Features and Prognosis of Paraquat Poisoning: A Review of 41 Cases. Int J Clin Exp Med 2015; 8(5): 8122-8.
5- Dinis-Oliveira R, Duarte J, Sánchez-Navarro A, Remião F, Bastos M, Carvalho F. Paraquat Poisonings: Mechanisms of Lung Toxicity, Clinical Features, and Treatment. Crit Rev Toxicol 2008; 38(1): 13-71.
6- Chatterjee A, Ansar M, Chandra A, Chakraborty U, Dasgupta S. An Overview of Paraquat Poisoning: A Review. Bengal Phys J 2024; 11(1): 24-9.
7- Gawarammana IB, Buckley NA. Medical Management of Paraquat Ingestion. Br J Clin Pharmacol 2011; 72(5): 745-57.
8- Eizadi-Mood N, Sabzghabaee AM, Yaraghi A, Montazeri K, Golabi M, Sharifian A, Badri S. Effect of Antioxidants on the Outcome of Therapy in Paraquat-Intoxicated Patients. Trop J Pharm Res 2011; 10(1): 27-31.
9- Okolonkwo BN. The Effect of Combined Vitamin Treatment on Paraquat-Inflicted Liver Damage. Asian J Biochem Genet Mol Biol 2022; 12(4): 132-8.
10- O'Connor D, Green S, Higgins JPT, editors. Cochrane handbook for systematic reviews of interventions. New Delhi: The Cochrane Collaboration and John Wiley & Sons Ltd; 2011. p. 81–94.
11- Kilkenny C, Browne WJ, Cuthill IC, Emerson M, Altman DG. The ARRIVE Guidelines Checklist: Animal Research Reporting In Vivo Experiments. Plos Biol 2010; 8(6): 1-5.
12- Higgins JP, Thompson SG. Quantifying Heterogeneity in a Meta-Analysis. Suku Stat Med 2002; 21(11): 1539-58
13- Okolonkwo BN, Nyenke CU, Ajibo DN, Ibitoroko GM, Odiabara KK. Chronic Paraquat Exposure on Kidney and Vitamin E and C Treatment Benefits. J Biomed Biosens 2023; 3(3): 3-10.
14- Okolonkwo BN, Brisibe N, Ibitoroko GM. Vitamin E and C Long-Term Treatment Effect on Paraquat Poisoned Liver in Rat. J Appl Health Sci Med 2023; 3(2): 1-8.
15- Okolonkwo BN, Brisibe N, Maureen I. Antidotal Effect of Vitamin E and C in the Management of Paraquat Intoxication in Rat. Health Stud 2023; 1(1): 24-9.
16- Okolonkwo BN, Adjekuko JN, Collins O, Jumbo I. Hematological Recovery by Vitamin E and C on Paraquat Inflicted Hematological Insult in Rattus Norvegicus. Curr J Appl Sci Technol 2022; 41(15): 16-22.
17- Divya VS. Studies on the Ameliorative Effects of Vitamin E on Paraquat Toxicity in Rats [dissertation]. Mannuthy, Kerala, India: College of Veterinary and Animal Sciences, Centre of Excellence in Pathology; 2010.
18- Okolonkwo BN, Adjekuko JN, Collins O, Jumbo I. Ameliorative Effect of Vitamin E on Paraquat Induced Hematological Disorder in Male Albino Rats. Biotechnol J Int 2022; 26(2): 9-17.
19- Okolonkwo BN, Brisibe N, Ibitoroko GM. Evaluating The Impact of Vitamin E Treatment on Paraquat Induced Toxicity in Liver. Curr Res Interdiscip Stud 2023; 2(2): 6-11.
20- Okolonkwo BN, Brisibe N, Ibitoroko GM. Ameliorative Effect of Vitamin E on Paraquat Induced Nephrotoxicity in Rat. Curr Res Interdiscip Stud 2023; 2(2): 1-5.
21- Okolonkwo BN, Ikpeama AR. The Antioxidant Effects of Vitamin C on Liver Enzyme (SGPT) Activity in Rats Under Paraquat Toxicity. Ann Food Sci Technol 2012; 13(1): 100-3.
22- Akinloye OA, Adamson I, Ademuyiwa O, Arowolo TA. Supplementation of Vitamins C, E And its Combination on Paraquat-Intoxicated Rats: Effects on Some Biochemical and Markers of Oxidative Stress Parameters. J Appl Pharm Sci 2011; 1(6): 85-91.
23- Shalaby MA, Emam SR, Soliman AM. Protective Effect of Vitamin E Against Herbicide Paraquat-Induced Enzymatic Leakage and Oxidative Damage in The Liver of Rats. Adv Anim Vet Sci 2020; 8(6): 639-46.
24- Harada N, Saito S, Minakata K. Effects of Vitamin E on Toxicity by Minute Amounts of Paraquat Fed Continuously to Rats. J Nutr Sci Vitaminol 1991; 37(1): 1-13.
25- Rodrigues da Silva M, Schapochnik A, Peres Leal M, Esteves J, Bichels Hebeda C, Sandri S, et al. Beneficial Effects of Ascorbic Acid to Treat Lung Fibrosis Induced by Paraquat. Plos One 2018; 13(11): 1-14.
26- Carr AC, Maggini S. Vitamin C and Immune Function. Nutrients 2017; 9(11): 1211.
27- Okolonkwo BN, Amadi CF, Chikwubike UO, Nyenke CU. The Comparative Effects of Vitamin E+ C on the Chronic Toxicity of Paraquat. Eur J Med Plants 2022; 33(6): 7-13.
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |







