دوره 33، شماره 11 - ( بهمن 1404 )
جلد 33 شماره 11 صفحات 9649-9639 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Daniyali S J, Rouhi L. Evaluation the influence of Spirulina platensis extract on cell viability and change the expression of apoptotic BAD gene in the AGS human gastric adenocarcinoma cells. JSSU 2026; 33 (11) :9639-9649
URL: http://jssu.ssu.ac.ir/article-1-6442-fa.html
URL: http://jssu.ssu.ac.ir/article-1-6442-fa.html
دانیالی سید جهانبخش، روحی لیلا. بررسی اثر عصاره اسپیرولینا پلاتنسیس بر بقای سلولی و تغییر بیان ژن آپوپتوزی BAD در سلولهای آدنوکارسینومای معده انسان AGS. مجله علمي پژوهشي دانشگاه علوم پزشكي شهید صدوقی يزد. 1404; 33 (11) :9639-9649
متن کامل [PDF 598 kb]
(265 دریافت)
| چکیده (HTML) (298 مشاهده)
متن کامل: (74 مشاهده)
مقدمه
سرطان به دستهای از تودههای سلولی که دارای خصوصیات بدخیم باشند، اطلاق میگردد. امروزه سرطانها شایعترین و شدیدترین بیماریهای مشاهده شده در طب بالینی میباشند (1،2). در بین انواع بدخیمیها، آدنوکارسینومای معده یکی از سرطانهای شایع در سراسر جهان میباشد. علیرغم کاهشی که در سالهای اخیر در میزان بروز این سرطان رخ داده است اما همچنان به عنوان پنجمین سرطان شایع در جهان و چهارمین علت مرگ در اثر سرطان به حساب میآید (3). سن شایع این بدخیمی دهه ششم عمر است اما وقوع آن در سنین پایینتر نیز شایع میباشد. سرطان معده از جمله بیماریهایی است که اگر زود تشخیص داده شود بهطور کامل قابلیت علاج داشته و برعکس در صورتیکه دیر تشخیص داده شود ممکن است متاستاز رخ دهد. درمان اصلی سرطان معده در مراحل اولیه جراحی و در مراحل پیشرفته اقدامات جراحی به همراه شیمیدرمانی و رادیو درمانی میباشد که معمولا با نتایج خوبی همراه نیستند (4). بنابراین یک نیاز فوری برای ایجاد راهکارهای درمانی موثرتر، به منظور بهبود طول بقاء مبتلایان وجود دارد. از آنجاییکه مقاومت به مرگ سلولی و عدم وجود تعادل بین تقسیم سلولی و مرگ سلولی، منجر به عدم کنترل تکثیر سلول های توموری می شود، هماکنون توجه¬ها به سوی شناسایی ترکیبات درمانی که قادر به مهار تکثیر سلولهای توموری باشند، جلب شده است. برخی از این ترکیبات با هدف قرار دادن پروتئین های ضد آپوپتوزی منجر به افزایش پروتئینهای پروآپوپتوزی میشوند و القاء آپوپتوز در سلولهای سرطانی را تسهیل می¬نمایند، و بدین طریق باعث مرگ سلولهای توموری می¬شوند. از جمله آنها میتوان به ترکیبات با منشاء طبیعی اشاره کرد (5،6). استفاده از ترکیبات طبیعی به عنوان دارو به دنبال دارا بودن اثرات جانبی کمتر در مقایسه با ترکیبات شمیایی، همواره مورد توجه بوده است و بهعنوان یک ترکیب هدف درمانی جدید در کارهای تحقیقاتی مبتنی بر فرآیندهای آزمایشگاهی و بالینی مورد بررسی قرار میگیرند. از گذشته ترکیبات طبیعی منبع منحصربهفردی برای تأمین داروهای مصرفی جامعه بشری بودهاند و به خاطر عدم بروز مشکلات بیشتر در اثر استفاده از آنها نقش مهمی در درمان بیماریهای انسانی ایفا نموده¬اند (7). بر این اساس، محققان همیشه در راستای یافتن ترکیباتی با خواص ضد توموری که توانایی جلوگیری از گسترش و رشد سلولهای سرطانی را داشته باشند، بوده¬اند، که در این میان آبزیان دریایی بواسطه خواص تغذیهای و دارویی آنها همواره مورد توجه قرار گرفتهاند (8). جلبک سبز- آبی اسپیرولینا، یکی از مهمترین این آبزیان است که از سوی محققان علوم تغذیه به آن اشاره شده است و کشفیات زیادی در خصوص خواص تغذیهای و دارویی آن موجود می¬باشد. این جلبک رشتهای، متعلق به خانواده سیانوباکترها، دارای فیلامنت¬های فنرمانند، فتوسنتزکننده و بسیار کوچک است که دو جنس آرترواسپریا و پلاتنسیس آن مهم¬ترین اسپیرولیناهای خوراکی به حساب میآیند و به طور تجاری در سرتاسر جهان تولید می¬گردند. اسپیرولینا پلاتنسیس به دلیل داشتن اجزا و ترکیبات آنتیاکسیدانی مانند فایکوسیانین، سلنیوم، کارتنوئیدها، اسید چرب گامالینولنیک، عامل دارویی بالقوه¬ای برای بیماری¬های القاء شده بهوسیله تنش اکسیداسیونی نظیر سرطان می¬باشد (9,10). از اینرو، هم اکنون اسپیرولینا پلاتنسیس از سوی سازمان بهداشت جهانی بهعنوان یک گزینه درمانی بالقوه جهت درمان سرطان اعلام گردیده است (11،12). در مطالعه حاضر نیز اثر عصاره اسپیرولینا پلاتنسیس بر بقای سلولی و تغییر بیان ژن آپوپتوزی BAD (پروتئین محصول ژن BAD با تشکیل هترودایمر با پروتئین BCL-2 عملکرد ضد آپوپتوزی BCL-2 را مهار می¬نماید و منجر به القاء آپوپتوز میشود (7) در سلولهای آدنوکارسینومای معده انسان (AGS) مورد بررسی قرار گرفت.
روش بررسی
این مطالعه بهصورت تجربی در شش ماهه اول سال 1403 در مراکز تحقیقاتی سلولی- تکوینی، بیوتکنولوژی و گیاهان دارویی مجتمع آزمایشگاهی دانشگاه آزاد اسلامی واحد
شهرکرد بهصورت تجربی با مجوز اخلاق در پژوهش انجام شد. رده سلولی AGS از مرکز ملی ذخایر ژنتیکی و زیستی ایران خریداری شد. در محیط کشت DMEM-F12 (Dulbecco's Modified Eagle's medium) (Gibco, USA) حاوی 10 درصد FBS (Foetal Bovine Serum) (Gibco, USA) و یک درصد Penstrep (Penicillin-Streptomycin) (Gibco, USA) در انکوباتور (Memmert, Germany) با فشار 5 درصد گاز CO2، رطوبت 90 درصد و دمای 37 درجه سانتی¬گراد، در فلاسک کشت سلول ۷۵ سانتیمتر مربع کشت داده شد. محیط کشت هفتهای سه بار تعویض و برای برداشت کردن سلولها از محلول تریپسین/EDTA استفاده شد. اسپیرولینا پلاتنسیس به صورت آماده و به حالت جامد از شرکت دانش پژوهان قشم با نام تجاری اسپیرولینا (سوپر فود) تهیه گردید. برای تهیه عصاره از این ماده در مرکز تحقیقات گیاهان دارویی دانشگاه آزاد اسلامی واحد شهرکرد، پودر اسپیرولینا پلاتنسیس درون فـالکون ریختــه شـد و حلال اتانولی 96 درصد به آن اضافه و اقدام به عصارهگیری با حرارت و درجه خلوص بالا شد (مدت زمان 20 دقیقه). مایع حاصل توسط تبخیرکننده چرخشی در دمای 40 درجه سانتیگراد تا خروج کامل حلال استخراجی و دستیابی به عصاره غلیظ و ویسکوز تغلیظ گردید. عمل عصارهگیری سه بار تکرار گردید و تا زمان استفاده در دمای 4 درجه سانتیگراد نگهداری شد.
سنجش بقای سلولی: بقای سلولی رده AGS تیمار شده با غلظتهای مختلف عصاره اسپیرولینا پلاتنسیس و گروه¬ کنترل (فاقد تیمار و صرفا در معرض محیط کشت) توسط تست MTT، با استفاده از کیت (CellTiter 96® Non-Radioactive Cell Proliferation Assay (MTT) با شماره محصول G4000 مورد ارزیابی قرار گرفت. به این ترتیب که تعداد 103×5 سلول در هر چاهک پلیت 96 چاهکی کشت داه شد و سپس با غلظتهای 10 (گروه I)، 20 (گروه II) و 40 (گروه III) میکروگرم/ میلی¬لیتر عصاره اسپیرولینا پلاتنسیس برای مدت زمان 24 و 48 ساعت تیمار و انکوبه گردید. پس از اتمام زمان انکوباسیون 24 و 48 ساعته، محیط رویی تیمار گردآوری شد و مقدار µl 20 محلول MTT به هر چاهک اضافه گردید و انکوباسیون چهار ساعته صورت گرفت. در نهایت جذب نمونهها توسط دستگاه (ELISA-reader, Awareness Technology, USA) با طول موج nm 540- 630 خوانش گردید (13). اطلاعات مربوط به اثر غلظتهای مختلف عصاره اسپیرولینا پلاتنسیس بر رشد سلول AGS با شاخص IC50 (غلظتی از دارو که رشد سلول را نسبت به کنترل 50 درصد کاهش میدهد) ارائه شدند. IC50ها از طریق رسم منحنیهای رشد سلول در برابر رقت-های مختلف سوپرناتانت و از طریق رسم معادله رگرسیون غیر خطی منحنی¬های رشد سلول در برابر غلظت سوپرناتانت محاسبه گردید.
سنجش بیان ژن: به منظور بررسی میزان بیان ژن BAD ، تعداد 105×3 سلول در پلیتهای 6 خانه کشت داده شد، و سپس، با غلظت 40 میکروگرم/ میلیلیتر عصاره اسپیرولینا پلاتنسیس در بازه زمانی 48 ساعت تیمار و انکوبه شدند. پس از گذشت زمان انکوباسیون 48 ساعته، سلول¬ها در دو گروه؛ گروه تست شامل غلظت 40 میکروگرم/ میلیلیتر از عصاره اسپیرولینا پلاتنسیس و گروه کنترل، برداشت و پس از شستشو با بافر PBS، Total RNA سلولی با استفاده از معرف RNXTM –PLUS (RNX-Plus Solution for total RNA isolation)، جدا گردید. به منظور انجام مرحله Heat block، نمونههای حاصل از مرحله قبل در دستگاه ترموسایکلر با دمای 60 درجه سانتیگراد به مدت 20 دقیقه قرار داده شدند. در ادامه تمام توالیهای RNA با استفاده از کیت سنتز cDNA (PrimeScriptTM RT Reagent kit (Perfect Real Time))، (Takara)، به cDNA تبدیل و به فریزر 20- درجه سانتی گراد منتقل شدند. سنجش میزان بیان ژن BAD با استفاده از دستگاه Real Time PCR مدل (Rotor gene 3000 corbett, Australia) مورد ارزیابی قرار گرفت. برای انجام واکنش، مخلوط واکنشی متشکل از cDNA، به مقدار 1 میکرولیتر، پرایمر رفت و برگشت هر کدام به مقدار 0/5 میکرولیتر، RNase-free water، به مقدار 5/5 میکرولیتر و 12/5 میکرولیتر مسترمیکس (Master Mix RT-PCR) (Ampliqon) تهیه گردید (14). توالی پرایمرهای پیشرو (Forward) و پسرو (Reverse) ژنهای GAPDH و BAD با استفاده از نرم افزار Oligo6 طراحی و سپس با Blast نمودن آنها در NBCI از صحیح بودن آنها اطمینان حاصل شد و نهایتا توسط شرکت Macrogen سنتز شدند (جدول 1). از ژن GAPDH، بهعنوان کنترل داخلی استفاده شد. سپس مخلوط واکنش پس از آمادهسازی با حجم نهایی 20 میکرولیتر تحت تاثیر برنامهی دمایی ذکر شده در (جدول 2) قرار گرفت.
تجزیه و تحلیل آماری
نهایتاً بررسی آماری با استفاده از آزمون منویتنی (بهطورکلی آزمون ناپارامتریک به نرمال بودن یا نبودن توزیع دادهها حساس نیست و در هر شرایطی قابل استفاده است) از طریق نرمافزارversion 16 SPSS انجام شد. حدود اطمینان برای همه آزمایشات 95% در نظر گرفته شد و 5% < P معنیدار محسوب گردید.
جدول1: مشخصات پرایمر مربوط به ژنهای BAD و GAPDH
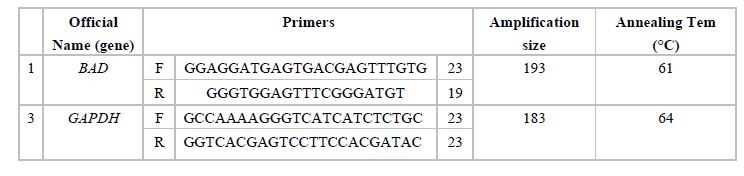
جدول2: شرایط دمایی واکنش Rael Time PCR
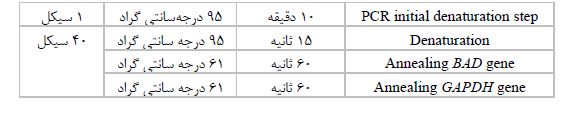
نتایج
سنجش میکروسکوپی سلول های تحت تیمار: سلول های سرطانی AGS در غلظت های مختلف عصاره جلبک اسپیرولینا پلاتنسیس (10، 20 و 40 میکروگرم/ میلیلیتر) برای مدت زمان 24 و 48 ساعت کشت داده شدند. تصویر زیر (شکل 1، A-D) انکوباسیون سلول های تحت تیمار با غلظتهای مختلف عصارهی جلبک اسپیرولینا را نشان میدهد که مشاهدات میکروسکوپی حاکی از کاهش تعداد سلول ها در گروه های تحت تیمار در مقایسه با گروه کنترل بهصورت وابسته به غلظت میباشد.
بقای سلولی و تعیین نقطه IC50: آنچه که از نتایج تست MTT می توان برآورد کرد، این است که بقای سلولی سلول-های رده آدنوکارسینومای معده انسان (AGS)، تحت تیمار با غلظتهای مختلف عصاره جلبک اسپیرولینا پلاتنسیس (10، 20 و 40 میکروگرم/ میلی لیتر) ظرف مدت زمان انکوباسیون 24 و 48 ساعت، در سایر گروههای آزمایشی نسبت به گروه کنترل کاهش یافته است. این کاهش در هر دو زمان به صورت وابسته به زمان و دوز عصاره میباشد (نمودار 1). در این پژوهش عصاره جلبک اسپیرولینا پلاتنسیس در نقطه IC50 بهعنوان غلظتی که بقای سلولی را 50 درصد کاهش میدهد 40 میکروگرم/ میلیلیتر بوده است (نمودار 2). بقای سلولی سلولهای رده AGS آدنوکارسینومای معده، در مقایسه با گروه کنترل در دوز 20 (P<0.001) و 40 (P<0.0001) میکروگرم/ میلیلیتر در زمان انکوباسیون 48 ساعت کاهش معنیداری را نشان داد.
تغییر بیان ژن BAD: تیمار سلولهای رده AGS با عصاره جلبک اسپیرولینا پلاتنسیس و انکوباسیون آنها برای مدت 48 ساعت نشان داد که میزان بیان ژن BAD افزایش یافته است. نمودار زیر (نمودار 3) این افزایش بیان معنیدار را در ژن BAD براساس CtΔΔ نمایش می¬دهد.
.JPG)
شکل1: تاثیر غلظت¬های مختلف عصاره جلبک اسپیرولینا پلاتنسیس بر رده سلولی AGS
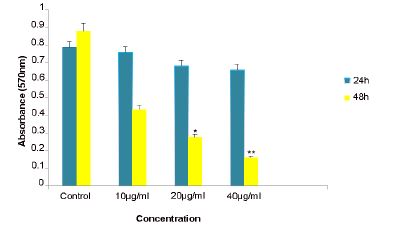
نمودار 1: اثر عصاره جلبک اسپیرولینا پلاتنسیس بر بقای سلولی رده سلولی AGS در مدت زمان انکوباسیون 24 و 48 ساعت.
P<0.001*،P<0.0001** در مقابل گروه کنترل
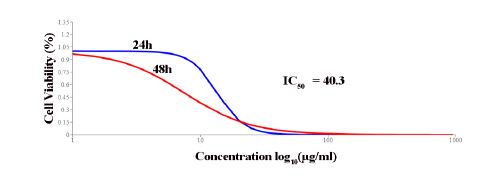
نموار 2: غلظت 40 میکروگرم/ میلیلیتر عصاره جلبک اسپیرولینا پلاتنسیس در نقطه IC50 در روش MTT
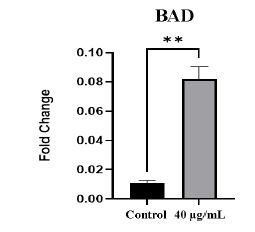
نمودار 3: نمودار میزان بیان ژن BAD براساس Ct در غلظت 40 میکروگرم/میلیلیتر و زمان انکوباسیون 48 ساعت.
P<0.001** اختلاف معنی¬دار در مقابل گروه کنترل
بحث
یکی از معضلات امروزی در جوامع بشری سرطان معده میباشد که بهعنوان یک بیماری چند عاملی در نتیجه تداوم آسیب¬های ناشی از مواجهه مداوم با عوامل سرطان¬زا ایجاد میشود. علیرغم کاهش قابلملاحظه در بروز این نوع بدخیمی در طول دهههای گذشته، در اکثر کشورهای صنعتی هنوز این بیماری دومین علت شایع مرگ و میر افراد در اثر سرطان میباشد که سالیانه باعث مرگ حدود یک میلیون نفر در سرتاسر جهان می شود (16,15). مبتلایان به آدنوکارسینومای معده دارای بقاء 5 ساله هستند و در بیش از 90% موارد درمان تومور معدی با جراحی، تنها شانس درمانی می باشد. اما به دلیل اینکه در حال حاضر تشخیص زودهنگام سرطان معده امکانپذیر نیست و معمولاً تشخیص زمانی صورت میگیرد که سرطان بهطور موضعی پیشرفت کرده است و به درون دیواره معده نفوذ نموده، این شانس به کمتر از 30% کاهش می یابد (17). لذا با توجه به افزایش روز افزون تعداد مبتلایان که شمار زیادی از آنها پس از گذراندن مراحل دشوار عمل های جراحی باز هم دچار عود بیماری می شوند و از آنجاییکه مقاومت به مرگ سلولی و عدم وجود تعادل بین تقسیم سلولی و مرگ سلولی منجر به عدم کنترل تکثیر سلولهای توموری می شود، امروزه نیاز به ترکیبات درمانی که قادر به مهار تکثیر سلول¬های توموری باشند، به شدت احساس می شود. امروزه تحقیق در راستای یافتن ترکیباتی با خواص ضد توموری که توانایی جلوگیری از گسترش و رشد سلول¬های سرطانی را داشته باشند پیشرفت های قابلتوجهی داشته است. با توجه به عوارض جانبی ترکیبات صناعی و داروهای فارماکولوژیک ضد سرطان، محققان همیشه در راستای یافتن ترکیبات طبیعی فاقد عوارض جانبی بوده اند و در این میان آبزیان دریائی بواسطه فراوانی و تنوع بسیار بالای آنها همواره قابلتوجه قرار گرفتهاند. یکی از مهمترین این آبزیان که آثار و فوائد فراوانی از سوی محققان علوم تغذیه برای آن بیان شده و کشفیات زیادی در خصوص خواص تغذیهای و دارویی آن بهدست آمده است، جلبک سبز - آبی اسپیرولینا¬ پلاتنسیس میباشد. اسپیرولینا یکی از نوید بخشترین ریز جلبکها بوده که از سوی سازمان بهداشت جهانی به عنوان راه حل درمانی سودمند برای فردا و همچنین به عنوان غذای برتر معرفی شده است. فواید و برتری این ریز جلبک نسبت به سایر منابع غذایی گیاهی و دیگر جلبکها، بسیار زیاد و قابل توجه میباشد. اسپیرولینا پلاتنسیس به صورت بالقوه منبع بزرگی از ترکیباتی است که میتوانند جهت تولید مواد اولیه فرآورده¬های غذایی استفاده شود. کاربرد اسپیرولینا پلاتنسیس و متابولیتهای آنها روند جالبی در بهبود ارزش فراوردههای غذایی سالم ایجاد کرده است. اسپیرولینا غنی¬ترین افزودنی به لحاظ پروتئین، اسیدهای چرب ضروری مثل گامالینولنیک، ویتامین¬ها خصوصا ویتامین B12 و پیشساز ویتامین A، مواد معدنی بهخصوص آهن و کلسیم، رنگدانه¬ها بهخصوص فایکوسیانین و سولفولیپیدها میباشد. نداشتن دیواره سلولی سلولزی باعث شده که جذب مواد مغذی آن بسیار راحتتر صورت گیرد. کم بودن میزان اسید نوکلئیک (کمتر از 4%) اسپیرولینا، یکی دیگر از برتریهای این ریزجلبک نسبت به سایر منابع پروتئینی مشابه می¬باشد. اسپیرولینا به دلیل داشتن اجزا و ترکیبات آنتیاکسیدانی مانند فایکوسیانین، سلنیوم، کارتنوئیدها اسیدچرب گامالینولنیک عامل دارویی بالقوهای جهت بیماریهای القاء شده بهوسیله تنش اکسیداسیونی میباشد. فیکوبیلی پروتئین موجود در اسپیرولینا به واسطه خاصیت جذب رادیکالهای آزاد میتواند به عنوان داروی ضد سرطان و ضد تومور مورد استفاده قرار بگیرد. در نتیجه فراوانی ترکیبات زیستی مهم در اسپیرولینا، فرصتهای جدیدی را در تولید محصولات غذایی فراسودمند فراهم میکنند که در ابن میان وعدههای غذایی میتوانند گزینه بسیار مناسبی برای غنیسازی با این ریزجلبک باشند (8). در تحقیق حاضر نیز توانایی عصاره جلبک اسپیرولینا پلاتنسیس در تغییر بیان ژن رمزکنندهی پروتئین پروآپوپتوزی BAD دخیل در مسیر مرگ سلولی و جلوگیری از تکثیر و رشد سلولهای آدنوکارسینومای معده، مورد بررسی قرار گرفت. در این تحقیق بقای سلولی سلولهای تحت تیمار با عصاره جلبک اسپیرولینا پلاتنسیس از طریق کیت MTT مورد ارزیابی قرار گرفت. بدین صورت که سلولها برای مدت زمان 24 و 48 ساعت تحت تاثیر غلظتهای مختلف عصاره جلبک اسپیرولینا پلاتنسیس (10،20 و 40 میکروگرم/ میلیلیتر) انکوبه شدند و غلظتی از عصاره که سبب کاهش 50 درصدی بقای سلولی میشود، محاسبه گردید. نتایج حاصل شده از این تست حاکی از آن میباشد که عصاره جلبک اسپیرولینا پلاتنسیس قادر است بقای سلولی سلولهای سرطانی معده را در دوز 40 میکروگرم/ میلیلیتر به پایینترین مقدار خود رساند. بهعلاوه در این تحقیق عصاره جلبک اسپیرولینا پلاتنسیس در تغییر بیان ژن آپوپتوزی BAD دخیل در مسیر مرگ سلولی در سلولهای رده AGS سرطان معده، مورد بررسی قرار گرفت. در این تحقیق تیمار سلولهای AGS سرطان معده، با دوز 40 میکروگرم/ میلیلیتر عصاره جلبک اسپیرولینا پلاتنسیس و انکوباسیون آن برای مدت 48 ساعت، افزایش معنیدار میزان بیان ژن BAD (P<0.001) را نشان داد. به علاوه تحقیقات ارائه شده در زیر شواهد محکمی بر اثبات صداقت نتایج حاصل شده از تحقیق حاضر میباشند: پینرو و همکارانش در سال 2001، به بررسی ساز و کار عملکردی پروتئین فیکوسیانین در عصاره جلبک اسپیرولینا پلاتنسیس پرداختند. نتایج حاصل از بررسی نشان داد که عملکرد آنتی اکسیدانی عصاره جلبک اسپیرولینا پلاتنسیس به واسطهی حضور پروتئین فیکوسیانین اعمال میگردد (18). رناتا و همکارانش، خواص ضد سرطانی ترکیب شمیایی تترا پیرول موجود در جلبک سبز- آبی اسپیرولینا پلاتنسیس را بر روی سلول های سرطانی پانکراس مورد بررسی قرار دادند. نتایج حاصل از بررسی نشان داد که این ترکیب باعث کاهش رشد سلول های سرطانی پانکراس تحت تیمار با اسپیرولینا می شود (19). چینگ هایا و همکارانش، اثر آنتیاکسیدانی، ایمنسازی و ضدالتهابی جلبک اسپیرولینا پلاتنسیس را در موش و انسان مورد بررسی قرار دادند. نتایج نشان داد که با مصرف جلبک اسپیرولینا پلاتنسیس بهعنوان مکمل غذایی فعالیت آنزیمهای آنتی-اکسیدانی سلولی، مهار پراکسیداسیون چربی، فعالیت آنزیم سوپراکسیداز دیسموتاز و آنزیم کاتالاز افزایش مییابد (20). لیو و همکارانش، به بررسی خواص ضد سرطانی ترکیب c-cp مشتق شده از جلبک اسپیرولینا پلاتنسیس پرداختند. نتایج نشان داد که این ترکیب دارای خواص آنتی اکسیدانی، ضد توموری و افزایش ایمنولوژیک دارد (21).
نتیجهگیری
نتایج حاصل از تست MTT و RT-Real Time PCR صورت گرفته در تحقیق حاضر، حاکی از آن است که عصاره جلبک اسپیرولینا پلاتنسیس قادر است احتمالاً از طریق تاثیرگذاری بر بیان ژن آپوپتوزی BAD، بقای سلولی سلولهای سرطانی معده انسان را کاهش دهد و از این طریق در درمان سرطان معده مؤثر واقع گردند.
سپاسگزاری
این مقاله حاصل پایاننامه تحت عنوان "بررسی اثر عصاره اسپیرولینا پلاتنسیس بر بقای سلولی و تغییر بیان ژن آپوپتوزی BAD در سلولهای آدنوکارسینومای معده انسان AGS" در مقطع کارشناسی ارشد در سال 1403 دانشگاه آزاد اسلامی واحد شهرکرد میباشد که با حمایت دانشگاه آزاد اسلامی واحد شهرکرد انجام شده است.
حامی مالی: ندارد
تعارض در منافع: وجود ندارد.
ملاحظات اخلاقی
پروپوزال این تحقیق توسط دانشگاه آزاد اسلامی واحد شهرکرد تایید شده است (کد اخلاق: IR.IAU.SHK.REC.1403.266).
مشارکت نویسندگان
لیلا روحی در ارائه ایده، لیلا روحی در طراحی مطالعه، جهانبخش دانیالی در جمعآوری دادهها، لیلا روحی و جهانبخش دانیالی در تجزیه و تحلیل دادهها مشارکت داشته و همه نویسندگان در تدوین، ویرایش اولیه و نهایی مقاله و پاسخگویی به سوالات مرتبط با مقاله سهیم هستند.
سرطان به دستهای از تودههای سلولی که دارای خصوصیات بدخیم باشند، اطلاق میگردد. امروزه سرطانها شایعترین و شدیدترین بیماریهای مشاهده شده در طب بالینی میباشند (1،2). در بین انواع بدخیمیها، آدنوکارسینومای معده یکی از سرطانهای شایع در سراسر جهان میباشد. علیرغم کاهشی که در سالهای اخیر در میزان بروز این سرطان رخ داده است اما همچنان به عنوان پنجمین سرطان شایع در جهان و چهارمین علت مرگ در اثر سرطان به حساب میآید (3). سن شایع این بدخیمی دهه ششم عمر است اما وقوع آن در سنین پایینتر نیز شایع میباشد. سرطان معده از جمله بیماریهایی است که اگر زود تشخیص داده شود بهطور کامل قابلیت علاج داشته و برعکس در صورتیکه دیر تشخیص داده شود ممکن است متاستاز رخ دهد. درمان اصلی سرطان معده در مراحل اولیه جراحی و در مراحل پیشرفته اقدامات جراحی به همراه شیمیدرمانی و رادیو درمانی میباشد که معمولا با نتایج خوبی همراه نیستند (4). بنابراین یک نیاز فوری برای ایجاد راهکارهای درمانی موثرتر، به منظور بهبود طول بقاء مبتلایان وجود دارد. از آنجاییکه مقاومت به مرگ سلولی و عدم وجود تعادل بین تقسیم سلولی و مرگ سلولی، منجر به عدم کنترل تکثیر سلول های توموری می شود، هماکنون توجه¬ها به سوی شناسایی ترکیبات درمانی که قادر به مهار تکثیر سلولهای توموری باشند، جلب شده است. برخی از این ترکیبات با هدف قرار دادن پروتئین های ضد آپوپتوزی منجر به افزایش پروتئینهای پروآپوپتوزی میشوند و القاء آپوپتوز در سلولهای سرطانی را تسهیل می¬نمایند، و بدین طریق باعث مرگ سلولهای توموری می¬شوند. از جمله آنها میتوان به ترکیبات با منشاء طبیعی اشاره کرد (5،6). استفاده از ترکیبات طبیعی به عنوان دارو به دنبال دارا بودن اثرات جانبی کمتر در مقایسه با ترکیبات شمیایی، همواره مورد توجه بوده است و بهعنوان یک ترکیب هدف درمانی جدید در کارهای تحقیقاتی مبتنی بر فرآیندهای آزمایشگاهی و بالینی مورد بررسی قرار میگیرند. از گذشته ترکیبات طبیعی منبع منحصربهفردی برای تأمین داروهای مصرفی جامعه بشری بودهاند و به خاطر عدم بروز مشکلات بیشتر در اثر استفاده از آنها نقش مهمی در درمان بیماریهای انسانی ایفا نموده¬اند (7). بر این اساس، محققان همیشه در راستای یافتن ترکیباتی با خواص ضد توموری که توانایی جلوگیری از گسترش و رشد سلولهای سرطانی را داشته باشند، بوده¬اند، که در این میان آبزیان دریایی بواسطه خواص تغذیهای و دارویی آنها همواره مورد توجه قرار گرفتهاند (8). جلبک سبز- آبی اسپیرولینا، یکی از مهمترین این آبزیان است که از سوی محققان علوم تغذیه به آن اشاره شده است و کشفیات زیادی در خصوص خواص تغذیهای و دارویی آن موجود می¬باشد. این جلبک رشتهای، متعلق به خانواده سیانوباکترها، دارای فیلامنت¬های فنرمانند، فتوسنتزکننده و بسیار کوچک است که دو جنس آرترواسپریا و پلاتنسیس آن مهم¬ترین اسپیرولیناهای خوراکی به حساب میآیند و به طور تجاری در سرتاسر جهان تولید می¬گردند. اسپیرولینا پلاتنسیس به دلیل داشتن اجزا و ترکیبات آنتیاکسیدانی مانند فایکوسیانین، سلنیوم، کارتنوئیدها، اسید چرب گامالینولنیک، عامل دارویی بالقوه¬ای برای بیماری¬های القاء شده بهوسیله تنش اکسیداسیونی نظیر سرطان می¬باشد (9,10). از اینرو، هم اکنون اسپیرولینا پلاتنسیس از سوی سازمان بهداشت جهانی بهعنوان یک گزینه درمانی بالقوه جهت درمان سرطان اعلام گردیده است (11،12). در مطالعه حاضر نیز اثر عصاره اسپیرولینا پلاتنسیس بر بقای سلولی و تغییر بیان ژن آپوپتوزی BAD (پروتئین محصول ژن BAD با تشکیل هترودایمر با پروتئین BCL-2 عملکرد ضد آپوپتوزی BCL-2 را مهار می¬نماید و منجر به القاء آپوپتوز میشود (7) در سلولهای آدنوکارسینومای معده انسان (AGS) مورد بررسی قرار گرفت.
روش بررسی
این مطالعه بهصورت تجربی در شش ماهه اول سال 1403 در مراکز تحقیقاتی سلولی- تکوینی، بیوتکنولوژی و گیاهان دارویی مجتمع آزمایشگاهی دانشگاه آزاد اسلامی واحد
شهرکرد بهصورت تجربی با مجوز اخلاق در پژوهش انجام شد. رده سلولی AGS از مرکز ملی ذخایر ژنتیکی و زیستی ایران خریداری شد. در محیط کشت DMEM-F12 (Dulbecco's Modified Eagle's medium) (Gibco, USA) حاوی 10 درصد FBS (Foetal Bovine Serum) (Gibco, USA) و یک درصد Penstrep (Penicillin-Streptomycin) (Gibco, USA) در انکوباتور (Memmert, Germany) با فشار 5 درصد گاز CO2، رطوبت 90 درصد و دمای 37 درجه سانتی¬گراد، در فلاسک کشت سلول ۷۵ سانتیمتر مربع کشت داده شد. محیط کشت هفتهای سه بار تعویض و برای برداشت کردن سلولها از محلول تریپسین/EDTA استفاده شد. اسپیرولینا پلاتنسیس به صورت آماده و به حالت جامد از شرکت دانش پژوهان قشم با نام تجاری اسپیرولینا (سوپر فود) تهیه گردید. برای تهیه عصاره از این ماده در مرکز تحقیقات گیاهان دارویی دانشگاه آزاد اسلامی واحد شهرکرد، پودر اسپیرولینا پلاتنسیس درون فـالکون ریختــه شـد و حلال اتانولی 96 درصد به آن اضافه و اقدام به عصارهگیری با حرارت و درجه خلوص بالا شد (مدت زمان 20 دقیقه). مایع حاصل توسط تبخیرکننده چرخشی در دمای 40 درجه سانتیگراد تا خروج کامل حلال استخراجی و دستیابی به عصاره غلیظ و ویسکوز تغلیظ گردید. عمل عصارهگیری سه بار تکرار گردید و تا زمان استفاده در دمای 4 درجه سانتیگراد نگهداری شد.
سنجش بقای سلولی: بقای سلولی رده AGS تیمار شده با غلظتهای مختلف عصاره اسپیرولینا پلاتنسیس و گروه¬ کنترل (فاقد تیمار و صرفا در معرض محیط کشت) توسط تست MTT، با استفاده از کیت (CellTiter 96® Non-Radioactive Cell Proliferation Assay (MTT) با شماره محصول G4000 مورد ارزیابی قرار گرفت. به این ترتیب که تعداد 103×5 سلول در هر چاهک پلیت 96 چاهکی کشت داه شد و سپس با غلظتهای 10 (گروه I)، 20 (گروه II) و 40 (گروه III) میکروگرم/ میلی¬لیتر عصاره اسپیرولینا پلاتنسیس برای مدت زمان 24 و 48 ساعت تیمار و انکوبه گردید. پس از اتمام زمان انکوباسیون 24 و 48 ساعته، محیط رویی تیمار گردآوری شد و مقدار µl 20 محلول MTT به هر چاهک اضافه گردید و انکوباسیون چهار ساعته صورت گرفت. در نهایت جذب نمونهها توسط دستگاه (ELISA-reader, Awareness Technology, USA) با طول موج nm 540- 630 خوانش گردید (13). اطلاعات مربوط به اثر غلظتهای مختلف عصاره اسپیرولینا پلاتنسیس بر رشد سلول AGS با شاخص IC50 (غلظتی از دارو که رشد سلول را نسبت به کنترل 50 درصد کاهش میدهد) ارائه شدند. IC50ها از طریق رسم منحنیهای رشد سلول در برابر رقت-های مختلف سوپرناتانت و از طریق رسم معادله رگرسیون غیر خطی منحنی¬های رشد سلول در برابر غلظت سوپرناتانت محاسبه گردید.
سنجش بیان ژن: به منظور بررسی میزان بیان ژن BAD ، تعداد 105×3 سلول در پلیتهای 6 خانه کشت داده شد، و سپس، با غلظت 40 میکروگرم/ میلیلیتر عصاره اسپیرولینا پلاتنسیس در بازه زمانی 48 ساعت تیمار و انکوبه شدند. پس از گذشت زمان انکوباسیون 48 ساعته، سلول¬ها در دو گروه؛ گروه تست شامل غلظت 40 میکروگرم/ میلیلیتر از عصاره اسپیرولینا پلاتنسیس و گروه کنترل، برداشت و پس از شستشو با بافر PBS، Total RNA سلولی با استفاده از معرف RNXTM –PLUS (RNX-Plus Solution for total RNA isolation)، جدا گردید. به منظور انجام مرحله Heat block، نمونههای حاصل از مرحله قبل در دستگاه ترموسایکلر با دمای 60 درجه سانتیگراد به مدت 20 دقیقه قرار داده شدند. در ادامه تمام توالیهای RNA با استفاده از کیت سنتز cDNA (PrimeScriptTM RT Reagent kit (Perfect Real Time))، (Takara)، به cDNA تبدیل و به فریزر 20- درجه سانتی گراد منتقل شدند. سنجش میزان بیان ژن BAD با استفاده از دستگاه Real Time PCR مدل (Rotor gene 3000 corbett, Australia) مورد ارزیابی قرار گرفت. برای انجام واکنش، مخلوط واکنشی متشکل از cDNA، به مقدار 1 میکرولیتر، پرایمر رفت و برگشت هر کدام به مقدار 0/5 میکرولیتر، RNase-free water، به مقدار 5/5 میکرولیتر و 12/5 میکرولیتر مسترمیکس (Master Mix RT-PCR) (Ampliqon) تهیه گردید (14). توالی پرایمرهای پیشرو (Forward) و پسرو (Reverse) ژنهای GAPDH و BAD با استفاده از نرم افزار Oligo6 طراحی و سپس با Blast نمودن آنها در NBCI از صحیح بودن آنها اطمینان حاصل شد و نهایتا توسط شرکت Macrogen سنتز شدند (جدول 1). از ژن GAPDH، بهعنوان کنترل داخلی استفاده شد. سپس مخلوط واکنش پس از آمادهسازی با حجم نهایی 20 میکرولیتر تحت تاثیر برنامهی دمایی ذکر شده در (جدول 2) قرار گرفت.
تجزیه و تحلیل آماری
نهایتاً بررسی آماری با استفاده از آزمون منویتنی (بهطورکلی آزمون ناپارامتریک به نرمال بودن یا نبودن توزیع دادهها حساس نیست و در هر شرایطی قابل استفاده است) از طریق نرمافزارversion 16 SPSS انجام شد. حدود اطمینان برای همه آزمایشات 95% در نظر گرفته شد و 5% < P معنیدار محسوب گردید.
جدول1: مشخصات پرایمر مربوط به ژنهای BAD و GAPDH

جدول2: شرایط دمایی واکنش Rael Time PCR

نتایج
سنجش میکروسکوپی سلول های تحت تیمار: سلول های سرطانی AGS در غلظت های مختلف عصاره جلبک اسپیرولینا پلاتنسیس (10، 20 و 40 میکروگرم/ میلیلیتر) برای مدت زمان 24 و 48 ساعت کشت داده شدند. تصویر زیر (شکل 1، A-D) انکوباسیون سلول های تحت تیمار با غلظتهای مختلف عصارهی جلبک اسپیرولینا را نشان میدهد که مشاهدات میکروسکوپی حاکی از کاهش تعداد سلول ها در گروه های تحت تیمار در مقایسه با گروه کنترل بهصورت وابسته به غلظت میباشد.
بقای سلولی و تعیین نقطه IC50: آنچه که از نتایج تست MTT می توان برآورد کرد، این است که بقای سلولی سلول-های رده آدنوکارسینومای معده انسان (AGS)، تحت تیمار با غلظتهای مختلف عصاره جلبک اسپیرولینا پلاتنسیس (10، 20 و 40 میکروگرم/ میلی لیتر) ظرف مدت زمان انکوباسیون 24 و 48 ساعت، در سایر گروههای آزمایشی نسبت به گروه کنترل کاهش یافته است. این کاهش در هر دو زمان به صورت وابسته به زمان و دوز عصاره میباشد (نمودار 1). در این پژوهش عصاره جلبک اسپیرولینا پلاتنسیس در نقطه IC50 بهعنوان غلظتی که بقای سلولی را 50 درصد کاهش میدهد 40 میکروگرم/ میلیلیتر بوده است (نمودار 2). بقای سلولی سلولهای رده AGS آدنوکارسینومای معده، در مقایسه با گروه کنترل در دوز 20 (P<0.001) و 40 (P<0.0001) میکروگرم/ میلیلیتر در زمان انکوباسیون 48 ساعت کاهش معنیداری را نشان داد.
تغییر بیان ژن BAD: تیمار سلولهای رده AGS با عصاره جلبک اسپیرولینا پلاتنسیس و انکوباسیون آنها برای مدت 48 ساعت نشان داد که میزان بیان ژن BAD افزایش یافته است. نمودار زیر (نمودار 3) این افزایش بیان معنیدار را در ژن BAD براساس CtΔΔ نمایش می¬دهد.
.JPG)
شکل1: تاثیر غلظت¬های مختلف عصاره جلبک اسپیرولینا پلاتنسیس بر رده سلولی AGS

نمودار 1: اثر عصاره جلبک اسپیرولینا پلاتنسیس بر بقای سلولی رده سلولی AGS در مدت زمان انکوباسیون 24 و 48 ساعت.
P<0.001*،P<0.0001** در مقابل گروه کنترل

نموار 2: غلظت 40 میکروگرم/ میلیلیتر عصاره جلبک اسپیرولینا پلاتنسیس در نقطه IC50 در روش MTT

نمودار 3: نمودار میزان بیان ژن BAD براساس Ct در غلظت 40 میکروگرم/میلیلیتر و زمان انکوباسیون 48 ساعت.
P<0.001** اختلاف معنی¬دار در مقابل گروه کنترل
بحث
یکی از معضلات امروزی در جوامع بشری سرطان معده میباشد که بهعنوان یک بیماری چند عاملی در نتیجه تداوم آسیب¬های ناشی از مواجهه مداوم با عوامل سرطان¬زا ایجاد میشود. علیرغم کاهش قابلملاحظه در بروز این نوع بدخیمی در طول دهههای گذشته، در اکثر کشورهای صنعتی هنوز این بیماری دومین علت شایع مرگ و میر افراد در اثر سرطان میباشد که سالیانه باعث مرگ حدود یک میلیون نفر در سرتاسر جهان می شود (16,15). مبتلایان به آدنوکارسینومای معده دارای بقاء 5 ساله هستند و در بیش از 90% موارد درمان تومور معدی با جراحی، تنها شانس درمانی می باشد. اما به دلیل اینکه در حال حاضر تشخیص زودهنگام سرطان معده امکانپذیر نیست و معمولاً تشخیص زمانی صورت میگیرد که سرطان بهطور موضعی پیشرفت کرده است و به درون دیواره معده نفوذ نموده، این شانس به کمتر از 30% کاهش می یابد (17). لذا با توجه به افزایش روز افزون تعداد مبتلایان که شمار زیادی از آنها پس از گذراندن مراحل دشوار عمل های جراحی باز هم دچار عود بیماری می شوند و از آنجاییکه مقاومت به مرگ سلولی و عدم وجود تعادل بین تقسیم سلولی و مرگ سلولی منجر به عدم کنترل تکثیر سلولهای توموری می شود، امروزه نیاز به ترکیبات درمانی که قادر به مهار تکثیر سلول¬های توموری باشند، به شدت احساس می شود. امروزه تحقیق در راستای یافتن ترکیباتی با خواص ضد توموری که توانایی جلوگیری از گسترش و رشد سلول¬های سرطانی را داشته باشند پیشرفت های قابلتوجهی داشته است. با توجه به عوارض جانبی ترکیبات صناعی و داروهای فارماکولوژیک ضد سرطان، محققان همیشه در راستای یافتن ترکیبات طبیعی فاقد عوارض جانبی بوده اند و در این میان آبزیان دریائی بواسطه فراوانی و تنوع بسیار بالای آنها همواره قابلتوجه قرار گرفتهاند. یکی از مهمترین این آبزیان که آثار و فوائد فراوانی از سوی محققان علوم تغذیه برای آن بیان شده و کشفیات زیادی در خصوص خواص تغذیهای و دارویی آن بهدست آمده است، جلبک سبز - آبی اسپیرولینا¬ پلاتنسیس میباشد. اسپیرولینا یکی از نوید بخشترین ریز جلبکها بوده که از سوی سازمان بهداشت جهانی به عنوان راه حل درمانی سودمند برای فردا و همچنین به عنوان غذای برتر معرفی شده است. فواید و برتری این ریز جلبک نسبت به سایر منابع غذایی گیاهی و دیگر جلبکها، بسیار زیاد و قابل توجه میباشد. اسپیرولینا پلاتنسیس به صورت بالقوه منبع بزرگی از ترکیباتی است که میتوانند جهت تولید مواد اولیه فرآورده¬های غذایی استفاده شود. کاربرد اسپیرولینا پلاتنسیس و متابولیتهای آنها روند جالبی در بهبود ارزش فراوردههای غذایی سالم ایجاد کرده است. اسپیرولینا غنی¬ترین افزودنی به لحاظ پروتئین، اسیدهای چرب ضروری مثل گامالینولنیک، ویتامین¬ها خصوصا ویتامین B12 و پیشساز ویتامین A، مواد معدنی بهخصوص آهن و کلسیم، رنگدانه¬ها بهخصوص فایکوسیانین و سولفولیپیدها میباشد. نداشتن دیواره سلولی سلولزی باعث شده که جذب مواد مغذی آن بسیار راحتتر صورت گیرد. کم بودن میزان اسید نوکلئیک (کمتر از 4%) اسپیرولینا، یکی دیگر از برتریهای این ریزجلبک نسبت به سایر منابع پروتئینی مشابه می¬باشد. اسپیرولینا به دلیل داشتن اجزا و ترکیبات آنتیاکسیدانی مانند فایکوسیانین، سلنیوم، کارتنوئیدها اسیدچرب گامالینولنیک عامل دارویی بالقوهای جهت بیماریهای القاء شده بهوسیله تنش اکسیداسیونی میباشد. فیکوبیلی پروتئین موجود در اسپیرولینا به واسطه خاصیت جذب رادیکالهای آزاد میتواند به عنوان داروی ضد سرطان و ضد تومور مورد استفاده قرار بگیرد. در نتیجه فراوانی ترکیبات زیستی مهم در اسپیرولینا، فرصتهای جدیدی را در تولید محصولات غذایی فراسودمند فراهم میکنند که در ابن میان وعدههای غذایی میتوانند گزینه بسیار مناسبی برای غنیسازی با این ریزجلبک باشند (8). در تحقیق حاضر نیز توانایی عصاره جلبک اسپیرولینا پلاتنسیس در تغییر بیان ژن رمزکنندهی پروتئین پروآپوپتوزی BAD دخیل در مسیر مرگ سلولی و جلوگیری از تکثیر و رشد سلولهای آدنوکارسینومای معده، مورد بررسی قرار گرفت. در این تحقیق بقای سلولی سلولهای تحت تیمار با عصاره جلبک اسپیرولینا پلاتنسیس از طریق کیت MTT مورد ارزیابی قرار گرفت. بدین صورت که سلولها برای مدت زمان 24 و 48 ساعت تحت تاثیر غلظتهای مختلف عصاره جلبک اسپیرولینا پلاتنسیس (10،20 و 40 میکروگرم/ میلیلیتر) انکوبه شدند و غلظتی از عصاره که سبب کاهش 50 درصدی بقای سلولی میشود، محاسبه گردید. نتایج حاصل شده از این تست حاکی از آن میباشد که عصاره جلبک اسپیرولینا پلاتنسیس قادر است بقای سلولی سلولهای سرطانی معده را در دوز 40 میکروگرم/ میلیلیتر به پایینترین مقدار خود رساند. بهعلاوه در این تحقیق عصاره جلبک اسپیرولینا پلاتنسیس در تغییر بیان ژن آپوپتوزی BAD دخیل در مسیر مرگ سلولی در سلولهای رده AGS سرطان معده، مورد بررسی قرار گرفت. در این تحقیق تیمار سلولهای AGS سرطان معده، با دوز 40 میکروگرم/ میلیلیتر عصاره جلبک اسپیرولینا پلاتنسیس و انکوباسیون آن برای مدت 48 ساعت، افزایش معنیدار میزان بیان ژن BAD (P<0.001) را نشان داد. به علاوه تحقیقات ارائه شده در زیر شواهد محکمی بر اثبات صداقت نتایج حاصل شده از تحقیق حاضر میباشند: پینرو و همکارانش در سال 2001، به بررسی ساز و کار عملکردی پروتئین فیکوسیانین در عصاره جلبک اسپیرولینا پلاتنسیس پرداختند. نتایج حاصل از بررسی نشان داد که عملکرد آنتی اکسیدانی عصاره جلبک اسپیرولینا پلاتنسیس به واسطهی حضور پروتئین فیکوسیانین اعمال میگردد (18). رناتا و همکارانش، خواص ضد سرطانی ترکیب شمیایی تترا پیرول موجود در جلبک سبز- آبی اسپیرولینا پلاتنسیس را بر روی سلول های سرطانی پانکراس مورد بررسی قرار دادند. نتایج حاصل از بررسی نشان داد که این ترکیب باعث کاهش رشد سلول های سرطانی پانکراس تحت تیمار با اسپیرولینا می شود (19). چینگ هایا و همکارانش، اثر آنتیاکسیدانی، ایمنسازی و ضدالتهابی جلبک اسپیرولینا پلاتنسیس را در موش و انسان مورد بررسی قرار دادند. نتایج نشان داد که با مصرف جلبک اسپیرولینا پلاتنسیس بهعنوان مکمل غذایی فعالیت آنزیمهای آنتی-اکسیدانی سلولی، مهار پراکسیداسیون چربی، فعالیت آنزیم سوپراکسیداز دیسموتاز و آنزیم کاتالاز افزایش مییابد (20). لیو و همکارانش، به بررسی خواص ضد سرطانی ترکیب c-cp مشتق شده از جلبک اسپیرولینا پلاتنسیس پرداختند. نتایج نشان داد که این ترکیب دارای خواص آنتی اکسیدانی، ضد توموری و افزایش ایمنولوژیک دارد (21).
نتیجهگیری
نتایج حاصل از تست MTT و RT-Real Time PCR صورت گرفته در تحقیق حاضر، حاکی از آن است که عصاره جلبک اسپیرولینا پلاتنسیس قادر است احتمالاً از طریق تاثیرگذاری بر بیان ژن آپوپتوزی BAD، بقای سلولی سلولهای سرطانی معده انسان را کاهش دهد و از این طریق در درمان سرطان معده مؤثر واقع گردند.
سپاسگزاری
این مقاله حاصل پایاننامه تحت عنوان "بررسی اثر عصاره اسپیرولینا پلاتنسیس بر بقای سلولی و تغییر بیان ژن آپوپتوزی BAD در سلولهای آدنوکارسینومای معده انسان AGS" در مقطع کارشناسی ارشد در سال 1403 دانشگاه آزاد اسلامی واحد شهرکرد میباشد که با حمایت دانشگاه آزاد اسلامی واحد شهرکرد انجام شده است.
حامی مالی: ندارد
تعارض در منافع: وجود ندارد.
ملاحظات اخلاقی
پروپوزال این تحقیق توسط دانشگاه آزاد اسلامی واحد شهرکرد تایید شده است (کد اخلاق: IR.IAU.SHK.REC.1403.266).
مشارکت نویسندگان
لیلا روحی در ارائه ایده، لیلا روحی در طراحی مطالعه، جهانبخش دانیالی در جمعآوری دادهها، لیلا روحی و جهانبخش دانیالی در تجزیه و تحلیل دادهها مشارکت داشته و همه نویسندگان در تدوین، ویرایش اولیه و نهایی مقاله و پاسخگویی به سوالات مرتبط با مقاله سهیم هستند.
References:
1- Nasr Isfahani H, Rouhi L, Ziya Jahromi N, Khashei Varnamkhasti K. Effect of citric acid on p53 and p21 genes expression of the human gastric Adenocarcinoma cell line (AGS). PJMS 2022; 18(4): 17-24. [Persian]
2- Molocea CE, Tsokanos FF, Herzig S. Exploiting common aspects of obesity and cancer cachexia for future therapeutic strategies. Curr Opin Pharmacol 2020;53:101-116.
3- Yang WJ, Zhao HP, Yu Y, Wang JH, Guo L, Liu JY, et al. Updates on Global Epidemiology, Risk and Prognostic Factors of Gastric Cancer. World J Gastroenterol 2023; 29(16): 2452-68.
4- Zaręba KP, Zińczuk J, Dawidziuk T, Pryczynicz A, Guzińska-Ustymowicz K, Kędra B. Stomach cancer in young people - a diagnostic and therapeutic problem. Prz Gastroenterol 2019;14(4):283-285.
5- Broecker-Preuss M, Viehof J, Jastrow H, Becher-Boveleth N, Fuhrer D, Mann K. Cell Death Induction by the BH3 Mimetic GX15-070 in Thyroid Carcinoma Cells. J Exp Clin Cancer Res 2015; 34(1): 69.
6- Broecker-Preuss M, Becher-Boveleth N, Müller S, Mann K. The BH3 Mimetic Drug ABT-737 Induces Apoptosis and Acts Synergistically with Chemotherapeutic Drugs in Thyroid Carcinoma Cells. Cancer Cell Int 2016; 16(1): 27.
7- Zhu L, Li L, Li Y, Wang J, Wang Q. Chinese Herbal Medicine as an Adjunctive Therapy for Breast Cancer. Evid Based Complement Alternat Med 2016; 2016: 9469276.
8- Romanos M, Andrada-Serpa MJ, dos S, Ribeiro A, Yoneshigue-Valentin Y, Costa SS. Inhibitory effect of extracts of Brazilian marine algae on human T-cell lymphotropic virus type 1 (HTLV-1)-induced syncytium formation in vitro. Cancer invests 2002; 20(1): 46-54.
9- Li L, Liu H, Zhang P. Effect of Spirulina Meal Supplementation on Growth Performance and Feed Utilization in Fish and Shrimp: A Meta-Analysis. Aquac Nutr 2022; 2022:8517733.
10- Karkos PD, Leong SC, Karkos CD, Sivaji N, Assimakopoulos DA. Spirulina in clinical practice: evidence-based human applications. Evid Based Complement Alternat Med 2011; 2011:531053.
11- Wang Z, Zhang X. Inhibitory Effects of Small Molecular Peptides from Spirulina (Arthrospira) Platensis on Cancer Cell Growth. Food Funct 2016; 7(2): 781-8.
12- Fayyad RJ, Ali ANM, Dwaish AS, Al-Abboodi AKA. Anticancer Activity of Spirulina Platensis Methanolic Extracts Against L20B and MCF7 Human Cancer Cell Lines. Plant Arch 2019; 19(1): 1419-26.
13- Malaki MS, Rouhi L, Khashei Varnamkhasti K. Cytotoxic and Antimicrobial Effects of Lactobacillus Sakei on Human Colorectal Adenocarcinoma Cell Line (HT29) and Some Pathogenic Microorganisms. Tehran Univ Med J 2021; 78(10): 644-50. [Persian]
14- Varnamkhasti KK, Tavakoli P, Rouhi L, Raisi S. Cytotoxicity, Apoptosis Induction and Change of P53, PARP, P21 and Bcl-2 Genes Expression in the Human Anaplastic Thyroid Carcinoma Cells Line (SW-1736) with Curcumin. Genetics & Applications 2021; 5(1): 10-17.
15- Caldas C, Carneiro F, Lynch HT, Yokota J, Wiesner GL, Powell SM, et al. Familial Gastric Cancer: Overview and Guidelines for Management. J Med Genet 1999; 36(12): 873-80.
16- Siegel RL, Kratzer TB, Giaquinto AN, Sung H, Jemal A. Cancer statistics, 2025. CA Cancer J Clin 2025;75(1):10-45.
17- Norouzinezhad F, Erfani H, Norouzinejad A, Ghaffari F, Kaveh F. Epidemiological Characteristics and Trend in the Incidence of Human Brucellosis in Iran from 2009 to 2017. J Res Health Sci 2021; 21(4): e00535.
18- Piñero Estrada JE, Bermejo Bescós P, Villar del Fresno AM. Antioxidant Activity of Different Fractions of Spirulina Platensis Protean Extract. Farmaco 2001; 56(5-7): 497-500.
19- Koníčková R, Vaňková K, Vaníková J, Váňová K, Muchová L, Subhanová I, et al. Anti-Cancer Effects of Blue-Green Alga Spirulina Platensis, A Natural Source of Bilirubin-Like Tetrapyrrolic Compounds. Ann Hepatol 2014; 13(2): 273-83.
20- Wu Q, Liu L, Miron A, Klímová B, Wan D, Kuča K. The Antioxidant, Immunomodulatory, and Anti-Inflammatory Activities of Spirulina: An Overview. Archives of toxicology 2016; 90(8): 1817-40.
21- Liu Q, Huang Y, Zhang R, Cai T, Cai Y. Medical Application of Spirulina Platensis Derived C-Phycocyanin. Evid Based Complement Alternat Med 2016; 2016: 7803846.
1- Nasr Isfahani H, Rouhi L, Ziya Jahromi N, Khashei Varnamkhasti K. Effect of citric acid on p53 and p21 genes expression of the human gastric Adenocarcinoma cell line (AGS). PJMS 2022; 18(4): 17-24. [Persian]
2- Molocea CE, Tsokanos FF, Herzig S. Exploiting common aspects of obesity and cancer cachexia for future therapeutic strategies. Curr Opin Pharmacol 2020;53:101-116.
3- Yang WJ, Zhao HP, Yu Y, Wang JH, Guo L, Liu JY, et al. Updates on Global Epidemiology, Risk and Prognostic Factors of Gastric Cancer. World J Gastroenterol 2023; 29(16): 2452-68.
4- Zaręba KP, Zińczuk J, Dawidziuk T, Pryczynicz A, Guzińska-Ustymowicz K, Kędra B. Stomach cancer in young people - a diagnostic and therapeutic problem. Prz Gastroenterol 2019;14(4):283-285.
5- Broecker-Preuss M, Viehof J, Jastrow H, Becher-Boveleth N, Fuhrer D, Mann K. Cell Death Induction by the BH3 Mimetic GX15-070 in Thyroid Carcinoma Cells. J Exp Clin Cancer Res 2015; 34(1): 69.
6- Broecker-Preuss M, Becher-Boveleth N, Müller S, Mann K. The BH3 Mimetic Drug ABT-737 Induces Apoptosis and Acts Synergistically with Chemotherapeutic Drugs in Thyroid Carcinoma Cells. Cancer Cell Int 2016; 16(1): 27.
7- Zhu L, Li L, Li Y, Wang J, Wang Q. Chinese Herbal Medicine as an Adjunctive Therapy for Breast Cancer. Evid Based Complement Alternat Med 2016; 2016: 9469276.
8- Romanos M, Andrada-Serpa MJ, dos S, Ribeiro A, Yoneshigue-Valentin Y, Costa SS. Inhibitory effect of extracts of Brazilian marine algae on human T-cell lymphotropic virus type 1 (HTLV-1)-induced syncytium formation in vitro. Cancer invests 2002; 20(1): 46-54.
9- Li L, Liu H, Zhang P. Effect of Spirulina Meal Supplementation on Growth Performance and Feed Utilization in Fish and Shrimp: A Meta-Analysis. Aquac Nutr 2022; 2022:8517733.
10- Karkos PD, Leong SC, Karkos CD, Sivaji N, Assimakopoulos DA. Spirulina in clinical practice: evidence-based human applications. Evid Based Complement Alternat Med 2011; 2011:531053.
11- Wang Z, Zhang X. Inhibitory Effects of Small Molecular Peptides from Spirulina (Arthrospira) Platensis on Cancer Cell Growth. Food Funct 2016; 7(2): 781-8.
12- Fayyad RJ, Ali ANM, Dwaish AS, Al-Abboodi AKA. Anticancer Activity of Spirulina Platensis Methanolic Extracts Against L20B and MCF7 Human Cancer Cell Lines. Plant Arch 2019; 19(1): 1419-26.
13- Malaki MS, Rouhi L, Khashei Varnamkhasti K. Cytotoxic and Antimicrobial Effects of Lactobacillus Sakei on Human Colorectal Adenocarcinoma Cell Line (HT29) and Some Pathogenic Microorganisms. Tehran Univ Med J 2021; 78(10): 644-50. [Persian]
14- Varnamkhasti KK, Tavakoli P, Rouhi L, Raisi S. Cytotoxicity, Apoptosis Induction and Change of P53, PARP, P21 and Bcl-2 Genes Expression in the Human Anaplastic Thyroid Carcinoma Cells Line (SW-1736) with Curcumin. Genetics & Applications 2021; 5(1): 10-17.
15- Caldas C, Carneiro F, Lynch HT, Yokota J, Wiesner GL, Powell SM, et al. Familial Gastric Cancer: Overview and Guidelines for Management. J Med Genet 1999; 36(12): 873-80.
16- Siegel RL, Kratzer TB, Giaquinto AN, Sung H, Jemal A. Cancer statistics, 2025. CA Cancer J Clin 2025;75(1):10-45.
17- Norouzinezhad F, Erfani H, Norouzinejad A, Ghaffari F, Kaveh F. Epidemiological Characteristics and Trend in the Incidence of Human Brucellosis in Iran from 2009 to 2017. J Res Health Sci 2021; 21(4): e00535.
18- Piñero Estrada JE, Bermejo Bescós P, Villar del Fresno AM. Antioxidant Activity of Different Fractions of Spirulina Platensis Protean Extract. Farmaco 2001; 56(5-7): 497-500.
19- Koníčková R, Vaňková K, Vaníková J, Váňová K, Muchová L, Subhanová I, et al. Anti-Cancer Effects of Blue-Green Alga Spirulina Platensis, A Natural Source of Bilirubin-Like Tetrapyrrolic Compounds. Ann Hepatol 2014; 13(2): 273-83.
20- Wu Q, Liu L, Miron A, Klímová B, Wan D, Kuča K. The Antioxidant, Immunomodulatory, and Anti-Inflammatory Activities of Spirulina: An Overview. Archives of toxicology 2016; 90(8): 1817-40.
21- Liu Q, Huang Y, Zhang R, Cai T, Cai Y. Medical Application of Spirulina Platensis Derived C-Phycocyanin. Evid Based Complement Alternat Med 2016; 2016: 7803846.
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |







