دوره 33، شماره 11 - ( بهمن 1404 )
جلد 33 شماره 11 صفحات 9612-9600 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Sheikhi Z, Zahraeefar M, Khakshour A, Kabiri M, Sadeghi T, Shojaei P. Evaluation of Urine Analysis in Children with covid-19 Hospitalized in Akbar Mashhad Hospital during the Period of 2021-2023. JSSU 2026; 33 (11) :9600-9612
URL: http://jssu.ssu.ac.ir/article-1-6410-fa.html
URL: http://jssu.ssu.ac.ir/article-1-6410-fa.html
شیخی ژیلا، زهرایی فر مهلا، خاکشور علی، کبیری منا، صادقی طاهره، شجاعی پریسا. ارزیابی آزمایشات ادراری در کودکان مبتلا به کووید-19 بستری در بیمارستان اکبر مشهد طی بازه زمانی 1400-1401. مجله علمي پژوهشي دانشگاه علوم پزشكي شهید صدوقی يزد. 1404; 33 (11) :9600-9612
ژیلا شیخی 

 ، مهلا زهرایی فر
، مهلا زهرایی فر 

 ، علی خاکشور
، علی خاکشور 

 ، منا کبیری
، منا کبیری 

 ، طاهره صادقی
، طاهره صادقی 

 ، پریسا شجاعی*
، پریسا شجاعی* 




 ، مهلا زهرایی فر
، مهلا زهرایی فر 

 ، علی خاکشور
، علی خاکشور 

 ، منا کبیری
، منا کبیری 

 ، طاهره صادقی
، طاهره صادقی 

 ، پریسا شجاعی*
، پریسا شجاعی* 


متن کامل [PDF 861 kb]
(77 دریافت)
| چکیده (HTML) (123 مشاهده)
References:
1- Karimi J. Epidemiological Review of the Coronavirus Disease 2019 (COVID-19) Pandemic up to 15 March 2020. Journal of Isfahan Medical School 2020; 38(561): 14-23.
2- Ebner B, Volz Y, Mumm J-N, Stief CG, Magistro G. The COVID-19 Pandemic—What Have Urologists Learned? Nat Rev Urol 2022; 19(6): 344-356.
3- Struyf T, Deeks JJ, Dinnes J, Takwoingi Y, Davenport C, Leeflang MM, et al. Signs and Symptoms to Determine If a Patient Presenting in Primary Care or Hospital Outpatient Settings Has COVID‐19. Cochrane Database Syst Rev 2022; 5(5): CD013665.
4- Li W, Zhang B, Lu J, Liu S, Chang Z, Peng C, et al. Characteristics of Household Transmission of COVID-19. Clin Infect Dis 2020; 71(8): 1943-46.
5- Bi Q, Wu Y, Mei S, Ye C, Zou X, Zhang Z, et al. Epidemiology and Transmission of COVID-19 in 391 Cases and 1286 of their Close Contacts in Shenzhen, China: A Retrospective Cohort Study. Lancet Infectious Diseases 2020; 20(8): 911-9.
6- Rosenberg ES, Dufort EM, Blog DS, Hall EW, Hoefer D, Backenson BP, et al. COVID-19 Testing, Epidemic Features, Hospital Outcomes, and Household Prevalence, New York State—March 2020. Clin Infect Dis 2020; 71(8): 1953-9.
7- Laws RL, Chancey RJ, Rabold EM, Chu VT, Lewis NM, Fajans M, et al. Symptoms and transmission of SARS-CoV-2 among children—Utah and Wisconsin, March–May 2020. Pediatrics 2021; 147(1): e2020027268.
8- Grijalva CG. Transmission of SARS-COV-2 Infections in Households—Tennessee and Wisconsin, April–September 2020. MMWR Morbidity and Mortality Weekly Report 2020; 69(44): 1631-4.
9- Madewell ZJ, Yang Y, Longini IM, Halloran ME, Dean NE. Household Secondary Attack Rates of SARS-Cov-2 by Variant and Vaccination Status: An Updated Systematic Review and Meta-Analysis. JAMA Network Open 2022; 5(4): e229317-e.
10- Paul LA, Daneman N, Schwartz KL, Brown KA, Whelan M, Chan E, et al. Association of Age and Pediatric Household Transmission of SARS-Cov-2 Infection. JAMA Pediatr 2021; 175(11): 1151-8.
11- Lee B, Raszka WV. COVID-19 in Children: Looking Forward, Not Back. Pediatrics 2021; 147(1): e2020029736.
12- Coffin SE, Rubin D. Yes, Children Can Transmit COVID, But We Need Not Fear. Pediatrics 2021; 175(11): 1110-2.
13- Chen F, Tian Y, Zhang L, Shi Y. The Role of Children in Household Transmission of COVID-19: A Systematic Review and Meta-Analysis. nt J Infect Dis 2022; 122: 266-75.
14- Sorkhi H, Esmaeili Dooki M, Nikpour M, Mohammadi M, Mohammadpour-Mir A, Kiani M, et al. COVID-19 and Renal Involvement in Children: A Retrospective Study. Caspian J Intern Med 2022; 13(Suppl 3): 193-8.
15- Raina R, Mawby I, Chakraborty R, Sethi SK, Mathur K, Mahesh S, et al. Acute Kidney Injury in COVID-19 Pediatric Patients in North America: Analysis of the Virtual Pediatric Systems Data. PLoS One 2022; 17(4): e0266737.
16- Erdogan O, Ok F, Carkci S, Durmus E. Is There an Association between Urine Biochemical Parameters on Admission and the Severity of COVID-19? Int J Clin Pract 2021; 75(11): e14809.
17- Shafigh A, Mohammadi-Garebagh A, Shahsavarinia K, Tayebi S, Mostafaei A, Salehi-Pourmehr H, et al. A Systematic Review on the Correlation between COVID-19 and Lower Urinary Tract Symptoms. Journal of Clinical Virology Plus 2025; 5(1): 100202.
18- Marcellino A, Bloise S, Pirone C, Brandino G, Barberi A, Del Giudice E, et al. Increased Measured GFR and Proteinuria in Children with Previous Infection by SARS-Cov-2: Should We Be Concerned? Microorganisms 2025; 13(5): 1008.
19- Brigadoi G, Tirelli F, Rossin S, Casotto V, Riello F, Gallinaro G, et al. Severe And Invasive Bacterial Infections in Infants Aged Less than 90 Days with and Without SARS-Cov-2 Infection. Ital J Pediatr 2024; 50(1): 148.
20- Mendez DR, Paul K, Richardson J, Jehle D. Risk of Urinary Tract Infection and Bacteremia in Infants Infected with COVID-19. Pediatr Emerg Care 2025; 41(3): 226-9.
21- Saygili S, Canpolat N, Cicek RY, Agbas A, Yilmaz EK, Sakalli AAK, et al. Clinical and Subclinical Acute Kidney Injury in Children with Mild-To-Moderate COVID-19. Pediatr Res 2023; 93(3): 654-60.
22- Martin SM, Meni Battaglia L, Ferraris J, Ramírez F, Coccia P, García Chervo L, et al. Prevalence of Renal Involvement among Pediatric Patients Hospitalized Due to Coronavirus Disease 2019: A Multicenter Study. Arch Argent Pediatr 2022; 120(5): 310-6.
23- Ağbaş A, Akkoç G, Kızılırmak C, Çalışkan Dolu N, Bayramoğlu E, Elevli M. Kidney Involvement in Pediatric COVID-19 Cases: A Single-Center Experience. Turk Arch Pediatr 2022; 57(5): 558-62.
متن کامل: (30 مشاهده)
مقدمه
در اوایل دی ماه سال 1398، نوع جدیدی از پنومونی ناشی از کرونا ویروس از شهر ووهان چین گزارش گردید. وزارت بهداشت چین این بیماری را جزء بیماریهای واجد قرنطینه قرار داد و اقدامات پیشگیرانه و کنترلی سختگیرانه را برای این بیماری عفونی اتخاذ نمود. در ایران، اولین موارد ابتلا به بیماری COVID-19 از شهر قم گزارش گردید و 15 روز پس از آن، موارد ابتلا از 31 استان کشور گزارش شد. ویروس کووید-19 با اتصال به آنزیم تبدیل کننده آنژیوتانسین (ACE2) II وارد سلولها میشود و برخلاف سایر سویههای کروناویروس، تکثیر اولیه آن فقط در اپیتلیوم مخاط تنفسی فوقانی روی نمیدهد (1). محققان دریافتهاند که گیرنده های ACE2 علاوه بر مخاط بینی، برونش، ریه، قلب، مری، معده، ایلئوم درکلیه و مثانه نیز بیان میشوند (2). بیشترین علائم گزارش شده سرفه، تب، تنگینفس و گلودرد بود که البته فقدان حس بویایی و حس شامه از اهمیت بیشتری در تشخیص این بیماری برخوردارند (3). در مطالعات مشاهدهای که قبل از ظهور واریانتهای مسریتر انجام شد میزان ابتلای ثانویه در بین کودکان (زیر 18 سال) بین 4 تا 57 درصد متغیر بود (8-4). در یک متاآنالیز از 87 مطالعه درباره انتقال خانگی که شامل 1،249،163تماس خانگی از چندین کشور بود، میزان ابتلا ثانویه در میان کودکان 18 درصد و در میان بزرگسالان 30درصد بود (9). مطالعات میزانهای مختلفی از انتقال ویروس توسط کودکان را در تماسهای خانگی ذکر کردهاند. این نرخهای متغیر ممکن است به دلیل تفاوت در شیوع بیماری و اقدامات پیشگیرانه مختلف در آن جوامع، روشهای تشخیص مختلف، زمانبندی نمونهگیری، واریانتهای مختلف و سطح رعایت اقدامات کنترل عفونت در خانه باشد. این شرایط ممکن است زمانیکه بیمار اولیه یک کودک باشد؛ چالش برانگیز شود (13-10). ریهها شایعترین عضوی هستند که توسط ویروس کرونا درگیر میشوند، اما اختلالات کلیوی نیز مکررا گزارش میشوند (14). میزان ابتلای کودکان به آسیب حاد کلیوی Acute kidney injury AKI در مطالعات مختلف بسته به حجم نمونه مطالعه، تعریف آن و منطقه جغرافیایی مطالعه انجام شده از کمتر از یک درصد تا 7% متغیر بوده است. در یک مطالعه با حجم نمونه با 2546 کودک مبتلا به کووید19 و بستری شده در ICU 10/8% از آنها دچار درجاتی از AKI شدهاند. که در میان آنها 62/8%. مبتلا به استیج یک،14/6% استیج دو و 22/6% در استیج سه بیماری بودند (15). عفونت با SARS-CoV-2 نهتنها میتواند باعث آسیب کلیوی جدید شود، بلکه دشواری درمان و مراقبت بیماری، و نرخ مرگ و میر افراد مبتلا به بیماریهای کلیوی را نیز افزایش میدهد (14). درگیری کلیه در عفونت SARS-CoV-2 عمدتاً بهصورت آسیب لولههای کلیه ظاهر میشود. پروتئینوری علامت بالینی اصلی است (16). برای کاهش صدمات وارده بر بیماران، باید به عوارض کلیوی در تشخیص و درمان بیماری کروناویروس توجه بیشتری شود (14). بنابراین با توجه به موارد ذکر شده ما بر آن شدیم که با طراحی مطالعهای ارزیابی آزمایشات ادراری در کودکان مبتلا به کووید-19 بستری در بیمارستان اکبر مشهد طی بازه زمانی 1401-1400 بپردازیم.
روش بررسی
مطالعه حاضر در سال 1401 در بیمارستان اکبر در مشهد به صورت مقطعی طراحی گردید. این مطالعه بهصورت تمام شماری کودکان زیر 18 سال مبتلا به کووید-19 با تشخیص قطعی ابتلا (تست PCR مثبت) بود که در بازه زمانی فروردین ماه 1400 تا اسفند ماه 1401 در بیمارستان اکبر مشهد بستری شدند. ابزار مورد استفاده در مطالعه چک لیستهای از پیش تهیه شدهای برای ثبت اطلاعات بیماران بود. آزمودنیها کودکان زیر 18 سال مبتلا به کووید-19 با تشخیص قطعی ابتلا (تست PCR مثبت) که بازه زمانی فروردین ماه 1400 تا اسفند ماه 1401 در بیمارستان اکبر مشهد بستری بودهاند.
معیار ورود: کودکان زیر 18 سال مبتلا به کووید-19 با تشخیص قطعی ابتلا (تست PCR مثبت) که بازه زمانی فروردین ماه 1400 تا اسفند ماه 1401 در بیمارستان اکبر مشهد بستری بودند.
معیار خروج: اطلاعات ناقص پرونده و عدم تکمیل آن بود. بر اساس چک لیست از پیش طراحی شده محقق، اطلاعات دموگرافیک نظیر سن، جنسیت، بیماریهای زمینهای و کوموربیدیتی، از پرونده بایگانی بیماران ورود یافته به مطالعه و سیستم HIS ثبت شد. همچنین، آزمایشهای ادارای (U/A) انجام شده در طی بستری بیماران در بیمارستان (نظیر وجود پروتئین، اوره، کراتینین، باکتری، نیتریت، کتون، pH، گلوکز، خون، یوروبیلینوژن و وجود گلبولهای قرمز و سفید در ادرار) استخراج و ثبت شدند. آزمایش ادرار بیماران به دو دسته نرمال و غیر نرمال تقسیم شد. معیارهای آزمایش غیر نرمال شامل موارد زیر بودند: WBC بیشتر از 5 در هر HPF، RBC بیشتر از 3 در هر HPF، پروتئینوری، کتونوری و باکتریوری. نظر به اینکه طرح مقطعی و بررسی پرونده بیماران طی سالهای 1400 تا 1401 بود، لذا پژوهشگران اصول محرمانگی و اخلاقی و گمنامسازی دادهها و اطلاعات هویتی در طی مطالعه را بهطور کامل رعایت کردند.
تجزیه و تحلیل آماری
دادهها پس از جمعآوری، وارد نرمافزارversion 16 SPSS شد و تجزیه و تحلیلهای آماری مربوطه انجام گرفت. یافتههای توصیفی با استفاده از شاخصهای پراکندگی و مرکزی مناسب در قالب جداول و نمودارها گزارش شد. برای توصیف دادههای کمی با توزیع نرمال از میانگین و انحراف معیار استفاده شده و برای داده های با توزیع غیر نرمال از میانه و دامنه چارکی استفاده شد. برای توصیف متغیرهای کیفی از فراوانی (درصد) استفاده شد. برای مقایسه متغیرهای کمی بین دو گروه (بر اساس U/A نرمال و غیرنرمال) از Independent samples t-test یا معادل غیرپارامتریک آن (Mann-Whitney) استفاده شد. به منظور مقایسه متغیرهای کیفی از آزمون Chi-square یا Fisher's exact test استفاده شد. سطح معناداری در تمامی محاسبات کمتر از 0/05 در نظر گرفته شد.
نتایج
در این پژوهش، 199 فرد شرکت کردند که شامل 89 نفر زن (44/7%) و 110 نفر مرد (55/3%) بودند. توزیع جنسیتی نشاندهنده تعادل نسبی بین دو گروه جنسیتی است. میانگین سنی شرکتکنندگان 4/80 سال با انحراف استاندارد 5/16 سال بود. نتایج حاصل از بررسی رنگ و ظاهر ادرار نشان داد که بیشترین فراوانی مربوط به ادرار زرد با ۱۸۱ مورد (91/4٪) بود. سایر رنگهای مشاهدهشده شامل بیرنگ (۵ مورد، 2/5٪)، قهوهای (۳ مورد، 1/5٪)، قرمز (۱ مورد، 0/5٪)، زرد روشن (۴ مورد، 2٪)، زرد تیره (۱ مورد، 0/5٪)، نارنجی (۱ مورد، 0/5٪) و خونآلود (۲ مورد، 0/1٪) بودند. این نتایج نشان میدهند که اکثریت نمونهها دارای رنگ زرد طبیعی بودهاند، اگرچه مواردی از رنگهای غیرطبیعی نیز مشاهده شده است. در خصوص ظاهر ادرار، 166 مورد (83/4%) از نمونهها شفاف گزارش شدند و 27 نمونه (13/6%) نیمه شفاف بودند. تنها 5 مورد (2/5%) از نمونهها بهصورت کدر مشاهده شدند و یک مورد (0/5%) نیمه کدر بود. در بررسی میزان پروتئین ادرار، ۱۵۹ مورد (80/3٪) فاقد پروتئین بودند. در ۱۶ مورد (8/1٪) پروتئین + مشاهده شد. همچنین، ۹ مورد (4/5٪) پروتئین 2+، ۲ مورد (1/0٪) پروتئین 3+ و ۲ مورد (1/0٪) پروتئین 4+ گزارش شد. در ۱۰ نمونه (5/1٪) پروتئین در حد trace وجود داشت. این نتایج حاکی از آن است که اکثریت نمونهها بدون پروتئین یا با مقادیر کمی پروتئین بودهاند. در بررسی گلوکز ادرار، ۱۶۹ مورد (85/4٪) فاقد گلوکز بودند. در ۱۶ مورد (8/1 %) گلوکز +، در ۳ مورد (1/5٪)گلوکز 2+، در ۴ مورد (2/0٪) گلوکز 3+ و در ۲ مورد (1/0٪) گلوکز 4+ گزارش شد. همچنین، ۴ نمونه (2/0٪) دارای گلوکز در حد trace بودند. شمارش گلبولهای سفید در ادرار بهطور میانگین 4/56 ± 59/3 در هر HPF، وزن مخصوص ادرار نیز با میانگین8/74± 1014/62، PH با میانگین 1 ± 5/91 و شمارش سلولهای اپیتلیال نیز با میانگین 2/58± 3/16 بود. آزمایشهای شیمیایی نشان داد که تمامی نمونههای مورد بررسی (199 مورد) از نظر وجود نیتریت و گلبولهای سفید در ادرار منفی بودند، که این موضوع نشاندهنده عدم وجود پیوری در نمونههای ادرار است. همچنین، هموگلوبین در 3 مورد (1/5%) از نمونهها مثبت گزارش شد، در حالیکه 195 مورد (98/5%) منفی بودند. از نظر وجود خون در ادرار، 152 مورد (76/8%) از نمونهها فاقد خون بودند. با اینحال، 15 مورد (7/6%) دارای خون +، 5 مورد (2/5%) خون 2+، 6 مورد (3%) خون 3+ و 4 مورد (2/0%) خون 4+ گزارش شدند. همچنین، 16 مورد (8/1%) دارای trace خون بودند که نشاندهنده وجود مقادیر کمی از خون در ادرار بود. مخمر در 5 مورد (2/5%) به صورت few و در 1 مورد (0/5%) به صورت rare گزارش شد. همچنین، 167 مورد (83/9%) فاقد گلبولهای سفید غیرطبیعی بودند و در 32 مورد (16/1%) این گلبولها مثبت بودند. گلبولهای قرمز غیرطبیعی نیز در 165 مورد (82/9%) منفی و در 34 مورد (17/1%) مثبت گزارش شدند. بررسی بیماریهای زمینهای نشان داد که از مجموع 199 فرد، 12 نفر (6%) مبتلا به صرع بودند و 37 نفر (18/6%) سابقه پنومونی داشتند. همچنین، 2 نفر (1%) مبتلا به بیماری MCD و 1 نفر (0/5%) دارای کیست کلیه بودند. در میان نمونهها، 11 نفر (5/5%) مبتلا به CP بودند. انسفالوپاتی کبد در 3 نفر (1/5%)، کتواسیدوز دیابتی در 6 نفر (3%)، و دیابت در 7 نفر (3/5%) از افراد مشاهده شد. علاوه بر این، 4 نفر (2/0%) دارای سندرم داون و 3 نفر (1/5%) مبتلا به هایپوتیروئیدی بودند. در نهایت، نارسایی کلیه در 2 نفر (1%) مشاهده شد که نشاندهنده شیوع پایین این بیماریها در بین نمونهها است.
نتایج آزمونهای آماری نشان داد که هیچ ارتباط معناداری بین جنسیت و وضعیت گروه UA (نرمال و غیرنرمال) (p =0/373)و همچنین تفاوت سنی معناداری بین دو گروه (p =0/431) وجود نداشت. جدول 2 ارتباط بین یافته های آزمایش ادرار با نرمال بودن یا نبودن آزمایش ادرار را بررسی میکند. همان طور که مشاهده می شود تفاوت معناداری در رنگ (p =0/029)، ظاهر (p<0/001)، مقدار پروتئین(p =0/004)، خون (p<0/001)، باکتری (p =0/002)، موکوس (p =0/037)، (p =0/038)pH و سلول اپیتلیال (p<0/001) بین دو گروه وجود داشت.
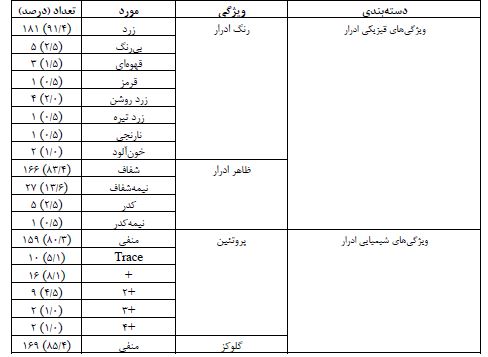
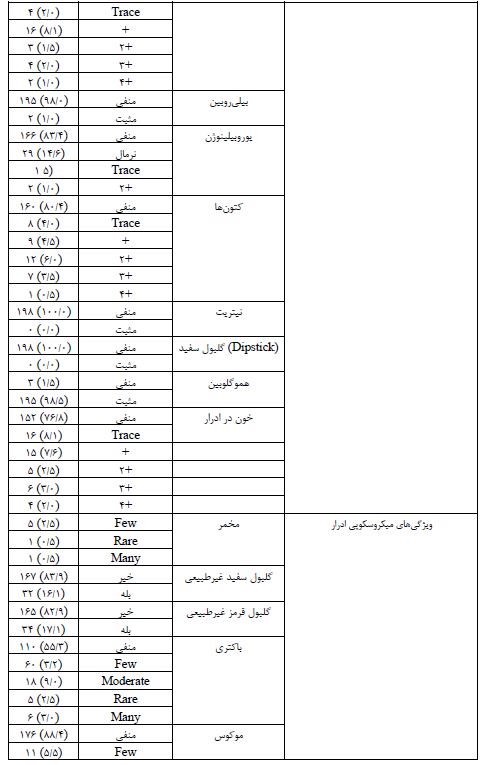
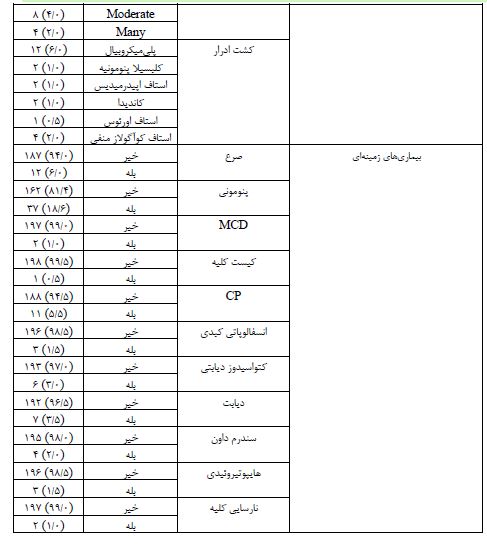
جدول1: ویژگیهای فیزیکی، شیمیایی، میکروسکوپی ادرار و بیماریهای زمینهای
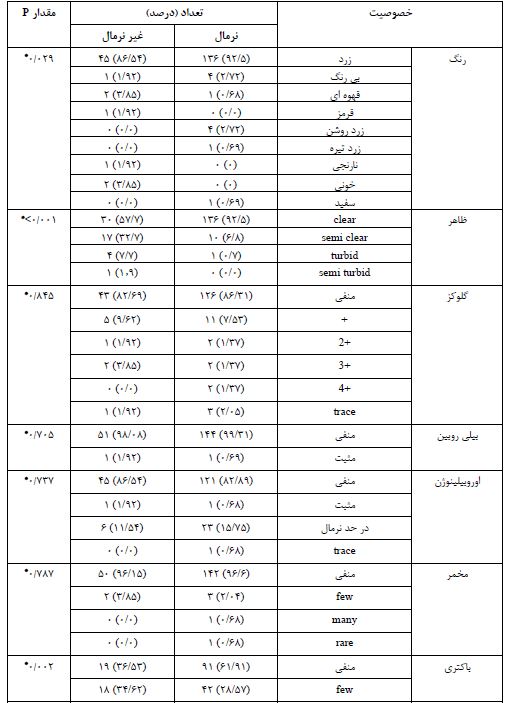
جدول 2: ارتباط بین یافتههای آزمایش ادرار و گروه UA (نرمال و غیرنرمال)
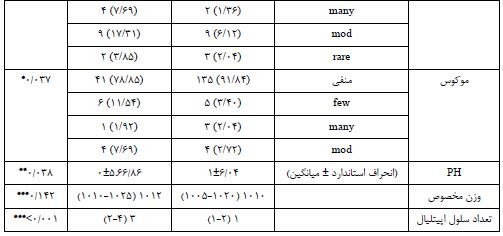
تست دقیق فیشر ** تست T مستقل *** تست من ویتنی
در بررسی کشت های ادرار گرفته شده از بیماران نتایج زیر بهدست آمد: دو مورد کلبسیلا پنومونیه گزارش شدند که برای یکی از آنها آنتیبیوگرام گزارش نشده بود (کلونی کانت 2000) و یک مورد باقیمانده به نیتروفورانتوئین حساس بود اما نسبت به آمیکاسین و سغتریاکسون مقاومت نسبی داشت و نسبت به تازوباکتام، آمپی سیلین، سفیکسیم، سفتازیدیم، کوتریموکسازول و پیپراسیلین مقاوم بود. دو مورد استافیلوکوک اپیدرمیدیس گزارش شدند که آنتیبیوگرام آنها گزارش نشده بود. یک مورد استافیلوکوک اورئوس گزارش شد که به لینزولاید و ونکومایسین حساس بود اما به نسبت به سفوکستین مقاومت نسبی داشت و به آزیترومایسین، اریترومایسین و کوتریموکسازول مقاوم بود. چهارمورد استافیلوکوک کوآگولاز منفی گزارش شدند که از این بین برای یک مورد آنتیبیوگرام گزارش نشده بود (کلونی کانت 2000). از سه مورد باقیمانده هر سه ایزوله به نیتروفورانتوئین و پیپراسیلین-تازوباکتام، دو ایزوله به آمیکاسین، سفوتاکسیم و سفیکسیم حساس بودند و یک ایزوله به کوتریموکسازول نیز حساس بود. هر سه ایزوله به آمپیسیلین مقاوم بودند، دو ایزوله به کوتریموکسازول مقاوم بودند و یک ایزوله نیز به سفتازیدیم، سفیکسیم، سفوتاکسیم مقاوم بود. دو مورد کاندیدا گزارش شدند. دوازده مورد از کشتها پلی میکروبیال بودند.
بحث
در این مطالعه، نتایج آزمایشات ادراری کودکان مبتلا به کووید-19 بستری در بیمارستان اکبر مشهد طی بازه زمانی 1400 تا 1401 مورد بررسی قرار گرفت. از 199 بیمار، بیشتر نمونههای ادراری بدون نیتریت و گلبولهای سفید بودند که نشاندهنده عدم وجود پیوری است. همچنین، در اکثریت موارد (91%) رنگ ادرار زرد طبیعی گزارش شد و ظاهر آن عمدتاً شفاف بود. همچنین، بررسی سایر شاخصهای ادراری مانند وجود پروتئین، گلوکز، بیلیروبین و کتونها نشان داد که در درصد بالایی از بیماران، این شاخصها در محدوده طبیعی قرار داشتند. ارتباط معناداری بین جنسیت و وضعیت UA (نرمال و غیرنرمال) مشاهده نشد. در مطالعه ما بر روی کودکان مبتلا به کووید-19، نتایج آزمایشات ادراری نشان داد که تعدادی از این بیماران تغییرات غیرطبیعی نظیر پروتئینوری و هماچوری داشتند. این نتایج میتواند به عنوان نشانگری از آسیب کلیوی زودرس در کودکان مبتلا به کووید-19 در نظر گرفته شود. اگرچه در بسیاری از کودکان آسیبهای کلیوی جدی مشاهده نشد، اما تغییرات ادراری وجود داشت. تحلیل مطالعات واجد شرایط در یک مرور سیستماتیک نشان داد که شیوع کلی علائم دستگاه ادراری تحتانی در بیماران مبتلا به کووید-۱۹ برابر با 3/3% بود ( با فاصله اطمینان 95%: 0/2% تا 3/5% مقدار Q: 1021.397، و I²: 97/45%). همچنین، تکرر ادرار و فوریت در ادرار شایعترین علائم در مطالعات وارد شده به متاآنالیز بودند؛ به ترتیب با شیوع 15/3% (فاصله اطمینان 95%: 7/5% – 9/34% در ۴ مطالعه) و 5/11% (فاصله اطمینان 95%: 7/1% – 1/18% در ۲ مطالعه) (17). یافتههای پژوهش Marcellino و همکاران نشان داد که ویروس SARS-CoV-2 میتواند در درصد قابلتوجهی از کودکان منجر به آسیب کلیوی شود که با هایپرفیلتراسیون، پروتئینوری و هماچوری مشخص میشود، و این موضوع نیاز به پیگیری دقیق این بیماران را ضروری میسازد (18). مطالعات دیگر نیز به بررسی تأثیر کووید-19 بر عملکرد کلیهها در کودکان پرداختهاند. در مقالهای که توسط Brigadoi و همکاران انجام شد، نتایج نشان داد که خطر عفونتهای جدی باکتریایی (SBI) در نوزادان مبتلا به کووید-19 نسبت به نوزادان بدون کووید-19 کمتر بوده است. این تحقیق نشان داد که نوزادان مبتلا به کووید-19 کمتر در معرض عفونتهای ادراری نظیر عفونت مجاری ادراری (UTI) قرار داشتند (19). همچنین در مطالعه Mendez و همکاران، نوزادانی که تست آنها برای کووید-۱۹ مثبت بود، در معرض خطر کمتری برای ابتلا به عفونت ادراری (UTI) و باکتریمی قرار داشتند. خطر ابتلا به عفونت ادراری در نوزادان مبتلا به کووید-۱۹ بهطور معناداری کمتر بود (20). در مطالعه ما که فقط بررسی در مورد کودکان مبتلا به کووید بوده است، اکثر کودکان فاقد عفونتهای ادراری جدی بودند و موارد نارسایی کلیوی شدید کمتر مشاهده شد. از سوی دیگر، مقاله Saygili و همکاران به بررسی کودکان مبتلا به کووید-19 با آسیب حاد کلیوی پرداخته است. این مطالعه نشان داد که حدود 16/9% از کودکان مورد بررسی دچار AKI شدهاند و در 31% از آنها AKI تحت بالینی مشاهده شد. این تحقیق همچنین تأکید کرد که استفاده از بیومارکرهای ادراری نظیر NGAL و KIM-1 میتواند به تشخیص زودهنگام AKI در کودکان کمک کند (21). یافتههای ما نیز نشان داد که اگرچه میزان شیوع AKI در مطالعه ما پایینتر بود، اما وجود تغییرات ادراری مشابه نشان میدهد که استفاده از بیومارکرها میتواند به شناسایی کودکان در معرض خطر کمک کند. در مقاله سرخی و همکاران که در سال 2022 انجام شد، محققان نشان دادند که 66% از کودکان مبتلا به کووید-19 کاهش نرخ فیلتراسیون گلومرولی داشتند و در برخی موارد این کاهش به حدی شدید بود که نیاز به درمان همودیالیز ایجاد شد (14). این یافتهها مشابه با نتایج مطالعه ما بود که در آن تغییرات در سطح پروتئین و هماچوری به عنوان نشانگرهای آسیب کلیوی در کودکان مشاهده شد. اگرچه در مطالعه ما هیچ موردی از نیاز به همودیالیز گزارش نشد، اما نتایج مشابهی در خصوص آسیب کلیوی زودرس وجود داشت. مقاله مارتین و همکاران نیز به بررسی شیوع پروتئینوری و هماچوری در کودکان مبتلا به کووید-19 پرداخته است. این مطالعه نشان داد که پروتئینوری در 16% از کودکان و هماچوری در 13/2% از آنها مشاهده شده است (22). یافتههای ما نیز نشاندهنده میزان نسبتاً مشابهی از پروتئینوری و هماچوری در کودکان مبتلا به کووید-19 بود. این نتایج نشان میدهد که حتی در موارد خفیفتر کووید-19، ممکن است تغییرات ادراری به عنوان نشانگرهای آسیب کلیوی وجود داشته باشد. در مجموع، مقایسه این مطالعات با نتایج ما نشان میدهد که تغییرات در نتایج آزمایشات ادراری میتواند به عنوان یک ابزار تشخیصی مهم برای ارزیابی آسیبهای کلیوی در کودکان مبتلا به کووید-19 مورد استفاده قرار گیرد. اگرچه میزان آسیب کلیوی جدی در کودکان کمتر از بزرگسالان است، اما این تغییرات بهویژه در کودکان بستری شده نشاندهنده خطر بالقوه آسیبهای کلیوی است که نیاز به پیگیری دقیقتر دارد. در مطالعه ما، یکی از نکات برجسته، مشاهده تغییرات ادراری در کودکان مبتلا به کووید-19 بود. این تغییرات میتواند ناشی از تأثیر مستقیم ویروس بر کلیهها باشد. شواهد موجود نشان میدهد که ویروس SARS-CoV-2 میتواند بهطور مستقیم به سلولهای کلیوی حمله کرده و موجب التهاب و آسیب به لولههای کلیوی شود. این یافته با نتایج مطالعات دیگر که به بررسی آسیبهای کلیوی در بیماران کووید-19 پرداختهاند، همخوانی دارد. در مقاله Saygili و همکاران، محققان به نقش نوتروفیلها در ایجاد آسیب کلیوی پرداختهاند و نشان دادهاند که افزایش تعداد نوتروفیلها در کودکان مبتلا به کووید-19 میتواند به عنوان نشانگری برای تشخیص آسیب کلیوی عمل کند (21). نکته دیگر، اهمیت پیگیری طولانیمدت کودکان مبتلا به کووید-19 بهویژه در زمینه عملکرد کلیوی است. شواهد نشان میدهد که حتی در موارد خفیف کووید-19، ممکن است تغییرات کلیوی بهطور طولانیمدت ادامه داشته باشد. در مقاله دیگری، اشاره شده است که تغییرات کلیوی نظیر پروتئینوری و هماچوری میتواند نشانگرهایی از آسیب طولانیمدت به کلیهها در بیماران کووید-19 باشد (23). این موضوع تأکید میکند که حتی پس از بهبودی کودکان، پیگیری و ارزیابی عملکرد کلیوی آنها ضروری است. در نهایت، یکی از نکات قابلتوجه دیگر در مطالعه ما، ارتباط بین عوارض ادراری و شدت بیماری در کودکان مبتلا به کووید-19 بود. هرچند که در مطالعه ما، بیشتر کودکان علائم خفیف تا متوسط داشتند، اما در مواردیکه تغییرات در آزمایشات ادراری مشاهده شد، احتمال افزایش عوارض کلیوی و نیاز به مداخلات بیشتر وجود داشت. این موضوع در مطالعات دیگر نیز تأیید شده است، بهویژه در کودکانی که دچار علائم شدیدتر کووید-19 شدهاند (14). در نتیجه، ارزیابی دقیق و بهموقع تغییرات ادراری میتواند به بهبود درمان و پیشگیری از عوارض جدی کمک کند. یافتههای این مطالعه میتواند به پزشکان و متخصصان اطفال کمک کند تا الگوهای آزمایشات ادراری در کودکان مبتلا به کووید-19 را بهتر درک کرده و در تشخیص و مدیریت این بیماری در بیماران بستری، بهویژه از لحاظ تشخیص عفونتهای ادراری و مشکلات کلیوی احتمالی، تصمیمات بهتری بگیرند. این اطلاعات به کاهش نگرانیها در رابطه با عوارض کلیوی ناشی از کووید-19 در کودکان کمک میکند و میتواند در مدیریت درمان بالینی مؤثر واقع شود. یکی از نقاط قوت این مطالعه، طراحی مقطعی و استفاده از دادههای واقعی بیماران بستری بوده که امکان بررسی دقیق وضعیت این بیماران را فراهم کرده است. همچنین، استفاده از چکلیستهای استاندارد برای ثبت اطلاعات، دقت و صحت دادهها را تضمین کرده است. از جمله محدودیتهای این مطالعه میتوان به طراحی مقطعی آن اشاره کرد که امکان بررسی روابط علّی بین عفونت کووید-۱۹ و تغییرات مشاهدهشده در شاخصهای ادراری را محدود میسازد. همچنین، نبود گروه کنترل از میان کودکان سالم یا مبتلا به سایر عفونتها مانع از مقایسه دقیق و تعیین اختصاصی بودن یافتهها برای کووید-۱۹ میشود. اتکا به دادههای ثبتشده در پروندههای پزشکی و سیستم HIS بیمارستان نیز ممکن است با خطای ثبت یا ناقص بودن اطلاعات همراه بوده باشد. علاوه بر این، در این مطالعه اطلاعاتی در مورد شدت بیماری، سابقه اختلالات کلیوی، یا نوع درمان دریافتی بیماران ذکر نشده است، که میتوانست بر نتایج آزمایشات ادراری تأثیرگذار باشد. نکته دیگر، نبود پیگیری طولی بیماران پس از ترخیص است که امکان بررسی سیر تغییرات در شاخصهای ادراری را در طول زمان محدود کرده است. در نهایت، انجام مطالعه در یک مرکز درمانی خاص (بیمارستان اکبر مشهد) باعث میشود تعمیمپذیری نتایج به سایر جمعیتهای کودکان با احتیاط بیشتری صورت گیرد.
نتیجهگیری
نتایج این مطالعه نشان داد که در کودکان مبتلا به کووید-19 بستری، عوارض کلیوی و نتایج غیرطبیعی آزمایشات ادراری چندان شایع نبوده و اکثر بیماران از نظر پارامترهای اصلی ادراری در وضعیت نرمال قرار داشتند. همچنین، هیچ ارتباط معناداری بین جنسیت و وضعیت UA مشاهده نشد، که این یافته میتواند در مدیریت درمانی و تصمیمگیریهای بالینی موثر باشد.
سپاسگزاری
این مقاله منتج از پایاننامه است و از واحد توسعه تحقیقات بالینی که در انجام این پژوهش مرا یاری رساندند، کمال تشکر را دارم.
حامی مالی: معاونت پژوهش و فناوری دانشگاه علوم پزشکی مشهد.
تعارض در منافع: وجود ندارد.
ملاحظات اخلاقی
پروپوزال این تحقیق توسط دانشگاه علوم پزشکی مشهد تایید شده است (کد اخلاق IR.MUMS.REC.1401.367).
مشارکت نویسندگان
مهلا زهراییفر، ژیلا شیخی و علی خاکشور در ارائه ایده، منا کبیری و طاهره صادقی در طراحی مطالعه، مهلا زهراییفر و ژیلا شیخی در جمعآوری دادهها، طاهره صادقی و پریسا شجاعی در تجزیه و تحلیل دادهها مشارکت داشته و همه نویسندگان در تدوین، ویرایش اولیه و نهایی مقاله و پاسخگویی به سوالات مرتبط با مقاله سهیم هستند.
در اوایل دی ماه سال 1398، نوع جدیدی از پنومونی ناشی از کرونا ویروس از شهر ووهان چین گزارش گردید. وزارت بهداشت چین این بیماری را جزء بیماریهای واجد قرنطینه قرار داد و اقدامات پیشگیرانه و کنترلی سختگیرانه را برای این بیماری عفونی اتخاذ نمود. در ایران، اولین موارد ابتلا به بیماری COVID-19 از شهر قم گزارش گردید و 15 روز پس از آن، موارد ابتلا از 31 استان کشور گزارش شد. ویروس کووید-19 با اتصال به آنزیم تبدیل کننده آنژیوتانسین (ACE2) II وارد سلولها میشود و برخلاف سایر سویههای کروناویروس، تکثیر اولیه آن فقط در اپیتلیوم مخاط تنفسی فوقانی روی نمیدهد (1). محققان دریافتهاند که گیرنده های ACE2 علاوه بر مخاط بینی، برونش، ریه، قلب، مری، معده، ایلئوم درکلیه و مثانه نیز بیان میشوند (2). بیشترین علائم گزارش شده سرفه، تب، تنگینفس و گلودرد بود که البته فقدان حس بویایی و حس شامه از اهمیت بیشتری در تشخیص این بیماری برخوردارند (3). در مطالعات مشاهدهای که قبل از ظهور واریانتهای مسریتر انجام شد میزان ابتلای ثانویه در بین کودکان (زیر 18 سال) بین 4 تا 57 درصد متغیر بود (8-4). در یک متاآنالیز از 87 مطالعه درباره انتقال خانگی که شامل 1،249،163تماس خانگی از چندین کشور بود، میزان ابتلا ثانویه در میان کودکان 18 درصد و در میان بزرگسالان 30درصد بود (9). مطالعات میزانهای مختلفی از انتقال ویروس توسط کودکان را در تماسهای خانگی ذکر کردهاند. این نرخهای متغیر ممکن است به دلیل تفاوت در شیوع بیماری و اقدامات پیشگیرانه مختلف در آن جوامع، روشهای تشخیص مختلف، زمانبندی نمونهگیری، واریانتهای مختلف و سطح رعایت اقدامات کنترل عفونت در خانه باشد. این شرایط ممکن است زمانیکه بیمار اولیه یک کودک باشد؛ چالش برانگیز شود (13-10). ریهها شایعترین عضوی هستند که توسط ویروس کرونا درگیر میشوند، اما اختلالات کلیوی نیز مکررا گزارش میشوند (14). میزان ابتلای کودکان به آسیب حاد کلیوی Acute kidney injury AKI در مطالعات مختلف بسته به حجم نمونه مطالعه، تعریف آن و منطقه جغرافیایی مطالعه انجام شده از کمتر از یک درصد تا 7% متغیر بوده است. در یک مطالعه با حجم نمونه با 2546 کودک مبتلا به کووید19 و بستری شده در ICU 10/8% از آنها دچار درجاتی از AKI شدهاند. که در میان آنها 62/8%. مبتلا به استیج یک،14/6% استیج دو و 22/6% در استیج سه بیماری بودند (15). عفونت با SARS-CoV-2 نهتنها میتواند باعث آسیب کلیوی جدید شود، بلکه دشواری درمان و مراقبت بیماری، و نرخ مرگ و میر افراد مبتلا به بیماریهای کلیوی را نیز افزایش میدهد (14). درگیری کلیه در عفونت SARS-CoV-2 عمدتاً بهصورت آسیب لولههای کلیه ظاهر میشود. پروتئینوری علامت بالینی اصلی است (16). برای کاهش صدمات وارده بر بیماران، باید به عوارض کلیوی در تشخیص و درمان بیماری کروناویروس توجه بیشتری شود (14). بنابراین با توجه به موارد ذکر شده ما بر آن شدیم که با طراحی مطالعهای ارزیابی آزمایشات ادراری در کودکان مبتلا به کووید-19 بستری در بیمارستان اکبر مشهد طی بازه زمانی 1401-1400 بپردازیم.
روش بررسی
مطالعه حاضر در سال 1401 در بیمارستان اکبر در مشهد به صورت مقطعی طراحی گردید. این مطالعه بهصورت تمام شماری کودکان زیر 18 سال مبتلا به کووید-19 با تشخیص قطعی ابتلا (تست PCR مثبت) بود که در بازه زمانی فروردین ماه 1400 تا اسفند ماه 1401 در بیمارستان اکبر مشهد بستری شدند. ابزار مورد استفاده در مطالعه چک لیستهای از پیش تهیه شدهای برای ثبت اطلاعات بیماران بود. آزمودنیها کودکان زیر 18 سال مبتلا به کووید-19 با تشخیص قطعی ابتلا (تست PCR مثبت) که بازه زمانی فروردین ماه 1400 تا اسفند ماه 1401 در بیمارستان اکبر مشهد بستری بودهاند.
معیار ورود: کودکان زیر 18 سال مبتلا به کووید-19 با تشخیص قطعی ابتلا (تست PCR مثبت) که بازه زمانی فروردین ماه 1400 تا اسفند ماه 1401 در بیمارستان اکبر مشهد بستری بودند.
معیار خروج: اطلاعات ناقص پرونده و عدم تکمیل آن بود. بر اساس چک لیست از پیش طراحی شده محقق، اطلاعات دموگرافیک نظیر سن، جنسیت، بیماریهای زمینهای و کوموربیدیتی، از پرونده بایگانی بیماران ورود یافته به مطالعه و سیستم HIS ثبت شد. همچنین، آزمایشهای ادارای (U/A) انجام شده در طی بستری بیماران در بیمارستان (نظیر وجود پروتئین، اوره، کراتینین، باکتری، نیتریت، کتون، pH، گلوکز، خون، یوروبیلینوژن و وجود گلبولهای قرمز و سفید در ادرار) استخراج و ثبت شدند. آزمایش ادرار بیماران به دو دسته نرمال و غیر نرمال تقسیم شد. معیارهای آزمایش غیر نرمال شامل موارد زیر بودند: WBC بیشتر از 5 در هر HPF، RBC بیشتر از 3 در هر HPF، پروتئینوری، کتونوری و باکتریوری. نظر به اینکه طرح مقطعی و بررسی پرونده بیماران طی سالهای 1400 تا 1401 بود، لذا پژوهشگران اصول محرمانگی و اخلاقی و گمنامسازی دادهها و اطلاعات هویتی در طی مطالعه را بهطور کامل رعایت کردند.
تجزیه و تحلیل آماری
دادهها پس از جمعآوری، وارد نرمافزارversion 16 SPSS شد و تجزیه و تحلیلهای آماری مربوطه انجام گرفت. یافتههای توصیفی با استفاده از شاخصهای پراکندگی و مرکزی مناسب در قالب جداول و نمودارها گزارش شد. برای توصیف دادههای کمی با توزیع نرمال از میانگین و انحراف معیار استفاده شده و برای داده های با توزیع غیر نرمال از میانه و دامنه چارکی استفاده شد. برای توصیف متغیرهای کیفی از فراوانی (درصد) استفاده شد. برای مقایسه متغیرهای کمی بین دو گروه (بر اساس U/A نرمال و غیرنرمال) از Independent samples t-test یا معادل غیرپارامتریک آن (Mann-Whitney) استفاده شد. به منظور مقایسه متغیرهای کیفی از آزمون Chi-square یا Fisher's exact test استفاده شد. سطح معناداری در تمامی محاسبات کمتر از 0/05 در نظر گرفته شد.
نتایج
در این پژوهش، 199 فرد شرکت کردند که شامل 89 نفر زن (44/7%) و 110 نفر مرد (55/3%) بودند. توزیع جنسیتی نشاندهنده تعادل نسبی بین دو گروه جنسیتی است. میانگین سنی شرکتکنندگان 4/80 سال با انحراف استاندارد 5/16 سال بود. نتایج حاصل از بررسی رنگ و ظاهر ادرار نشان داد که بیشترین فراوانی مربوط به ادرار زرد با ۱۸۱ مورد (91/4٪) بود. سایر رنگهای مشاهدهشده شامل بیرنگ (۵ مورد، 2/5٪)، قهوهای (۳ مورد، 1/5٪)، قرمز (۱ مورد، 0/5٪)، زرد روشن (۴ مورد، 2٪)، زرد تیره (۱ مورد، 0/5٪)، نارنجی (۱ مورد، 0/5٪) و خونآلود (۲ مورد، 0/1٪) بودند. این نتایج نشان میدهند که اکثریت نمونهها دارای رنگ زرد طبیعی بودهاند، اگرچه مواردی از رنگهای غیرطبیعی نیز مشاهده شده است. در خصوص ظاهر ادرار، 166 مورد (83/4%) از نمونهها شفاف گزارش شدند و 27 نمونه (13/6%) نیمه شفاف بودند. تنها 5 مورد (2/5%) از نمونهها بهصورت کدر مشاهده شدند و یک مورد (0/5%) نیمه کدر بود. در بررسی میزان پروتئین ادرار، ۱۵۹ مورد (80/3٪) فاقد پروتئین بودند. در ۱۶ مورد (8/1٪) پروتئین + مشاهده شد. همچنین، ۹ مورد (4/5٪) پروتئین 2+، ۲ مورد (1/0٪) پروتئین 3+ و ۲ مورد (1/0٪) پروتئین 4+ گزارش شد. در ۱۰ نمونه (5/1٪) پروتئین در حد trace وجود داشت. این نتایج حاکی از آن است که اکثریت نمونهها بدون پروتئین یا با مقادیر کمی پروتئین بودهاند. در بررسی گلوکز ادرار، ۱۶۹ مورد (85/4٪) فاقد گلوکز بودند. در ۱۶ مورد (8/1 %) گلوکز +، در ۳ مورد (1/5٪)گلوکز 2+، در ۴ مورد (2/0٪) گلوکز 3+ و در ۲ مورد (1/0٪) گلوکز 4+ گزارش شد. همچنین، ۴ نمونه (2/0٪) دارای گلوکز در حد trace بودند. شمارش گلبولهای سفید در ادرار بهطور میانگین 4/56 ± 59/3 در هر HPF، وزن مخصوص ادرار نیز با میانگین8/74± 1014/62، PH با میانگین 1 ± 5/91 و شمارش سلولهای اپیتلیال نیز با میانگین 2/58± 3/16 بود. آزمایشهای شیمیایی نشان داد که تمامی نمونههای مورد بررسی (199 مورد) از نظر وجود نیتریت و گلبولهای سفید در ادرار منفی بودند، که این موضوع نشاندهنده عدم وجود پیوری در نمونههای ادرار است. همچنین، هموگلوبین در 3 مورد (1/5%) از نمونهها مثبت گزارش شد، در حالیکه 195 مورد (98/5%) منفی بودند. از نظر وجود خون در ادرار، 152 مورد (76/8%) از نمونهها فاقد خون بودند. با اینحال، 15 مورد (7/6%) دارای خون +، 5 مورد (2/5%) خون 2+، 6 مورد (3%) خون 3+ و 4 مورد (2/0%) خون 4+ گزارش شدند. همچنین، 16 مورد (8/1%) دارای trace خون بودند که نشاندهنده وجود مقادیر کمی از خون در ادرار بود. مخمر در 5 مورد (2/5%) به صورت few و در 1 مورد (0/5%) به صورت rare گزارش شد. همچنین، 167 مورد (83/9%) فاقد گلبولهای سفید غیرطبیعی بودند و در 32 مورد (16/1%) این گلبولها مثبت بودند. گلبولهای قرمز غیرطبیعی نیز در 165 مورد (82/9%) منفی و در 34 مورد (17/1%) مثبت گزارش شدند. بررسی بیماریهای زمینهای نشان داد که از مجموع 199 فرد، 12 نفر (6%) مبتلا به صرع بودند و 37 نفر (18/6%) سابقه پنومونی داشتند. همچنین، 2 نفر (1%) مبتلا به بیماری MCD و 1 نفر (0/5%) دارای کیست کلیه بودند. در میان نمونهها، 11 نفر (5/5%) مبتلا به CP بودند. انسفالوپاتی کبد در 3 نفر (1/5%)، کتواسیدوز دیابتی در 6 نفر (3%)، و دیابت در 7 نفر (3/5%) از افراد مشاهده شد. علاوه بر این، 4 نفر (2/0%) دارای سندرم داون و 3 نفر (1/5%) مبتلا به هایپوتیروئیدی بودند. در نهایت، نارسایی کلیه در 2 نفر (1%) مشاهده شد که نشاندهنده شیوع پایین این بیماریها در بین نمونهها است.
نتایج آزمونهای آماری نشان داد که هیچ ارتباط معناداری بین جنسیت و وضعیت گروه UA (نرمال و غیرنرمال) (p =0/373)و همچنین تفاوت سنی معناداری بین دو گروه (p =0/431) وجود نداشت. جدول 2 ارتباط بین یافته های آزمایش ادرار با نرمال بودن یا نبودن آزمایش ادرار را بررسی میکند. همان طور که مشاهده می شود تفاوت معناداری در رنگ (p =0/029)، ظاهر (p<0/001)، مقدار پروتئین(p =0/004)، خون (p<0/001)، باکتری (p =0/002)، موکوس (p =0/037)، (p =0/038)pH و سلول اپیتلیال (p<0/001) بین دو گروه وجود داشت.
جدول1: ویژگیهای فیزیکی، شیمیایی، میکروسکوپی ادرار و بیماریهای زمینهای



جدول 2: ارتباط بین یافتههای آزمایش ادرار و گروه UA (نرمال و غیرنرمال)


تست دقیق فیشر ** تست T مستقل *** تست من ویتنی
در بررسی کشت های ادرار گرفته شده از بیماران نتایج زیر بهدست آمد: دو مورد کلبسیلا پنومونیه گزارش شدند که برای یکی از آنها آنتیبیوگرام گزارش نشده بود (کلونی کانت 2000) و یک مورد باقیمانده به نیتروفورانتوئین حساس بود اما نسبت به آمیکاسین و سغتریاکسون مقاومت نسبی داشت و نسبت به تازوباکتام، آمپی سیلین، سفیکسیم، سفتازیدیم، کوتریموکسازول و پیپراسیلین مقاوم بود. دو مورد استافیلوکوک اپیدرمیدیس گزارش شدند که آنتیبیوگرام آنها گزارش نشده بود. یک مورد استافیلوکوک اورئوس گزارش شد که به لینزولاید و ونکومایسین حساس بود اما به نسبت به سفوکستین مقاومت نسبی داشت و به آزیترومایسین، اریترومایسین و کوتریموکسازول مقاوم بود. چهارمورد استافیلوکوک کوآگولاز منفی گزارش شدند که از این بین برای یک مورد آنتیبیوگرام گزارش نشده بود (کلونی کانت 2000). از سه مورد باقیمانده هر سه ایزوله به نیتروفورانتوئین و پیپراسیلین-تازوباکتام، دو ایزوله به آمیکاسین، سفوتاکسیم و سفیکسیم حساس بودند و یک ایزوله به کوتریموکسازول نیز حساس بود. هر سه ایزوله به آمپیسیلین مقاوم بودند، دو ایزوله به کوتریموکسازول مقاوم بودند و یک ایزوله نیز به سفتازیدیم، سفیکسیم، سفوتاکسیم مقاوم بود. دو مورد کاندیدا گزارش شدند. دوازده مورد از کشتها پلی میکروبیال بودند.
بحث
در این مطالعه، نتایج آزمایشات ادراری کودکان مبتلا به کووید-19 بستری در بیمارستان اکبر مشهد طی بازه زمانی 1400 تا 1401 مورد بررسی قرار گرفت. از 199 بیمار، بیشتر نمونههای ادراری بدون نیتریت و گلبولهای سفید بودند که نشاندهنده عدم وجود پیوری است. همچنین، در اکثریت موارد (91%) رنگ ادرار زرد طبیعی گزارش شد و ظاهر آن عمدتاً شفاف بود. همچنین، بررسی سایر شاخصهای ادراری مانند وجود پروتئین، گلوکز، بیلیروبین و کتونها نشان داد که در درصد بالایی از بیماران، این شاخصها در محدوده طبیعی قرار داشتند. ارتباط معناداری بین جنسیت و وضعیت UA (نرمال و غیرنرمال) مشاهده نشد. در مطالعه ما بر روی کودکان مبتلا به کووید-19، نتایج آزمایشات ادراری نشان داد که تعدادی از این بیماران تغییرات غیرطبیعی نظیر پروتئینوری و هماچوری داشتند. این نتایج میتواند به عنوان نشانگری از آسیب کلیوی زودرس در کودکان مبتلا به کووید-19 در نظر گرفته شود. اگرچه در بسیاری از کودکان آسیبهای کلیوی جدی مشاهده نشد، اما تغییرات ادراری وجود داشت. تحلیل مطالعات واجد شرایط در یک مرور سیستماتیک نشان داد که شیوع کلی علائم دستگاه ادراری تحتانی در بیماران مبتلا به کووید-۱۹ برابر با 3/3% بود ( با فاصله اطمینان 95%: 0/2% تا 3/5% مقدار Q: 1021.397، و I²: 97/45%). همچنین، تکرر ادرار و فوریت در ادرار شایعترین علائم در مطالعات وارد شده به متاآنالیز بودند؛ به ترتیب با شیوع 15/3% (فاصله اطمینان 95%: 7/5% – 9/34% در ۴ مطالعه) و 5/11% (فاصله اطمینان 95%: 7/1% – 1/18% در ۲ مطالعه) (17). یافتههای پژوهش Marcellino و همکاران نشان داد که ویروس SARS-CoV-2 میتواند در درصد قابلتوجهی از کودکان منجر به آسیب کلیوی شود که با هایپرفیلتراسیون، پروتئینوری و هماچوری مشخص میشود، و این موضوع نیاز به پیگیری دقیق این بیماران را ضروری میسازد (18). مطالعات دیگر نیز به بررسی تأثیر کووید-19 بر عملکرد کلیهها در کودکان پرداختهاند. در مقالهای که توسط Brigadoi و همکاران انجام شد، نتایج نشان داد که خطر عفونتهای جدی باکتریایی (SBI) در نوزادان مبتلا به کووید-19 نسبت به نوزادان بدون کووید-19 کمتر بوده است. این تحقیق نشان داد که نوزادان مبتلا به کووید-19 کمتر در معرض عفونتهای ادراری نظیر عفونت مجاری ادراری (UTI) قرار داشتند (19). همچنین در مطالعه Mendez و همکاران، نوزادانی که تست آنها برای کووید-۱۹ مثبت بود، در معرض خطر کمتری برای ابتلا به عفونت ادراری (UTI) و باکتریمی قرار داشتند. خطر ابتلا به عفونت ادراری در نوزادان مبتلا به کووید-۱۹ بهطور معناداری کمتر بود (20). در مطالعه ما که فقط بررسی در مورد کودکان مبتلا به کووید بوده است، اکثر کودکان فاقد عفونتهای ادراری جدی بودند و موارد نارسایی کلیوی شدید کمتر مشاهده شد. از سوی دیگر، مقاله Saygili و همکاران به بررسی کودکان مبتلا به کووید-19 با آسیب حاد کلیوی پرداخته است. این مطالعه نشان داد که حدود 16/9% از کودکان مورد بررسی دچار AKI شدهاند و در 31% از آنها AKI تحت بالینی مشاهده شد. این تحقیق همچنین تأکید کرد که استفاده از بیومارکرهای ادراری نظیر NGAL و KIM-1 میتواند به تشخیص زودهنگام AKI در کودکان کمک کند (21). یافتههای ما نیز نشان داد که اگرچه میزان شیوع AKI در مطالعه ما پایینتر بود، اما وجود تغییرات ادراری مشابه نشان میدهد که استفاده از بیومارکرها میتواند به شناسایی کودکان در معرض خطر کمک کند. در مقاله سرخی و همکاران که در سال 2022 انجام شد، محققان نشان دادند که 66% از کودکان مبتلا به کووید-19 کاهش نرخ فیلتراسیون گلومرولی داشتند و در برخی موارد این کاهش به حدی شدید بود که نیاز به درمان همودیالیز ایجاد شد (14). این یافتهها مشابه با نتایج مطالعه ما بود که در آن تغییرات در سطح پروتئین و هماچوری به عنوان نشانگرهای آسیب کلیوی در کودکان مشاهده شد. اگرچه در مطالعه ما هیچ موردی از نیاز به همودیالیز گزارش نشد، اما نتایج مشابهی در خصوص آسیب کلیوی زودرس وجود داشت. مقاله مارتین و همکاران نیز به بررسی شیوع پروتئینوری و هماچوری در کودکان مبتلا به کووید-19 پرداخته است. این مطالعه نشان داد که پروتئینوری در 16% از کودکان و هماچوری در 13/2% از آنها مشاهده شده است (22). یافتههای ما نیز نشاندهنده میزان نسبتاً مشابهی از پروتئینوری و هماچوری در کودکان مبتلا به کووید-19 بود. این نتایج نشان میدهد که حتی در موارد خفیفتر کووید-19، ممکن است تغییرات ادراری به عنوان نشانگرهای آسیب کلیوی وجود داشته باشد. در مجموع، مقایسه این مطالعات با نتایج ما نشان میدهد که تغییرات در نتایج آزمایشات ادراری میتواند به عنوان یک ابزار تشخیصی مهم برای ارزیابی آسیبهای کلیوی در کودکان مبتلا به کووید-19 مورد استفاده قرار گیرد. اگرچه میزان آسیب کلیوی جدی در کودکان کمتر از بزرگسالان است، اما این تغییرات بهویژه در کودکان بستری شده نشاندهنده خطر بالقوه آسیبهای کلیوی است که نیاز به پیگیری دقیقتر دارد. در مطالعه ما، یکی از نکات برجسته، مشاهده تغییرات ادراری در کودکان مبتلا به کووید-19 بود. این تغییرات میتواند ناشی از تأثیر مستقیم ویروس بر کلیهها باشد. شواهد موجود نشان میدهد که ویروس SARS-CoV-2 میتواند بهطور مستقیم به سلولهای کلیوی حمله کرده و موجب التهاب و آسیب به لولههای کلیوی شود. این یافته با نتایج مطالعات دیگر که به بررسی آسیبهای کلیوی در بیماران کووید-19 پرداختهاند، همخوانی دارد. در مقاله Saygili و همکاران، محققان به نقش نوتروفیلها در ایجاد آسیب کلیوی پرداختهاند و نشان دادهاند که افزایش تعداد نوتروفیلها در کودکان مبتلا به کووید-19 میتواند به عنوان نشانگری برای تشخیص آسیب کلیوی عمل کند (21). نکته دیگر، اهمیت پیگیری طولانیمدت کودکان مبتلا به کووید-19 بهویژه در زمینه عملکرد کلیوی است. شواهد نشان میدهد که حتی در موارد خفیف کووید-19، ممکن است تغییرات کلیوی بهطور طولانیمدت ادامه داشته باشد. در مقاله دیگری، اشاره شده است که تغییرات کلیوی نظیر پروتئینوری و هماچوری میتواند نشانگرهایی از آسیب طولانیمدت به کلیهها در بیماران کووید-19 باشد (23). این موضوع تأکید میکند که حتی پس از بهبودی کودکان، پیگیری و ارزیابی عملکرد کلیوی آنها ضروری است. در نهایت، یکی از نکات قابلتوجه دیگر در مطالعه ما، ارتباط بین عوارض ادراری و شدت بیماری در کودکان مبتلا به کووید-19 بود. هرچند که در مطالعه ما، بیشتر کودکان علائم خفیف تا متوسط داشتند، اما در مواردیکه تغییرات در آزمایشات ادراری مشاهده شد، احتمال افزایش عوارض کلیوی و نیاز به مداخلات بیشتر وجود داشت. این موضوع در مطالعات دیگر نیز تأیید شده است، بهویژه در کودکانی که دچار علائم شدیدتر کووید-19 شدهاند (14). در نتیجه، ارزیابی دقیق و بهموقع تغییرات ادراری میتواند به بهبود درمان و پیشگیری از عوارض جدی کمک کند. یافتههای این مطالعه میتواند به پزشکان و متخصصان اطفال کمک کند تا الگوهای آزمایشات ادراری در کودکان مبتلا به کووید-19 را بهتر درک کرده و در تشخیص و مدیریت این بیماری در بیماران بستری، بهویژه از لحاظ تشخیص عفونتهای ادراری و مشکلات کلیوی احتمالی، تصمیمات بهتری بگیرند. این اطلاعات به کاهش نگرانیها در رابطه با عوارض کلیوی ناشی از کووید-19 در کودکان کمک میکند و میتواند در مدیریت درمان بالینی مؤثر واقع شود. یکی از نقاط قوت این مطالعه، طراحی مقطعی و استفاده از دادههای واقعی بیماران بستری بوده که امکان بررسی دقیق وضعیت این بیماران را فراهم کرده است. همچنین، استفاده از چکلیستهای استاندارد برای ثبت اطلاعات، دقت و صحت دادهها را تضمین کرده است. از جمله محدودیتهای این مطالعه میتوان به طراحی مقطعی آن اشاره کرد که امکان بررسی روابط علّی بین عفونت کووید-۱۹ و تغییرات مشاهدهشده در شاخصهای ادراری را محدود میسازد. همچنین، نبود گروه کنترل از میان کودکان سالم یا مبتلا به سایر عفونتها مانع از مقایسه دقیق و تعیین اختصاصی بودن یافتهها برای کووید-۱۹ میشود. اتکا به دادههای ثبتشده در پروندههای پزشکی و سیستم HIS بیمارستان نیز ممکن است با خطای ثبت یا ناقص بودن اطلاعات همراه بوده باشد. علاوه بر این، در این مطالعه اطلاعاتی در مورد شدت بیماری، سابقه اختلالات کلیوی، یا نوع درمان دریافتی بیماران ذکر نشده است، که میتوانست بر نتایج آزمایشات ادراری تأثیرگذار باشد. نکته دیگر، نبود پیگیری طولی بیماران پس از ترخیص است که امکان بررسی سیر تغییرات در شاخصهای ادراری را در طول زمان محدود کرده است. در نهایت، انجام مطالعه در یک مرکز درمانی خاص (بیمارستان اکبر مشهد) باعث میشود تعمیمپذیری نتایج به سایر جمعیتهای کودکان با احتیاط بیشتری صورت گیرد.
نتیجهگیری
نتایج این مطالعه نشان داد که در کودکان مبتلا به کووید-19 بستری، عوارض کلیوی و نتایج غیرطبیعی آزمایشات ادراری چندان شایع نبوده و اکثر بیماران از نظر پارامترهای اصلی ادراری در وضعیت نرمال قرار داشتند. همچنین، هیچ ارتباط معناداری بین جنسیت و وضعیت UA مشاهده نشد، که این یافته میتواند در مدیریت درمانی و تصمیمگیریهای بالینی موثر باشد.
سپاسگزاری
این مقاله منتج از پایاننامه است و از واحد توسعه تحقیقات بالینی که در انجام این پژوهش مرا یاری رساندند، کمال تشکر را دارم.
حامی مالی: معاونت پژوهش و فناوری دانشگاه علوم پزشکی مشهد.
تعارض در منافع: وجود ندارد.
ملاحظات اخلاقی
پروپوزال این تحقیق توسط دانشگاه علوم پزشکی مشهد تایید شده است (کد اخلاق IR.MUMS.REC.1401.367).
مشارکت نویسندگان
مهلا زهراییفر، ژیلا شیخی و علی خاکشور در ارائه ایده، منا کبیری و طاهره صادقی در طراحی مطالعه، مهلا زهراییفر و ژیلا شیخی در جمعآوری دادهها، طاهره صادقی و پریسا شجاعی در تجزیه و تحلیل دادهها مشارکت داشته و همه نویسندگان در تدوین، ویرایش اولیه و نهایی مقاله و پاسخگویی به سوالات مرتبط با مقاله سهیم هستند.
References:
1- Karimi J. Epidemiological Review of the Coronavirus Disease 2019 (COVID-19) Pandemic up to 15 March 2020. Journal of Isfahan Medical School 2020; 38(561): 14-23.
2- Ebner B, Volz Y, Mumm J-N, Stief CG, Magistro G. The COVID-19 Pandemic—What Have Urologists Learned? Nat Rev Urol 2022; 19(6): 344-356.
3- Struyf T, Deeks JJ, Dinnes J, Takwoingi Y, Davenport C, Leeflang MM, et al. Signs and Symptoms to Determine If a Patient Presenting in Primary Care or Hospital Outpatient Settings Has COVID‐19. Cochrane Database Syst Rev 2022; 5(5): CD013665.
4- Li W, Zhang B, Lu J, Liu S, Chang Z, Peng C, et al. Characteristics of Household Transmission of COVID-19. Clin Infect Dis 2020; 71(8): 1943-46.
5- Bi Q, Wu Y, Mei S, Ye C, Zou X, Zhang Z, et al. Epidemiology and Transmission of COVID-19 in 391 Cases and 1286 of their Close Contacts in Shenzhen, China: A Retrospective Cohort Study. Lancet Infectious Diseases 2020; 20(8): 911-9.
6- Rosenberg ES, Dufort EM, Blog DS, Hall EW, Hoefer D, Backenson BP, et al. COVID-19 Testing, Epidemic Features, Hospital Outcomes, and Household Prevalence, New York State—March 2020. Clin Infect Dis 2020; 71(8): 1953-9.
7- Laws RL, Chancey RJ, Rabold EM, Chu VT, Lewis NM, Fajans M, et al. Symptoms and transmission of SARS-CoV-2 among children—Utah and Wisconsin, March–May 2020. Pediatrics 2021; 147(1): e2020027268.
8- Grijalva CG. Transmission of SARS-COV-2 Infections in Households—Tennessee and Wisconsin, April–September 2020. MMWR Morbidity and Mortality Weekly Report 2020; 69(44): 1631-4.
9- Madewell ZJ, Yang Y, Longini IM, Halloran ME, Dean NE. Household Secondary Attack Rates of SARS-Cov-2 by Variant and Vaccination Status: An Updated Systematic Review and Meta-Analysis. JAMA Network Open 2022; 5(4): e229317-e.
10- Paul LA, Daneman N, Schwartz KL, Brown KA, Whelan M, Chan E, et al. Association of Age and Pediatric Household Transmission of SARS-Cov-2 Infection. JAMA Pediatr 2021; 175(11): 1151-8.
11- Lee B, Raszka WV. COVID-19 in Children: Looking Forward, Not Back. Pediatrics 2021; 147(1): e2020029736.
12- Coffin SE, Rubin D. Yes, Children Can Transmit COVID, But We Need Not Fear. Pediatrics 2021; 175(11): 1110-2.
13- Chen F, Tian Y, Zhang L, Shi Y. The Role of Children in Household Transmission of COVID-19: A Systematic Review and Meta-Analysis. nt J Infect Dis 2022; 122: 266-75.
14- Sorkhi H, Esmaeili Dooki M, Nikpour M, Mohammadi M, Mohammadpour-Mir A, Kiani M, et al. COVID-19 and Renal Involvement in Children: A Retrospective Study. Caspian J Intern Med 2022; 13(Suppl 3): 193-8.
15- Raina R, Mawby I, Chakraborty R, Sethi SK, Mathur K, Mahesh S, et al. Acute Kidney Injury in COVID-19 Pediatric Patients in North America: Analysis of the Virtual Pediatric Systems Data. PLoS One 2022; 17(4): e0266737.
16- Erdogan O, Ok F, Carkci S, Durmus E. Is There an Association between Urine Biochemical Parameters on Admission and the Severity of COVID-19? Int J Clin Pract 2021; 75(11): e14809.
17- Shafigh A, Mohammadi-Garebagh A, Shahsavarinia K, Tayebi S, Mostafaei A, Salehi-Pourmehr H, et al. A Systematic Review on the Correlation between COVID-19 and Lower Urinary Tract Symptoms. Journal of Clinical Virology Plus 2025; 5(1): 100202.
18- Marcellino A, Bloise S, Pirone C, Brandino G, Barberi A, Del Giudice E, et al. Increased Measured GFR and Proteinuria in Children with Previous Infection by SARS-Cov-2: Should We Be Concerned? Microorganisms 2025; 13(5): 1008.
19- Brigadoi G, Tirelli F, Rossin S, Casotto V, Riello F, Gallinaro G, et al. Severe And Invasive Bacterial Infections in Infants Aged Less than 90 Days with and Without SARS-Cov-2 Infection. Ital J Pediatr 2024; 50(1): 148.
20- Mendez DR, Paul K, Richardson J, Jehle D. Risk of Urinary Tract Infection and Bacteremia in Infants Infected with COVID-19. Pediatr Emerg Care 2025; 41(3): 226-9.
21- Saygili S, Canpolat N, Cicek RY, Agbas A, Yilmaz EK, Sakalli AAK, et al. Clinical and Subclinical Acute Kidney Injury in Children with Mild-To-Moderate COVID-19. Pediatr Res 2023; 93(3): 654-60.
22- Martin SM, Meni Battaglia L, Ferraris J, Ramírez F, Coccia P, García Chervo L, et al. Prevalence of Renal Involvement among Pediatric Patients Hospitalized Due to Coronavirus Disease 2019: A Multicenter Study. Arch Argent Pediatr 2022; 120(5): 310-6.
23- Ağbaş A, Akkoç G, Kızılırmak C, Çalışkan Dolu N, Bayramoğlu E, Elevli M. Kidney Involvement in Pediatric COVID-19 Cases: A Single-Center Experience. Turk Arch Pediatr 2022; 57(5): 558-62.
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |




