دوره 33، شماره 2 - ( اردیبهشت 1404 )
جلد 33 شماره 2 صفحات 8704-8698 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Ahadian H, Mohiti A, Ghadiri-Anari A, Heidary A. Evaluation of the Correlation between Salivary Glucose and Ph and Blood Sugar in Diabetic Patients (A Pilot Study). JSSU 2025; 33 (2) :8698-8704
URL: http://jssu.ssu.ac.ir/article-1-6298-fa.html
URL: http://jssu.ssu.ac.ir/article-1-6298-fa.html
احدیان حکیمه، محیطی عذرا، قدیری اناری اکرم، حیدری آرزو. بررسی ارتباط بین قند و pH بزاق و قند خون در بیماران دیابتی (یک مطالعهPilot ). مجله علمي پژوهشي دانشگاه علوم پزشكي شهید صدوقی يزد. 1404; 33 (2) :8698-8704
متن کامل [PDF 658 kb]
(299 دریافت)
| چکیده (HTML) (969 مشاهده)
References:
1- Ladgotra A, Verma P, Raj SS. Estimation of Salivary and Serum Biomarkers in Diabetic and Non-Diabetic Patients - A Comparative Study. J Clin Diagn Res 2016; 10(6): ZC56-61
2- Ghafarzadegan R, Masror D, Parvizy S, Ebrahim Khamse, Hamid Haghan. Quality of Life in Patients with Type II Diabetes. Journal of the Iranian Institute for Health Sciences Research 2013; 12(5): 489-95. [Persian]
3- Farahani H, Naimi A R. Comparison of Glycosylated Hemoglobin and Oral Glucose Tolerance Test in Diagnosis of Diabetes in Person with Impaired Fasting Glucose. J Arak Uni Med Sci 2004; 7(4): 33-8. [Persian]
4- Afkhami Ardakani M, Rashidi M. Type 2 Diabetes and Its Risk Factors. Journal of Rafsanjan University of Medical Sciences 2006; 4(5): 348. [Persian]
5- Taaheri J, Bakhshi M, Aryankia A, Noormohammadi R. Use of Saliva for Diagnosis of Diseases. Journal of Islamic Dental Association of Iran 2014; 27(1); 74-85. [Persian]
6- Singh S, Kumar V, Kumar S, Subbappa A. The Effect of Periodontal Therapy on the Improvement of Glycemic Control in Patients with Type 2 Diabetes Mellitus: A Randomized Controlled Clinical Trial. Int J Diabetes Dev Ctries 2008; 28(2): 38-44.
7- Ahadian H, Mohiti A, GHadiri Anari K, Heidary A. Evaluation of the Effect of Routine Periodontal Treatment (SRP and Oral Hygiene Instruction) on Salivary Characteristics and Blood Sugar Control in Diabetic Patients: A Clinical Trial. Journal of Kerman University of Medical Sciences 2024; 31(6): 318-24.[Persian]
8- Mahdavi SO, Boostani N, Ghanei A, Solimanian A. Evaluation of FPG by Salivary Glucose in Diabetic Patients. Journal of Mashhad Dental School 2014; 37(4): 319-28. [Persian]
9- Tiongco REG, Arceo ES, Rivera NS, Flake CCD, Policarpio AR. Estimation of Salivary Glucose, Amylase, Calcium, and Phosphorus among Non-Diabetics and Diabetics: Potential Identification of Non-Invasive Diagnostic Markers. Diabetes Metab Syndr 2019; 13(4): 2601-5
10- Amini S, Mohammadi M. The Effect of Phase 1 Periodontal Therapy on Blood Glucose Level in Patients with Type 2 Diabetes. Journal of Isfahan Dental School 2(3): 12-15 [Persian]
11- Mahdavi O, Boostani N, Ghanei A, Solimanian A. Evaluation of FPG by Salivary Glucose in Diabetic Patients. J Mash Dent Sch 2014; 37(4): 319-28. [Persian]
12- Panchbhai AS, Degwekar SS, Bhowte RR. Estimation of Salivary Glucose, Salivary Amylase, Salivary Total Protein and Salivary Flow Rate in Diabetics in India. J Oral Sci 2010; 52(3): 359-68.
13- Owlia F, Akhavan Karbassi M, Ahadian H. Comparison of Salivary Ph in Diabetic Patients Referring to Diabetes Center of Shahid Sadoughi University of Medical Sciences with Non-Diabetic Controls. SSU_Journals 2012; 20(1): 82-9. [Persian]
14- Mohiti A, Ghadiri-Anari A, Entezary F. Comparison of Ph and Viscosity of Unstimulated Saliva in Type 2 Diabetic Patients and Control Group. Journal of Dental School 2017; 35(3): 89-92.
15- Collin H-L, Uusitupa M, Niskanen L, Koivisto AM, Markkanen H, Meurman JH. Caries in Patients with Non-Insulin-Dependent Diabetes Mellitus. Oral Surg Oral Med Oral Pathol Oral Radiol Endod 1998; 85(6): 680-5.
متن کامل: (297 مشاهده)
مقدمه
دیابت ملیتوس یک وضعیت مزمن با عوارض شدید و طولانیمدت است که بهصورت افزایش قند خون تعریف میشود که ناشی از نقص ترشح انسولین، عملکرد انسولین یا هردو است. در حال حاضر دیابت نوع دو توسط WHO به عنوان ششمین عامل مرگ شناخته شده است (1). مزمن بودن دیابت و عوارض بالقوه آن اغلب باعث تحمیل هزینههای مالی زیاد وکاهش کیفیت زندگی و تغییرات مهمی در سبک زندگی برای بیمار و خانواده میشود. بیماران دیابتی با مشکلات جسمی و روانی متعددی مانند افسردگی، اضطراب، ناتوانی، کمتحرکی و چاقی روبهرو هستند که در نهایت منجر به کاهش کیفیت زندگی میگردد (2). با توجه به سیر مزمن و عوارض بالای دیابت با شناسایی سریع بیماری میتوان از عوارض بیماری به مقدار قابلتوجهی کاست (3). تغییرات ماکروواسکولار و میکروواسکولار دیابت باعث ایجاد عوارض مختلفی در دهان میشوند: از جمله خشکی دهان، عفونتهای مختلف قارچی (کاندیدیازیس)، عفونتهای ویروسی (تبخالهای وسیع و طولانیمدت)، عفونتهای باکتریایی (پوسیدگیها و آبسههای دهانی، ژنژویت و پریودنتیت، سیالادنتیت)، تاخیر در ترمیم زخم (زخم و عفونتهای طولانی بعد از کشیدن دندان)، لیکنپلان، سوزش دهان، تغییر در ترشح بزاق و حتی ایجاد پوسیدگی دندان (4). از آنجا که تشخیص سریع و به موقع بیماریها نقش عمدهای در درمان بهموقع و موفق بیماریها را دارد، دسترسی به روشهای نمونهگیری غیرتهاجمی، مانند بزاق در بررسی بیماریها و نتایج درمانی آنها، هدف مطلوبی محسوب میشود. روی کار آمدن ابزارهای تشخیصی جدید در آنالیز اجزای بزاقی، اهمیت بزاق را به عنوان یک ابزار تشخیصی چند برابر کرده است (5). هدف از این مطالعه اولیه بررسی همبستگی بین قند بزاقی و قند خون بیماران دیابتی نوع 2 بود که در صورت وجود این همبستگی مطالعه کارازمایی بالینی جهت بررسی تاثیر مداخلات پریودنتال بر قند خون و بزاق انجام شود.
روش بررسی
این مطالعه آزمایشی (Pilot) بر روی 13 بیمار مبتلا به دیابت نوع 2 مراجعه کننده به مرکز تحقیقات دیابت یزد براساس تمایل به انجام مطالعه انجام شد. معیارهای ورود شامل بیماران مبتلا به دیابت نوع 2 ( FBS≥ 126mg/dlو HbA1C≥6.5%) (6) در مرکز تحقیقات دیابت یزد بود که بیماری همزمان دیگری نداشتند، فقط تحت درمان با داروهای کاهنده قند خون خوراکی بودند و آخرین آزمایش خون بیماران حداکثر مربوط 3 ماه اخیر بود. بیماران در صورت عدم رضایت و عدم همکاری از تحقیق خارج شدند. دادهها براساس پرسشنامه و به کمک پرونده بیمار و با استفاده از نتایج آزمایشهای خونی و بزاقی از نمونههای جمعآوری شده از بیماران بهدست آمد. نتایج تستهای خونی مربوط به یک ماه اخیر بود. پس از کسب رضایت کتبی آگاهانه از بیماران اطلاعات دموگرافیک شامل سن و جنس و اطلاعات پزشکی و نتایج آزمایش های قندخون (FBS و HbA1C) بیمار ثبت شد. نمونه بزاق غیرتحریکی جهت ارزیابی گلوکز بزاق تحت شرایط استاندارد اخذ شد. جهت اخذ نمونه بزاق 2 سیسی بزاق غیرتحریکی تجمعی به روش spitting جمعآوری شد بدین صورت که بیماران مورد نظر از 90 دقیقه قبل از نمونهگیری به منظور کاهش اثر تغییرات روزانه ترکیب بزاق از خوردن، آشامیدن، سیگار کشیدن و مسواک زدن منع شدند. قبل از جمعآوری نمونهها افراد آرام در حالت نشسته روی صندلی باقی مانده و از آنها خواسته شد بزاق خود را جمع کرده و در داخل ظرف استریل شده مخصوص تخلیه کنند به این صورت که هر 60 ثانیه یکبار بزاق خود را خارج کنند و اینکار را به مدت 5 دقیقه انجام دهند (7). سپس نمونههای بزاق جهت ارزیابی گلوکز سریعا به آزمایشگاه ارسال شد. نمونههای بزاقی بلافاصله با سرعت rpm 4400 به مدت 15 دقیقه به منظور جداسازی هر گونه ناخالصی سانتریفیوژ شدند. نمونههای جداسازی شده سپس بهوسیله پیپت به لولههای پلاستیکی منتقل و پارافینه شدند و سپس در دمای 70- درجه جهت غیر فعالسازی چرخه گلیکولیز مصرف گلوکز توسط باکتریها برای آزمایشات بعدی در فریزر مدلU410 ساخت کشور انگلستان فریز شدند. نمونههای بزاقی بوسیله کیت گلوکوز اکسیداز/پراکسیداز شرکت (Biosystems S.A.Costa Brava30, Barcelona, Spain) با محدوده تشخیص حداقل mg/dl23/0 در آزمایشگاه بوعلی یزد تحت بررسی تعیین میزان گلوکز قرار گرفتند. برای این منظور ابتدا غلظتهای گلوکز استاندارد 0/312، 0/625، 1/25، 2/5، 5 و 10 تهیه شد. سپس از هر کدام 100 لاندا جداگانه در لولههای آزمایش ریخته شد و 1000 لاندا Reagent به هر کدام اضافه و به مدت 30 دقیقه در Incubator با دمای C°37 نگهداری شدند. میزان جذب غلظتها توسط دستگاه Spectrophotometer خوانده شد. با توجه به غلظت و جذب خوانده شده توسط دستگاه، Standard curve در Excel رسم شد. سپس 100 لاندا از هر یک از نمونههای بزاقی در لولههای آزمایش مجزا ریخته شد و به هر کدام 1000 لاندا Reagent اضافه گردید و نمونهها دوباره به مدت 30 دقیقه در Incubator با دمای °c37 قرار داده شدند. میزان جذب غلظت هر نمونه بزاقی توسط دستگاه Spectrophotometer مجدداً خوانده شد و غلظت گلوکز نمونههای بزاقی بهدست آمد (8). برای ارزیابی pH بزاق از دستگاه digital pH meter که بهصورتpen type و ساخت کمپانی AZتایوان میباشد استفاده شد. قبل از انجام مطالعه با توضیح هدف از انجام تحقیق برای تک تک افراد واجد شرایط شرکت در مطالعه، فرم رضایت آگاهانه توسط آن ها تکمیل شد.
اطلاعات بهدست آمده در نرمافزار اماری version 16 SPSS وارد شده و به تفکیک هریک از متغیرها ارزیابی و جهت آنالیز ارتباط بین متغیرها از تحلیل رگرسیون استفاده شد. ضریب α در کلیه محاسبات 0/05 در نظر گرفته شد.
نتایج
این مطالعه بر روی 13 بیمار مبتلا به دیابت ملیتوس نوع 2 با میانگین سنی 9/72 ± 50/38 سال انجام شد. میانگین قند خون ناشتا (FBS) mg/dl 60/59 ±184/38،HbA1C 0/09 ± 7/32% و همچنین میانگین قند بزاق در بیماران 1/61±1/84 بود. میانگین pHبزاق بیماران 0/58± 6/46 بهدست آمد. بین میانگین قند بزاق (FSG) با قند خون (FBS HbA1C,) همبستگی مثبت و معنیدار وجود داشت (جدول1). pH بزاق با همه فاکتورهای قند خون و بزاق رابطه معکوس دارد اما در هیچکدام این ارتباط معنیدار نبود. (جدول 2) یعنی با افزایش قند خون و قند بزاق اسیدیته بزاق افزایش و در واقع PH آن کاهش مییابد.
جدول 1:همبستگی بین میانگین قند خون و بزاق در بیماران دیابتی نوع 2

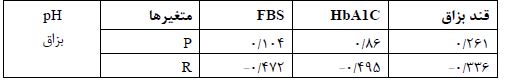
جدول2: ارتباط بین pH بزاق با قند خون و بزاق در بیماران دیابتی نوع 2
بحث
بیماری دیابت ملیتوس باعث تغییرات کمی و کیفی بزاق شده که میتواند در نهایت منجر به تغییراتی در حفره دهان شود. تغییر اجزای بزاق میتواند بر علایم و شدت تغییرات دهان موثر باشد. گروهی از محققین معتقدند که بزاق میتواند به عنوان یک مایع تشخیصی برای ارزیابی دیابت استفاده شود (9). در مطالعه حاضر مقایسه نتایج قند خون و قند بزاق نشان داد که بین نتایج قند خون با قند بزاق رابطه مثبت و معنیدار وجود دارد. در مطالعه امینی (10) طبق آنالیز آماری ضریب همبستگی پیرسون، ارتباط بین قند خون ناشتا و گلوکز بزاقی ناشتا بهدست آمد که از نظر آماری معنیدار بود (P<0.001 ) بیانگر ارتباط قوی بین قند خون ناشتا و قند بزاقی در افراد دیابتی میباشد همچنین ضریب همبستگی بالایی بین HbA1C و گلوکز بزاقی بهدست آمد که این ارتباط نیز از نظر آماری معنیدار بود P<0.001) ). یافتههای مطالعه حاضر همسو با نتایج گزارش شده امینی بود. همچنین بررسی نتایج مطالعه Amit(1) ارتباط قابلتوجهی بین قند خون و قند بزاق در بیماران دیابتی نشان داد (P =0.018). در مطالعه مهدوی نتایج نشان داد که بین قند خون و قند بزاق ارتباط خطی و معنادار وجود دارد (11) در مطالعه Panchbhai در سال 2010 در هند با هدف ارزیابی و تخمین گلوکز بزاق در بیماران دیابتی نتایج نشان داد که در گروه دیابتی کنترل شده با افزایش قند خون، قند بزاق افزایش میباید اما این ارتباط معنیدار نبود (12). در مطالعات مختلف میانگین قند بزاق در بیماران دیابتی نتایج متفاوتی را نشان داده است که میتواند مرتبط با شرایط و روش جمعآوری نمونه، نوع نمونه بزاق، مدت زمان انتقال به آزمایشگاه و روشهای ازمایشگاهی متفاوت و همچنین تغییرات مربوط به وضعیت کنترل دیابت بیماران، داروهای مصرفی و سن بیماران باشد. مطالعات نشان داده که سطح گلوکز بزاق در بیماران دیابتی بالاتر از افراد غیردیابتی است که به علت ارتشاح گلوکز درون بزاق ناشی از نشت اجزای مشتق از سرم در بزاق از طریق مایع شیار لثهای میباشد همچنین بیماران دیابتی نفوذپذیری غشایی بیشتری دارند که به علت تغییرات میکروواسکولار در عروق خونی ناشی از هایپرگلایسمی ایجاد میشود. ملکول قند کوچک است و در نتیجه میتواند از طریق غشای نیمه تراوا عبور کند و باعث نشت گلوکز در بزاق شود (9). در مطالعه حاضر بین نتایج PH بزاق با قند خون و بزاق رابطه معکوس و غیر معنیدار وجود دارد. در مطالعه اولیا (13) در بیماران دیابتی بین قند خون ناشتا با افت PH بزاق ارتباط معنیداری مشاهده شد. همچنین در مطالعه محیطی (14) بین قند خون با افت PH بزاق در بیماران دیابتی ارتباط مثبتی گزارش شد. نتایج دو مطالعه فوق همسو با نتایج مطالعه حاضر بود اما برخی مطالعات از جمله مطالعه Collin و همکاران (15) بیان کرد که اسیدیته بزاق در بیماران دیابتی نقریبا مشابه بیماران غیردیابتی میباشد. با توجه ارتباط بین اسیدیته بزاق با قند خون و بزاق در مطالعه حاضر احتمالا کاهش PH بزاق در بیماران دیابتی به دلیل کاهش جریان بزاق میباشد. یکی دیگر از مکانیسمهای پیشنهادی در افزایش اسیدیته بزاق در بیماران با قند خون بالا متابولیسم مختل گلوکز و همچنین نقص در متابولیسم چربی و تولید مقدار زیادی استون و بتاهیدروکسی بوتیریک اسید در بزاق میباشد (14).
نتیجهگیری
با توجه به نتایج مطالعه حاضر مبنی بر ارتباط معنیدار بین قند خون و قند بزاق در بیماران دیابتی، میتوان استفاده از نمونه بزاق به عنوان یک روش مقرون به صرفه، غیرتهاجمی و معتبر برای بررسی و تشخیص و پیگیری بیماران دیابتی را توصیه نمود.
محدودیتها: عدم همکاری بیمار با پژوهشگر و دشوار بودن هماهنگی با مرکز دیابت، ازمایشگاه و بیماران و همچنین دشواری و محدودیت زمان جهت ارزیابی فاکتورهای بزاقی
سپاسگزاری
از معاونت پژوهشی دانشگاه علوم پزشکی شهید صدوقی یزد، مرکز تحقیقات دیابت استان یزد، ازمایشگاه بوعلی و جناب اقای دکتر حسین فلاحزاده جهت همکاری در این مطالعه تقدیر و تشکر میگردد.
حامی مالی: بخشی از هزینههای این پژوهش توسط دانشگاه علوم پزشکی شهید صدوقی یزد تامین شد.
تعارض در منافع: وجود ندارد.
ملاحظات اخلاقی
این مطالعه در «کمیته اخلاق در پژوهش دانشگاه علوم پزشکی شهید صدوقی یزد» شماره 1399.144IR.SSU.REC. به تصویب رسیده است.
مشارکت نویسندگان
دکتر محیطی و دکتر قدیری اناری در ارائه ایده، دکتر احدیان در طراحی مطالعه، دکتر حیدری در جمعآوری دادهها، .دکتر احدیان و دکتر حیدری و دکتر فلاح زاده (مشاور آمار )در تجزیه و تحلیل دادهها مشارکت داشته و همه نویسندگان در تدوین، ویرایش اولیه و نهایی مقاله و پاسخگویی به سوالات مرتبط با مقاله سهیم هستند.
دیابت ملیتوس یک وضعیت مزمن با عوارض شدید و طولانیمدت است که بهصورت افزایش قند خون تعریف میشود که ناشی از نقص ترشح انسولین، عملکرد انسولین یا هردو است. در حال حاضر دیابت نوع دو توسط WHO به عنوان ششمین عامل مرگ شناخته شده است (1). مزمن بودن دیابت و عوارض بالقوه آن اغلب باعث تحمیل هزینههای مالی زیاد وکاهش کیفیت زندگی و تغییرات مهمی در سبک زندگی برای بیمار و خانواده میشود. بیماران دیابتی با مشکلات جسمی و روانی متعددی مانند افسردگی، اضطراب، ناتوانی، کمتحرکی و چاقی روبهرو هستند که در نهایت منجر به کاهش کیفیت زندگی میگردد (2). با توجه به سیر مزمن و عوارض بالای دیابت با شناسایی سریع بیماری میتوان از عوارض بیماری به مقدار قابلتوجهی کاست (3). تغییرات ماکروواسکولار و میکروواسکولار دیابت باعث ایجاد عوارض مختلفی در دهان میشوند: از جمله خشکی دهان، عفونتهای مختلف قارچی (کاندیدیازیس)، عفونتهای ویروسی (تبخالهای وسیع و طولانیمدت)، عفونتهای باکتریایی (پوسیدگیها و آبسههای دهانی، ژنژویت و پریودنتیت، سیالادنتیت)، تاخیر در ترمیم زخم (زخم و عفونتهای طولانی بعد از کشیدن دندان)، لیکنپلان، سوزش دهان، تغییر در ترشح بزاق و حتی ایجاد پوسیدگی دندان (4). از آنجا که تشخیص سریع و به موقع بیماریها نقش عمدهای در درمان بهموقع و موفق بیماریها را دارد، دسترسی به روشهای نمونهگیری غیرتهاجمی، مانند بزاق در بررسی بیماریها و نتایج درمانی آنها، هدف مطلوبی محسوب میشود. روی کار آمدن ابزارهای تشخیصی جدید در آنالیز اجزای بزاقی، اهمیت بزاق را به عنوان یک ابزار تشخیصی چند برابر کرده است (5). هدف از این مطالعه اولیه بررسی همبستگی بین قند بزاقی و قند خون بیماران دیابتی نوع 2 بود که در صورت وجود این همبستگی مطالعه کارازمایی بالینی جهت بررسی تاثیر مداخلات پریودنتال بر قند خون و بزاق انجام شود.
روش بررسی
این مطالعه آزمایشی (Pilot) بر روی 13 بیمار مبتلا به دیابت نوع 2 مراجعه کننده به مرکز تحقیقات دیابت یزد براساس تمایل به انجام مطالعه انجام شد. معیارهای ورود شامل بیماران مبتلا به دیابت نوع 2 ( FBS≥ 126mg/dlو HbA1C≥6.5%) (6) در مرکز تحقیقات دیابت یزد بود که بیماری همزمان دیگری نداشتند، فقط تحت درمان با داروهای کاهنده قند خون خوراکی بودند و آخرین آزمایش خون بیماران حداکثر مربوط 3 ماه اخیر بود. بیماران در صورت عدم رضایت و عدم همکاری از تحقیق خارج شدند. دادهها براساس پرسشنامه و به کمک پرونده بیمار و با استفاده از نتایج آزمایشهای خونی و بزاقی از نمونههای جمعآوری شده از بیماران بهدست آمد. نتایج تستهای خونی مربوط به یک ماه اخیر بود. پس از کسب رضایت کتبی آگاهانه از بیماران اطلاعات دموگرافیک شامل سن و جنس و اطلاعات پزشکی و نتایج آزمایش های قندخون (FBS و HbA1C) بیمار ثبت شد. نمونه بزاق غیرتحریکی جهت ارزیابی گلوکز بزاق تحت شرایط استاندارد اخذ شد. جهت اخذ نمونه بزاق 2 سیسی بزاق غیرتحریکی تجمعی به روش spitting جمعآوری شد بدین صورت که بیماران مورد نظر از 90 دقیقه قبل از نمونهگیری به منظور کاهش اثر تغییرات روزانه ترکیب بزاق از خوردن، آشامیدن، سیگار کشیدن و مسواک زدن منع شدند. قبل از جمعآوری نمونهها افراد آرام در حالت نشسته روی صندلی باقی مانده و از آنها خواسته شد بزاق خود را جمع کرده و در داخل ظرف استریل شده مخصوص تخلیه کنند به این صورت که هر 60 ثانیه یکبار بزاق خود را خارج کنند و اینکار را به مدت 5 دقیقه انجام دهند (7). سپس نمونههای بزاق جهت ارزیابی گلوکز سریعا به آزمایشگاه ارسال شد. نمونههای بزاقی بلافاصله با سرعت rpm 4400 به مدت 15 دقیقه به منظور جداسازی هر گونه ناخالصی سانتریفیوژ شدند. نمونههای جداسازی شده سپس بهوسیله پیپت به لولههای پلاستیکی منتقل و پارافینه شدند و سپس در دمای 70- درجه جهت غیر فعالسازی چرخه گلیکولیز مصرف گلوکز توسط باکتریها برای آزمایشات بعدی در فریزر مدلU410 ساخت کشور انگلستان فریز شدند. نمونههای بزاقی بوسیله کیت گلوکوز اکسیداز/پراکسیداز شرکت (Biosystems S.A.Costa Brava30, Barcelona, Spain) با محدوده تشخیص حداقل mg/dl23/0 در آزمایشگاه بوعلی یزد تحت بررسی تعیین میزان گلوکز قرار گرفتند. برای این منظور ابتدا غلظتهای گلوکز استاندارد 0/312، 0/625، 1/25، 2/5، 5 و 10 تهیه شد. سپس از هر کدام 100 لاندا جداگانه در لولههای آزمایش ریخته شد و 1000 لاندا Reagent به هر کدام اضافه و به مدت 30 دقیقه در Incubator با دمای C°37 نگهداری شدند. میزان جذب غلظتها توسط دستگاه Spectrophotometer خوانده شد. با توجه به غلظت و جذب خوانده شده توسط دستگاه، Standard curve در Excel رسم شد. سپس 100 لاندا از هر یک از نمونههای بزاقی در لولههای آزمایش مجزا ریخته شد و به هر کدام 1000 لاندا Reagent اضافه گردید و نمونهها دوباره به مدت 30 دقیقه در Incubator با دمای °c37 قرار داده شدند. میزان جذب غلظت هر نمونه بزاقی توسط دستگاه Spectrophotometer مجدداً خوانده شد و غلظت گلوکز نمونههای بزاقی بهدست آمد (8). برای ارزیابی pH بزاق از دستگاه digital pH meter که بهصورتpen type و ساخت کمپانی AZتایوان میباشد استفاده شد. قبل از انجام مطالعه با توضیح هدف از انجام تحقیق برای تک تک افراد واجد شرایط شرکت در مطالعه، فرم رضایت آگاهانه توسط آن ها تکمیل شد.
اطلاعات بهدست آمده در نرمافزار اماری version 16 SPSS وارد شده و به تفکیک هریک از متغیرها ارزیابی و جهت آنالیز ارتباط بین متغیرها از تحلیل رگرسیون استفاده شد. ضریب α در کلیه محاسبات 0/05 در نظر گرفته شد.
نتایج
این مطالعه بر روی 13 بیمار مبتلا به دیابت ملیتوس نوع 2 با میانگین سنی 9/72 ± 50/38 سال انجام شد. میانگین قند خون ناشتا (FBS) mg/dl 60/59 ±184/38،HbA1C 0/09 ± 7/32% و همچنین میانگین قند بزاق در بیماران 1/61±1/84 بود. میانگین pHبزاق بیماران 0/58± 6/46 بهدست آمد. بین میانگین قند بزاق (FSG) با قند خون (FBS HbA1C,) همبستگی مثبت و معنیدار وجود داشت (جدول1). pH بزاق با همه فاکتورهای قند خون و بزاق رابطه معکوس دارد اما در هیچکدام این ارتباط معنیدار نبود. (جدول 2) یعنی با افزایش قند خون و قند بزاق اسیدیته بزاق افزایش و در واقع PH آن کاهش مییابد.
جدول 1:همبستگی بین میانگین قند خون و بزاق در بیماران دیابتی نوع 2

جدول2: ارتباط بین pH بزاق با قند خون و بزاق در بیماران دیابتی نوع 2

بحث
بیماری دیابت ملیتوس باعث تغییرات کمی و کیفی بزاق شده که میتواند در نهایت منجر به تغییراتی در حفره دهان شود. تغییر اجزای بزاق میتواند بر علایم و شدت تغییرات دهان موثر باشد. گروهی از محققین معتقدند که بزاق میتواند به عنوان یک مایع تشخیصی برای ارزیابی دیابت استفاده شود (9). در مطالعه حاضر مقایسه نتایج قند خون و قند بزاق نشان داد که بین نتایج قند خون با قند بزاق رابطه مثبت و معنیدار وجود دارد. در مطالعه امینی (10) طبق آنالیز آماری ضریب همبستگی پیرسون، ارتباط بین قند خون ناشتا و گلوکز بزاقی ناشتا بهدست آمد که از نظر آماری معنیدار بود (P<0.001 ) بیانگر ارتباط قوی بین قند خون ناشتا و قند بزاقی در افراد دیابتی میباشد همچنین ضریب همبستگی بالایی بین HbA1C و گلوکز بزاقی بهدست آمد که این ارتباط نیز از نظر آماری معنیدار بود P<0.001) ). یافتههای مطالعه حاضر همسو با نتایج گزارش شده امینی بود. همچنین بررسی نتایج مطالعه Amit(1) ارتباط قابلتوجهی بین قند خون و قند بزاق در بیماران دیابتی نشان داد (P =0.018). در مطالعه مهدوی نتایج نشان داد که بین قند خون و قند بزاق ارتباط خطی و معنادار وجود دارد (11) در مطالعه Panchbhai در سال 2010 در هند با هدف ارزیابی و تخمین گلوکز بزاق در بیماران دیابتی نتایج نشان داد که در گروه دیابتی کنترل شده با افزایش قند خون، قند بزاق افزایش میباید اما این ارتباط معنیدار نبود (12). در مطالعات مختلف میانگین قند بزاق در بیماران دیابتی نتایج متفاوتی را نشان داده است که میتواند مرتبط با شرایط و روش جمعآوری نمونه، نوع نمونه بزاق، مدت زمان انتقال به آزمایشگاه و روشهای ازمایشگاهی متفاوت و همچنین تغییرات مربوط به وضعیت کنترل دیابت بیماران، داروهای مصرفی و سن بیماران باشد. مطالعات نشان داده که سطح گلوکز بزاق در بیماران دیابتی بالاتر از افراد غیردیابتی است که به علت ارتشاح گلوکز درون بزاق ناشی از نشت اجزای مشتق از سرم در بزاق از طریق مایع شیار لثهای میباشد همچنین بیماران دیابتی نفوذپذیری غشایی بیشتری دارند که به علت تغییرات میکروواسکولار در عروق خونی ناشی از هایپرگلایسمی ایجاد میشود. ملکول قند کوچک است و در نتیجه میتواند از طریق غشای نیمه تراوا عبور کند و باعث نشت گلوکز در بزاق شود (9). در مطالعه حاضر بین نتایج PH بزاق با قند خون و بزاق رابطه معکوس و غیر معنیدار وجود دارد. در مطالعه اولیا (13) در بیماران دیابتی بین قند خون ناشتا با افت PH بزاق ارتباط معنیداری مشاهده شد. همچنین در مطالعه محیطی (14) بین قند خون با افت PH بزاق در بیماران دیابتی ارتباط مثبتی گزارش شد. نتایج دو مطالعه فوق همسو با نتایج مطالعه حاضر بود اما برخی مطالعات از جمله مطالعه Collin و همکاران (15) بیان کرد که اسیدیته بزاق در بیماران دیابتی نقریبا مشابه بیماران غیردیابتی میباشد. با توجه ارتباط بین اسیدیته بزاق با قند خون و بزاق در مطالعه حاضر احتمالا کاهش PH بزاق در بیماران دیابتی به دلیل کاهش جریان بزاق میباشد. یکی دیگر از مکانیسمهای پیشنهادی در افزایش اسیدیته بزاق در بیماران با قند خون بالا متابولیسم مختل گلوکز و همچنین نقص در متابولیسم چربی و تولید مقدار زیادی استون و بتاهیدروکسی بوتیریک اسید در بزاق میباشد (14).
نتیجهگیری
با توجه به نتایج مطالعه حاضر مبنی بر ارتباط معنیدار بین قند خون و قند بزاق در بیماران دیابتی، میتوان استفاده از نمونه بزاق به عنوان یک روش مقرون به صرفه، غیرتهاجمی و معتبر برای بررسی و تشخیص و پیگیری بیماران دیابتی را توصیه نمود.
محدودیتها: عدم همکاری بیمار با پژوهشگر و دشوار بودن هماهنگی با مرکز دیابت، ازمایشگاه و بیماران و همچنین دشواری و محدودیت زمان جهت ارزیابی فاکتورهای بزاقی
سپاسگزاری
از معاونت پژوهشی دانشگاه علوم پزشکی شهید صدوقی یزد، مرکز تحقیقات دیابت استان یزد، ازمایشگاه بوعلی و جناب اقای دکتر حسین فلاحزاده جهت همکاری در این مطالعه تقدیر و تشکر میگردد.
حامی مالی: بخشی از هزینههای این پژوهش توسط دانشگاه علوم پزشکی شهید صدوقی یزد تامین شد.
تعارض در منافع: وجود ندارد.
ملاحظات اخلاقی
این مطالعه در «کمیته اخلاق در پژوهش دانشگاه علوم پزشکی شهید صدوقی یزد» شماره 1399.144IR.SSU.REC. به تصویب رسیده است.
مشارکت نویسندگان
دکتر محیطی و دکتر قدیری اناری در ارائه ایده، دکتر احدیان در طراحی مطالعه، دکتر حیدری در جمعآوری دادهها، .دکتر احدیان و دکتر حیدری و دکتر فلاح زاده (مشاور آمار )در تجزیه و تحلیل دادهها مشارکت داشته و همه نویسندگان در تدوین، ویرایش اولیه و نهایی مقاله و پاسخگویی به سوالات مرتبط با مقاله سهیم هستند.
References:
1- Ladgotra A, Verma P, Raj SS. Estimation of Salivary and Serum Biomarkers in Diabetic and Non-Diabetic Patients - A Comparative Study. J Clin Diagn Res 2016; 10(6): ZC56-61
2- Ghafarzadegan R, Masror D, Parvizy S, Ebrahim Khamse, Hamid Haghan. Quality of Life in Patients with Type II Diabetes. Journal of the Iranian Institute for Health Sciences Research 2013; 12(5): 489-95. [Persian]
3- Farahani H, Naimi A R. Comparison of Glycosylated Hemoglobin and Oral Glucose Tolerance Test in Diagnosis of Diabetes in Person with Impaired Fasting Glucose. J Arak Uni Med Sci 2004; 7(4): 33-8. [Persian]
4- Afkhami Ardakani M, Rashidi M. Type 2 Diabetes and Its Risk Factors. Journal of Rafsanjan University of Medical Sciences 2006; 4(5): 348. [Persian]
5- Taaheri J, Bakhshi M, Aryankia A, Noormohammadi R. Use of Saliva for Diagnosis of Diseases. Journal of Islamic Dental Association of Iran 2014; 27(1); 74-85. [Persian]
6- Singh S, Kumar V, Kumar S, Subbappa A. The Effect of Periodontal Therapy on the Improvement of Glycemic Control in Patients with Type 2 Diabetes Mellitus: A Randomized Controlled Clinical Trial. Int J Diabetes Dev Ctries 2008; 28(2): 38-44.
7- Ahadian H, Mohiti A, GHadiri Anari K, Heidary A. Evaluation of the Effect of Routine Periodontal Treatment (SRP and Oral Hygiene Instruction) on Salivary Characteristics and Blood Sugar Control in Diabetic Patients: A Clinical Trial. Journal of Kerman University of Medical Sciences 2024; 31(6): 318-24.[Persian]
8- Mahdavi SO, Boostani N, Ghanei A, Solimanian A. Evaluation of FPG by Salivary Glucose in Diabetic Patients. Journal of Mashhad Dental School 2014; 37(4): 319-28. [Persian]
9- Tiongco REG, Arceo ES, Rivera NS, Flake CCD, Policarpio AR. Estimation of Salivary Glucose, Amylase, Calcium, and Phosphorus among Non-Diabetics and Diabetics: Potential Identification of Non-Invasive Diagnostic Markers. Diabetes Metab Syndr 2019; 13(4): 2601-5
10- Amini S, Mohammadi M. The Effect of Phase 1 Periodontal Therapy on Blood Glucose Level in Patients with Type 2 Diabetes. Journal of Isfahan Dental School 2(3): 12-15 [Persian]
11- Mahdavi O, Boostani N, Ghanei A, Solimanian A. Evaluation of FPG by Salivary Glucose in Diabetic Patients. J Mash Dent Sch 2014; 37(4): 319-28. [Persian]
12- Panchbhai AS, Degwekar SS, Bhowte RR. Estimation of Salivary Glucose, Salivary Amylase, Salivary Total Protein and Salivary Flow Rate in Diabetics in India. J Oral Sci 2010; 52(3): 359-68.
13- Owlia F, Akhavan Karbassi M, Ahadian H. Comparison of Salivary Ph in Diabetic Patients Referring to Diabetes Center of Shahid Sadoughi University of Medical Sciences with Non-Diabetic Controls. SSU_Journals 2012; 20(1): 82-9. [Persian]
14- Mohiti A, Ghadiri-Anari A, Entezary F. Comparison of Ph and Viscosity of Unstimulated Saliva in Type 2 Diabetic Patients and Control Group. Journal of Dental School 2017; 35(3): 89-92.
15- Collin H-L, Uusitupa M, Niskanen L, Koivisto AM, Markkanen H, Meurman JH. Caries in Patients with Non-Insulin-Dependent Diabetes Mellitus. Oral Surg Oral Med Oral Pathol Oral Radiol Endod 1998; 85(6): 680-5.
نوع مطالعه: کارآزمایی بالینی |
موضوع مقاله:
دندانپزشکی
دریافت: 1403/7/22 | پذیرش: 1403/10/2 | انتشار: 1404/2/15
دریافت: 1403/7/22 | پذیرش: 1403/10/2 | انتشار: 1404/2/15
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |







