دوره 32، شماره 6 - ( شهریور 1403 )
جلد 32 شماره 6 صفحات 7893-7887 |
برگشت به فهرست نسخه ها
Ethics code: IR.SSU.SRH.REC.1403.006
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Eslami M, Tabatabaei S H, Sabaghzadegan F, Navvabi S E. Ameloblastic Fibro Odontoma in a 10-Year-Old Boy: Case Report. JSSU 2024; 32 (6) :7887-7893
URL: http://jssu.ssu.ac.ir/article-1-6239-fa.html
URL: http://jssu.ssu.ac.ir/article-1-6239-fa.html
اسلامی مهدی، طباطبایی سید حسین، صباغزادگان فریناز، نوابی سید احسان. املوبلاستیک فیبروادونتوما در کودک ۱۰ ساله، گزارش مورد. مجله علمي پژوهشي دانشگاه علوم پزشكي شهید صدوقی يزد. 1403; 32 (6) :7887-7893
متن کامل [PDF 615 kb]
(486 دریافت)
| چکیده (HTML) (1271 مشاهده)
References:
1- Cossiez M, Pin DD. A Rare Case of Maxillary Ameloblastic Fibro-Odontoma and a Review of the Literature. J Oral Med Oral Surg 2020; 26(2): 17-22.
2- Bharat D, Vahanwala J, Dabir A, Jobanputra P. Ameloblastic Fibro-Odontoma in the Mandible-Clinical, Radiological and Surgical Aspect. Adv Oral Maxillofac Surg 2021; 2: 100066.
3- Wright JM, Vered M. Update from the 4th Edition of the World Health Organization Classification of Head and Neck Tumours: Odontogenic and Maxillofacial Bone Tumors. Head Neck Pathol 2017; 11: 68-77.
4- Saeed DM, Setty S, Markiewicz MR, Cabay RJ. Ameloblastic Fibro-Odontoma Associated with Paresthesia of the Chin and Lower Lip in a 12-Year-Old Girl. SAGE Open Med Case Rep 2019; 7: 2050313X19870642.
5- Omar N, Ullah A, Ghleilib I, Patel N, Abdelsayed RA. A Locally Aggressive Ameloblastic Fibro-Odontoma: A Case Report and Literature Review. Cureus 2021; 13(12): E20366.
6- Suvarna KS, Layton C, Bancroft JD. Bancroft’s Theory and Practice of Histological Techniques. 8th ed. Elsevier Health Sciences: Amsterdam; 2018: 126-69.
7- Soluk-Tekkesin M, Wright JM. The World Health Organization Classification of Odontogenic Lesions: A Summary of The Changes of the 2022. 5th edition. Turk Patoloji Derg 2022; 38: 168-84.
8- Barnes L, Eveson JW, Reichart P, Sidransky D. World Health Organization Classification of Tumours: Pathology and Genetics, Head and Neck Tumours. Int Agency Res Cancer 2005; 85: 75-81.
9- Thulasirman SK, Thuasidoss G, Prabhu NK, Raja VB. A Rare Case of Ameloblastic Fibro-Odontoma of Mandible with Literature Review. Ann Maxillofac Surg 2018; 8(2): 324-26.
10- Soluk-Tekkesin M, Vered M. Ameloblastic Fibro-Odontoma: At the Crossroad between ‘Developing Odontoma’ and ‘True Odontogenic Tumour’. Head Neck Pathol 2021; 15(4): 1202-11.
11- Sanjai K, Pandey B, Shivalingaiah D, Kumar HM. Odontoameloblastoma: A Report of a Rare Case. J Oral Maxillofacpathol 2018; 22(2): 254-59.
12- Kaushal S, Mathur SR, Vijay M, Rustagi A. Calcifying Epithelial Odontogenic Tumor (Pindborg Tumor) without Calcification: A Rare Entity. J Oral Maxillofac Pathol 2012; 16: 110-2.
13- Nasir A, Khare A, Ali I, Khan MI. Ameloblastic Fibroma: A Case Report. J Oral Maxillofac Pathol 2023; 27 (Suppl 1): S60-S63.
14- Sabu AM, Gandhi S, Singh I, Solanki M, Sakharia AR. Ameloblastic Fibrodentinoma: A Rarity in Odontogenic Tumors. J Maxillofac Oral Surg 2018; 17(4): 444-48.
15- Guerra RC, Carvalho PH, Thieringer FM, Pereira RS, Hochuli-Vieira E. Recurrence of Ameloblastic Fibro-Odontoma in a Child: A Case Report. Craniomaxillofacial Trauma & Reconstruction Open 2020; 5: 1-4.
16- Reis SR, De Freitas CE, Do Espírito Santo AR. Management of Ameloblastic Fibro-Odontoma in a 6-Year-Old Girl Preserving the Associated Impacted Permanent Tooth. J Oral Sci 2007; 49(4): 331-35.
17- Howell RM, Burkes EJ Jr. Malignant Transformation of Ameloblastic Fibro-Odontoma to Ameloblastic Fibrosarcoma. Oral Surg Oral Med Oral Pathol 1977; 43(3): 391-401.
متن کامل: (578 مشاهده)
مقدمه
املوبلاستیک فیبروادونتوما (AFO) یک نئوپلاسم ادنتوژنیک اپیتلیالی - مزانشیمی نادر و بهتدریج پیشرونده است (۱). این ضایعه ویژگیهای بافتشناسی و بیولوژیکی مشابه املوبلاستیک فیبروما (AF) را نشان میدهد. با اینحال، در املوبلاستیک فیبرو ادونتوما (AFO)، یک یا چند کانون سلولی اپیتلیوم القایی در طول فرآیند تمایز باقی میماند که منجر به تولید مینا و عاج میشود (۲). با توجه به انتشار سال ۲۰۱۷ طبقهبندی سازمان بهداشت جهانیWHO املوبلاستیک فیبروادونتوما بهتر است بهعنوان ادونتوما دستهبندی شود (۳). معمولاً در افراد جوانتر ظاهر میشود و هیچ تمایل قابلتوجهی به هیچیک از دو جنس نشان نمیدهد. مشاهده شده است که با فراوانی یکسانی در فک بالا و فک پایین رخ میدهد و محل بروز آن در ناحیه خلفی پرمولرها و مولرها است (۴). تشخیص املوبلاستیک فیبروادونتوما با تکیه بر شواهد بالینی و رادیوگرافی چالش برانگیز است و برای تشخیص قطعی نیاز به بررسی پاتولوژیک دارد (۱). شرایط و علائم بالینی نقش مهمی در تعیین روشهای نمونهبرداری و امکان حفظ دندانهای واقع در نزدیکی ضایعه، ایفا میکند (۵). با توجه به سیر کلینیکی خوشخیم و شواهد رادیولوژیکی از جمله بوردر مشخص و کورتیکه و همچنین عدم پرفوراسیون کورتکس عمل جراحی اولیه بهصورت بیوپسی اکسیژنال انجام میشود که ضایعه بهصورت کامل از استخوان اطراف کورتاژ میشود. مطالعه حاضر مورد بالینی یک فرد ۱۰ ساله مبتلا به املوبلاستیک فیبرو ادونتوما (AFO)را با یک ضایعه در ناحیه خلف فک پایین که از طریق انوکلیشن مدیریت شد، توصیف میکند.
گزارش مورد:
یک پسر نوجوان ۱۰ ساله در اسفند ۱۳۹۹ با شکایت اصلی تورم سمت چپ صورت به بخش جراحی دهان و فک و صورت دانشکده دندانپزشکی یزد ارجاع شد. سوابق پزشکی بیمار هیچ یافته قابلتوجهی را نشان نداد و سابقه دندانی هیچ شواهدی از آسیب موضعی یا فعالیت عفونی در محل ضایعه را نشان نداد. معاینه خارج دهانی بیمار حاکی از وجود یک برآمدگی با حدود نامشخص، بدون درد بود که به آهستگی در طی ۶ ماه ایجاد شده بود و منجر به عدم تقارن مشهود در صورت شده بود و به درگیری ناحیه خلفی استخوان فک پایین مرتبط بود. در معاینه خارج دهانی، بزرگ شدن با قوام استخوانی را نشان داد که پوست سطحی نرمال بهنظر میرسید (شکل 1A ,1B). هیچ فلج یا اختلال عصبی در ناحیه آسیب دیده شناسایی نشد، اگرچه جابجایی عصب آلوئولار تحتانی تشخیص داده شد. در معاینه داخل دهانی، برآمدگی بدون علامت بالینی در قسمت خلفی فک پایین مشاهده شد. لایه مخاطی رنگ طبیعی نشان میدهد که با پوست پوشانده سازگار بود (شکل 2A , 2B). تورم از ناحیه مولر اول تا بوردر راموس گسترش یافته و در رادیوگرافی تورم کورتکس باکال و لینگوال مشهود بود.
رادیوگرافی پانورامیک و سیتیاسکن (CBCT) برای بررسی ناحیه استفاده شد. راموس و تنه فک پایین درگیر بود. این ناحیه از مولر اول پایین سمت چپ تا ابتدای راموس صعودی امتداد یافته بود. همانطور که در شکل 3A نشان داده شده است. ابعاد این ناحیه ۴۰ میلیمتر در بعد قدامی خلفی، 26/71 میلیمتر در بعد باکولینگوالی و 21/66 میلیمتر در بعد اکلوزواپیکالی در بالای تاج دندان نهفته مولر دوم بود. یک مولر دوم که بهصورت اپیکالی جابجا شده بود نیز در نزدیکی بوردر تحتانی فک پایین مشاهده شد که در ارتباط با لکههای کلسیفیکاسیون اطراف ان بود (شکل 3B). با اینحال، بهنظر میرسد که هر دو صفحه کورتیکال باکال و لینگوال به شدت نازک شدهاند و هیچگونه پرفوراسیون مشهودی در کورتکس نشان نمیدهد. بر اساس یک ارزیابی جامع بالینی و رادیوگرافیک، تشخیصهای افتراقی ابتدایی، ادونتوآملوبلاستوما، تومور پیندبورگ (تومور ادونتوژنیک اپیتلیالی کلسیفیه شونده)، ادونتوم کامپلکس یا کامپاند و کیست ادونتوژنیک کلسیفیه شونده گذاشته شد. پس از ارزیابیهای اولیه بیمار تحت بیهوشی عمومی قرار گرفت و با رویکرد داخل دهانی ضایعه به همراه تاج دندان مولر دوم نهفته همانطور که در شکل4A , 4B نشان داده شده است، خارج شد سپس کورتاژ دیواره های استخوانی اطراف انجام شد. صاف کردن تیزیهای استخوانی نیز به انجام رسید و محل برش با نخ ویکریل ۳-۰ بخیه شد. بافت بهدست آمده از ضایعه تحت بررسی هیستوپاتولوژیک قرار گرفت. بافت به آزمایشگاه پاتولوژی دانشکده دندانپزشکی یزد در محلول ثابت کننده فرمالدئید ۱۰% فرستاده شد. مقاطع به ضخامت ۵ میکرومتر تعبیه شده با پارافین با رنگآمیزی هماتوکسیلین و ائوزین در دمای اتاق طبق پروتکل Bancroft رنگآمیزی شدند (۶). بررسی میکروسکوپی، جزایر، طنابها و رشتههایی از سلولهای شبه املوبلاستی را در یک بافت همبند شل و نابالغ مشابه پاپیلای دندان نشان داد. اجزای کلسیفیه شامل ماتریکس مینایی بازوفیلیک و صفحاتی از دنتین ائوزینوفیلیک در استروما در نزدیکی جزایر فوق مشاهده شد (تصویر5). تشخیص نهایی، آملوبلاستیک فیبروادنتوما مطرح گردید. روند بهبودی بافت نرم بهخوبی سپری شد و در بررسی ۶ ماه بعد عمل روند ترمیم استخوان مطلوب بود و علائمی از عود ضایعه مشاهده نشد (تصویر4C).

تصویر۱ : 1A) نمای خارج دهانی، 2A) نمای داخل دهانی، 1B) نمای خارج دهانی، 2B) نمای داخل دهانی. تصویر2: 3A ,3B) نمای CBCT
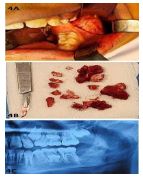
تصویر۲ : 4A) دسترسی داخل دهانی، 48) بیوپسی اکسیژنال، 4C) روند بهبودی ۶ ماه پس از عمل جراحی.
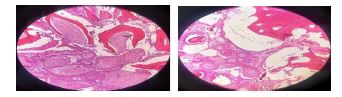
تصویر ۵ : نمای هیستوپاتولوژی ضایعه: جزایری از سلولهای شبه املوبلاستی در یک بافت همبندی همراه با اجزای کلسیفیه ماتریکس مینایی و دنتین
بحث
املوبلاستیک فیبرو ادونتوما (AFO) یک وضعیت پاتولوژیک است که میتواند به عنوان یک نئوپلاسم خوشخیم و مخلوط ادنتوژنیک اهسته پیشرونده طبقهبندی شود (۱). این نوع تومور عمدتاً در استخوانهای فک با میزان بروز کم ۳-۱% مشاهده میشود (۴). مقالات موجود ثابت میکند که AFO عمدتاً نوجوانانی را هدف قرار میدهد که میانگین سنی آنها 3/5±9/4 سال است و اغلب تمایل به بروز در مردان دارد که معمولاً نسبت مرد به زن ۲.۳:۱ میباشد (۷). علاوه بر این، قابلتوجه است که این وضعیت عمدتاً فک پایین را تحت تأثیر قرار میدهد که با نتایج ارائه شده در طبقهبندی WHO در سال ۲۰۰۵ متفاوت است (۸). مقاله اخیر بیان میکند این ضایعه در ماگزیلا و مندیبل و در ناحیه مولری به صورت مساوی مشاهده میشود (۷). بهطور قابلتوجهی، چندین مورد از ضایعه با دندان نهفته یا با جابجایی دندان مربوطه در جهت آپیکالی همراه بود. این مشاهدات نشان میدهد که منشاء ضایعه، بافتهای فولیکول دندانی و عمدتاً لامینای دندانی میباشد (۹). با توجه به طبقهبندی تومورهای ادنتوژنیک WHO در سال ۲۰۲۲، AFO به عنوان مراحل ابتدایی ادونتومای پیچیده دستهبندی شده است (۷). با این حال، سولوک و همکاران (۱۰) یک سری از موارد املوبلاستیک فیبرو ادونتوما (AFO) و ادونتوما را تجزیه و تحلیل کرد و به این نتیجه رسید که AFO افراد بین سنین ۳ تا ۱۶ سال را تحت تأثیر قرار میدهد و اندازه آنها بیش از ۲ سانتیمتر است. در مقابل، ادونتوما معمولاً افراد مسنتری را تحتتأثیر قرار میدهد که محدوده سنی آنها ۲۷ سال و اندازه آنها کمتر از ۲ سانتیمتر است. از اینرو، ضروری است که AFO با اندازههای بیش از ۲ سانتیمتر به عنوان یک نئوپلاسم واقعی نه صرفا یک ادنتوما در نظر گرفته شود (۱۰). ویژگیهای رادیوگرافیک AFO یک رادیولوسنسی مشخص را توصیف میکند که به شکل گرد تا بیضی میباشد. این رادیولوسنسی توسط یک حاشیه اسکلروتیک نازک احاطه شده است که حاوی مقادیر مختلفی از مواد رادیواپک با اندازه و فرم نامنظم است. قابلذکر است، نسبت مناطق رادیواپک به رادیولوسنت ممکن است از یک ضایعه به ضایعه دیگر متفاوت باشد که نشاندهنده منحصربهفرد بودن هر مورد است (۲). گزارش حاضر در یک پسر ۱۰ ساله ثبت شد که با بزرگ شدن بیش از ۴ سانتیمتر در قسمت خلفی فک پایین همراه با لکههای کلسیفیکاسیون که نشاندهنده AFO بود، مراجعه کرد. معاینه هیستوپاتولوژیک میتواند تشخیص دقیقی را برای افتراق ادونتوآملوبلاستوما، ادنتومهای پیچیده، تومور ادنتوژنیک اپیتلیالی کلسیفیه شونده (calcifying epithelial odontogenic tumor )، Ameloblastic Fibroma و Ameloblastic Fibro Dentinoma که دارای ویژگیهای بالینی و رادیولوژیکی مشابه هستند ارائه دهد (۱). ادونتوآملوبلاستوما ترکیبی از ادونتوما پیچیده و آملوبلاستوم با ماهیت تهاجمی است که در آملوبلاستومای کلاسیک مشاهده میشود. از نظر رادیوگرافی، ادونتو املوبلاستوما نشان دهنده یک رادیولوسنسی تک حفرهای است که با مولرهای نهفته مرتبط است و حاوی مواد اپک میباشد. آنها ممکن است سوراخ شدن کورتکس استخوانی را نشان دهند که از ویژگیهای AFO نیست. از نظر بافتشناسی، ادونتواملوبلاستوما استرومای بالغ را با جزایر اپیتلیال سلولهای آملوبلاستیک و کلسیفیکاسیون نشان میدهد (۱۱). یک بحث جاری و در حال انجام در مورد در نظر گرفتن AF (املوبلاستیک فیبروما)، AFO (املوبلاستیک فیبرو ادونتوما)، AFD (املوبلاستیک فیبرو دنتینوما ) و ادونتوما بهعنوان موجودیتهای متمایز یا مراحل مختلف در روند رشد odontomas وجود دارد (۱۰). طبق طبقهبندی WHO در سال ۲۰۱۷، ضایعات خاصی که شباهت هیستوپاتولوژیک به AFO نشان میدهند، احتمالاً نشاندهنده ایجاد ادنتوم هستند (۳). علاوه بر این، قابلقبول است که ظاهر هیستوپاتولوژیک یک AFO از ظاهر ادنتوما در حال توسعه غیر قابل تشخیص باشد. در چنین مواردی، ارزیابی ویژگیهای بالینی و رادیولوژی همزمان ممکن است ابزار ارزشمندی برای ایجاد تمایز تشخیصی باشد. از نظر هیستوپاتولوژیکی، ذکر این نکته ضروری است که یک CEOT (calcifying epithelial odontogenic tumor) با حضور قابلتوجه سلولهای اپیتلیال، مواد شبهآمیلوئید ائوزینوفیلیک و کلسیفیکاسیون مشخص میشود. سلولهای اپیتلیال سازمان یافتهاند و صفحاتی را تشکیل میدهند که از نظر شکل و ساختار چند ضلعی هستند. علاوه بر این، سلولها دارای سیتوپلاسم شفاف تا ائوزینوفیلیک و هستههای وزیکولار برجسته هستند (۱۲). با اینحال، قابلتوجه است که ویژگیهای ذکر شده در موردیکه در اینجا توضیح داده شد وجود نداشت. از نظر میکروسکوپی، AF رشتههای مختلف و جزایر کوچکی از اپیتلیوم ادنتوژنیک را شامل میشود. با اینحال، بر خلاف ساختارهای اندام مانند مینا که معمولاً در AFO (املوبلاستیک فیبروادونتوما) مشاهده میشوند، AF (املوبلاستیک فیبروما) چنین ساختارهایی را ندارد. علاوه بر این، عناصر فیبری در AF ممکن است از بافت کلاژنی سلولی تا بالغ متغیر باشد. با وجود این واقعیت، قابلتوجه است که ظاهر اولیه پاپیلا مانند دندان در AF آشکار نیست (۱۳). علاوه بر این، جزء اکتومزانشیمی AFO شباهت قابلتوجهی به پاپیلای دندانی دارد. AFO شباهتهایی با AFD دارد. با اینحال، AFO حاوی مواد مینا و عاجی میباشد، در حالیکه AFD (املوبلاستیک فیبرو دنتینوما ) تنها شامل مواد عاجی است. در نتیجه، میتوان اشاره کرد که با مشاهده نمای رادیوگرافی، ویژگیهای AFO مستلزم حضور بیشتر عناصر اپک متراکم در داخل ضایعه در مقایسه با AFD است. تفاوت قابل مشاهده در رادیولوژی بین AFD و AFO بهطور مشخص بهواسطه ماهیت مولتی لاکولار ضایعات AFD مشهود است که آنها را از ضایعات یونی لاکولار AFO متمایز میکند (۱۴). از نظر رادیولوژی و بافتشناسی، برخلاف AFO، ادونتوما شامل یک جزء کلسیفیه واضح است که از مینا، عاج، سمنتوم و پالپ بافت همبند تشکیل شده است. اجزای فوق در مراحل پیشرفته ادنتوم کامپاند مشاهده میشوند، جاییکه بلوغ دهانی به حالت کامل میرسد (۱۰). در موردیکه در مطالعه حاضر توضیح داده شد، AFO اندازه قابلتوجهی بیش از ۴ سانتیمتر را نشان داد و به خوبی با حداقل تمایل به تهاجم موضعی محصور شد. در نتیجه، درمان توصیه شده شامل مداخله جراحی محافظهکارانه انوکلیشن همراه با کشیدن دندانی که رویش نیافته می باشد. با اینحال، شایان ذکر است که موارد مستندی وجود دارد که در آن دندانهای درگیر حفظ شدهاند (۱6،۱5). علیرغم تمایل محدود ضایعه به عود، مواردی وجود داشته است که درمان محافظهکارانه با هدف حفظ دندانهای مرتبط گزارشهایی از عود را به همراه داشته است (۱۵). در نتیجه، برای از بین بردن احتمال عود، مولر دوم رشد نکرده همراه با انوکلیشن AFO خارج شد.
نتیجهگیری
ویژگیهای بالینی و رادیوگرافی AFO(املوبلاستیک فیبروادونتوما) برای تشخیص قطعی کافی نیست و تشخیص آن را میتوان تنها با یک بررسی بافتشناسی تعیین کرد. اگر چه املوبلاستیک فیبروادونتوما شیوع کمی دارد ولی لازم است که در ضایعات رادیولوسنت داخل دهانی کودکان که حاوی مواد رادیواپک میباشند در تشخیص افتراقی در نظر گرفته شود. با توجه به رفتار خوشخیم، حداقل تهاجم به ساختارهای اطراف و میزان عود کم، روش درمانی ترجیحی یک رویکرد محافظهکارانه است که شامل انوکلیشن ضایعه و کشیدن دندان نهفته برای جلوگیری از عودهای بعدی است. مورد شرح داده شده در مطالعه حاضر سیر بهبودی مطلوبی را بعد از عمل از خود نشان داد. همچنین در بررسیهای بعد عمل علائمی از عود مشاهده نشد. با توجه به پتانسیل تبدیل املوبلاستیک فیبروادونتوما و املوبلاستیک فیبروما به املوبلاستیک فیبروسارکوما و مشکلات مدیریت بدخیمی در کودکان، خارجسازی کامل و سریع این ضایعه و فالوآپ طولانیمدت آن توصیه میشود (۱۷) .
سپاسگزاری
از تمامی کسانی که در روند تشخیص و درمان و فالوآپ بیمار کمک کردند نهایت سپاسگزاری را دارم.
حامی مالی: ندارد
تعارض در منافع: وجود ندارند.
ملاحظات اخلاقی
این گزارش موردی با رعایت تمامی موازین اخلاقی وکسب رضایت اگاهانه از بیمار و همچنین با کسب کد اخلاق به شماره IR.SSU.SRH.REC.1403.006 از کمیته اخلاق بیمارستان شهید رهنمون انجام شده است.
مشارکت نویسندگان
در ایده، نگارش و ویرایش مقاله کلیه نویسندگان مشارکت داشتند.
املوبلاستیک فیبروادونتوما (AFO) یک نئوپلاسم ادنتوژنیک اپیتلیالی - مزانشیمی نادر و بهتدریج پیشرونده است (۱). این ضایعه ویژگیهای بافتشناسی و بیولوژیکی مشابه املوبلاستیک فیبروما (AF) را نشان میدهد. با اینحال، در املوبلاستیک فیبرو ادونتوما (AFO)، یک یا چند کانون سلولی اپیتلیوم القایی در طول فرآیند تمایز باقی میماند که منجر به تولید مینا و عاج میشود (۲). با توجه به انتشار سال ۲۰۱۷ طبقهبندی سازمان بهداشت جهانیWHO املوبلاستیک فیبروادونتوما بهتر است بهعنوان ادونتوما دستهبندی شود (۳). معمولاً در افراد جوانتر ظاهر میشود و هیچ تمایل قابلتوجهی به هیچیک از دو جنس نشان نمیدهد. مشاهده شده است که با فراوانی یکسانی در فک بالا و فک پایین رخ میدهد و محل بروز آن در ناحیه خلفی پرمولرها و مولرها است (۴). تشخیص املوبلاستیک فیبروادونتوما با تکیه بر شواهد بالینی و رادیوگرافی چالش برانگیز است و برای تشخیص قطعی نیاز به بررسی پاتولوژیک دارد (۱). شرایط و علائم بالینی نقش مهمی در تعیین روشهای نمونهبرداری و امکان حفظ دندانهای واقع در نزدیکی ضایعه، ایفا میکند (۵). با توجه به سیر کلینیکی خوشخیم و شواهد رادیولوژیکی از جمله بوردر مشخص و کورتیکه و همچنین عدم پرفوراسیون کورتکس عمل جراحی اولیه بهصورت بیوپسی اکسیژنال انجام میشود که ضایعه بهصورت کامل از استخوان اطراف کورتاژ میشود. مطالعه حاضر مورد بالینی یک فرد ۱۰ ساله مبتلا به املوبلاستیک فیبرو ادونتوما (AFO)را با یک ضایعه در ناحیه خلف فک پایین که از طریق انوکلیشن مدیریت شد، توصیف میکند.
گزارش مورد:
یک پسر نوجوان ۱۰ ساله در اسفند ۱۳۹۹ با شکایت اصلی تورم سمت چپ صورت به بخش جراحی دهان و فک و صورت دانشکده دندانپزشکی یزد ارجاع شد. سوابق پزشکی بیمار هیچ یافته قابلتوجهی را نشان نداد و سابقه دندانی هیچ شواهدی از آسیب موضعی یا فعالیت عفونی در محل ضایعه را نشان نداد. معاینه خارج دهانی بیمار حاکی از وجود یک برآمدگی با حدود نامشخص، بدون درد بود که به آهستگی در طی ۶ ماه ایجاد شده بود و منجر به عدم تقارن مشهود در صورت شده بود و به درگیری ناحیه خلفی استخوان فک پایین مرتبط بود. در معاینه خارج دهانی، بزرگ شدن با قوام استخوانی را نشان داد که پوست سطحی نرمال بهنظر میرسید (شکل 1A ,1B). هیچ فلج یا اختلال عصبی در ناحیه آسیب دیده شناسایی نشد، اگرچه جابجایی عصب آلوئولار تحتانی تشخیص داده شد. در معاینه داخل دهانی، برآمدگی بدون علامت بالینی در قسمت خلفی فک پایین مشاهده شد. لایه مخاطی رنگ طبیعی نشان میدهد که با پوست پوشانده سازگار بود (شکل 2A , 2B). تورم از ناحیه مولر اول تا بوردر راموس گسترش یافته و در رادیوگرافی تورم کورتکس باکال و لینگوال مشهود بود.
رادیوگرافی پانورامیک و سیتیاسکن (CBCT) برای بررسی ناحیه استفاده شد. راموس و تنه فک پایین درگیر بود. این ناحیه از مولر اول پایین سمت چپ تا ابتدای راموس صعودی امتداد یافته بود. همانطور که در شکل 3A نشان داده شده است. ابعاد این ناحیه ۴۰ میلیمتر در بعد قدامی خلفی، 26/71 میلیمتر در بعد باکولینگوالی و 21/66 میلیمتر در بعد اکلوزواپیکالی در بالای تاج دندان نهفته مولر دوم بود. یک مولر دوم که بهصورت اپیکالی جابجا شده بود نیز در نزدیکی بوردر تحتانی فک پایین مشاهده شد که در ارتباط با لکههای کلسیفیکاسیون اطراف ان بود (شکل 3B). با اینحال، بهنظر میرسد که هر دو صفحه کورتیکال باکال و لینگوال به شدت نازک شدهاند و هیچگونه پرفوراسیون مشهودی در کورتکس نشان نمیدهد. بر اساس یک ارزیابی جامع بالینی و رادیوگرافیک، تشخیصهای افتراقی ابتدایی، ادونتوآملوبلاستوما، تومور پیندبورگ (تومور ادونتوژنیک اپیتلیالی کلسیفیه شونده)، ادونتوم کامپلکس یا کامپاند و کیست ادونتوژنیک کلسیفیه شونده گذاشته شد. پس از ارزیابیهای اولیه بیمار تحت بیهوشی عمومی قرار گرفت و با رویکرد داخل دهانی ضایعه به همراه تاج دندان مولر دوم نهفته همانطور که در شکل4A , 4B نشان داده شده است، خارج شد سپس کورتاژ دیواره های استخوانی اطراف انجام شد. صاف کردن تیزیهای استخوانی نیز به انجام رسید و محل برش با نخ ویکریل ۳-۰ بخیه شد. بافت بهدست آمده از ضایعه تحت بررسی هیستوپاتولوژیک قرار گرفت. بافت به آزمایشگاه پاتولوژی دانشکده دندانپزشکی یزد در محلول ثابت کننده فرمالدئید ۱۰% فرستاده شد. مقاطع به ضخامت ۵ میکرومتر تعبیه شده با پارافین با رنگآمیزی هماتوکسیلین و ائوزین در دمای اتاق طبق پروتکل Bancroft رنگآمیزی شدند (۶). بررسی میکروسکوپی، جزایر، طنابها و رشتههایی از سلولهای شبه املوبلاستی را در یک بافت همبند شل و نابالغ مشابه پاپیلای دندان نشان داد. اجزای کلسیفیه شامل ماتریکس مینایی بازوفیلیک و صفحاتی از دنتین ائوزینوفیلیک در استروما در نزدیکی جزایر فوق مشاهده شد (تصویر5). تشخیص نهایی، آملوبلاستیک فیبروادنتوما مطرح گردید. روند بهبودی بافت نرم بهخوبی سپری شد و در بررسی ۶ ماه بعد عمل روند ترمیم استخوان مطلوب بود و علائمی از عود ضایعه مشاهده نشد (تصویر4C).

تصویر۱ : 1A) نمای خارج دهانی، 2A) نمای داخل دهانی، 1B) نمای خارج دهانی، 2B) نمای داخل دهانی. تصویر2: 3A ,3B) نمای CBCT

تصویر۲ : 4A) دسترسی داخل دهانی، 48) بیوپسی اکسیژنال، 4C) روند بهبودی ۶ ماه پس از عمل جراحی.

تصویر ۵ : نمای هیستوپاتولوژی ضایعه: جزایری از سلولهای شبه املوبلاستی در یک بافت همبندی همراه با اجزای کلسیفیه ماتریکس مینایی و دنتین
بحث
املوبلاستیک فیبرو ادونتوما (AFO) یک وضعیت پاتولوژیک است که میتواند به عنوان یک نئوپلاسم خوشخیم و مخلوط ادنتوژنیک اهسته پیشرونده طبقهبندی شود (۱). این نوع تومور عمدتاً در استخوانهای فک با میزان بروز کم ۳-۱% مشاهده میشود (۴). مقالات موجود ثابت میکند که AFO عمدتاً نوجوانانی را هدف قرار میدهد که میانگین سنی آنها 3/5±9/4 سال است و اغلب تمایل به بروز در مردان دارد که معمولاً نسبت مرد به زن ۲.۳:۱ میباشد (۷). علاوه بر این، قابلتوجه است که این وضعیت عمدتاً فک پایین را تحت تأثیر قرار میدهد که با نتایج ارائه شده در طبقهبندی WHO در سال ۲۰۰۵ متفاوت است (۸). مقاله اخیر بیان میکند این ضایعه در ماگزیلا و مندیبل و در ناحیه مولری به صورت مساوی مشاهده میشود (۷). بهطور قابلتوجهی، چندین مورد از ضایعه با دندان نهفته یا با جابجایی دندان مربوطه در جهت آپیکالی همراه بود. این مشاهدات نشان میدهد که منشاء ضایعه، بافتهای فولیکول دندانی و عمدتاً لامینای دندانی میباشد (۹). با توجه به طبقهبندی تومورهای ادنتوژنیک WHO در سال ۲۰۲۲، AFO به عنوان مراحل ابتدایی ادونتومای پیچیده دستهبندی شده است (۷). با این حال، سولوک و همکاران (۱۰) یک سری از موارد املوبلاستیک فیبرو ادونتوما (AFO) و ادونتوما را تجزیه و تحلیل کرد و به این نتیجه رسید که AFO افراد بین سنین ۳ تا ۱۶ سال را تحت تأثیر قرار میدهد و اندازه آنها بیش از ۲ سانتیمتر است. در مقابل، ادونتوما معمولاً افراد مسنتری را تحتتأثیر قرار میدهد که محدوده سنی آنها ۲۷ سال و اندازه آنها کمتر از ۲ سانتیمتر است. از اینرو، ضروری است که AFO با اندازههای بیش از ۲ سانتیمتر به عنوان یک نئوپلاسم واقعی نه صرفا یک ادنتوما در نظر گرفته شود (۱۰). ویژگیهای رادیوگرافیک AFO یک رادیولوسنسی مشخص را توصیف میکند که به شکل گرد تا بیضی میباشد. این رادیولوسنسی توسط یک حاشیه اسکلروتیک نازک احاطه شده است که حاوی مقادیر مختلفی از مواد رادیواپک با اندازه و فرم نامنظم است. قابلذکر است، نسبت مناطق رادیواپک به رادیولوسنت ممکن است از یک ضایعه به ضایعه دیگر متفاوت باشد که نشاندهنده منحصربهفرد بودن هر مورد است (۲). گزارش حاضر در یک پسر ۱۰ ساله ثبت شد که با بزرگ شدن بیش از ۴ سانتیمتر در قسمت خلفی فک پایین همراه با لکههای کلسیفیکاسیون که نشاندهنده AFO بود، مراجعه کرد. معاینه هیستوپاتولوژیک میتواند تشخیص دقیقی را برای افتراق ادونتوآملوبلاستوما، ادنتومهای پیچیده، تومور ادنتوژنیک اپیتلیالی کلسیفیه شونده (calcifying epithelial odontogenic tumor )، Ameloblastic Fibroma و Ameloblastic Fibro Dentinoma که دارای ویژگیهای بالینی و رادیولوژیکی مشابه هستند ارائه دهد (۱). ادونتوآملوبلاستوما ترکیبی از ادونتوما پیچیده و آملوبلاستوم با ماهیت تهاجمی است که در آملوبلاستومای کلاسیک مشاهده میشود. از نظر رادیوگرافی، ادونتو املوبلاستوما نشان دهنده یک رادیولوسنسی تک حفرهای است که با مولرهای نهفته مرتبط است و حاوی مواد اپک میباشد. آنها ممکن است سوراخ شدن کورتکس استخوانی را نشان دهند که از ویژگیهای AFO نیست. از نظر بافتشناسی، ادونتواملوبلاستوما استرومای بالغ را با جزایر اپیتلیال سلولهای آملوبلاستیک و کلسیفیکاسیون نشان میدهد (۱۱). یک بحث جاری و در حال انجام در مورد در نظر گرفتن AF (املوبلاستیک فیبروما)، AFO (املوبلاستیک فیبرو ادونتوما)، AFD (املوبلاستیک فیبرو دنتینوما ) و ادونتوما بهعنوان موجودیتهای متمایز یا مراحل مختلف در روند رشد odontomas وجود دارد (۱۰). طبق طبقهبندی WHO در سال ۲۰۱۷، ضایعات خاصی که شباهت هیستوپاتولوژیک به AFO نشان میدهند، احتمالاً نشاندهنده ایجاد ادنتوم هستند (۳). علاوه بر این، قابلقبول است که ظاهر هیستوپاتولوژیک یک AFO از ظاهر ادنتوما در حال توسعه غیر قابل تشخیص باشد. در چنین مواردی، ارزیابی ویژگیهای بالینی و رادیولوژی همزمان ممکن است ابزار ارزشمندی برای ایجاد تمایز تشخیصی باشد. از نظر هیستوپاتولوژیکی، ذکر این نکته ضروری است که یک CEOT (calcifying epithelial odontogenic tumor) با حضور قابلتوجه سلولهای اپیتلیال، مواد شبهآمیلوئید ائوزینوفیلیک و کلسیفیکاسیون مشخص میشود. سلولهای اپیتلیال سازمان یافتهاند و صفحاتی را تشکیل میدهند که از نظر شکل و ساختار چند ضلعی هستند. علاوه بر این، سلولها دارای سیتوپلاسم شفاف تا ائوزینوفیلیک و هستههای وزیکولار برجسته هستند (۱۲). با اینحال، قابلتوجه است که ویژگیهای ذکر شده در موردیکه در اینجا توضیح داده شد وجود نداشت. از نظر میکروسکوپی، AF رشتههای مختلف و جزایر کوچکی از اپیتلیوم ادنتوژنیک را شامل میشود. با اینحال، بر خلاف ساختارهای اندام مانند مینا که معمولاً در AFO (املوبلاستیک فیبروادونتوما) مشاهده میشوند، AF (املوبلاستیک فیبروما) چنین ساختارهایی را ندارد. علاوه بر این، عناصر فیبری در AF ممکن است از بافت کلاژنی سلولی تا بالغ متغیر باشد. با وجود این واقعیت، قابلتوجه است که ظاهر اولیه پاپیلا مانند دندان در AF آشکار نیست (۱۳). علاوه بر این، جزء اکتومزانشیمی AFO شباهت قابلتوجهی به پاپیلای دندانی دارد. AFO شباهتهایی با AFD دارد. با اینحال، AFO حاوی مواد مینا و عاجی میباشد، در حالیکه AFD (املوبلاستیک فیبرو دنتینوما ) تنها شامل مواد عاجی است. در نتیجه، میتوان اشاره کرد که با مشاهده نمای رادیوگرافی، ویژگیهای AFO مستلزم حضور بیشتر عناصر اپک متراکم در داخل ضایعه در مقایسه با AFD است. تفاوت قابل مشاهده در رادیولوژی بین AFD و AFO بهطور مشخص بهواسطه ماهیت مولتی لاکولار ضایعات AFD مشهود است که آنها را از ضایعات یونی لاکولار AFO متمایز میکند (۱۴). از نظر رادیولوژی و بافتشناسی، برخلاف AFO، ادونتوما شامل یک جزء کلسیفیه واضح است که از مینا، عاج، سمنتوم و پالپ بافت همبند تشکیل شده است. اجزای فوق در مراحل پیشرفته ادنتوم کامپاند مشاهده میشوند، جاییکه بلوغ دهانی به حالت کامل میرسد (۱۰). در موردیکه در مطالعه حاضر توضیح داده شد، AFO اندازه قابلتوجهی بیش از ۴ سانتیمتر را نشان داد و به خوبی با حداقل تمایل به تهاجم موضعی محصور شد. در نتیجه، درمان توصیه شده شامل مداخله جراحی محافظهکارانه انوکلیشن همراه با کشیدن دندانی که رویش نیافته می باشد. با اینحال، شایان ذکر است که موارد مستندی وجود دارد که در آن دندانهای درگیر حفظ شدهاند (۱6،۱5). علیرغم تمایل محدود ضایعه به عود، مواردی وجود داشته است که درمان محافظهکارانه با هدف حفظ دندانهای مرتبط گزارشهایی از عود را به همراه داشته است (۱۵). در نتیجه، برای از بین بردن احتمال عود، مولر دوم رشد نکرده همراه با انوکلیشن AFO خارج شد.
نتیجهگیری
ویژگیهای بالینی و رادیوگرافی AFO(املوبلاستیک فیبروادونتوما) برای تشخیص قطعی کافی نیست و تشخیص آن را میتوان تنها با یک بررسی بافتشناسی تعیین کرد. اگر چه املوبلاستیک فیبروادونتوما شیوع کمی دارد ولی لازم است که در ضایعات رادیولوسنت داخل دهانی کودکان که حاوی مواد رادیواپک میباشند در تشخیص افتراقی در نظر گرفته شود. با توجه به رفتار خوشخیم، حداقل تهاجم به ساختارهای اطراف و میزان عود کم، روش درمانی ترجیحی یک رویکرد محافظهکارانه است که شامل انوکلیشن ضایعه و کشیدن دندان نهفته برای جلوگیری از عودهای بعدی است. مورد شرح داده شده در مطالعه حاضر سیر بهبودی مطلوبی را بعد از عمل از خود نشان داد. همچنین در بررسیهای بعد عمل علائمی از عود مشاهده نشد. با توجه به پتانسیل تبدیل املوبلاستیک فیبروادونتوما و املوبلاستیک فیبروما به املوبلاستیک فیبروسارکوما و مشکلات مدیریت بدخیمی در کودکان، خارجسازی کامل و سریع این ضایعه و فالوآپ طولانیمدت آن توصیه میشود (۱۷) .
سپاسگزاری
از تمامی کسانی که در روند تشخیص و درمان و فالوآپ بیمار کمک کردند نهایت سپاسگزاری را دارم.
حامی مالی: ندارد
تعارض در منافع: وجود ندارند.
ملاحظات اخلاقی
این گزارش موردی با رعایت تمامی موازین اخلاقی وکسب رضایت اگاهانه از بیمار و همچنین با کسب کد اخلاق به شماره IR.SSU.SRH.REC.1403.006 از کمیته اخلاق بیمارستان شهید رهنمون انجام شده است.
مشارکت نویسندگان
در ایده، نگارش و ویرایش مقاله کلیه نویسندگان مشارکت داشتند.
References:
1- Cossiez M, Pin DD. A Rare Case of Maxillary Ameloblastic Fibro-Odontoma and a Review of the Literature. J Oral Med Oral Surg 2020; 26(2): 17-22.
2- Bharat D, Vahanwala J, Dabir A, Jobanputra P. Ameloblastic Fibro-Odontoma in the Mandible-Clinical, Radiological and Surgical Aspect. Adv Oral Maxillofac Surg 2021; 2: 100066.
3- Wright JM, Vered M. Update from the 4th Edition of the World Health Organization Classification of Head and Neck Tumours: Odontogenic and Maxillofacial Bone Tumors. Head Neck Pathol 2017; 11: 68-77.
4- Saeed DM, Setty S, Markiewicz MR, Cabay RJ. Ameloblastic Fibro-Odontoma Associated with Paresthesia of the Chin and Lower Lip in a 12-Year-Old Girl. SAGE Open Med Case Rep 2019; 7: 2050313X19870642.
5- Omar N, Ullah A, Ghleilib I, Patel N, Abdelsayed RA. A Locally Aggressive Ameloblastic Fibro-Odontoma: A Case Report and Literature Review. Cureus 2021; 13(12): E20366.
6- Suvarna KS, Layton C, Bancroft JD. Bancroft’s Theory and Practice of Histological Techniques. 8th ed. Elsevier Health Sciences: Amsterdam; 2018: 126-69.
7- Soluk-Tekkesin M, Wright JM. The World Health Organization Classification of Odontogenic Lesions: A Summary of The Changes of the 2022. 5th edition. Turk Patoloji Derg 2022; 38: 168-84.
8- Barnes L, Eveson JW, Reichart P, Sidransky D. World Health Organization Classification of Tumours: Pathology and Genetics, Head and Neck Tumours. Int Agency Res Cancer 2005; 85: 75-81.
9- Thulasirman SK, Thuasidoss G, Prabhu NK, Raja VB. A Rare Case of Ameloblastic Fibro-Odontoma of Mandible with Literature Review. Ann Maxillofac Surg 2018; 8(2): 324-26.
10- Soluk-Tekkesin M, Vered M. Ameloblastic Fibro-Odontoma: At the Crossroad between ‘Developing Odontoma’ and ‘True Odontogenic Tumour’. Head Neck Pathol 2021; 15(4): 1202-11.
11- Sanjai K, Pandey B, Shivalingaiah D, Kumar HM. Odontoameloblastoma: A Report of a Rare Case. J Oral Maxillofacpathol 2018; 22(2): 254-59.
12- Kaushal S, Mathur SR, Vijay M, Rustagi A. Calcifying Epithelial Odontogenic Tumor (Pindborg Tumor) without Calcification: A Rare Entity. J Oral Maxillofac Pathol 2012; 16: 110-2.
13- Nasir A, Khare A, Ali I, Khan MI. Ameloblastic Fibroma: A Case Report. J Oral Maxillofac Pathol 2023; 27 (Suppl 1): S60-S63.
14- Sabu AM, Gandhi S, Singh I, Solanki M, Sakharia AR. Ameloblastic Fibrodentinoma: A Rarity in Odontogenic Tumors. J Maxillofac Oral Surg 2018; 17(4): 444-48.
15- Guerra RC, Carvalho PH, Thieringer FM, Pereira RS, Hochuli-Vieira E. Recurrence of Ameloblastic Fibro-Odontoma in a Child: A Case Report. Craniomaxillofacial Trauma & Reconstruction Open 2020; 5: 1-4.
16- Reis SR, De Freitas CE, Do Espírito Santo AR. Management of Ameloblastic Fibro-Odontoma in a 6-Year-Old Girl Preserving the Associated Impacted Permanent Tooth. J Oral Sci 2007; 49(4): 331-35.
17- Howell RM, Burkes EJ Jr. Malignant Transformation of Ameloblastic Fibro-Odontoma to Ameloblastic Fibrosarcoma. Oral Surg Oral Med Oral Pathol 1977; 43(3): 391-401.
نوع مطالعه: گزارش مورد |
موضوع مقاله:
دندانپزشکی
دریافت: 1403/4/16 | پذیرش: 1403/4/24 | انتشار: 1403/6/15
دریافت: 1403/4/16 | پذیرش: 1403/4/24 | انتشار: 1403/6/15
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |







