دوره 33، شماره 12 - ( اسفند 1404 )
جلد 33 شماره 12 صفحات 9723-9711 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Forghani M S, Jafari F, Mirhosseini H, Avazbakhsh M H. Investigating the Effect of the Injection Speed of the Combination of Neostigmine and Atropine on the Heart Rate of Patients under General Anesthesia in Shahid Rahnamoun Hospital, in Yazd City in 2021. JSSU 2026; 33 (12) :9711-9723
URL: http://jssu.ssu.ac.ir/article-1-6211-fa.html
URL: http://jssu.ssu.ac.ir/article-1-6211-fa.html
فرقانی محمدصالح، جعفری فاطمه، میرحسینی حمید، عوض بخش محمد حسین. بررسی تأثیر سرعت تزریق ترکیب نئوستیگمین و آتروپین بر ضربان قلب در بیماران تحت بیهوشی عمومی در بیمارستان شهید رهنمون یزد در سال 1400. مجله علمي پژوهشي دانشگاه علوم پزشكي شهید صدوقی يزد. 1404; 33 (12) :9711-9723
متن کامل [PDF 833 kb]
(11 دریافت)
| چکیده (HTML) (12 مشاهده)
References:
1- Shaydenfish D, Scheffenbichler FT, Kelly BJ, Lihn AL, Deng H, Nourmahnad A, et al. Effects of Anticholinesterase Reversal Under General Anesthesia on Postoperative Cardiovascular Complications: A Retrospective Cohort Study. Anesthesia and analgesia 2020; 130(3): 685-95.
2- Arbabpour R, Ganji Fard M, Tabiee S, Saadatjoo SA. The Effect of Bi-Spectral Index on Recovery and Postoperative Complications in Patients Undergoing Caesarean section. Journal of Birjand University of Medical Sciences. 2015;22(2):94-103.
3- Luo J, Chen S, Min S, Peng L. Reevaluation and update on efficacy and safety of neostigmine for reversal of neuromuscular blockade. Therapeutics and Clinical Risk Management 2018; 14: 2397.
4- Brown EN, Purdon PL, Van Dort CJ. General Anesthesia and Altered States of Arousal: A Systems Neuroscience Analysis. Annual Review of Neuroscience 2011; 34: 601-28.
5- Jabal Ameli M, Izadi-Mood N, Sharif M, Shafa A, Shetabi H. Evaluation of Hemodynamic and O2sat Conditions. Scientific Journal of Ilam University Of Medical Sciences 2011; 19(3): 51-6.
6- Oh TK, Ryu J-H, Nam S, Oh A-Y. Association of neuromuscular reversal by sugammadex and neostigmine with 90-day mortality after non-cardiac surgery. BMC anesthesiology 2020; 20(1): 1-11.
7- Dhande K, Kshirsagar J, Dhande A, Patil N, V Jr P. Hemodynamic Stability, Patient Acceptance and Cost of Intravenous Propofol and Inhalational Sevoflurane for Induction of Anaesthesia: A Prospective, Randomized Comparative Study. Cureus 2020; 12(4).
8- Kawasaki S, Kiyohara C, Tokunaga S, Hoka S. Prediction of hemodynamic fluctuations after induction of general anesthesia using propofol in non-cardiac surgery: a retrospective cohort study. BMC anesthesiology. 2018;18(1):167.
9- Murphy G, Kopman A. “To Reverse or Not To Reverse?”: The Answer Is Clear! Survey of Anesthesiology. 2017; 61(1): 24.
10- Bohringer C, Liu H. Is it always necessary to reverse the neuromuscular blockade at the end of surgery? Journal of Biomedical Research 2019; 33(4): 217.
11- Boon M, Martini C, Dahan A. Recent advances in neuromuscular block during anesthesia. F1000Research. 2018; 7.
12- Hristovska AM, Duch P, Allingstrup M, Afshari A. The comparative efficacy and safety of sugammadex and neostigmine in reversing neuromuscular blockade in adults. A Cochrane systematic review with meta‐analysis and trial sequential analysis. Anaesthesia 2018; 73(5): 631-41.
13- Fuchs‐Buder T, Mencke T. Use of Reversal Agents in Day Care Procedures (with Special Reference to Postoperative Nausea and Vomiting). European Journal of Anaesthesiology 2001; 18: 53-9.
14- Lien CA, Eikermann M. Neuromuscular Blockers and Reversal Drugs. Pharmacology and Physiology for Anesthesia: Elsevier; 2019: 428-54.
15- Kizilay D, Dal D, Saracoglu KT, Eti Z, Gogus FY. Comparison of Neostigmine and Sugammadex for Hemodynamic Parameters in Cardiac Patients Undergoing Noncardiac Surgery. Journal of Clinical Anesthesia 2016; 28: 30-5.
16- Bali IM, Mirakhur RK. Comparison of Glycopyrrolate, Atropine and Hyoscine in Mixture with Neostigmine for Reversal of Neuromuscular Block Following Closed Mitral Valvotomy. Acta Anaesthesiol Scand 1980; 24(4): 331-5.
17- Brull SJ, Kopman AF. Current Status of Neuromuscular Reversal and Monitoring: Challenges and Opportunities. Anesthesiology 2017; 126(1): 173-90.
18- Pani N, Dongare PA, Mishra RK. Reversal Agents in Anaesthesia and Critical Care. Indian journal of anaesthesia 2015; 59(10): 664.
19- Yamashita Y, Takasusuki T, Kimura Y, Komatsuzaki M, Yamaguchi S. Effects of Neostigmine and Sugammadex for Reversal of Neuromuscular Blockade on QT Dispersion Under Propofol Anesthesia: A Randomized Controlled Trial. Cardiology and Therapy 2018; 7(2): 163-72.
20- Tribuddharat S, Sathitkarnmanee T, Naewthong P. Less Tachycardia in Adults When Using Atropine 0.9 Mg Compared With 1.2 Mg Plus Neostigmine 2.5 Mg. J Med Assoc Thai 2008; 91(5): 665-8
21- Salem M, Ylagan L, Angel J, Vedam V, Collins V. Reversal of Curarization with Atropine-Neostigmine Mixture in Patients with Congenital Cardiac Disease. British Journal of Anaesthesia 1970; 42(11): 991-8.
22- Goldhill D. Reversal of Neuromuscular Block: Optimum Dosage of Neostigmine. J R Soc Med 1986; 79(6): 372-3.
23- Kjellberg M, Tammisto T. Heart‐Rate Changes after Atropine and Neostigmine Given for the Reversion of Muscle Paralysis. Acta Anaesthesiol Scand 1970; 14(3): 203-10.
24- Zeidan A, Baraka A. Ventricular Fibrillation Following Atropine‐Neostigmine Mixture in A Patient with Undiagnosed Mitral Valve Prolapse. Anaesthesia 2005; 60(7): 724-5.
25- Salem MR, Toyama T, Wong AY, Jacobs HK, Bennett EJ. Haemodynamic Responses to Antagonism of Bocurarine Block with Atropine-Neostigmine Mixture in Children. Br J Anaesth 1977; 49(9): 901-5.
26- Mirakhur R. Antagonism of Neuromuscular Block in The Elderly: A Comparison of Atropine and Glycopyrronium in A Mixture with Neostigmine. Anaesthesia 1985; 40(3): 254-8.
27- Rosner V, Kepes E, Foldes F. The Effects of Atropine and Neostigmine on Heart Rate and Rhythm. British Journal of Anaesthesia 1971; 43(11): 1066-74.
28- Harper K, Bali I, Gibson F, Carlisle R, Black I, Grainger D, et al. Reversal of Neuromuscular Block: Heart Rate Changes with Slow Injection of Neostigmine and Atropine Mixtures. Anaesthesia 1984; 39(8): 772-5.
29- OVASSAPIAN A. Effects of Administration of Atropine and Neostigmine in Man. Anesthesia & Analgesia 1969; 48(2): 219-23.
30- Limapichat R, Phuphiphat L, Pulnitiporn A. A Randomized Controlled Comparison of Difference Heart Rate after the Reversal of Non-Depolarized Muscle Relaxant with Atropine 0.6 Mg, 0.9 Mg and 1.2 Mg Plus Neostigmine 2.5 Mg. Thai J Anesthesiol 2017; 43(2): 135-43.
متن کامل: (6 مشاهده)
مقدمه
سالانه بیش از 230 میلیون عمل جراحی برای درمان بسیاری از بیماریها در سراسر جهان صورت میگیرد (1,2). بیهوشی عمومی در غالب موارد برای انجام عمل جراحی ضروری و اجتنابناپذیر است، زیرا با کاهش تحریکات و استرس حین جراحی، انجام ایمن و صحیح امور جراحی و غیرجراحی را فراهم می کند (3-5). پروپوفول به دلیل ایمنی نسبی، گشاد شدن خفیف برونشها از رایجترین داروهای خوابآور برای القای بیهوشی است. با اینحال ممکن است باعث عوارض جانبی مانند؛ ترومبوفلبیت و سرکوب تنفسی در هنگام تزریق و تضعیف قلبی عروقی شود. علاوه بر این، تزریق سریع آن، افت فشار خون را بهدنبال دارد که ممکن است منجر به آسیب میوکارد، آسیب کلیوی و مرگ شود (6,7). شل کنندههای عضلانی اغلب از اجزای اساسی روش بیهوشی متعادل است که با اتصال به گیرنده استیلکولین و قطع ارتباط عصب-عضله از انتقال پیام جلوگیری میکنند و برای سهولت مدیریت راه هوایی و تهویه کنترله ،اطمینان از عدم حرکت بیمار و بهبود شرایط جراحی بدون اثرات تضعیف قلبی عروقی استفاده می شود (8-11). با این حال اگر کنترل دوز به درستی انجام نشود عوارض مخرب ایجاد میکند (8). در مطالعهای گزارش شد استفاده از داروهای شل کننده عضلانی، رقابتی با مرگ و میر مرتبط با بیهوشی را به همراه دارد و به دنبال آن اثرات باقیمانده عصبی-عضلانی نشان داد که باعث افزایش عوارض جدی تنفسی و بستری طولانیمدت در دوره بهبودی میشود (12,13). اگرچه بلوک عصبی عضلانی ممکن است خودبهخود بهبود یابد (14) ولی احتمال بروز فلج باقیمانده ناشی از شل کننده عضلانی با اثر متوسط، ۴۰ تا ۶۰ درصد است (13) که لزوم استفاده از عوامل دارویی در پایان عمل برای جلوگیری از فلج احتمالی باقیمانده، دوبینی، ضعف حنجره، احتباس کربندیاکسید و اسیدوز تنفسی،کما، مرگ و پنومونی را نشان میدهد (3,9,14,15) و ازمشکلات شایع بیماران در بخش مراقبت بعد از بیهوشی است (16). داروهای اصلی برای ریورس شل کنندههای عضلانی رقابتی، مهارکنندههای کولین استراز هستند (17). مهارکنندههای کولیناستراز با جلوگیری از تخریب استیلکولین باعث افزایش غلظت آن در محل اتصال عصب- عضله میشوند (18). به دلیل اثرات کولینرژیک استیلکولین که منجر به کاهش ضربان قلب، کاهش فشارخون و ایست ناگهانی قلب، انقباض برونش و افزایش ترشحات راه هوایی و افزایش حرکات روده میشود (11,19). برای به حداقل رساندن این عوارض به همراه آن، داروهای آنتی کولینرژیک مانند آتروپین و گلیکوپیرولات داده میشود که ممکن است منجر به بروز افزایش ضربان قلب، دهان خشک، احتباس ادرار و گشادی برونش شود (11,14). درطی مطالعات صورت گرفته برای مقایسه اثر بین آتروپین وگلیکوپیرولات محققان به این نتیجه رسیدند که گلیکوپیرولات افزایش کمتری در ضربان قلب میدهد و باید داروی انتخابی باشد با این وجود گلیکوپیرولات گرانتر است (15,20) و در کشور ایران در دسترس نیست. بنابراین از آتروپین استفاده میشود. مکانیسم احتمالی بدین گونه است که آتروپین با اتصال به فیبرهای کولینرژیک قلبی با تجمع استیلکولین به رقابت میپردازد و بدین ترتیب خطر اثر نئوستیگمین بر قلب با تاثیر اولیه آتروپین به حداقل میرسد (21). عوامل زیادی ازجمله پاکسازی حلق، درد و مسکن، داروهای بیهوشی مورد استفاده و عمق بیهوشی، سن بیماران، تعادل اسید و باز، نوع عمل و سرعت تزریق ریورس ممکن است بر ضربان قلب اثر بگذارند (23, 22). بیشترین افزایش ضربان قلب بعد از تجویز نئوستیگمین و آتروپین بستگی به ضربان قلب ابتدایی دارد بیمارانی که تعداد ضربان قلب کمتری دارند افزایش شدیدتری در ضربان قلب پیدا میکنند (25, 24). این تغییرات ضربان قلب برای بیماران با بیماری قلبی عروقی، تیروتوکسیکوز، کمبود حجم داخل عروقی و افراد مسن نامطلوب است (26, 20). بسیاری از مرگ و میرهای ناشی از تجویز این دو دارو را بیماران با اختلالات قلبی عروقی دربر میگیرند. نظرات در مورد روش بهینه تجویز کاملا متناقض بهنظر میرسد بهعنوان مثال پیشنهاد شده است که باید تا 15 دقیقه قبل از تجویز نئوستیگمین آتروپین داده شود یا حداقل صبر کرد تا افزایش ضربان قلب ناشی از آتروپین مشخص شود در مقابل در مطالعهای دیگر بیان شده است که نئوستیگمین باید قبل ازآتروپین داده شود (23) اما تغییرات ضربان قلب زمانی که آتروپین و نئوستیگمین بهصورت ترکیبی بهعنوان ریورس داده میشود کمتراست تا بهصورت جداگانه؛ با اینحال افزایش قابلتوجهی در ضربان قلب رخ میدهد که پس از مدتی کاهش مییابد (16). در مطالعهای سرعت تزریق ترکیب نئوستیگمین و آتروپین اثر یکسانی در افزایش اولیه ضربان قلب دارد اما هرچه سرعت تزریق بیشتر باشد کاهش ضربان قلب شدیدتر است (27). با توجه به آنچه اشاره شد، از آنجا که نتایج حاصل از مطالعات مشابه دارای تناقضاتی میباشد و مطالعات انجام شده به تعداد محدود و قدیمی است، مطالعه حاضر با هدف بررسی تأثیر تزریق توأم نئوستیگمین و آتروپین بر تعداد ضربان قلب در بیماران تحت بیهوشی عمومی در بیمارستان شهید رهنمون یزد در سال 1400 انجام شد.
روش بررسی
این مطالعه از نوع کارآزمایی بالینی سه سوکور بود. به گونهای که پژوهشگر از سرعت تزریق توام نئوستیگمین و آتروپین که توسط همکار پژوهشی انجام گرفت، بیاطلاع بود. بیمار هم از آنجاکه در زمان تزریق هوشیار نبود از نوع مداخله اطلاعی نداشت و تحلیلگر آماری هم بادریافت کد، دادهها را آنالیز نموده است. پس ازکسب کد اخلاق ((IR.SSU.REC.1400.210 از سوی دانشگاه علوم پزشکی شهید صدوقی یزد، مطالعه بر روی بیماران بستری که کاندید اعمال جراحی مختلف در سال 1400 در بیمارستان شهید رهنمون یزد بودند، انجام و 69 بیمار (47 مرد، 22 زن) که کاندیداتورهای عمل جراحی (فراوانی هر عمل ارتوپدی 42% جراحی عمومی 20% جراحی چشم 4% و اورولوژی3%) بودند شرکت داده شدند. بهوسیله چک لیست اطلاعات ثبت شد و نمونهها بهطور تصادفی به سه گروه از نظر زمان تزریق ریورس تقسیم شدند. معیار ورود به مطالعه، بیماران با سن بین 50-16 سال، میزان هموگلوبین بالاتر از 14 گرم بر دسیلیتر با بیهوشی کلاس یک ASA.PS بود (American Society of Anesthesiologists – Physical Status). معیار خروج از مطالعه بیماران با خونریزی بیش از 10% حجم خون، دارای اختلالات قلبی، عروقی و تنفسی، دریافت کننده داروهای موثر بر تعداد ضربان قلب یا سیستم عصبی مرکزی و بیماران با سابقه سوءمصرف مواد و حساسیت دارویی وحساسیت به زرده تخم مرغ بود. روش نمونهگیری بهصورت در دسترس و هدفمند بود. حجم نمونه با احتساب 10% ریزش وبا توجه به تجربی بودن مطالعه و مطالعه مشابه (28) 69 نفر (23 نفر در هر یک از سه گروه) که کاندید اعمال جراحی مختلف اعم از ارتوپدی، جراحی عمومی، جراحی چشم و اورولوژی بودند با وضعیت جسمی کلاس1یا2 در رده سنی80 -15 و بدون داشتن بیماری قلبی عروقی وارد مطالعه شدند.. بیماران کاندید عمل جراحی در بخش پره آپ ( بخش قبل از ورود به اتاق عمل) از نظر متغیرهای مطالعه (سن، جنس، نوع عمل، میزان هموگلوبین) مورد بررسی قرارگرفتند. اطلاعات دموگرافیک چک لیست تکمیل و فشار خون توسط دستگاه مانیتورینگ گرفته شد. میزان هموگلوبین با استفاده از آزمایش خون ضمیمه در پرونده بهدست آمد. برای تخصیص شرکتکنندگان به سه گروه مطالعه، از جدول اعداد تصادفی استفاده شد. پس از تعیین یک نقطه شروع تصادفی، اعداد جدول بهصورت پیدرپی خوانده شدند و بر اساس ارقام 1، 2 و 3 (یا باقیمانده تقسیم بر 3)، هر شرکتکننده به یکی از سه گروه مداخله تخصیص یافت. این فرایند تا تکمیل حجم نمونه ادامه یافت. گروه اول 10 ثانیه، گروه دوم 1 دقیقه و گروه سوم 3 دقیقه بود. مراحل بیهوشی توسط کارشناسان هوشبری بیمارستان و ثبت دادهها توسط دانشجو هوشبری انجام گرفت. پیش داروی دریافتی شامل میدازولامmg/kg 05/0 و فنتانیل µg/kg2 بود. القای وریدی بیهوشی با پروپوفول mg/kg5/1 و آتراکوریوم mg/kg 5/0 صورت گرفت. جهت برقراری راه هوایی کلیه بیماران، از لارنژیال ماسک برای کاهش تحریکات حلق و سیستم عصبی اتونوم استفاده شد. از ایزوفلوران 1% و دی نیتروژن اکسید به همراه اکسیژن با نسبت مساوی برای نگهداری بیهوشی استفاده شد و تنفس کنترله بود. با گذشت زمان و در صورت نیاز آتراکوریوم تکرار شد. در پایان بیهوشی، ایزوفلوران حداقل 5 دقیقه و دی نیتروژن اکسید 3 دقیقه قبل از تزریق داروی ریورس قطع شد. بعد از مشاهده کوچکترین تلاش تنفسی، قبل از تزریق ریورس جهت جلوگیری از تحریکات ناخواسته و حفظ عمق بیهوشی mg20 پرپوفول بهصورت بلوس تزریق و سپس µg/kg/min100 ادامه یافت. به منظور کنترل دقیق زمان تزریق، حجم کل دارو به 10 میلیلیتر رسانده شد و برای اطمینان از اثرگذاری ریورس فرصت کافی بین آخرین دوز تکرار داروی شل کننده و شروع تزریق ریورس داده شد. ریورس تزریق گردید و تنفس کنترله ادامه یافت. در طول مدت 10 دقیقه اگر تنفس خودبخودی بیمار برقرار شد برای جلوگیری از تحریک و همچنین پیشگیری از افزایش غلظت کربن دی اکسید شریانی، به ازای هر تنفس خود بهخودی بیمار که ونتیلاتور دریافت و شناسایی کرد یک تنفس مکانیکی با دم و بازدم همزمان به بیمار داده شد. در صورت کفایت تنفس، لارنژیال ماسک خارج و ترشحات دهان و حلق پاکسازی شد. در طی مدت اندازهگیری ضربان قلب، از ساکشن دهان خودداری شد. در چکلیستهایی که برای هر بیمار مهیا شده بود، تعداد ضربان قلب که بهوسیله ECG مانیتورینگ و پالساکسیمتر، درطی زمانهای مشخص شده (قبل از تزریق ریورس و سپس به مدت 10 دقیقه پس از آن با فواصل منظم 1 دقیقه و سپس در دقیقه پانزدهم و بیستم) گرفته شده بود و همچنین میزان خونریزی و مدت زمان عمل جراحی نیز ثبت شد.
تجزیه و تحلیل آماری
در نهایت دادهها توسط نرمافزارversion 16 SPSS و آمار توصیفی مناسب مورد تجزیه و تحلیل قرارگرفت.
نتایج
نتایج این مطالعه نشان میدهد که از لحاظ میانگین سن، جنس و میزان هموگلوبین تفاوت معنیداری نداشتند. جنسیت و سرعت تزریق بر تغییرات تعداد ضربان قلب موثر بوده است به گونهای که میانگین تغییرات ضربان قلب در زنان بیشتر از مردان است (84 به 76) و برخلاف گروه اول و دوم تفاوت چشمگیری درگروه سوم رخ داده و ضربان قلب به سمت نرمال شدن پیش رفته است. میزان هموگلوبین و سن تفاوت معنیداری نداشته است. تغییرات تعداد ضربان قلب گروه سنی 16 تا 20 سال بالاترین میانگین و گروه سنی 21 تا 35 سال پایینترین میانگین را به خود اختصاص داده است، تعداد ضربان قلب در ﮔﺮوه¬های تزریق 3 دقیقه نسبت به گروه تزریق 10 ثانیه و 1 دقیقه کاهش داشته است.
نمرات تعداد ضربان قلب زنان بالاترین میانگین و گروه مردان پایین ترین میانگین را به خود اختصاص داده است. نمرات تعداد ضربان قلب بیماران تحت جراحی های ارتوپدی بالاترین میانگین و گروه بیماران تحت جراحی عمومی پایین ترین میانگین را به خود اختصاص داده است. نمرات تعداد ضربان قلب بیماران با 1 دقیقه تزریق بالاترین میانگین و گروه بیماران با 3 دقیقه تزریق پایین ترین میانگین را به خود اختصاص داده است.در بین میانگین تعدیل شده نمرات تعداد ضربان قلب گروه بیماران با 3 دقیقه تزریق با گروه بیماران با 10 ثانیه و 1 دقیقه تزریق تفاوت معنیدار وجود دارد.
ﻧﺘﺎیﺞ (جدول 1) نشان می¬دهد که اثرات نوع تزریق معنادار است (01/0>P و 913/5= F). یعنی بین سه گروه متفاوت تزریق تفاوت وجود دارد. نتایج حاکی از آن است که میانگین گروه 3 دقیقه تزریق پایین ترین ضربان قلب را داشته اند. ولی اثرات سن (05/0<P و 956/1= F) و اﺛﺮات تعاملی سن و نوع تزریق (05/0<P و 152/1= F) ﻣﻌﻨﺎدار نیست. یعنی سن عامل تاثیرگذاری بر نوع تزریق نیست. نتایج (جدول 2) نشان می¬دهد تغییرات تعداد ضربان قلب گروه سنی 16 تا 20 سال بالاترین میانگین و گروه سنی 21 تا 35 سال پایین ترین میانگین را به خود اختصاص داده است. نتایج (جدول 3) نشان می¬دهد تغییرات تعداد ضربان قلب گروه 10 ثانیه بالاترین میانگین و گروه 3 دقیقه پایین ترین میانگین را به خود اختصاص داده است. نتایج (جدول 4) نشان می¬دهد تغییرات تعداد ضربان قلب گروه تزریق 3 دقیقه نسبت به گروه تزریق 1 دقیقه و 10 ثانیه تفاوت داشته است و ضربان قلب گروه تزریق 3 دقیقه به طور معنی داری از دو گروه دیگر کمتر بوده است. ﻧﺘﺎیﺞ (جدول 5) نشان می¬دهد که اثرات نوع تزریق معنادار است (01/0>P و 913/5= F). یعنی بین سه گروه متفاوت تزریق تفاوت وجود دارد. نتایج حاکی از آن است که میانگین گروه 3 دقیقه تزریق پایین ترین ضربان قلب را داشته اند. اثرات جنسیت (05/0>P و 945/5= F) معنیدار است. ولی اﺛﺮات تعاملی جنسیت و نوع تزریق (05/0<P و 489/0= F) ﻣﻌﻨﺎدار نیست. یعنی جنسیت عامل تاثیرگذاری بر نوع تزریق نیست. نتایج (جدول 6) نشان می¬دهد تغییرات تعداد ضربان قلب زنان بالاترین میانگین و گروه مردان پایین ترین میانگین را به خود اختصاص داده است. همان طور که (جدول7) نشان می¬دهد در بین میانگین تعدیل شده تغییرات تعداد ضربان قلب مردان و زنان تفاوت معنیدار وجود دارد. یعنی میانگین تعداد ضربان قلب زنان در هر سه گروه به طور معنیداری از تعداد ضربان قلب مردان بیشتر است. ﻧﺘﺎیﺞ (جدول 8) نشان می¬دهد که اثرات نوع تزریق معنادار است (01/0>P و 913/5= F). یعنی بین سه گروه متفاوت تزریق تفاوت وجود دارد. نتایج حاکی از آن است که میانگین گروه 3 دقیقه تزریق پایین ترین ضربان قلب را داشته اند. ولی اثرات نوع عمل (05/0<P و 572/0= F) و اﺛﺮات تعاملی نوع عمل و نوع تزریق (05/0<P و 195/0= F) ﻣﻌﻨﺎدار نیست. یعنی نوع عمل عامل تاثیرگذاری بر نوع تزریق نیست. نتایج (جدول9) نشان می¬دهد تغییرات تعداد ضربان قلب بیماران تحت جراحی های ارتوپدی بالاترین میانگین و گروه بیماران تحت جراحی عمومی پایین ترین میانگین را به خود اختصاص داده است. ﻧﺘﺎیﺞ (جدول 10) نشان می¬دهد که اثرات نوع تزریق معنادار است (01/0>P و 913/5= F). یعنی بین سه گروه متفاوت تزریق تفاوت وجود دارد. نتایج حاکی از آن است که میانگین گروه 3 دقیقه تزریق پایین ترین ضربان قلب را داشته اند. ولی اثرات میزان هموگلوبین (05/0<P و 802/0= F) و اﺛﺮات تعاملی میزان هموگلوبین و نوع تزریق (05/0<P و 453/1= F) ﻣﻌﻨﺎدار نیست. یعنی میزان هموگلوبین عامل تاثیرگذاری بر نوع تزریق نیست.
نتایج (جدول 11) نشان می¬دهد تغییرات تعداد ضربان قلب بیماران با هموگلوبین غیرنرمال بالاترین میانگین و گروه بیماران با هموگلوبین نرمال پایین ترین میانگین را به خود اختصاص داده است.
ﻧﺘﺎیﺞ (جدول 12) نشان می¬دهد که اثرات نوع تزریق معنادار است ﺑﺎ ﺗﻮﺟﻪ ﺑﻪ ﻧﻤﻮدار که ﻣﯿﺎﻧﮕﯿﻦ تعداد ضربان قلب در گروهها را ﻧﺸـﺎن ﻣـﯽ¬دﻫـﺪ، تعداد ضربان قلب در ﮔﺮوه¬های تزریق 3 دقیقه نسبت به گروه تزریق 10 ثانیه و 1 دقیقه کاهش داشته است. نتایج (جدول 13) نشان می¬دهد تغییرات تعداد ضربان قلب بیماران با 1 دقیقه تزریق بالاترین میانگین و گروه بیماران با 3 دقیقه تزریق پایین ترین میانگین را به خود اختصاص داده است. همان طور که (جدول 14) نشان می¬دهد در بین میانگین تعدیل شده تغییرات تعداد ضربان قلب گروه بیماران با 3 دقیقه تزریق با گروه بیماران با 10 ثانیه و 1 دقیقه تزریق تفاوت معنیدار وجود داردکه با نتایج کار آقای هارپر (27) همسوست
جدول 1: ﻧﺘﺎیﺞ اﺛﺮات درون ﻓﺮدی ﺑﺮ اﺳﺎس آزﻣﻮن اﻧﺪازهﮔﯿﺮی ﺗﮑﺮاری تغییرات تعداد ضربان قلب بیماران تحت بیهوشی عمومی در بیمارستان شهید رهنمون یزد در سال 1400 در گروه های مورد مطالعه
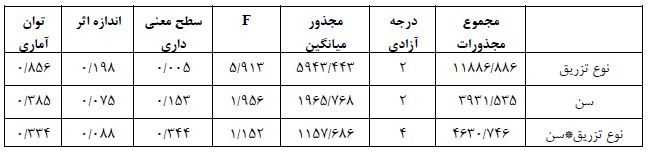
جدول 2: میانگین و انحراف معیار تعدیل شده تغییرات تعداد ضربان قلب

جدول 3: میانگین و انحراف معیار تعدیل شده تغییرات تعداد ضربان قلب
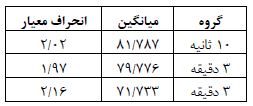
جدول 4: تفاوت زوجی تغییرات تعداد ضربان قلب
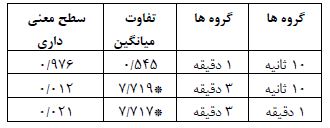
جدول 5: ﻧﺘﺎیﺞ اﺛﺮات درون ﻓﺮدی ﺑﺮ اﺳﺎس آزﻣﻮن اﻧﺪازهﮔﯿﺮی ﺗﮑﺮاری تغییرات تعداد ضربان قلب بیماران تحت بیهوشی عمومی در بیمارستان شهید رهنمون یزد در سال 1400 در گروه های مورد مطالعه
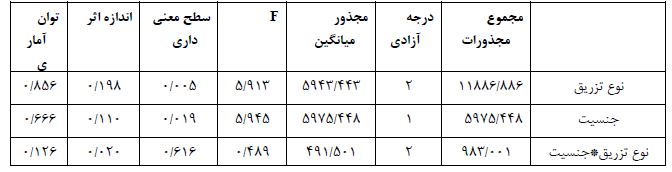
جدول6: میانگین و انحراف معیار تعدیل شده تغییرات تعداد ضربان قلب

جدول 7: مقایسه زوجی تغییرات تعداد ضربان قلب بیماران تحت بیهوشی عمومی در بیمارستان شهید رهنمون یزد در سال 1400 در گروه¬های مورد مطالعه

جدول 8: ﻧﺘﺎیﺞ اﺛﺮات درون ﻓﺮدی ﺑﺮ اﺳﺎس آزﻣﻮن اﻧﺪازهﮔﯿﺮی ﺗﮑﺮاری تغییرات تعداد ضربان قلب بیماران تحت بیهوشی عمومی در بیمارستان شهید رهنمون یزد در سال 1400 در گروه های مورد مطالعه
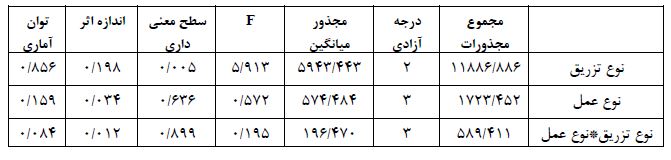
جدول 9: میانگین و انحراف معیار تعدیل شده تغییرات تعداد ضربان قلب
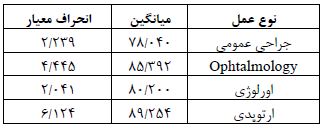
جدول 10: ﻧﺘﺎیﺞ اﺛﺮات درون ﻓﺮدی ﺑﺮ اﺳﺎس آزﻣﻮن اﻧﺪازهﮔﯿﺮی ﺗﮑﺮاری تغییرات تعداد ضربان قلب بیماران تحت بیهوشی عمومی در بیمارستان شهید رهنمون یزد در سال 1400 در گروه های مورد مطالعه
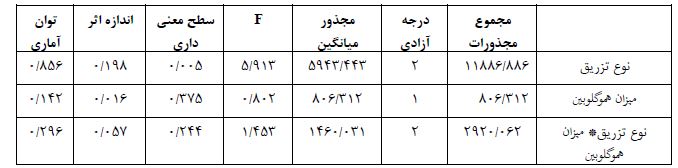
جدول 11: میانگین و انحراف معیار تعدیل شده تغییرات تعداد ضربان قلب
.JPG)
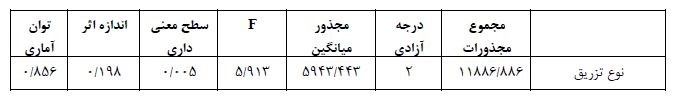
جدول 12: ﻧﺘﺎیﺞ اﺛﺮات درون ﻓﺮدی ﺑﺮ اﺳﺎس آزﻣﻮن اﻧﺪازهﮔﯿﺮی ﺗﮑﺮاری تغییرات تعداد ضربان قلب بیماران تحت بیهوشی عمومی در بیمارستان شهید رهنمون یزد در سال 1400 در گروه های مورد مطالعه
جدول 13: میانگین و انحراف معیار تعدیل شده تغییرات تعداد ضربان قلب

جدول 14: مقایسه زوجی تغییرات تعداد ضربان قلب بیماران تحت بیهوشی عمومی در بیمارستان شهید رهنمون یزد در سال 1400 در گروه¬های مورد مطالعه
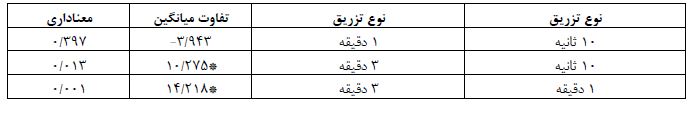
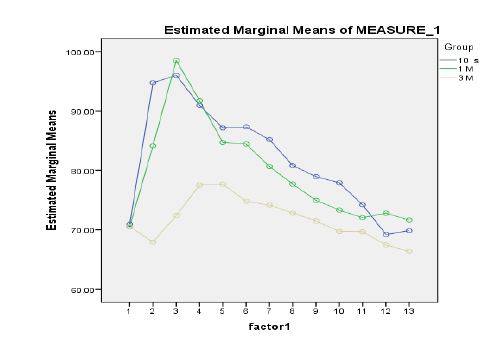
شکل 1: نمودار مقایسه میانگین تغییرات تعداد ضربان قلب بیماران تحت بیهوشی عمومی در بیمارستان شهید رهنمون یزد در سال 1400 در مراحل سیزده گانه در گروه های تزریق 10 ثانیه، 1 دقیقه و 3 دقیقه مورد مطالعه
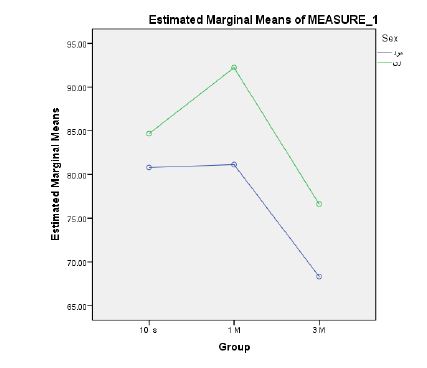
شکل 2: نمودار مقایسه میانگین نمرات تعداد ضربان قلب بیماران تحت بیهوشی عمومی در بیمارستان شهید رهنمون یزد در سال 1400 در مراحل سیزده گانه در گروه های تزریق 10 ثانیه، 1 دقیقه و 3 دقیقه مورد مطالعه
بحث
نتایج حاصل از این مطالعه نشان داد، تزریق ریورس طی3 دقیقه کمترین تغییرات ضربان قلب را به همراه دارد. همچنین میانگین تغییرات ضربان قلب در زنان بیشتر از مردان بود. همسو با این نتایج، در مطالعه ای که با هدف بررسی تاثیر سرعت های مختلف تزریق ترکیب نئوستیگمین و آتروپین بر ریتم و ضربان قلب صورت گرفت، ،تزریق آهسته تر ریورس باعث تاخیر و کاهش در افزایش اولیه ضربان قلب شد (27). در تبیین این شباهت می توان گفت متعاقب تزریق آهسته تر آتروپین اثر مرکزی آن افزایش می یابد که در تضاد با اثر محیطی عمل نموده و میزان افزایش تعداد ضربان قلب به حداقل می رسد. نا همسو با نتایج این مطالعه، در مطالعه ای که با هدف بررسی تاثیرات قلبی تجویز آتروپین و نئوستیگمین در انسان صورت گرفت، مشخص شد که بیشترین افزایش ضربان قلب زمانی است که آتروپین قبل از نئوستیگمین داده شود و بیشترین کاهش در شرایطی است که دو دارو توام باهم (28) یا آتروپین بلافاصله بعد از نئوستیگمین به آرامی داده شود (22). در تبیین این تناقض می توان گفت از آنجا که اثرات مرکزی آتروپین که منجر به برادیکاردی گذرا می شود زودتر از اثرات محیطی آن که تاکیکاردی است شروع می شود لذا طی تزریق قبلی با پشت سر گذاشتن اثر مرکزی باعث تاکیکاردی می شود و تزریق توام آن منجر به همراه شدن اثر پاراسمپاتوممتیکی نئوستیگمین با اثر مرکزی آتروپین شده و شاهد برادیکاردی خواهیم بود و دلیل ثبات بیشتر سیستم قلبی عروقی طی تزریق با سرعت آهسته تر در این مطالعه احتمالا به این علت بود که با کاهش سرعت تزریق توام، تاثیرات یاد شده با ملایمت بیشتری خود را نشان داده و ثبات قلبی عروقی بیشتری را داریم. همراستا با مطالعه حاضر، در مطالعه دیگری که تاثیر جدا و توام تزریق گلیکوپیرولات و نئوستیگمین برای توقف اثر شلکنندههای عضلانی طی بیهوشی عمومی استفاده شد مشخص شد که ثبات قلبی عروقی متعاقب تزریق توام آنها به مراتب بیشتر بود (DOI: https://doi.org/10.53350/pjmhs22169344). در تبیین این شباهت میتوان گفت علت آن یکسان بودن تاثیر آتروپین و گلیکوپیرولات بر گیرندههای M3 موسکارینی میباشد از طرفی تزریق دوزهای بیشتر از 5/0 میلیگرم آتروپین در تثبیت ناپایداری قلبی عروقی ناشی از نئوستیگمین موثرتر عمل می کند. در تبیین تاثیر جنسیت بر اختلاف میانگین تغییرات ضربان قلب در زنان میتوان دلیل آن را تاثیر هورمون تستسترون بر دوره استراحت بطنی دانست که باعث ثبات بیشتر ضربان قلب در مردان بهطورکلی میگردد و در مطالعات مرتبط نیز مشاهده میشود (https://doi.org/10.3389/fphys.2022.831179). بـا توجـه بـه اهمیـت موضـوع، پیشـنهاد میگـردد، تعداد نمونه جهت دستیابی به نتیجه مقبولتر افزایش یابد، دراعمال جراحی تنوع بیشتری صورت گیرد، مشارکت تعداد مساوی از هردوجنسیت جهت حذف تاثیر آن، تکرار کار با سایر داروهای بیهوشی، عدم توجه به تاثیر ساکشن بر ضربان قلب و مشارکت افراد بالای 50 سال در مطالعه انجام گیرد.
نتیجهگیری
نتایج پژوهش حاضر نشان داد؛ متغیرهای جنس و سرعت تزریق توأم نئوستیگمین و آتروپین بر تعداد ضربان قلب در بیماران تحت بیهوشی عمومی موثر بودند. در نتیجه پیشگیری از تغییرات شدید ضربان قلب و ثبات پاسخهای همودینامیک موثر هستند. این یافتهها، تزریق 3 دقیقهای ریورس را بهعنوان یک روش بهینه برای کمترین تغییرات ضربان قلب و در نتیجه، بهبود وضعیت همودینامیک بیماران پس از عملهای جراحی وابسته به تزریق ریورس را تایید میکنند.
سپاسگزاری
با صدور اجازه از بیمارستان شهید دکتر رهنمون بستر انجام این عمل بالینی فراهم شد؛ بدین وسیله از همکاری صمیمانه این مرکز و همچنین کمیته تحقیقات دانشجویی قدردانی میگردد. همچنین از همکاری جناب دکتر میرحسینی که در انجام این طرح تحقیقاتی نهایت همکاری را نمودند، کمال تشکر و قدردانی را داریم.
حامی مالی: ندارد.
تعارض در منافع: وجود ندارد.
ملاحظات اخلاقی
این مطالعه مطابق با اصول اخلاقی اعلامیه هلسینکی انجام شد، تمامی شرکتکنندگان پس از دریافت توضیحات کامل، رضایتنامه آگاهانه را امضا کردند و اطلاعات آنان بهصورت محرمانه نگهداری شد. همچنین مطالعه دارای کد اخلاق به شناسه IR.IAU.B.REC.1401.030 از دانشگاه علوم پزشکی شهید صدوقی یزد می باشد.
مشارکت نویسندگان
محمد صالح فرقانی در نمونه گیری و جمع آوری داده ها و تهیه نسخه نهایی مقاله، فاطمه جعفری نجفآبادی در ارائه ایده و طراحی مطالعه ، حمید میرحسینی درطراحی ونگارش نسخه اولیه مقاله و اصلاح نهائی و محمدحسین عوضبخش در تجزیه و تحلیل دادهها مشارکت داشته و همه نویسندگان در تدوین، ویرایش اولیه و نهایی مقاله و پاسخگویی به سوالات مرتبط با مقاله سهیم هستند.
سالانه بیش از 230 میلیون عمل جراحی برای درمان بسیاری از بیماریها در سراسر جهان صورت میگیرد (1,2). بیهوشی عمومی در غالب موارد برای انجام عمل جراحی ضروری و اجتنابناپذیر است، زیرا با کاهش تحریکات و استرس حین جراحی، انجام ایمن و صحیح امور جراحی و غیرجراحی را فراهم می کند (3-5). پروپوفول به دلیل ایمنی نسبی، گشاد شدن خفیف برونشها از رایجترین داروهای خوابآور برای القای بیهوشی است. با اینحال ممکن است باعث عوارض جانبی مانند؛ ترومبوفلبیت و سرکوب تنفسی در هنگام تزریق و تضعیف قلبی عروقی شود. علاوه بر این، تزریق سریع آن، افت فشار خون را بهدنبال دارد که ممکن است منجر به آسیب میوکارد، آسیب کلیوی و مرگ شود (6,7). شل کنندههای عضلانی اغلب از اجزای اساسی روش بیهوشی متعادل است که با اتصال به گیرنده استیلکولین و قطع ارتباط عصب-عضله از انتقال پیام جلوگیری میکنند و برای سهولت مدیریت راه هوایی و تهویه کنترله ،اطمینان از عدم حرکت بیمار و بهبود شرایط جراحی بدون اثرات تضعیف قلبی عروقی استفاده می شود (8-11). با این حال اگر کنترل دوز به درستی انجام نشود عوارض مخرب ایجاد میکند (8). در مطالعهای گزارش شد استفاده از داروهای شل کننده عضلانی، رقابتی با مرگ و میر مرتبط با بیهوشی را به همراه دارد و به دنبال آن اثرات باقیمانده عصبی-عضلانی نشان داد که باعث افزایش عوارض جدی تنفسی و بستری طولانیمدت در دوره بهبودی میشود (12,13). اگرچه بلوک عصبی عضلانی ممکن است خودبهخود بهبود یابد (14) ولی احتمال بروز فلج باقیمانده ناشی از شل کننده عضلانی با اثر متوسط، ۴۰ تا ۶۰ درصد است (13) که لزوم استفاده از عوامل دارویی در پایان عمل برای جلوگیری از فلج احتمالی باقیمانده، دوبینی، ضعف حنجره، احتباس کربندیاکسید و اسیدوز تنفسی،کما، مرگ و پنومونی را نشان میدهد (3,9,14,15) و ازمشکلات شایع بیماران در بخش مراقبت بعد از بیهوشی است (16). داروهای اصلی برای ریورس شل کنندههای عضلانی رقابتی، مهارکنندههای کولین استراز هستند (17). مهارکنندههای کولیناستراز با جلوگیری از تخریب استیلکولین باعث افزایش غلظت آن در محل اتصال عصب- عضله میشوند (18). به دلیل اثرات کولینرژیک استیلکولین که منجر به کاهش ضربان قلب، کاهش فشارخون و ایست ناگهانی قلب، انقباض برونش و افزایش ترشحات راه هوایی و افزایش حرکات روده میشود (11,19). برای به حداقل رساندن این عوارض به همراه آن، داروهای آنتی کولینرژیک مانند آتروپین و گلیکوپیرولات داده میشود که ممکن است منجر به بروز افزایش ضربان قلب، دهان خشک، احتباس ادرار و گشادی برونش شود (11,14). درطی مطالعات صورت گرفته برای مقایسه اثر بین آتروپین وگلیکوپیرولات محققان به این نتیجه رسیدند که گلیکوپیرولات افزایش کمتری در ضربان قلب میدهد و باید داروی انتخابی باشد با این وجود گلیکوپیرولات گرانتر است (15,20) و در کشور ایران در دسترس نیست. بنابراین از آتروپین استفاده میشود. مکانیسم احتمالی بدین گونه است که آتروپین با اتصال به فیبرهای کولینرژیک قلبی با تجمع استیلکولین به رقابت میپردازد و بدین ترتیب خطر اثر نئوستیگمین بر قلب با تاثیر اولیه آتروپین به حداقل میرسد (21). عوامل زیادی ازجمله پاکسازی حلق، درد و مسکن، داروهای بیهوشی مورد استفاده و عمق بیهوشی، سن بیماران، تعادل اسید و باز، نوع عمل و سرعت تزریق ریورس ممکن است بر ضربان قلب اثر بگذارند (23, 22). بیشترین افزایش ضربان قلب بعد از تجویز نئوستیگمین و آتروپین بستگی به ضربان قلب ابتدایی دارد بیمارانی که تعداد ضربان قلب کمتری دارند افزایش شدیدتری در ضربان قلب پیدا میکنند (25, 24). این تغییرات ضربان قلب برای بیماران با بیماری قلبی عروقی، تیروتوکسیکوز، کمبود حجم داخل عروقی و افراد مسن نامطلوب است (26, 20). بسیاری از مرگ و میرهای ناشی از تجویز این دو دارو را بیماران با اختلالات قلبی عروقی دربر میگیرند. نظرات در مورد روش بهینه تجویز کاملا متناقض بهنظر میرسد بهعنوان مثال پیشنهاد شده است که باید تا 15 دقیقه قبل از تجویز نئوستیگمین آتروپین داده شود یا حداقل صبر کرد تا افزایش ضربان قلب ناشی از آتروپین مشخص شود در مقابل در مطالعهای دیگر بیان شده است که نئوستیگمین باید قبل ازآتروپین داده شود (23) اما تغییرات ضربان قلب زمانی که آتروپین و نئوستیگمین بهصورت ترکیبی بهعنوان ریورس داده میشود کمتراست تا بهصورت جداگانه؛ با اینحال افزایش قابلتوجهی در ضربان قلب رخ میدهد که پس از مدتی کاهش مییابد (16). در مطالعهای سرعت تزریق ترکیب نئوستیگمین و آتروپین اثر یکسانی در افزایش اولیه ضربان قلب دارد اما هرچه سرعت تزریق بیشتر باشد کاهش ضربان قلب شدیدتر است (27). با توجه به آنچه اشاره شد، از آنجا که نتایج حاصل از مطالعات مشابه دارای تناقضاتی میباشد و مطالعات انجام شده به تعداد محدود و قدیمی است، مطالعه حاضر با هدف بررسی تأثیر تزریق توأم نئوستیگمین و آتروپین بر تعداد ضربان قلب در بیماران تحت بیهوشی عمومی در بیمارستان شهید رهنمون یزد در سال 1400 انجام شد.
روش بررسی
این مطالعه از نوع کارآزمایی بالینی سه سوکور بود. به گونهای که پژوهشگر از سرعت تزریق توام نئوستیگمین و آتروپین که توسط همکار پژوهشی انجام گرفت، بیاطلاع بود. بیمار هم از آنجاکه در زمان تزریق هوشیار نبود از نوع مداخله اطلاعی نداشت و تحلیلگر آماری هم بادریافت کد، دادهها را آنالیز نموده است. پس ازکسب کد اخلاق ((IR.SSU.REC.1400.210 از سوی دانشگاه علوم پزشکی شهید صدوقی یزد، مطالعه بر روی بیماران بستری که کاندید اعمال جراحی مختلف در سال 1400 در بیمارستان شهید رهنمون یزد بودند، انجام و 69 بیمار (47 مرد، 22 زن) که کاندیداتورهای عمل جراحی (فراوانی هر عمل ارتوپدی 42% جراحی عمومی 20% جراحی چشم 4% و اورولوژی3%) بودند شرکت داده شدند. بهوسیله چک لیست اطلاعات ثبت شد و نمونهها بهطور تصادفی به سه گروه از نظر زمان تزریق ریورس تقسیم شدند. معیار ورود به مطالعه، بیماران با سن بین 50-16 سال، میزان هموگلوبین بالاتر از 14 گرم بر دسیلیتر با بیهوشی کلاس یک ASA.PS بود (American Society of Anesthesiologists – Physical Status). معیار خروج از مطالعه بیماران با خونریزی بیش از 10% حجم خون، دارای اختلالات قلبی، عروقی و تنفسی، دریافت کننده داروهای موثر بر تعداد ضربان قلب یا سیستم عصبی مرکزی و بیماران با سابقه سوءمصرف مواد و حساسیت دارویی وحساسیت به زرده تخم مرغ بود. روش نمونهگیری بهصورت در دسترس و هدفمند بود. حجم نمونه با احتساب 10% ریزش وبا توجه به تجربی بودن مطالعه و مطالعه مشابه (28) 69 نفر (23 نفر در هر یک از سه گروه) که کاندید اعمال جراحی مختلف اعم از ارتوپدی، جراحی عمومی، جراحی چشم و اورولوژی بودند با وضعیت جسمی کلاس1یا2 در رده سنی80 -15 و بدون داشتن بیماری قلبی عروقی وارد مطالعه شدند.. بیماران کاندید عمل جراحی در بخش پره آپ ( بخش قبل از ورود به اتاق عمل) از نظر متغیرهای مطالعه (سن، جنس، نوع عمل، میزان هموگلوبین) مورد بررسی قرارگرفتند. اطلاعات دموگرافیک چک لیست تکمیل و فشار خون توسط دستگاه مانیتورینگ گرفته شد. میزان هموگلوبین با استفاده از آزمایش خون ضمیمه در پرونده بهدست آمد. برای تخصیص شرکتکنندگان به سه گروه مطالعه، از جدول اعداد تصادفی استفاده شد. پس از تعیین یک نقطه شروع تصادفی، اعداد جدول بهصورت پیدرپی خوانده شدند و بر اساس ارقام 1، 2 و 3 (یا باقیمانده تقسیم بر 3)، هر شرکتکننده به یکی از سه گروه مداخله تخصیص یافت. این فرایند تا تکمیل حجم نمونه ادامه یافت. گروه اول 10 ثانیه، گروه دوم 1 دقیقه و گروه سوم 3 دقیقه بود. مراحل بیهوشی توسط کارشناسان هوشبری بیمارستان و ثبت دادهها توسط دانشجو هوشبری انجام گرفت. پیش داروی دریافتی شامل میدازولامmg/kg 05/0 و فنتانیل µg/kg2 بود. القای وریدی بیهوشی با پروپوفول mg/kg5/1 و آتراکوریوم mg/kg 5/0 صورت گرفت. جهت برقراری راه هوایی کلیه بیماران، از لارنژیال ماسک برای کاهش تحریکات حلق و سیستم عصبی اتونوم استفاده شد. از ایزوفلوران 1% و دی نیتروژن اکسید به همراه اکسیژن با نسبت مساوی برای نگهداری بیهوشی استفاده شد و تنفس کنترله بود. با گذشت زمان و در صورت نیاز آتراکوریوم تکرار شد. در پایان بیهوشی، ایزوفلوران حداقل 5 دقیقه و دی نیتروژن اکسید 3 دقیقه قبل از تزریق داروی ریورس قطع شد. بعد از مشاهده کوچکترین تلاش تنفسی، قبل از تزریق ریورس جهت جلوگیری از تحریکات ناخواسته و حفظ عمق بیهوشی mg20 پرپوفول بهصورت بلوس تزریق و سپس µg/kg/min100 ادامه یافت. به منظور کنترل دقیق زمان تزریق، حجم کل دارو به 10 میلیلیتر رسانده شد و برای اطمینان از اثرگذاری ریورس فرصت کافی بین آخرین دوز تکرار داروی شل کننده و شروع تزریق ریورس داده شد. ریورس تزریق گردید و تنفس کنترله ادامه یافت. در طول مدت 10 دقیقه اگر تنفس خودبخودی بیمار برقرار شد برای جلوگیری از تحریک و همچنین پیشگیری از افزایش غلظت کربن دی اکسید شریانی، به ازای هر تنفس خود بهخودی بیمار که ونتیلاتور دریافت و شناسایی کرد یک تنفس مکانیکی با دم و بازدم همزمان به بیمار داده شد. در صورت کفایت تنفس، لارنژیال ماسک خارج و ترشحات دهان و حلق پاکسازی شد. در طی مدت اندازهگیری ضربان قلب، از ساکشن دهان خودداری شد. در چکلیستهایی که برای هر بیمار مهیا شده بود، تعداد ضربان قلب که بهوسیله ECG مانیتورینگ و پالساکسیمتر، درطی زمانهای مشخص شده (قبل از تزریق ریورس و سپس به مدت 10 دقیقه پس از آن با فواصل منظم 1 دقیقه و سپس در دقیقه پانزدهم و بیستم) گرفته شده بود و همچنین میزان خونریزی و مدت زمان عمل جراحی نیز ثبت شد.
تجزیه و تحلیل آماری
در نهایت دادهها توسط نرمافزارversion 16 SPSS و آمار توصیفی مناسب مورد تجزیه و تحلیل قرارگرفت.
نتایج
نتایج این مطالعه نشان میدهد که از لحاظ میانگین سن، جنس و میزان هموگلوبین تفاوت معنیداری نداشتند. جنسیت و سرعت تزریق بر تغییرات تعداد ضربان قلب موثر بوده است به گونهای که میانگین تغییرات ضربان قلب در زنان بیشتر از مردان است (84 به 76) و برخلاف گروه اول و دوم تفاوت چشمگیری درگروه سوم رخ داده و ضربان قلب به سمت نرمال شدن پیش رفته است. میزان هموگلوبین و سن تفاوت معنیداری نداشته است. تغییرات تعداد ضربان قلب گروه سنی 16 تا 20 سال بالاترین میانگین و گروه سنی 21 تا 35 سال پایینترین میانگین را به خود اختصاص داده است، تعداد ضربان قلب در ﮔﺮوه¬های تزریق 3 دقیقه نسبت به گروه تزریق 10 ثانیه و 1 دقیقه کاهش داشته است.
نمرات تعداد ضربان قلب زنان بالاترین میانگین و گروه مردان پایین ترین میانگین را به خود اختصاص داده است. نمرات تعداد ضربان قلب بیماران تحت جراحی های ارتوپدی بالاترین میانگین و گروه بیماران تحت جراحی عمومی پایین ترین میانگین را به خود اختصاص داده است. نمرات تعداد ضربان قلب بیماران با 1 دقیقه تزریق بالاترین میانگین و گروه بیماران با 3 دقیقه تزریق پایین ترین میانگین را به خود اختصاص داده است.در بین میانگین تعدیل شده نمرات تعداد ضربان قلب گروه بیماران با 3 دقیقه تزریق با گروه بیماران با 10 ثانیه و 1 دقیقه تزریق تفاوت معنیدار وجود دارد.
ﻧﺘﺎیﺞ (جدول 1) نشان می¬دهد که اثرات نوع تزریق معنادار است (01/0>P و 913/5= F). یعنی بین سه گروه متفاوت تزریق تفاوت وجود دارد. نتایج حاکی از آن است که میانگین گروه 3 دقیقه تزریق پایین ترین ضربان قلب را داشته اند. ولی اثرات سن (05/0<P و 956/1= F) و اﺛﺮات تعاملی سن و نوع تزریق (05/0<P و 152/1= F) ﻣﻌﻨﺎدار نیست. یعنی سن عامل تاثیرگذاری بر نوع تزریق نیست. نتایج (جدول 2) نشان می¬دهد تغییرات تعداد ضربان قلب گروه سنی 16 تا 20 سال بالاترین میانگین و گروه سنی 21 تا 35 سال پایین ترین میانگین را به خود اختصاص داده است. نتایج (جدول 3) نشان می¬دهد تغییرات تعداد ضربان قلب گروه 10 ثانیه بالاترین میانگین و گروه 3 دقیقه پایین ترین میانگین را به خود اختصاص داده است. نتایج (جدول 4) نشان می¬دهد تغییرات تعداد ضربان قلب گروه تزریق 3 دقیقه نسبت به گروه تزریق 1 دقیقه و 10 ثانیه تفاوت داشته است و ضربان قلب گروه تزریق 3 دقیقه به طور معنی داری از دو گروه دیگر کمتر بوده است. ﻧﺘﺎیﺞ (جدول 5) نشان می¬دهد که اثرات نوع تزریق معنادار است (01/0>P و 913/5= F). یعنی بین سه گروه متفاوت تزریق تفاوت وجود دارد. نتایج حاکی از آن است که میانگین گروه 3 دقیقه تزریق پایین ترین ضربان قلب را داشته اند. اثرات جنسیت (05/0>P و 945/5= F) معنیدار است. ولی اﺛﺮات تعاملی جنسیت و نوع تزریق (05/0<P و 489/0= F) ﻣﻌﻨﺎدار نیست. یعنی جنسیت عامل تاثیرگذاری بر نوع تزریق نیست. نتایج (جدول 6) نشان می¬دهد تغییرات تعداد ضربان قلب زنان بالاترین میانگین و گروه مردان پایین ترین میانگین را به خود اختصاص داده است. همان طور که (جدول7) نشان می¬دهد در بین میانگین تعدیل شده تغییرات تعداد ضربان قلب مردان و زنان تفاوت معنیدار وجود دارد. یعنی میانگین تعداد ضربان قلب زنان در هر سه گروه به طور معنیداری از تعداد ضربان قلب مردان بیشتر است. ﻧﺘﺎیﺞ (جدول 8) نشان می¬دهد که اثرات نوع تزریق معنادار است (01/0>P و 913/5= F). یعنی بین سه گروه متفاوت تزریق تفاوت وجود دارد. نتایج حاکی از آن است که میانگین گروه 3 دقیقه تزریق پایین ترین ضربان قلب را داشته اند. ولی اثرات نوع عمل (05/0<P و 572/0= F) و اﺛﺮات تعاملی نوع عمل و نوع تزریق (05/0<P و 195/0= F) ﻣﻌﻨﺎدار نیست. یعنی نوع عمل عامل تاثیرگذاری بر نوع تزریق نیست. نتایج (جدول9) نشان می¬دهد تغییرات تعداد ضربان قلب بیماران تحت جراحی های ارتوپدی بالاترین میانگین و گروه بیماران تحت جراحی عمومی پایین ترین میانگین را به خود اختصاص داده است. ﻧﺘﺎیﺞ (جدول 10) نشان می¬دهد که اثرات نوع تزریق معنادار است (01/0>P و 913/5= F). یعنی بین سه گروه متفاوت تزریق تفاوت وجود دارد. نتایج حاکی از آن است که میانگین گروه 3 دقیقه تزریق پایین ترین ضربان قلب را داشته اند. ولی اثرات میزان هموگلوبین (05/0<P و 802/0= F) و اﺛﺮات تعاملی میزان هموگلوبین و نوع تزریق (05/0<P و 453/1= F) ﻣﻌﻨﺎدار نیست. یعنی میزان هموگلوبین عامل تاثیرگذاری بر نوع تزریق نیست.
نتایج (جدول 11) نشان می¬دهد تغییرات تعداد ضربان قلب بیماران با هموگلوبین غیرنرمال بالاترین میانگین و گروه بیماران با هموگلوبین نرمال پایین ترین میانگین را به خود اختصاص داده است.
ﻧﺘﺎیﺞ (جدول 12) نشان می¬دهد که اثرات نوع تزریق معنادار است ﺑﺎ ﺗﻮﺟﻪ ﺑﻪ ﻧﻤﻮدار که ﻣﯿﺎﻧﮕﯿﻦ تعداد ضربان قلب در گروهها را ﻧﺸـﺎن ﻣـﯽ¬دﻫـﺪ، تعداد ضربان قلب در ﮔﺮوه¬های تزریق 3 دقیقه نسبت به گروه تزریق 10 ثانیه و 1 دقیقه کاهش داشته است. نتایج (جدول 13) نشان می¬دهد تغییرات تعداد ضربان قلب بیماران با 1 دقیقه تزریق بالاترین میانگین و گروه بیماران با 3 دقیقه تزریق پایین ترین میانگین را به خود اختصاص داده است. همان طور که (جدول 14) نشان می¬دهد در بین میانگین تعدیل شده تغییرات تعداد ضربان قلب گروه بیماران با 3 دقیقه تزریق با گروه بیماران با 10 ثانیه و 1 دقیقه تزریق تفاوت معنیدار وجود داردکه با نتایج کار آقای هارپر (27) همسوست
جدول 1: ﻧﺘﺎیﺞ اﺛﺮات درون ﻓﺮدی ﺑﺮ اﺳﺎس آزﻣﻮن اﻧﺪازهﮔﯿﺮی ﺗﮑﺮاری تغییرات تعداد ضربان قلب بیماران تحت بیهوشی عمومی در بیمارستان شهید رهنمون یزد در سال 1400 در گروه های مورد مطالعه

جدول 2: میانگین و انحراف معیار تعدیل شده تغییرات تعداد ضربان قلب

جدول 3: میانگین و انحراف معیار تعدیل شده تغییرات تعداد ضربان قلب

جدول 4: تفاوت زوجی تغییرات تعداد ضربان قلب

جدول 5: ﻧﺘﺎیﺞ اﺛﺮات درون ﻓﺮدی ﺑﺮ اﺳﺎس آزﻣﻮن اﻧﺪازهﮔﯿﺮی ﺗﮑﺮاری تغییرات تعداد ضربان قلب بیماران تحت بیهوشی عمومی در بیمارستان شهید رهنمون یزد در سال 1400 در گروه های مورد مطالعه

جدول6: میانگین و انحراف معیار تعدیل شده تغییرات تعداد ضربان قلب

جدول 7: مقایسه زوجی تغییرات تعداد ضربان قلب بیماران تحت بیهوشی عمومی در بیمارستان شهید رهنمون یزد در سال 1400 در گروه¬های مورد مطالعه

جدول 8: ﻧﺘﺎیﺞ اﺛﺮات درون ﻓﺮدی ﺑﺮ اﺳﺎس آزﻣﻮن اﻧﺪازهﮔﯿﺮی ﺗﮑﺮاری تغییرات تعداد ضربان قلب بیماران تحت بیهوشی عمومی در بیمارستان شهید رهنمون یزد در سال 1400 در گروه های مورد مطالعه

جدول 9: میانگین و انحراف معیار تعدیل شده تغییرات تعداد ضربان قلب

جدول 10: ﻧﺘﺎیﺞ اﺛﺮات درون ﻓﺮدی ﺑﺮ اﺳﺎس آزﻣﻮن اﻧﺪازهﮔﯿﺮی ﺗﮑﺮاری تغییرات تعداد ضربان قلب بیماران تحت بیهوشی عمومی در بیمارستان شهید رهنمون یزد در سال 1400 در گروه های مورد مطالعه

جدول 11: میانگین و انحراف معیار تعدیل شده تغییرات تعداد ضربان قلب
.JPG)
جدول 12: ﻧﺘﺎیﺞ اﺛﺮات درون ﻓﺮدی ﺑﺮ اﺳﺎس آزﻣﻮن اﻧﺪازهﮔﯿﺮی ﺗﮑﺮاری تغییرات تعداد ضربان قلب بیماران تحت بیهوشی عمومی در بیمارستان شهید رهنمون یزد در سال 1400 در گروه های مورد مطالعه

جدول 13: میانگین و انحراف معیار تعدیل شده تغییرات تعداد ضربان قلب

جدول 14: مقایسه زوجی تغییرات تعداد ضربان قلب بیماران تحت بیهوشی عمومی در بیمارستان شهید رهنمون یزد در سال 1400 در گروه¬های مورد مطالعه


شکل 1: نمودار مقایسه میانگین تغییرات تعداد ضربان قلب بیماران تحت بیهوشی عمومی در بیمارستان شهید رهنمون یزد در سال 1400 در مراحل سیزده گانه در گروه های تزریق 10 ثانیه، 1 دقیقه و 3 دقیقه مورد مطالعه

شکل 2: نمودار مقایسه میانگین نمرات تعداد ضربان قلب بیماران تحت بیهوشی عمومی در بیمارستان شهید رهنمون یزد در سال 1400 در مراحل سیزده گانه در گروه های تزریق 10 ثانیه، 1 دقیقه و 3 دقیقه مورد مطالعه
بحث
نتایج حاصل از این مطالعه نشان داد، تزریق ریورس طی3 دقیقه کمترین تغییرات ضربان قلب را به همراه دارد. همچنین میانگین تغییرات ضربان قلب در زنان بیشتر از مردان بود. همسو با این نتایج، در مطالعه ای که با هدف بررسی تاثیر سرعت های مختلف تزریق ترکیب نئوستیگمین و آتروپین بر ریتم و ضربان قلب صورت گرفت، ،تزریق آهسته تر ریورس باعث تاخیر و کاهش در افزایش اولیه ضربان قلب شد (27). در تبیین این شباهت می توان گفت متعاقب تزریق آهسته تر آتروپین اثر مرکزی آن افزایش می یابد که در تضاد با اثر محیطی عمل نموده و میزان افزایش تعداد ضربان قلب به حداقل می رسد. نا همسو با نتایج این مطالعه، در مطالعه ای که با هدف بررسی تاثیرات قلبی تجویز آتروپین و نئوستیگمین در انسان صورت گرفت، مشخص شد که بیشترین افزایش ضربان قلب زمانی است که آتروپین قبل از نئوستیگمین داده شود و بیشترین کاهش در شرایطی است که دو دارو توام باهم (28) یا آتروپین بلافاصله بعد از نئوستیگمین به آرامی داده شود (22). در تبیین این تناقض می توان گفت از آنجا که اثرات مرکزی آتروپین که منجر به برادیکاردی گذرا می شود زودتر از اثرات محیطی آن که تاکیکاردی است شروع می شود لذا طی تزریق قبلی با پشت سر گذاشتن اثر مرکزی باعث تاکیکاردی می شود و تزریق توام آن منجر به همراه شدن اثر پاراسمپاتوممتیکی نئوستیگمین با اثر مرکزی آتروپین شده و شاهد برادیکاردی خواهیم بود و دلیل ثبات بیشتر سیستم قلبی عروقی طی تزریق با سرعت آهسته تر در این مطالعه احتمالا به این علت بود که با کاهش سرعت تزریق توام، تاثیرات یاد شده با ملایمت بیشتری خود را نشان داده و ثبات قلبی عروقی بیشتری را داریم. همراستا با مطالعه حاضر، در مطالعه دیگری که تاثیر جدا و توام تزریق گلیکوپیرولات و نئوستیگمین برای توقف اثر شلکنندههای عضلانی طی بیهوشی عمومی استفاده شد مشخص شد که ثبات قلبی عروقی متعاقب تزریق توام آنها به مراتب بیشتر بود (DOI: https://doi.org/10.53350/pjmhs22169344). در تبیین این شباهت میتوان گفت علت آن یکسان بودن تاثیر آتروپین و گلیکوپیرولات بر گیرندههای M3 موسکارینی میباشد از طرفی تزریق دوزهای بیشتر از 5/0 میلیگرم آتروپین در تثبیت ناپایداری قلبی عروقی ناشی از نئوستیگمین موثرتر عمل می کند. در تبیین تاثیر جنسیت بر اختلاف میانگین تغییرات ضربان قلب در زنان میتوان دلیل آن را تاثیر هورمون تستسترون بر دوره استراحت بطنی دانست که باعث ثبات بیشتر ضربان قلب در مردان بهطورکلی میگردد و در مطالعات مرتبط نیز مشاهده میشود (https://doi.org/10.3389/fphys.2022.831179). بـا توجـه بـه اهمیـت موضـوع، پیشـنهاد میگـردد، تعداد نمونه جهت دستیابی به نتیجه مقبولتر افزایش یابد، دراعمال جراحی تنوع بیشتری صورت گیرد، مشارکت تعداد مساوی از هردوجنسیت جهت حذف تاثیر آن، تکرار کار با سایر داروهای بیهوشی، عدم توجه به تاثیر ساکشن بر ضربان قلب و مشارکت افراد بالای 50 سال در مطالعه انجام گیرد.
نتیجهگیری
نتایج پژوهش حاضر نشان داد؛ متغیرهای جنس و سرعت تزریق توأم نئوستیگمین و آتروپین بر تعداد ضربان قلب در بیماران تحت بیهوشی عمومی موثر بودند. در نتیجه پیشگیری از تغییرات شدید ضربان قلب و ثبات پاسخهای همودینامیک موثر هستند. این یافتهها، تزریق 3 دقیقهای ریورس را بهعنوان یک روش بهینه برای کمترین تغییرات ضربان قلب و در نتیجه، بهبود وضعیت همودینامیک بیماران پس از عملهای جراحی وابسته به تزریق ریورس را تایید میکنند.
سپاسگزاری
با صدور اجازه از بیمارستان شهید دکتر رهنمون بستر انجام این عمل بالینی فراهم شد؛ بدین وسیله از همکاری صمیمانه این مرکز و همچنین کمیته تحقیقات دانشجویی قدردانی میگردد. همچنین از همکاری جناب دکتر میرحسینی که در انجام این طرح تحقیقاتی نهایت همکاری را نمودند، کمال تشکر و قدردانی را داریم.
حامی مالی: ندارد.
تعارض در منافع: وجود ندارد.
ملاحظات اخلاقی
این مطالعه مطابق با اصول اخلاقی اعلامیه هلسینکی انجام شد، تمامی شرکتکنندگان پس از دریافت توضیحات کامل، رضایتنامه آگاهانه را امضا کردند و اطلاعات آنان بهصورت محرمانه نگهداری شد. همچنین مطالعه دارای کد اخلاق به شناسه IR.IAU.B.REC.1401.030 از دانشگاه علوم پزشکی شهید صدوقی یزد می باشد.
مشارکت نویسندگان
محمد صالح فرقانی در نمونه گیری و جمع آوری داده ها و تهیه نسخه نهایی مقاله، فاطمه جعفری نجفآبادی در ارائه ایده و طراحی مطالعه ، حمید میرحسینی درطراحی ونگارش نسخه اولیه مقاله و اصلاح نهائی و محمدحسین عوضبخش در تجزیه و تحلیل دادهها مشارکت داشته و همه نویسندگان در تدوین، ویرایش اولیه و نهایی مقاله و پاسخگویی به سوالات مرتبط با مقاله سهیم هستند.
References:
1- Shaydenfish D, Scheffenbichler FT, Kelly BJ, Lihn AL, Deng H, Nourmahnad A, et al. Effects of Anticholinesterase Reversal Under General Anesthesia on Postoperative Cardiovascular Complications: A Retrospective Cohort Study. Anesthesia and analgesia 2020; 130(3): 685-95.
2- Arbabpour R, Ganji Fard M, Tabiee S, Saadatjoo SA. The Effect of Bi-Spectral Index on Recovery and Postoperative Complications in Patients Undergoing Caesarean section. Journal of Birjand University of Medical Sciences. 2015;22(2):94-103.
3- Luo J, Chen S, Min S, Peng L. Reevaluation and update on efficacy and safety of neostigmine for reversal of neuromuscular blockade. Therapeutics and Clinical Risk Management 2018; 14: 2397.
4- Brown EN, Purdon PL, Van Dort CJ. General Anesthesia and Altered States of Arousal: A Systems Neuroscience Analysis. Annual Review of Neuroscience 2011; 34: 601-28.
5- Jabal Ameli M, Izadi-Mood N, Sharif M, Shafa A, Shetabi H. Evaluation of Hemodynamic and O2sat Conditions. Scientific Journal of Ilam University Of Medical Sciences 2011; 19(3): 51-6.
6- Oh TK, Ryu J-H, Nam S, Oh A-Y. Association of neuromuscular reversal by sugammadex and neostigmine with 90-day mortality after non-cardiac surgery. BMC anesthesiology 2020; 20(1): 1-11.
7- Dhande K, Kshirsagar J, Dhande A, Patil N, V Jr P. Hemodynamic Stability, Patient Acceptance and Cost of Intravenous Propofol and Inhalational Sevoflurane for Induction of Anaesthesia: A Prospective, Randomized Comparative Study. Cureus 2020; 12(4).
8- Kawasaki S, Kiyohara C, Tokunaga S, Hoka S. Prediction of hemodynamic fluctuations after induction of general anesthesia using propofol in non-cardiac surgery: a retrospective cohort study. BMC anesthesiology. 2018;18(1):167.
9- Murphy G, Kopman A. “To Reverse or Not To Reverse?”: The Answer Is Clear! Survey of Anesthesiology. 2017; 61(1): 24.
10- Bohringer C, Liu H. Is it always necessary to reverse the neuromuscular blockade at the end of surgery? Journal of Biomedical Research 2019; 33(4): 217.
11- Boon M, Martini C, Dahan A. Recent advances in neuromuscular block during anesthesia. F1000Research. 2018; 7.
12- Hristovska AM, Duch P, Allingstrup M, Afshari A. The comparative efficacy and safety of sugammadex and neostigmine in reversing neuromuscular blockade in adults. A Cochrane systematic review with meta‐analysis and trial sequential analysis. Anaesthesia 2018; 73(5): 631-41.
13- Fuchs‐Buder T, Mencke T. Use of Reversal Agents in Day Care Procedures (with Special Reference to Postoperative Nausea and Vomiting). European Journal of Anaesthesiology 2001; 18: 53-9.
14- Lien CA, Eikermann M. Neuromuscular Blockers and Reversal Drugs. Pharmacology and Physiology for Anesthesia: Elsevier; 2019: 428-54.
15- Kizilay D, Dal D, Saracoglu KT, Eti Z, Gogus FY. Comparison of Neostigmine and Sugammadex for Hemodynamic Parameters in Cardiac Patients Undergoing Noncardiac Surgery. Journal of Clinical Anesthesia 2016; 28: 30-5.
16- Bali IM, Mirakhur RK. Comparison of Glycopyrrolate, Atropine and Hyoscine in Mixture with Neostigmine for Reversal of Neuromuscular Block Following Closed Mitral Valvotomy. Acta Anaesthesiol Scand 1980; 24(4): 331-5.
17- Brull SJ, Kopman AF. Current Status of Neuromuscular Reversal and Monitoring: Challenges and Opportunities. Anesthesiology 2017; 126(1): 173-90.
18- Pani N, Dongare PA, Mishra RK. Reversal Agents in Anaesthesia and Critical Care. Indian journal of anaesthesia 2015; 59(10): 664.
19- Yamashita Y, Takasusuki T, Kimura Y, Komatsuzaki M, Yamaguchi S. Effects of Neostigmine and Sugammadex for Reversal of Neuromuscular Blockade on QT Dispersion Under Propofol Anesthesia: A Randomized Controlled Trial. Cardiology and Therapy 2018; 7(2): 163-72.
20- Tribuddharat S, Sathitkarnmanee T, Naewthong P. Less Tachycardia in Adults When Using Atropine 0.9 Mg Compared With 1.2 Mg Plus Neostigmine 2.5 Mg. J Med Assoc Thai 2008; 91(5): 665-8
21- Salem M, Ylagan L, Angel J, Vedam V, Collins V. Reversal of Curarization with Atropine-Neostigmine Mixture in Patients with Congenital Cardiac Disease. British Journal of Anaesthesia 1970; 42(11): 991-8.
22- Goldhill D. Reversal of Neuromuscular Block: Optimum Dosage of Neostigmine. J R Soc Med 1986; 79(6): 372-3.
23- Kjellberg M, Tammisto T. Heart‐Rate Changes after Atropine and Neostigmine Given for the Reversion of Muscle Paralysis. Acta Anaesthesiol Scand 1970; 14(3): 203-10.
24- Zeidan A, Baraka A. Ventricular Fibrillation Following Atropine‐Neostigmine Mixture in A Patient with Undiagnosed Mitral Valve Prolapse. Anaesthesia 2005; 60(7): 724-5.
25- Salem MR, Toyama T, Wong AY, Jacobs HK, Bennett EJ. Haemodynamic Responses to Antagonism of Bocurarine Block with Atropine-Neostigmine Mixture in Children. Br J Anaesth 1977; 49(9): 901-5.
26- Mirakhur R. Antagonism of Neuromuscular Block in The Elderly: A Comparison of Atropine and Glycopyrronium in A Mixture with Neostigmine. Anaesthesia 1985; 40(3): 254-8.
27- Rosner V, Kepes E, Foldes F. The Effects of Atropine and Neostigmine on Heart Rate and Rhythm. British Journal of Anaesthesia 1971; 43(11): 1066-74.
28- Harper K, Bali I, Gibson F, Carlisle R, Black I, Grainger D, et al. Reversal of Neuromuscular Block: Heart Rate Changes with Slow Injection of Neostigmine and Atropine Mixtures. Anaesthesia 1984; 39(8): 772-5.
29- OVASSAPIAN A. Effects of Administration of Atropine and Neostigmine in Man. Anesthesia & Analgesia 1969; 48(2): 219-23.
30- Limapichat R, Phuphiphat L, Pulnitiporn A. A Randomized Controlled Comparison of Difference Heart Rate after the Reversal of Non-Depolarized Muscle Relaxant with Atropine 0.6 Mg, 0.9 Mg and 1.2 Mg Plus Neostigmine 2.5 Mg. Thai J Anesthesiol 2017; 43(2): 135-43.
نوع مطالعه: کارآزمایی بالینی |
موضوع مقاله:
فارماکولوژی
دریافت: 1403/2/23 | پذیرش: 1403/12/11 | انتشار: 1404/2/15
دریافت: 1403/2/23 | پذیرش: 1403/12/11 | انتشار: 1404/2/15
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |







