دوره 29، شماره 12 - ( اسفند 1400 )
جلد 29 شماره 12 صفحات 4381-4373 |
برگشت به فهرست نسخه ها
Ethics code: IR.SSU.SPH.REC.1400.099
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Azod L, Miresmaeili S M, Fesahat F. Evaluating the Serum Levels of Inflammatory Cytokines in Women with Various Causes of Infertility during Controlled Ovarian Stimulation Cycles. JSSU 2022; 29 (12) :4373-4381
URL: http://jssu.ssu.ac.ir/article-1-5592-fa.html
URL: http://jssu.ssu.ac.ir/article-1-5592-fa.html
عضد لیلا، میراسماعیلی سید محسن، فصاحت فرزانه. بررسی سطوح سرمی سایتوکاینهای التهابی در زنان با علل مختلف ناباروری طی سیکلهای تحریک کنترل شده تخمدان. مجله علمي پژوهشي دانشگاه علوم پزشكي شهید صدوقی يزد. 1400; 29 (12) :4373-4381
متن کامل [PDF 975 kb]
(709 دریافت)
| چکیده (HTML) (1935 مشاهده)
متن کامل: (802 مشاهده)
مقدمه
ناباروری با علت ناشناخته یکی از شایعترین نوع تشخیصهای ناباروری است (1). اگر یک زن و شوهر پس از یک سال مقاربت منظم محافظت نشده علیرغم طبیعی بودن آزمایشات استاندارد، حامله نشوند،"ناباروری با علت ناشناخته" نامیده میشود (2). شیوع ناباروری با علت ناشناخته 37% از زوجین نابارور است (3). مطالعات متعددی نشان دادهاند که بسیاری از عوامل ایمونولوژیک مانند سایتوکاینها نقش مهم نظارتی در عملکرد تخمدان به ویژه برای رشد فولیکول، تخمکگذاری، لانه گزینی و حاملگی طبیعی دارند (5, 4). از میان سایتوکاینها، اینترلوکینها (IL) در کنترل تعداد زیادی از فرآیندهای فیزیولوژیکی و پاتوفیزیولوژیک تخمدان نقش دارند و تنظیمکنندههای مهم در عملکرد تولید مثل میباشند (6, 3). اینترلوکین 6 در سلولهای گرانولوزای فولیکول گرافیان، در سلولهای پوششی تخمدان و در جنین چند هستهای پیش از لانهگزینی تولید میشود (7). تحقیقات روی نمونههایی از فولیکول های تخمدان نشان داده است که کاهش سطح اینترلوکین 6 IL-6))، شانس بارداری در بیمارانی که از روش IVF استفاده میکنند را افزایش می¬دهد. بالا بودن سطح IL-6 در موارد ناباروری با علت ناشناخته، سقط جنین مکرر، پره اکلامپسی و زایمان زودرس همچنین در آندومتریوز دیده شده است (9, 8). بنابراین به نظر میرسد که در یک حاملگی طبیعی سطوح اینترلوکین-۶ در مایع فولیکولی کاهش یابد و در حاملگیهایی که دچاراختلال هستند افزایش یابد (10). تومور نکروز آلفا یکی از سایتوکاینهای التهابی است که از تخمدان، لولههای رحمی و رحم ترشح شده و برای رشد و عملکرد جفت و ادامه حیات جنین کاملاً ضروری است و میتواند باعث تکثیر سلولهای تخمدان و مهار استروئیدوژنز در سلولهای تخمدان تمایز نیافته و تحریک سنتز پروژسترون در موارد متفاوت باشد (11). سایتوکاینها نه فقط تنظیم کننده فرآیندههای فیزیولوژیک بوده بلکه میتوانند نقش مهمی در واکنشهای ایمنوپاتولوژیک نیز داشته باشند. از آنجا که میزان غلظت سایتوکاینهای التهابی در سطوح سرمی و نقش آنها در موفقیت سیکلهای باروری بیماران مبتلا فاکتورهای زنانه ناباروری ناشناخته است، هدف از این مطالعه نیز بررسی سطوح سرمی سایتوکاینهای التهابی درزنان با علل ناباروری زنانه طی سیکلهای تحریک کنترل شده تخمدان تعیین شد.
روش بررسی
مطالعه حاضر از نوع مورد-شاهدی بود. جامعه مورد بررسی شامل50 زن که 25 زن دارای اتیولوژی ناباروری زنانه یا ناشناخته (گروه مورد) و 25 زن دارای اتیولوژی ناباروری فاکتور مردانه (گروه شاهد) بودند که جهت درمان ناباروری به کلینیک درمانی الزهرا اصفهان در فاصله زمانی آذر ماه 1398تا اسفند ماه 1399مراجعه کرده بودند. پرسشنامه شامل اطلاعات دموگرافیک و اتیولوژی و علل و مدت ناباروری تکمیل و انتخاب بر اساس معیارهای ورود به مطالعه و خروج از مطالعه انجام گرفت. معیارهای ورود به مطالعه گروه شاهد شامل: تمایل به همکاری، داشتن تخمکگذاری کافی، سطح هورمونهای جنسی (پرولاکتین، محرک فولیکول و جسم زرد) مناسب، محدوده سنی بین 20 تا 35 سال و داشتن توده چربی زیر 25، سلامت رحم، تخمدان و لولههای رحمی، منظم بودن چرخه قاعدگی و نیز عدم داشتن عفونت سیستم تناسلی یا ناهنجاری ژنتیک بود. در گروه مورد انتخاب بر اساس تمایل به همکاری، محدوده سنی بین 20 تا 35 سال، داشتن توده چربی زیر 25 و داشتن حداقل یکی از علل ناباروری شامل وجود تخمدان پلیکیستیک، اختلالات لولههای فالوپ در زنان و یا علل ناشناخته زوجین بود. معیارهای خروج از مطالعه شامل: افراد دیابتی، مصرف داروهای ضد افسردگی، مشکلات حاد روانی تشخیص داده شده و تحت درمان، داشتن بیماریهای قلبی- عروقی، ترمبوآمبولیک، فشارخون، عفونتهای بیش از حد، هیپرلیپیدمی ارثی و نیز داشتن سقط جنین بودند. از همه افراد شرکتکننده در مطالعه رضایتنامه آگاهانه اخذ گردید.
تحریک تخمدان، جمعآوری و ارزیابی تخمک و جنینهای حاصله
تحریک تخمدان به این صورت انجام شد که از روز 21 سیکل قبلی تحت درمان با 0/5 سیسی بوسرلین به صورت زیر جلدی قرار گرفتند و با شروع سیکل بوسرلین به 0/25 سیسی کاهش یافت. از روز دوم سیکل بیماران 225-150 واحد FSH (Follicle-Stimulating Hormone) دریافت کردند و از روز هشتم سیکل تحت سونوگرافی واژینال قرار گرفتند. دوز FSH بر اساس سونوگرافی تنظیم شد. زمانیکه حداقل دو فولیکول با قطر بالای 18mm وجود داشت، بیماران 10000 واحد HCG (Human Chorionic Gonadotropin) دریافت کردند و 36 ساعت بعد جمعآوری تخمکها انجام شد. جمعآوری تخمکها 36 ساعت بعد از تزریق 10000 واحد HCG با استفاده از سونوگرافی واژینال انجام شد. آسپیراسیون فولیکولها با استفاده از سوزنهای 17 G و فشار 150 میلیمتر جیوه صورت گرفت. تخمکهای جمع آوری شده با استفاده از 80 واحد هیالورونیداز (Sigma Co ,USA) و روش پیپت نمودن از سلولهای کومولوس جدا شدند. ارزیابی تخمکها با استفاده از استریو میکروسکوپ (Olympus Co ,Japan) انجام شد. لقاح آزمایشگاهی همه تخمکهای گرفته شده از بیماران در این مطالعه جهت از بین بردن عامل مخدوش کننده به یک روش واحد میکرواینجکشن (ICSI) و توسط یک جنین شناس انجام گرفت. بعد از انتقال جنین به بیماران در روز دوم از تشکیل جنین، بیماران تا نتیجه حاملگی اعم از حاملگی مثبت یا منفی پیگیری شدند.
جمعآوری سرم خون و ارزیابی سایتوکاینهای مورد مطالعه
ابتدا 5 میلیلیتر خون جهت جداسازی سرم بیماران در روز تخمکگیری از بیمار گرفته شد. در لوله ساده بدون هیج ماده ضد انعقاد جمعآوری گردید و حدوداً نیم ساعت در دمای محیط نگهداری شد تا خون منعقد گردد. در نهایت نمونه به مدت 5 دقیقه در دور 3500 RPM سانتریفوژ شد. سرم خون جدا شده و در میکروتیوب یا لوله به حجم 2 میلیلیتر ریخته شده و در دمای20- درجه فریز شد. در زمانی که تمامی سرمها تهیه و جمع آوری گردید، همه آنها از فریز خارج شده و جهت اندازهگیری سطوح سایتوکاینهای مورد نظر استفاده شدند. غلظت سرمی فاکتور نکروز تومور آلفا (TNF-α) و IL-6 به روشالایزا با استفاده از پروتکل کیت تجاری karmania pars gene, Iran)) تعیین شد. طول موج خوانش نمونهها، 450 نانومتر بود. حساسیت اندازهگیری برای سایتوکاینIL-6 ، pg/mL2 و برای سایر سایتوکاینها (IL-12، TGFβ و TNFα)، pg/mL 5 بود.
تجزیه و تحلیل آماری
همه دادهها با استفاده از نرمافزارversion 16 SPSS آنالیز آماری شدند. از تست آماری Independent T test برای مقایسه متغیرها در دو گروه استفاده شد. ارتباط بین سایتوکاینهای TNF-α و IL-6 با علت ناباروری با استفاده از تست آماری Kruskal-Wallis test بررسی شد. سطح معنیداری دادهها کمتر از 0/05 در نظر گرفته شد. از نرمافزار گراف پد ورژن 9 جهت رسم نمودار استفاده شد.
ملاحظات اخلاقی
پروپوزال این تحقیق توسط دانشگاه علوم پزشکی شهید صدوقی تایید شده است (کد اخلاق IR.SSU.SPH.REC.1400.099)
نتایج
مطالعه حاضر بر روی 50 بیمار واجد شرایط انجام شد و یک نفر به دلیل انصراف از مطالعه خارج شد و مطالعه با 49 بیمار ادامه یافت. سپس بیماران به دو گروه تقسیم شدند و 25 نفر در گروه مورد و 24 نفر در گروه شاهد قرار گرفتند. جدول 1مقایسه متغیرهایی مانند سن، اووسیت و جنین را در دو گروه مورد و شاهد نشان میدهد. بر اساس نتایج، تفاوتی بین میزان سن، تعداد اووسیت و جنین در دو گروه مورد و شاهد وجود نداشت (P> 0/05). در صورتی که همبستگی مثبت معنیداری بین سطح سرمی IL6 و تعداد اووسیت
(P =0/04 r =0/41) و جنین (P =0/001 r =0/48) وجود داشت. نتایج همچنین نشان داد که تفاوتی بین سطح IL6 (P< 0/95) و TNF-α ((P< 0/80) ) بین دو گروه مورد و شاهد وجود نداشت (جدول 2). تفاوت معناداری بین سطح IL6 در گروههایی با علت ناباروری متفاوت وجود داشت (P= 0/02). اما این تفاوت در سطح سرمی TNF-α در گروههایی با علت ناباروری معنیدار نبود (P= 0/24) (شکل 1). تفاوت معناداری بین سطح سرمی IL6 در گروه PCO و(P= 0/008) Unknown و male factor و unknown(P= 0/02) وجود داشت. همچنین بالاترین سطحIL6 در بیماران مربوط به گروه ناباروری با علت ناشناخته است. (ناباروری به علت تخمدان پلیکیستیک = PCO و ناباروری به علت اختلالات لوله رحمی/تخمدانی =Ovarian factor و ناباروری با علل ناشناخته = Unknown و ناباروری به علت فاکتور مردانه= Male factor). دادهها به صورت میانگین ± انحراف از میانگین و با سطح معنیداری (P< 0/05) مشخص شدهاند. جدول 3 میزان فراوانی نتایج حاملگی مثبت و منفی بیماران را در روند سیکل درمانی تحریک کنترل شده تخمدان بر حسب نوع علت ناباروری نشان میدهد. نشان نشان داد که بیشترین بارداری مثبت مرتبط با گروه نابارور با علت اختلال در لولههای رحمی/تخمدانی میباشد (جدول 3).
جدول 1: مقایسه متغیرهایی مانند سن، اووسیت و جنین در دو گروه مورد و شاهد
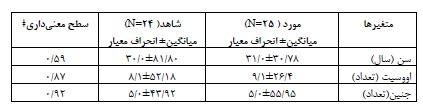
ǂ Mann Whitney test
جدول 2: مقایسه سطح اینترلوکین-6 و تومور نکروز آلفای سرم در دو گروه مورد و شاهد

ǂKruskal-Wallis test

شکل1: ارتباط بین اینترلوکین-6 و سطح تومور نکروز آلفا با علت ناباروری
جدول 3: فراوانی نتایج بارداری در زنان نابارور برحسب اتیولوژی ناباروری

دادهها به صورت تعداد (درصد) به تفکیک هر گروه مشخص شده است.
بحث
مطالعه حاضر با بررسی سطوح سرمی سایتوکاینهای التهابی IL6 و TNFα درزنان با علل ناباروری مختلف طی سیکلهای کنترل شده تحریک تخمدان انجام شد و مشاهد شد که میزان سطح سرمی IL6 در گروهها بر حسب علت ناباروری متغیر بوده و بیشترین سطح سرمی (3/36±28/20) متعلق به بیماران با علل ناشناخته ناباروری میباشد. به بیان دیگر، افزایش معناداری در سطح این سایتوکاین در بین زنان با علل ناباروری ناشناخته با بیماران با علل ناباروری تخمدان پلیکیستیک و فاکتور ناباروری مردانه مشاهده گردید (بهترتیب با 0/02 = Pو P=0/008). در مطالعهای که با هدف بررسی ارتباط سطوح سرمی سایتوکاین التهابی IL6 با میزان موفقیت بارداری در بیماران تحت درمان سیکل ICSI انجام شد، گزارش گردید که بین غلظت سرمی IL6 در بیماران با باروری موفق و ناموفق ارتباط معنیداری وجود ندارد (12). همچنین در مطالعهای با هدف مقایسه سطوح IL6 در دو گروه از زنان بارور و نابارور گزارش کردند که سطح IL6 در گروه نابارور 1/81±5/71 و در گروه بارور 1/79±4/31 بود که افزایش معناداری بین دو گروه را نشان میداد (7). محمد نوری و همکاران با بررسی سطح اینترلوکین6 در نمونه سرمی و مایع فولیکولی و ارتباط آن با میزان حاملگی در زنان نابارور مبتلا به اندومتریوز تحت درمان تکنیکهای کمک باروری، به این نتیجه رسیدند که میزانIL-6 در سرم و مایع فولیکولی بیماران حامله و غیرحامله بعد از انتقال جنین یکسان بوده و اختلاف معنیداری بین آنها وجود ندارد (P>0/05) ولی رابطه معنیداری بین سطح IL-6 مایع فولیکولی در بین بیماران اندومتریوز غیرحامله و حامله وجود داشت. (P<0/05) این شواهد نشان داد که افزایش سطح IL-6 در مایع فولیکولی میتواند با کاهش میزان حاملگی خصوصا در بیماران اندومتریوز همراه باشد (13). همچنین طبق مطالعهای که در سال 2011 با هدف اندازهگیری سطح سرمی سایتوکاینهای پیش التهابی TNF-α، اینترفرون گاما (IFN-γ) و سایتوکینهای ضد التهابی (IL-10 و IL-6) در زنان نابارور انجام شد، تفاوت معنیداری بین زنان نابارور و گروه شاهد مشاهده نشد (14). با وجود تفاوت در طراحی مطالعات مختلف و انتخاب گروههای مختلف در مطالعه که وابسته به هدف آن مطالعات میباشد نتایج بهدست آمده نیز با یکدیگر در تضاد میباشد. آنچه از نتایج مطالعه ما مشخص بود بیماران با علل مختلف ناباروری سطوح متفاوتی از IL6 را نشان میدهند و احتمال میرود که یکی از علل پاتولوژیک نتایج ضعیف ناباروری در بیماران با علل ناشناخته مرتبط با بالابودن غیر طبیعی سطح این سایتوکاین در ارتباط باشد. علاوه بر این، در مطالعه حاضر اگر چه تفاوت معناداری بین سطح TNFα در گروههای مختلف با علل ناباروری متفاوت مشاهده نشد، بالاترین سطح تومور نکروز آلفا مربوط به گروه ناباروری با علل ناشناخته بود. دو مطالعه با هدف مقایسه سطح TNFα در دو گروه از زنان بارور و نابارور به این نتیجه رسیدند که تفاوت معناداری بین سطح سرمی TNFα در زنان بارور و نابارور وجود ندارد (15، 7). یافتههای این مطالعه نیز با مطالعه حاضر همخوانی داشت. مطالعهای روی 63 زن نابارور با علل اندومتریوز، پلیکیستیک تخمدان و علل ناشناخته که تحت درمان ناباروری بودند انجام شد و ارزیابی سطح سرمی TNFα در این بیماران نشاندهنده بالاتر بودن سطح سرمی این سایتوکاین در بیماران با علل ناباروری ناشناخته نسبت به دیگر گروهها بود (9) که با یافتههای مطالعه حاضر همخوان میباشد (9). مطالعه دیگری نیز ارتباط مستقیم بین سطوح بالای TNFα و ناباروری با علل نامشخص را در مقایسه با علل ناباروری دیگر را نشان داد (16). همچنین در مطالعه حاضر، سطح سرمی αTNF- در بیماران دارای تخمدان پلیکیستیک در مقایسه با دیگر گروههای مطالعه کمتر بود ولی این تفاوت معنیدار نبود. در مطالعهای که به بررسی سطح سرمی αTNF- در بیماران مبتلا به تخمدان پلیکیستیک، نارسایی زودرس تخمدان در مقایسه با زنان سالم پرداخت، گزارش شد که پایینترین سطح سرمی αTNF- متعلق به بیماران دارای نارسایی زودرس تخمدان نسبت به گروه بیماران دارای تخمدان پلیکیستیک و گروه کنترل بود. مطالعه مذکور اثبات کرد که TNF-α نقش مهمی در عملکرد تخمدان دارد، بنابراین اختلال در رشد فولیکول، عملکرد لوتئال و atresia با تغییر سطح TNF-α در ارتباط است (17). اما مطالعهای دیگر سطح αTNF- سرم را در بیماران مبتلا به PCO و زنان سالم کنترل مقایسه کرد و گزارش کرد که سطح αTNF- در بیماران مبتلا به PCO بالاتر از گروه شاهد است که البته گروه شاهد در مطالعه ما زنان فاقد فرزند و دارای ناباروری با علت مردانه بودند که از این نظر با این مطالعه متفاوت بود (18). اوکپالاجی و همکارانش در سال 2016 سطح سرمی سایتوکاینهایی از قبیل αTNF-و گاما و اینترلوکین-6 و اینترلوکین10 را در بیماران نابارور با علت ناشناخته اندازهگیری کردند. آنها نشان دادند که هیچ تفاوت معنیداری بین فاکتور نکروزدهنده تومور آلفا و اینترلوکین-6 و اینترلوکین-10 بین دو گروه وجود ندارد اما فاکتور نکروز دهنده تومور گاما میتواند در ناباروری این افراد نقش داشته باشد (4). مهدی و همکاران در سال 2011 سطح سرمی سایتوکاینها از جملهIL-6 ,IL-10 TNFα و IFN-γ اندازهگیری کردند. نتایج حاصل نشان داد در زنان نابارور افزایش قابلتوجهی درIL-10 (P= 0/002) و (p= 0/0001c) IFN-وجود داشت ولی TNFα و IL-6 هیچ تفاوتی با گروه بارور نشان ندادند (14). در مجموع طبق یافتههای مطالعه حاضر و دیگر مطالعات، به نظر می¬رسد TNFα نقش تاثیرگذاری در ناباروری افراد نداشته باشد هر چند که در اکثر مطالعات این میزان TNFα در بین علل مختلف ناباروری مقایسه نشده است و در مطالعه ما با وجود حجم نمونه اندک این میزان در بیماران با علل ناباوری ناشناخته از بقیه بالاتر بود. در مطالعه حاضر، همچنین همبستگی مثبت و معنیداری بین IL6 و تعداد کلی اووسیت مشاهده شد. یک مطالعه نیز به بررسی سطح IL6 در مایع فولیکولی پرداخت و گزارش کرد که غلظت IL6 در مایع فولیکولی حاوی اووسیت بالغ بالاتر از فولیکولهایی با تخمک نارس است (19). مطالعهای دیگر به بررسی ارتباط تعداد اووسیت و IL6 مایع فولیکولی پرداخت و ارتباطی بین تعداد اووسیت و IL6اثبات نشد (20). با توجه به اینکه بیشتر مطالعات منتشر شده به بررسی ارتباط سطوح مایع فولیکولی سایتوکاینهای التهابی با میزان و کیفیت تخمکهای حاصله پرداخته است و نظر به اینکه در این مطالعه همبستگی معناداری بین فراوانی حاملگی با سطوح سرمی سایتوکاینها یافت نشد، مطالعات جامعتری با هدف اندازهگیری سطوح انواع سایتوکاینهای التهابی هم در مایع فولیکولی و هم در سرم در بیماران با علل ناباروری مختلف خصوصاً علل ناباروری ناشناخته مورد نیاز میباشد که بتوان به نتیجهگیری قطعیتری در این مورد دست یافت.
نتیجهگیری
بالاتر بودن سطح سرمیIL6 در گروه ناباروری با علت ناشناخته میتواند به عنوان یکی از معیارهای پاتولوژی ناباروری و یک پارامتر تاثیرگذار بر تعداد اووسیت و جنین در این گروه محسوب گردد. با این وجود به مطالعات با تعداد جامعه هدف بیشتر برای توصیف این شاخص احتمالی نیاز است.
سپاسگزاری
نویسندگان از حامی مالی این مطالعه که منتج شده از طرح تحقیقاتی مصوب با کد 8957 دانشگاه علوم پزشکی شهید صدوقی یزد میباشد قدردانی مینماید.
حامی مالی: دانشگاه علوم پزشکی شهید صدوقی یزد.
تعارض در منافع: وجود ندارد.
ناباروری با علت ناشناخته یکی از شایعترین نوع تشخیصهای ناباروری است (1). اگر یک زن و شوهر پس از یک سال مقاربت منظم محافظت نشده علیرغم طبیعی بودن آزمایشات استاندارد، حامله نشوند،"ناباروری با علت ناشناخته" نامیده میشود (2). شیوع ناباروری با علت ناشناخته 37% از زوجین نابارور است (3). مطالعات متعددی نشان دادهاند که بسیاری از عوامل ایمونولوژیک مانند سایتوکاینها نقش مهم نظارتی در عملکرد تخمدان به ویژه برای رشد فولیکول، تخمکگذاری، لانه گزینی و حاملگی طبیعی دارند (5, 4). از میان سایتوکاینها، اینترلوکینها (IL) در کنترل تعداد زیادی از فرآیندهای فیزیولوژیکی و پاتوفیزیولوژیک تخمدان نقش دارند و تنظیمکنندههای مهم در عملکرد تولید مثل میباشند (6, 3). اینترلوکین 6 در سلولهای گرانولوزای فولیکول گرافیان، در سلولهای پوششی تخمدان و در جنین چند هستهای پیش از لانهگزینی تولید میشود (7). تحقیقات روی نمونههایی از فولیکول های تخمدان نشان داده است که کاهش سطح اینترلوکین 6 IL-6))، شانس بارداری در بیمارانی که از روش IVF استفاده میکنند را افزایش می¬دهد. بالا بودن سطح IL-6 در موارد ناباروری با علت ناشناخته، سقط جنین مکرر، پره اکلامپسی و زایمان زودرس همچنین در آندومتریوز دیده شده است (9, 8). بنابراین به نظر میرسد که در یک حاملگی طبیعی سطوح اینترلوکین-۶ در مایع فولیکولی کاهش یابد و در حاملگیهایی که دچاراختلال هستند افزایش یابد (10). تومور نکروز آلفا یکی از سایتوکاینهای التهابی است که از تخمدان، لولههای رحمی و رحم ترشح شده و برای رشد و عملکرد جفت و ادامه حیات جنین کاملاً ضروری است و میتواند باعث تکثیر سلولهای تخمدان و مهار استروئیدوژنز در سلولهای تخمدان تمایز نیافته و تحریک سنتز پروژسترون در موارد متفاوت باشد (11). سایتوکاینها نه فقط تنظیم کننده فرآیندههای فیزیولوژیک بوده بلکه میتوانند نقش مهمی در واکنشهای ایمنوپاتولوژیک نیز داشته باشند. از آنجا که میزان غلظت سایتوکاینهای التهابی در سطوح سرمی و نقش آنها در موفقیت سیکلهای باروری بیماران مبتلا فاکتورهای زنانه ناباروری ناشناخته است، هدف از این مطالعه نیز بررسی سطوح سرمی سایتوکاینهای التهابی درزنان با علل ناباروری زنانه طی سیکلهای تحریک کنترل شده تخمدان تعیین شد.
روش بررسی
مطالعه حاضر از نوع مورد-شاهدی بود. جامعه مورد بررسی شامل50 زن که 25 زن دارای اتیولوژی ناباروری زنانه یا ناشناخته (گروه مورد) و 25 زن دارای اتیولوژی ناباروری فاکتور مردانه (گروه شاهد) بودند که جهت درمان ناباروری به کلینیک درمانی الزهرا اصفهان در فاصله زمانی آذر ماه 1398تا اسفند ماه 1399مراجعه کرده بودند. پرسشنامه شامل اطلاعات دموگرافیک و اتیولوژی و علل و مدت ناباروری تکمیل و انتخاب بر اساس معیارهای ورود به مطالعه و خروج از مطالعه انجام گرفت. معیارهای ورود به مطالعه گروه شاهد شامل: تمایل به همکاری، داشتن تخمکگذاری کافی، سطح هورمونهای جنسی (پرولاکتین، محرک فولیکول و جسم زرد) مناسب، محدوده سنی بین 20 تا 35 سال و داشتن توده چربی زیر 25، سلامت رحم، تخمدان و لولههای رحمی، منظم بودن چرخه قاعدگی و نیز عدم داشتن عفونت سیستم تناسلی یا ناهنجاری ژنتیک بود. در گروه مورد انتخاب بر اساس تمایل به همکاری، محدوده سنی بین 20 تا 35 سال، داشتن توده چربی زیر 25 و داشتن حداقل یکی از علل ناباروری شامل وجود تخمدان پلیکیستیک، اختلالات لولههای فالوپ در زنان و یا علل ناشناخته زوجین بود. معیارهای خروج از مطالعه شامل: افراد دیابتی، مصرف داروهای ضد افسردگی، مشکلات حاد روانی تشخیص داده شده و تحت درمان، داشتن بیماریهای قلبی- عروقی، ترمبوآمبولیک، فشارخون، عفونتهای بیش از حد، هیپرلیپیدمی ارثی و نیز داشتن سقط جنین بودند. از همه افراد شرکتکننده در مطالعه رضایتنامه آگاهانه اخذ گردید.
تحریک تخمدان، جمعآوری و ارزیابی تخمک و جنینهای حاصله
تحریک تخمدان به این صورت انجام شد که از روز 21 سیکل قبلی تحت درمان با 0/5 سیسی بوسرلین به صورت زیر جلدی قرار گرفتند و با شروع سیکل بوسرلین به 0/25 سیسی کاهش یافت. از روز دوم سیکل بیماران 225-150 واحد FSH (Follicle-Stimulating Hormone) دریافت کردند و از روز هشتم سیکل تحت سونوگرافی واژینال قرار گرفتند. دوز FSH بر اساس سونوگرافی تنظیم شد. زمانیکه حداقل دو فولیکول با قطر بالای 18mm وجود داشت، بیماران 10000 واحد HCG (Human Chorionic Gonadotropin) دریافت کردند و 36 ساعت بعد جمعآوری تخمکها انجام شد. جمعآوری تخمکها 36 ساعت بعد از تزریق 10000 واحد HCG با استفاده از سونوگرافی واژینال انجام شد. آسپیراسیون فولیکولها با استفاده از سوزنهای 17 G و فشار 150 میلیمتر جیوه صورت گرفت. تخمکهای جمع آوری شده با استفاده از 80 واحد هیالورونیداز (Sigma Co ,USA) و روش پیپت نمودن از سلولهای کومولوس جدا شدند. ارزیابی تخمکها با استفاده از استریو میکروسکوپ (Olympus Co ,Japan) انجام شد. لقاح آزمایشگاهی همه تخمکهای گرفته شده از بیماران در این مطالعه جهت از بین بردن عامل مخدوش کننده به یک روش واحد میکرواینجکشن (ICSI) و توسط یک جنین شناس انجام گرفت. بعد از انتقال جنین به بیماران در روز دوم از تشکیل جنین، بیماران تا نتیجه حاملگی اعم از حاملگی مثبت یا منفی پیگیری شدند.
جمعآوری سرم خون و ارزیابی سایتوکاینهای مورد مطالعه
ابتدا 5 میلیلیتر خون جهت جداسازی سرم بیماران در روز تخمکگیری از بیمار گرفته شد. در لوله ساده بدون هیج ماده ضد انعقاد جمعآوری گردید و حدوداً نیم ساعت در دمای محیط نگهداری شد تا خون منعقد گردد. در نهایت نمونه به مدت 5 دقیقه در دور 3500 RPM سانتریفوژ شد. سرم خون جدا شده و در میکروتیوب یا لوله به حجم 2 میلیلیتر ریخته شده و در دمای20- درجه فریز شد. در زمانی که تمامی سرمها تهیه و جمع آوری گردید، همه آنها از فریز خارج شده و جهت اندازهگیری سطوح سایتوکاینهای مورد نظر استفاده شدند. غلظت سرمی فاکتور نکروز تومور آلفا (TNF-α) و IL-6 به روشالایزا با استفاده از پروتکل کیت تجاری karmania pars gene, Iran)) تعیین شد. طول موج خوانش نمونهها، 450 نانومتر بود. حساسیت اندازهگیری برای سایتوکاینIL-6 ، pg/mL2 و برای سایر سایتوکاینها (IL-12، TGFβ و TNFα)، pg/mL 5 بود.
تجزیه و تحلیل آماری
همه دادهها با استفاده از نرمافزارversion 16 SPSS آنالیز آماری شدند. از تست آماری Independent T test برای مقایسه متغیرها در دو گروه استفاده شد. ارتباط بین سایتوکاینهای TNF-α و IL-6 با علت ناباروری با استفاده از تست آماری Kruskal-Wallis test بررسی شد. سطح معنیداری دادهها کمتر از 0/05 در نظر گرفته شد. از نرمافزار گراف پد ورژن 9 جهت رسم نمودار استفاده شد.
ملاحظات اخلاقی
پروپوزال این تحقیق توسط دانشگاه علوم پزشکی شهید صدوقی تایید شده است (کد اخلاق IR.SSU.SPH.REC.1400.099)
نتایج
مطالعه حاضر بر روی 50 بیمار واجد شرایط انجام شد و یک نفر به دلیل انصراف از مطالعه خارج شد و مطالعه با 49 بیمار ادامه یافت. سپس بیماران به دو گروه تقسیم شدند و 25 نفر در گروه مورد و 24 نفر در گروه شاهد قرار گرفتند. جدول 1مقایسه متغیرهایی مانند سن، اووسیت و جنین را در دو گروه مورد و شاهد نشان میدهد. بر اساس نتایج، تفاوتی بین میزان سن، تعداد اووسیت و جنین در دو گروه مورد و شاهد وجود نداشت (P> 0/05). در صورتی که همبستگی مثبت معنیداری بین سطح سرمی IL6 و تعداد اووسیت
(P =0/04 r =0/41) و جنین (P =0/001 r =0/48) وجود داشت. نتایج همچنین نشان داد که تفاوتی بین سطح IL6 (P< 0/95) و TNF-α ((P< 0/80) ) بین دو گروه مورد و شاهد وجود نداشت (جدول 2). تفاوت معناداری بین سطح IL6 در گروههایی با علت ناباروری متفاوت وجود داشت (P= 0/02). اما این تفاوت در سطح سرمی TNF-α در گروههایی با علت ناباروری معنیدار نبود (P= 0/24) (شکل 1). تفاوت معناداری بین سطح سرمی IL6 در گروه PCO و(P= 0/008) Unknown و male factor و unknown(P= 0/02) وجود داشت. همچنین بالاترین سطحIL6 در بیماران مربوط به گروه ناباروری با علت ناشناخته است. (ناباروری به علت تخمدان پلیکیستیک = PCO و ناباروری به علت اختلالات لوله رحمی/تخمدانی =Ovarian factor و ناباروری با علل ناشناخته = Unknown و ناباروری به علت فاکتور مردانه= Male factor). دادهها به صورت میانگین ± انحراف از میانگین و با سطح معنیداری (P< 0/05) مشخص شدهاند. جدول 3 میزان فراوانی نتایج حاملگی مثبت و منفی بیماران را در روند سیکل درمانی تحریک کنترل شده تخمدان بر حسب نوع علت ناباروری نشان میدهد. نشان نشان داد که بیشترین بارداری مثبت مرتبط با گروه نابارور با علت اختلال در لولههای رحمی/تخمدانی میباشد (جدول 3).
جدول 1: مقایسه متغیرهایی مانند سن، اووسیت و جنین در دو گروه مورد و شاهد

ǂ Mann Whitney test
جدول 2: مقایسه سطح اینترلوکین-6 و تومور نکروز آلفای سرم در دو گروه مورد و شاهد

ǂKruskal-Wallis test

شکل1: ارتباط بین اینترلوکین-6 و سطح تومور نکروز آلفا با علت ناباروری
جدول 3: فراوانی نتایج بارداری در زنان نابارور برحسب اتیولوژی ناباروری

دادهها به صورت تعداد (درصد) به تفکیک هر گروه مشخص شده است.
بحث
مطالعه حاضر با بررسی سطوح سرمی سایتوکاینهای التهابی IL6 و TNFα درزنان با علل ناباروری مختلف طی سیکلهای کنترل شده تحریک تخمدان انجام شد و مشاهد شد که میزان سطح سرمی IL6 در گروهها بر حسب علت ناباروری متغیر بوده و بیشترین سطح سرمی (3/36±28/20) متعلق به بیماران با علل ناشناخته ناباروری میباشد. به بیان دیگر، افزایش معناداری در سطح این سایتوکاین در بین زنان با علل ناباروری ناشناخته با بیماران با علل ناباروری تخمدان پلیکیستیک و فاکتور ناباروری مردانه مشاهده گردید (بهترتیب با 0/02 = Pو P=0/008). در مطالعهای که با هدف بررسی ارتباط سطوح سرمی سایتوکاین التهابی IL6 با میزان موفقیت بارداری در بیماران تحت درمان سیکل ICSI انجام شد، گزارش گردید که بین غلظت سرمی IL6 در بیماران با باروری موفق و ناموفق ارتباط معنیداری وجود ندارد (12). همچنین در مطالعهای با هدف مقایسه سطوح IL6 در دو گروه از زنان بارور و نابارور گزارش کردند که سطح IL6 در گروه نابارور 1/81±5/71 و در گروه بارور 1/79±4/31 بود که افزایش معناداری بین دو گروه را نشان میداد (7). محمد نوری و همکاران با بررسی سطح اینترلوکین6 در نمونه سرمی و مایع فولیکولی و ارتباط آن با میزان حاملگی در زنان نابارور مبتلا به اندومتریوز تحت درمان تکنیکهای کمک باروری، به این نتیجه رسیدند که میزانIL-6 در سرم و مایع فولیکولی بیماران حامله و غیرحامله بعد از انتقال جنین یکسان بوده و اختلاف معنیداری بین آنها وجود ندارد (P>0/05) ولی رابطه معنیداری بین سطح IL-6 مایع فولیکولی در بین بیماران اندومتریوز غیرحامله و حامله وجود داشت. (P<0/05) این شواهد نشان داد که افزایش سطح IL-6 در مایع فولیکولی میتواند با کاهش میزان حاملگی خصوصا در بیماران اندومتریوز همراه باشد (13). همچنین طبق مطالعهای که در سال 2011 با هدف اندازهگیری سطح سرمی سایتوکاینهای پیش التهابی TNF-α، اینترفرون گاما (IFN-γ) و سایتوکینهای ضد التهابی (IL-10 و IL-6) در زنان نابارور انجام شد، تفاوت معنیداری بین زنان نابارور و گروه شاهد مشاهده نشد (14). با وجود تفاوت در طراحی مطالعات مختلف و انتخاب گروههای مختلف در مطالعه که وابسته به هدف آن مطالعات میباشد نتایج بهدست آمده نیز با یکدیگر در تضاد میباشد. آنچه از نتایج مطالعه ما مشخص بود بیماران با علل مختلف ناباروری سطوح متفاوتی از IL6 را نشان میدهند و احتمال میرود که یکی از علل پاتولوژیک نتایج ضعیف ناباروری در بیماران با علل ناشناخته مرتبط با بالابودن غیر طبیعی سطح این سایتوکاین در ارتباط باشد. علاوه بر این، در مطالعه حاضر اگر چه تفاوت معناداری بین سطح TNFα در گروههای مختلف با علل ناباروری متفاوت مشاهده نشد، بالاترین سطح تومور نکروز آلفا مربوط به گروه ناباروری با علل ناشناخته بود. دو مطالعه با هدف مقایسه سطح TNFα در دو گروه از زنان بارور و نابارور به این نتیجه رسیدند که تفاوت معناداری بین سطح سرمی TNFα در زنان بارور و نابارور وجود ندارد (15، 7). یافتههای این مطالعه نیز با مطالعه حاضر همخوانی داشت. مطالعهای روی 63 زن نابارور با علل اندومتریوز، پلیکیستیک تخمدان و علل ناشناخته که تحت درمان ناباروری بودند انجام شد و ارزیابی سطح سرمی TNFα در این بیماران نشاندهنده بالاتر بودن سطح سرمی این سایتوکاین در بیماران با علل ناباروری ناشناخته نسبت به دیگر گروهها بود (9) که با یافتههای مطالعه حاضر همخوان میباشد (9). مطالعه دیگری نیز ارتباط مستقیم بین سطوح بالای TNFα و ناباروری با علل نامشخص را در مقایسه با علل ناباروری دیگر را نشان داد (16). همچنین در مطالعه حاضر، سطح سرمی αTNF- در بیماران دارای تخمدان پلیکیستیک در مقایسه با دیگر گروههای مطالعه کمتر بود ولی این تفاوت معنیدار نبود. در مطالعهای که به بررسی سطح سرمی αTNF- در بیماران مبتلا به تخمدان پلیکیستیک، نارسایی زودرس تخمدان در مقایسه با زنان سالم پرداخت، گزارش شد که پایینترین سطح سرمی αTNF- متعلق به بیماران دارای نارسایی زودرس تخمدان نسبت به گروه بیماران دارای تخمدان پلیکیستیک و گروه کنترل بود. مطالعه مذکور اثبات کرد که TNF-α نقش مهمی در عملکرد تخمدان دارد، بنابراین اختلال در رشد فولیکول، عملکرد لوتئال و atresia با تغییر سطح TNF-α در ارتباط است (17). اما مطالعهای دیگر سطح αTNF- سرم را در بیماران مبتلا به PCO و زنان سالم کنترل مقایسه کرد و گزارش کرد که سطح αTNF- در بیماران مبتلا به PCO بالاتر از گروه شاهد است که البته گروه شاهد در مطالعه ما زنان فاقد فرزند و دارای ناباروری با علت مردانه بودند که از این نظر با این مطالعه متفاوت بود (18). اوکپالاجی و همکارانش در سال 2016 سطح سرمی سایتوکاینهایی از قبیل αTNF-و گاما و اینترلوکین-6 و اینترلوکین10 را در بیماران نابارور با علت ناشناخته اندازهگیری کردند. آنها نشان دادند که هیچ تفاوت معنیداری بین فاکتور نکروزدهنده تومور آلفا و اینترلوکین-6 و اینترلوکین-10 بین دو گروه وجود ندارد اما فاکتور نکروز دهنده تومور گاما میتواند در ناباروری این افراد نقش داشته باشد (4). مهدی و همکاران در سال 2011 سطح سرمی سایتوکاینها از جملهIL-6 ,IL-10 TNFα و IFN-γ اندازهگیری کردند. نتایج حاصل نشان داد در زنان نابارور افزایش قابلتوجهی درIL-10 (P= 0/002) و (p= 0/0001c) IFN-وجود داشت ولی TNFα و IL-6 هیچ تفاوتی با گروه بارور نشان ندادند (14). در مجموع طبق یافتههای مطالعه حاضر و دیگر مطالعات، به نظر می¬رسد TNFα نقش تاثیرگذاری در ناباروری افراد نداشته باشد هر چند که در اکثر مطالعات این میزان TNFα در بین علل مختلف ناباروری مقایسه نشده است و در مطالعه ما با وجود حجم نمونه اندک این میزان در بیماران با علل ناباوری ناشناخته از بقیه بالاتر بود. در مطالعه حاضر، همچنین همبستگی مثبت و معنیداری بین IL6 و تعداد کلی اووسیت مشاهده شد. یک مطالعه نیز به بررسی سطح IL6 در مایع فولیکولی پرداخت و گزارش کرد که غلظت IL6 در مایع فولیکولی حاوی اووسیت بالغ بالاتر از فولیکولهایی با تخمک نارس است (19). مطالعهای دیگر به بررسی ارتباط تعداد اووسیت و IL6 مایع فولیکولی پرداخت و ارتباطی بین تعداد اووسیت و IL6اثبات نشد (20). با توجه به اینکه بیشتر مطالعات منتشر شده به بررسی ارتباط سطوح مایع فولیکولی سایتوکاینهای التهابی با میزان و کیفیت تخمکهای حاصله پرداخته است و نظر به اینکه در این مطالعه همبستگی معناداری بین فراوانی حاملگی با سطوح سرمی سایتوکاینها یافت نشد، مطالعات جامعتری با هدف اندازهگیری سطوح انواع سایتوکاینهای التهابی هم در مایع فولیکولی و هم در سرم در بیماران با علل ناباروری مختلف خصوصاً علل ناباروری ناشناخته مورد نیاز میباشد که بتوان به نتیجهگیری قطعیتری در این مورد دست یافت.
نتیجهگیری
بالاتر بودن سطح سرمیIL6 در گروه ناباروری با علت ناشناخته میتواند به عنوان یکی از معیارهای پاتولوژی ناباروری و یک پارامتر تاثیرگذار بر تعداد اووسیت و جنین در این گروه محسوب گردد. با این وجود به مطالعات با تعداد جامعه هدف بیشتر برای توصیف این شاخص احتمالی نیاز است.
سپاسگزاری
نویسندگان از حامی مالی این مطالعه که منتج شده از طرح تحقیقاتی مصوب با کد 8957 دانشگاه علوم پزشکی شهید صدوقی یزد میباشد قدردانی مینماید.
حامی مالی: دانشگاه علوم پزشکی شهید صدوقی یزد.
تعارض در منافع: وجود ندارد.
References:
1- Brandes M, Hamilton CJ, van der Steen JO, de Bruin JP, Bots RS, Nelen WL, et al. Unexplained Infertility: Overall Ongoing Pregnancy Rate and Mode of Conception. Hum Reprod 2011; 26(2): 360-8.
2- Kamath MS, Deepti MK. Unexplained Infertility: An Approach to Diagnosis and Management. Curr Med Issues 2016; 14(4): 94-100.
3- Sheldon IM, Cronin JG, Healey GD, Gabler C, Heuwieser W, Streyl D, et al. Innate Immunity and Inflammation of the Bovine Female Reproductive Tract in Health and Disease. Reproduction 2014; 148(3): R41-51.
4- Okpalaji Cb, OkerengwoAa, Okpani Aou, Chinko Bc, Bamigbowu Eo, B. Serum Cytokine Concentrations in Infertile and Fertile Women. A Preliminary Study in Port Harcourt, Nigeria. IOSR Journal of Dental and Medical Sciences 2016; 15(9): 77-9.
5- Sarapik A, Velthut A, Haller-Kikkatalo K, Faure GC, Béné M-C, de Carvalho Bittencourt M, et al. Follicular Proinflammatory Cytokines and Chemokines as Markers of IVF Success. Clin Dev Immunol 2012; 2012: 606459.
6- Field SL, Dasgupta T, Cummings M, Orsi NM. Cytokines in Ovarian Folliculogenesis, Oocyte Maturation and Luteinisation. Mol Reprod Dev 2014; 81(4): 284-314.
7- Demir B, Guven S, Guvendag Guven ES, Atamer Y, Gul T. Serum IL‐6 Level may have Role in the Pathophysiology of Unexplained Infertility. Am J Reprod Immunol 2009; 62(4): 261-7.
8- Prins JR, Gomez-Lopez N, Robertson SA. Interleukin-6 in Pregnancy and Gestational Disorders. J Reprod Immunol 2012; 95(1-2): 1-14.
9- Younis A, Hawkins K, Mahini H, Butler W, Garelnabi M. Serum Tumor Necrosis Factor-Α, Interleukin-6, Monocyte Chemotactic Protein-1 and Paraoxonase-1 Profiles in Women with Endometriosis, PCOS, or Unexplained Infertility. J Assist Reprod Genet 2014; 31(11): 1445-51.
10- Ghodsi M, Hojati V, Atarzadeh A, Saifi B. Assessment Interleukins 3, 5 and 6 Concentration in Follicular Fluid and Their Diagnostic Value in Patients with Unexplained Infertility.J Animal Physiology and Development (Quarterly Journal of Biological Sciences) 2020; 13(1(48)): 35-45. [Persian]
11- Sirotkin AV. Cytokines: Signalling Molecules Controlling Ovarian Functions. Int J Biochem Cell Biol 2011; 43(6): 857-61.
12- Asimakopoulos B, Demirel C, Felberbaum R, Waczek S, Nikolettos N, Koester F, et al. Concentrations of Inflammatory Cytokines and the Outcome in ICSI Cycles. In Vivo 2010; 24(4): 495-500.
13- Nouri M, Ghaffari M, Salmasi A, Ghasemzadeh A. Serum and Follicular Fluid IL-6 and Sex Steroid Hormone Levels and Their Correlation of Undergoing IVF-ET with Endometriosis and Pregnancy Rate in Women. Medical Journal of Reproduction & Infertility2000; 1(4). [Persian]
14- Mahdi BM. Role of Some Cytokines on Reproduction. Middle East Fertility Society Journal 2011; 16(3): 220-3.
15- Thum MY, Abdalla HI, Bhaskaran S, Harden EL, Ford B, Sumar N, et al. The Relationship of Systemic TNF‐Α and IFN‐Γ with IVF Treatment Outcome and Peripheral Blood NK Cells. Am J Reprod Immunol 2007; 57(3): 210-7.
16- Souter I, Huang A, Martinez-Maza O, Breen EC, Decherney AH, Chaudhuri G, et al. Serum Levels of Soluble Vascular Cell Adhesion Molecule-1, Tumor Necrosis Tumor Necrosis Factor-Α, and Interleukin-6 in in Vitro Fertilization Cycles. Fertilhty and Sterilhty 2009; 91(5): 2012-9.
17- Naz RK, Thurston D, Santoro N. Circulating Tumor Necrosis Factor (TNF)-Alpha in Normally Cycling Women and Patients with Premature Ovarian Failure and Polycystic Ovaries . Am J Reprod Immunol 1995; 34(3): 170-5.
18- Sayin NC, Gücer F, Balkanli-Kaplan P, Yüce MA, Ciftci S, Kücük M, et al. Elevated Serum TNF-Alpha Levels in Normal-Weight Women with Polycystic Ovaries or the Polycystic Ovary Syndrome. J Reprod Med 2003; 48(3): 165-70.
19- Kawasaki F, Kawano Y,Kosay Hasan ZK, Narahara H, Miyakawa I. The Clinical Role of Interleukin-6 and Interleukin-6 Soluble Receptor in Human Follicular Fluids. Clin Exp Med 2003; 3: 27-31.
20- Geva E, Lessing JB, Lerner-Geva L, Azem F, Yovel I, Amit A. Elevated Levels of Interleukin-6 in the Follicular Fluid at the Time of Oocyte Retrieval for in Vitro Fertilization may Predict the Development of Early-Form Ovarian Hyperstimulation Syndrome. Fertil Steril 1997; 68(1): 133-7.
1- Brandes M, Hamilton CJ, van der Steen JO, de Bruin JP, Bots RS, Nelen WL, et al. Unexplained Infertility: Overall Ongoing Pregnancy Rate and Mode of Conception. Hum Reprod 2011; 26(2): 360-8.
2- Kamath MS, Deepti MK. Unexplained Infertility: An Approach to Diagnosis and Management. Curr Med Issues 2016; 14(4): 94-100.
3- Sheldon IM, Cronin JG, Healey GD, Gabler C, Heuwieser W, Streyl D, et al. Innate Immunity and Inflammation of the Bovine Female Reproductive Tract in Health and Disease. Reproduction 2014; 148(3): R41-51.
4- Okpalaji Cb, OkerengwoAa, Okpani Aou, Chinko Bc, Bamigbowu Eo, B. Serum Cytokine Concentrations in Infertile and Fertile Women. A Preliminary Study in Port Harcourt, Nigeria. IOSR Journal of Dental and Medical Sciences 2016; 15(9): 77-9.
5- Sarapik A, Velthut A, Haller-Kikkatalo K, Faure GC, Béné M-C, de Carvalho Bittencourt M, et al. Follicular Proinflammatory Cytokines and Chemokines as Markers of IVF Success. Clin Dev Immunol 2012; 2012: 606459.
6- Field SL, Dasgupta T, Cummings M, Orsi NM. Cytokines in Ovarian Folliculogenesis, Oocyte Maturation and Luteinisation. Mol Reprod Dev 2014; 81(4): 284-314.
7- Demir B, Guven S, Guvendag Guven ES, Atamer Y, Gul T. Serum IL‐6 Level may have Role in the Pathophysiology of Unexplained Infertility. Am J Reprod Immunol 2009; 62(4): 261-7.
8- Prins JR, Gomez-Lopez N, Robertson SA. Interleukin-6 in Pregnancy and Gestational Disorders. J Reprod Immunol 2012; 95(1-2): 1-14.
9- Younis A, Hawkins K, Mahini H, Butler W, Garelnabi M. Serum Tumor Necrosis Factor-Α, Interleukin-6, Monocyte Chemotactic Protein-1 and Paraoxonase-1 Profiles in Women with Endometriosis, PCOS, or Unexplained Infertility. J Assist Reprod Genet 2014; 31(11): 1445-51.
10- Ghodsi M, Hojati V, Atarzadeh A, Saifi B. Assessment Interleukins 3, 5 and 6 Concentration in Follicular Fluid and Their Diagnostic Value in Patients with Unexplained Infertility.J Animal Physiology and Development (Quarterly Journal of Biological Sciences) 2020; 13(1(48)): 35-45. [Persian]
11- Sirotkin AV. Cytokines: Signalling Molecules Controlling Ovarian Functions. Int J Biochem Cell Biol 2011; 43(6): 857-61.
12- Asimakopoulos B, Demirel C, Felberbaum R, Waczek S, Nikolettos N, Koester F, et al. Concentrations of Inflammatory Cytokines and the Outcome in ICSI Cycles. In Vivo 2010; 24(4): 495-500.
13- Nouri M, Ghaffari M, Salmasi A, Ghasemzadeh A. Serum and Follicular Fluid IL-6 and Sex Steroid Hormone Levels and Their Correlation of Undergoing IVF-ET with Endometriosis and Pregnancy Rate in Women. Medical Journal of Reproduction & Infertility2000; 1(4). [Persian]
14- Mahdi BM. Role of Some Cytokines on Reproduction. Middle East Fertility Society Journal 2011; 16(3): 220-3.
15- Thum MY, Abdalla HI, Bhaskaran S, Harden EL, Ford B, Sumar N, et al. The Relationship of Systemic TNF‐Α and IFN‐Γ with IVF Treatment Outcome and Peripheral Blood NK Cells. Am J Reprod Immunol 2007; 57(3): 210-7.
16- Souter I, Huang A, Martinez-Maza O, Breen EC, Decherney AH, Chaudhuri G, et al. Serum Levels of Soluble Vascular Cell Adhesion Molecule-1, Tumor Necrosis Tumor Necrosis Factor-Α, and Interleukin-6 in in Vitro Fertilization Cycles. Fertilhty and Sterilhty 2009; 91(5): 2012-9.
17- Naz RK, Thurston D, Santoro N. Circulating Tumor Necrosis Factor (TNF)-Alpha in Normally Cycling Women and Patients with Premature Ovarian Failure and Polycystic Ovaries . Am J Reprod Immunol 1995; 34(3): 170-5.
18- Sayin NC, Gücer F, Balkanli-Kaplan P, Yüce MA, Ciftci S, Kücük M, et al. Elevated Serum TNF-Alpha Levels in Normal-Weight Women with Polycystic Ovaries or the Polycystic Ovary Syndrome. J Reprod Med 2003; 48(3): 165-70.
19- Kawasaki F, Kawano Y,Kosay Hasan ZK, Narahara H, Miyakawa I. The Clinical Role of Interleukin-6 and Interleukin-6 Soluble Receptor in Human Follicular Fluids. Clin Exp Med 2003; 3: 27-31.
20- Geva E, Lessing JB, Lerner-Geva L, Azem F, Yovel I, Amit A. Elevated Levels of Interleukin-6 in the Follicular Fluid at the Time of Oocyte Retrieval for in Vitro Fertilization may Predict the Development of Early-Form Ovarian Hyperstimulation Syndrome. Fertil Steril 1997; 68(1): 133-7.
نوع مطالعه: پژوهشي |
موضوع مقاله:
ایمونولوژی
دریافت: 1400/8/8 | پذیرش: 1400/9/10 | انتشار: 1400/12/15
دریافت: 1400/8/8 | پذیرش: 1400/9/10 | انتشار: 1400/12/15
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |







