دوره 28، شماره 9 - ( آذر 1399 )
جلد 28 شماره 9 صفحات 3008-2993 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Darabi L, Homayouni Moghadam F, Nasr Esfahani M H. Review on Brain Decellularization Methods and their Applications for Tissue Engineering. JSSU 2020; 28 (9) :2993-3008
URL: http://jssu.ssu.ac.ir/article-1-5087-fa.html
URL: http://jssu.ssu.ac.ir/article-1-5087-fa.html
دارابی لیلا، همایونیمقدم فرشاد، نصر اصفهانی محمدحسین. بررسی روشهای سلولزدایی بافت مغز و کاربرد آن در مهندسی بافت. مجله علمي پژوهشي دانشگاه علوم پزشكي شهید صدوقی يزد. 1399; 28 (9) :2993-3008
متن کامل [PDF 924 kb]
(1138 دریافت)
| چکیده (HTML) (3371 مشاهده)
متن کامل: (4505 مشاهده)
مقدمه
ماتریکس خارج سلولی شامل ترکیبات زیستی ترشح شده از سلولها است که یک بستر مناسب جهت حفظ رشد طبیعی سلولها، بافتها و اندامهای بدن فراهم میکند (1). ترکیبات این ساختار سه بعدی شامل پروتئوگلیکانها، گلیکوزآمینوگلیکانها و پروتئینهای فیبری میشوند. پروتئوگلیکانها دارای یک یا چند زنجیره گلیکوزآمینوگلیکانی هستند که توسط پیوند کووالانسی با یک هسته پروتئینی در ارتباط میباشند. پروتئوگلیکانها بهعنوان مولکولهایی که در سطح سلول یافت میگردند، میتوانند با غشای پلاسمایی در ارتباط باشند (2). گلیکوزآمینوگلیکانها، زنجیرههای پلیساکاریدی طولانی و اغلب سولفیده شدهای هستند که بهچهار دسته هیالورونیک اسید (هیالورونان)، کندروئیتین سولفات (یا درماتان سولفات)، هپاران سولفات و کراتین سولفات تقسیمبندی میشوند. به جز هیالورونیک اسید مابقی گلیکوزآمینوگلیکانها بهصورت پروتئوگلیکان با یک پروتیئن در ارتباط هستند. این پروتئینها، شامل دو نوع عملکردی (فیبرونکتین، لامینین، ویترونکتین) و ساختاری (کلاژنها و الاستینها) هستند. این پروتئوگلیکانها، گلیکوزآمینوگلیکانها و پروتئینهای فیبری هستند که در عملکردهای سلولی مانند: چسبندگی، تکثیر، مهاجرت، تمایز، مورفولوژی و ایجاد سدهای فیزیکی، بین بافتها نقش ایفا میکنند (2).
ماتریکس خارج سلولی مغز
بافت مغز حاوی ماتریکس خارج سلولی (Extracellular Matrix, ECM) منحصربفردی است، بهصورتیکه سه دسته ترکیب اصلی (پروتئوگلیکانها، گلیکوزآمینوگلیکانها و پروتئینهای فیبری) در ECM آن وجود دارند و 20 درصد از حجم مغز را به خود اختصاص میدهند (3). بهطور کلی میتوان گفت پروتئینهای رایجی که در ECM دیگر بافتها یافت میشوند در بافت مغز تقریباً وجود ندارند. ECM مغز در مرحله جنینی در تکوین سلولهای عصبی و نوریتها (Neuritis) و در بزرگسالان در شکلدهی به بافت مغز و در مقابله با حمله تومورهای غیرعصبی نقش ایفا میکند (4). در ادامه بهطور کامل در مورد ترکیبات ECM مغز بحث میشود.
پروتئوگلیکانها: پروتئوگلیکانها نقش مهمی در بافت مغز ایفا میکنند، آنها میتوانند در چسبندگی و رشد سلولها، تنظیم فاکتورهای رشد و همچنین مقاومت در برابر تهاجم سلولهای توموری نقش داشته باشند. از بین پروتئوگلیکانها، خانواده لکتیکانها (Lecticans Family) در بافت مغز فراوانند. لکتیکانها نیز مشابه تمامی پروتئوگلیکانها حاوی یک هسته پروتیئنی و یک جزء گلیکوزآمینوگلیکانی هستند. جزء گلیکوزآمینوگلیکان در این خانواده کندرویتین سولفات (Chondroitin Sulfate) است که طول این زنجیره در بین هر کدام از اعضای این خانواده متفاوت است. این خانواده شامل چهار پروتئوگلیکان به نامهای ورسیکان (Versican)، اگریکان (Aggrecan)، نوروکان (Neurocan) و برویکان (Brevican) هستند که در ادامه توضیح داده میشوند (4).
ورسیکان: این پروتئوگلیکان حاوی زنجیره کوتاهی از گلیکوزآمینوگلیکان میباشد و سه ایزوفرم V0، V1 و V2 دارد که ایزوفرم V2 آن بهطور عمدهای در ECM بافت مغز یافت میشود (4). ورسیکان در مغز بزرگسالان توسط سلولهای گلیال پس از آسیبهای عصبی بیان میشود (5) و بهنظر میرسد که با فعال کردن مسیرهای سیگنالی وابسته به گیرنده فاکتور رشد اپیدرمی (Epidermal Growth Factor Receptor, EGFR) در تنظیم عملکرد سیناپسی نورونهای هیپوکامپ، رشد سلولهای عصبی (6) و در چسبندگی سلول (4) نقش داشته باشد.
اگریکان: یک نوع پروتئوگلیکان بزرگ است که بهطور ویژه در بافتهای غضروفی مشاهده میشود اما در بافت مغز نیز میتواند بیان داشته باشد (4). اگریکان نقش مهمی در سازماندهی فضای خارج سلولی از طریق تعامل با تناسین (Tenascin) و پروتئینهای پیوندی (Linked proteins) دارد و باعث شکلدهی و بلوغ عصبی میشود (7). علاوه بر این تسریع انتقال سیناپسی در نورونها، تثبیت مکانیکی اتصالات سیناپسی و فعالیتهای حمایتی از نورونها از جمله نقشهای اگریکان میباشد (7).
نوروکان: یک نوع از پروتئوگلیکانهای خاص بافت مغز است که در دیگر بافتها قابل شناسایی نیست (2). علیرغم اینکه نوروکان در مرحله جنینی بیان کمی دارد اما در مرحله پس از تولد بیان آن افزایش یافته و به مرور در مقدار ثابتی حفظ میشود (2). این پروتئوگلیکان در اتصال سلولی، رشد نوریتها و هدایت آکسونها نقش دارد (8).
برویکان: همانند نوروکان یک پروتئوگلیکان مختص بافت مغز است (2) که در مغز جوندگان بالغ به وفور یافت میشود (9). برویکان در سطح خارجی نورونها در مکانهای پیش سیناپسی واقع شده و جزء اصلی از ماتریکس خارج سلولی است که میتواند با تناسین-آر (Tenascin-R)تعامل داشته باشد (9).
سایر پروتئوگلیکانها: در مغز پروتئوگلیکانهای دیگری وجود دارد که جزء گلیکوزآمینوگلیکانی متفاوتی نسبت بهخانواده لکتیکانها را دارند. از جمله این پروتئوگلیکانها میتوان به آگرین (Agrin) و فسفوکان ( Phosphocan) اشاره کرد. آگرین بهطور گستردهای در مرحله سیناپسزایی جوندگان و پرندگان نقش دارد و جزء گلیکوزآمینوگلیکانی آن هپارین سولفات است (10). فسفوکان در بافتهای عصبی بهوسیله سلولهای آستروسیت بیان میشود و در تعاملات نورون-گلیا و در ارتباط با تمایز نورون و میلینسازی نقش دارد (11). رلین (Reelin) و تنسکین از دیگر پروتئوگلیکانهایی هستند که در بافت مغز بیان میشوند (2).
گلیکوزآمینوگلیکانها
گلیکوزآمینوگلیکانها در ارتباط با پروتئوگلیکانها هستند و عملکردهای متفاوتی در بافت مغز مانند میلینزایی دارند. از اینرو غلظت GAGها در گرههای رانویه به وفور مشاهده میشود (12). از بین GAGها در انسان هیالورونیک اسید، کندرویتین سولفات و درماتان سولفات (Dermatan sulfate) در سیستم عصبی مرکزی به وفور یافت میشوند (12).
پروتیئن های فیبری
این دسته از پروتئینها در مغز نقشهای عملکردی، ساختاری و چسبندگی سلولها را بر عهده دارند. اما در کل میزان حضور این پروتیئنها در بافت مغز کم است (2). این پروتیئنها شامل کلاژنها (Collagen)، فیبرونکتین (Fibronectin)، ویترونکتین (Vitronectin) و لامینین (Laminin) است که در زیر شرح داده میشود.
کلاژن: در سیستم عصبی مرکزی، کلاژن تنها در عروق یافت میشود، این در حالی است که در سیستم عصبی محیطی مقادیر بالایی از کلاژن، عملکردهای سلولی را تحتتأثیر قرار میدهد. کلاژنهای موجود در مغز از نوع کلاژن نوع یک، دو و چهار هستند. نسبت کلاژنها به گلیکوزآمینوگلیکانهای سولفاته (Sulphated GAG, sGAG) نقش مهمی در تعیین ظرفیت و استحکام مکانیکی بافت ایفا میکند. SGAG باعث جذب آب بیشتر و حضور کلاژن استحکام مکانیکی را به بافت اعطاء میکند (3).
فیبرونکتین: یک نوع پروتئین عملکردی است که در چسبندگی سلولها نقش دارد. در سیستم عصبی مرکزی این پروتئین در مجاورت نورونهای در حال تکوین، بهطور وسیعی دیده میشود (13). این در حالی است که مقدار این پروتیئن در زمان آسیبهای مغزی نیز افزایش مییابد که بیانگر نقش حفاظتی فیبرونکتین در پاسخ به آسیب است (14).
ماتریکس خارج سلولی مغز
بافت مغز حاوی ماتریکس خارج سلولی (Extracellular Matrix, ECM) منحصربفردی است، بهصورتیکه سه دسته ترکیب اصلی (پروتئوگلیکانها، گلیکوزآمینوگلیکانها و پروتئینهای فیبری) در ECM آن وجود دارند و 20 درصد از حجم مغز را به خود اختصاص میدهند (3). بهطور کلی میتوان گفت پروتئینهای رایجی که در ECM دیگر بافتها یافت میشوند در بافت مغز تقریباً وجود ندارند. ECM مغز در مرحله جنینی در تکوین سلولهای عصبی و نوریتها (Neuritis) و در بزرگسالان در شکلدهی به بافت مغز و در مقابله با حمله تومورهای غیرعصبی نقش ایفا میکند (4). در ادامه بهطور کامل در مورد ترکیبات ECM مغز بحث میشود.
پروتئوگلیکانها: پروتئوگلیکانها نقش مهمی در بافت مغز ایفا میکنند، آنها میتوانند در چسبندگی و رشد سلولها، تنظیم فاکتورهای رشد و همچنین مقاومت در برابر تهاجم سلولهای توموری نقش داشته باشند. از بین پروتئوگلیکانها، خانواده لکتیکانها (Lecticans Family) در بافت مغز فراوانند. لکتیکانها نیز مشابه تمامی پروتئوگلیکانها حاوی یک هسته پروتیئنی و یک جزء گلیکوزآمینوگلیکانی هستند. جزء گلیکوزآمینوگلیکان در این خانواده کندرویتین سولفات (Chondroitin Sulfate) است که طول این زنجیره در بین هر کدام از اعضای این خانواده متفاوت است. این خانواده شامل چهار پروتئوگلیکان به نامهای ورسیکان (Versican)، اگریکان (Aggrecan)، نوروکان (Neurocan) و برویکان (Brevican) هستند که در ادامه توضیح داده میشوند (4).
ورسیکان: این پروتئوگلیکان حاوی زنجیره کوتاهی از گلیکوزآمینوگلیکان میباشد و سه ایزوفرم V0، V1 و V2 دارد که ایزوفرم V2 آن بهطور عمدهای در ECM بافت مغز یافت میشود (4). ورسیکان در مغز بزرگسالان توسط سلولهای گلیال پس از آسیبهای عصبی بیان میشود (5) و بهنظر میرسد که با فعال کردن مسیرهای سیگنالی وابسته به گیرنده فاکتور رشد اپیدرمی (Epidermal Growth Factor Receptor, EGFR) در تنظیم عملکرد سیناپسی نورونهای هیپوکامپ، رشد سلولهای عصبی (6) و در چسبندگی سلول (4) نقش داشته باشد.
اگریکان: یک نوع پروتئوگلیکان بزرگ است که بهطور ویژه در بافتهای غضروفی مشاهده میشود اما در بافت مغز نیز میتواند بیان داشته باشد (4). اگریکان نقش مهمی در سازماندهی فضای خارج سلولی از طریق تعامل با تناسین (Tenascin) و پروتئینهای پیوندی (Linked proteins) دارد و باعث شکلدهی و بلوغ عصبی میشود (7). علاوه بر این تسریع انتقال سیناپسی در نورونها، تثبیت مکانیکی اتصالات سیناپسی و فعالیتهای حمایتی از نورونها از جمله نقشهای اگریکان میباشد (7).
نوروکان: یک نوع از پروتئوگلیکانهای خاص بافت مغز است که در دیگر بافتها قابل شناسایی نیست (2). علیرغم اینکه نوروکان در مرحله جنینی بیان کمی دارد اما در مرحله پس از تولد بیان آن افزایش یافته و به مرور در مقدار ثابتی حفظ میشود (2). این پروتئوگلیکان در اتصال سلولی، رشد نوریتها و هدایت آکسونها نقش دارد (8).
برویکان: همانند نوروکان یک پروتئوگلیکان مختص بافت مغز است (2) که در مغز جوندگان بالغ به وفور یافت میشود (9). برویکان در سطح خارجی نورونها در مکانهای پیش سیناپسی واقع شده و جزء اصلی از ماتریکس خارج سلولی است که میتواند با تناسین-آر (Tenascin-R)تعامل داشته باشد (9).
سایر پروتئوگلیکانها: در مغز پروتئوگلیکانهای دیگری وجود دارد که جزء گلیکوزآمینوگلیکانی متفاوتی نسبت بهخانواده لکتیکانها را دارند. از جمله این پروتئوگلیکانها میتوان به آگرین (Agrin) و فسفوکان ( Phosphocan) اشاره کرد. آگرین بهطور گستردهای در مرحله سیناپسزایی جوندگان و پرندگان نقش دارد و جزء گلیکوزآمینوگلیکانی آن هپارین سولفات است (10). فسفوکان در بافتهای عصبی بهوسیله سلولهای آستروسیت بیان میشود و در تعاملات نورون-گلیا و در ارتباط با تمایز نورون و میلینسازی نقش دارد (11). رلین (Reelin) و تنسکین از دیگر پروتئوگلیکانهایی هستند که در بافت مغز بیان میشوند (2).
گلیکوزآمینوگلیکانها
گلیکوزآمینوگلیکانها در ارتباط با پروتئوگلیکانها هستند و عملکردهای متفاوتی در بافت مغز مانند میلینزایی دارند. از اینرو غلظت GAGها در گرههای رانویه به وفور مشاهده میشود (12). از بین GAGها در انسان هیالورونیک اسید، کندرویتین سولفات و درماتان سولفات (Dermatan sulfate) در سیستم عصبی مرکزی به وفور یافت میشوند (12).
پروتیئن های فیبری
این دسته از پروتئینها در مغز نقشهای عملکردی، ساختاری و چسبندگی سلولها را بر عهده دارند. اما در کل میزان حضور این پروتیئنها در بافت مغز کم است (2). این پروتیئنها شامل کلاژنها (Collagen)، فیبرونکتین (Fibronectin)، ویترونکتین (Vitronectin) و لامینین (Laminin) است که در زیر شرح داده میشود.
کلاژن: در سیستم عصبی مرکزی، کلاژن تنها در عروق یافت میشود، این در حالی است که در سیستم عصبی محیطی مقادیر بالایی از کلاژن، عملکردهای سلولی را تحتتأثیر قرار میدهد. کلاژنهای موجود در مغز از نوع کلاژن نوع یک، دو و چهار هستند. نسبت کلاژنها به گلیکوزآمینوگلیکانهای سولفاته (Sulphated GAG, sGAG) نقش مهمی در تعیین ظرفیت و استحکام مکانیکی بافت ایفا میکند. SGAG باعث جذب آب بیشتر و حضور کلاژن استحکام مکانیکی را به بافت اعطاء میکند (3).
فیبرونکتین: یک نوع پروتئین عملکردی است که در چسبندگی سلولها نقش دارد. در سیستم عصبی مرکزی این پروتئین در مجاورت نورونهای در حال تکوین، بهطور وسیعی دیده میشود (13). این در حالی است که مقدار این پروتیئن در زمان آسیبهای مغزی نیز افزایش مییابد که بیانگر نقش حفاظتی فیبرونکتین در پاسخ به آسیب است (14).
ویترونکتین: در سیستم عصبی مرکزی بیان ویترونکتین در مغز و شبکیه فراوان است. در گلیوما (Glioma، سرطان مغز از نوع سلولهای گلیال تهاجمی) میزان سنتز ویترونکتین با پیشرفت سرطان ارتباط مستقیم دارد (15).
لامینین: این پروتیئن توسط سلولهای آستروسیت بیان میشود و همچنین متعاقب آسیب مغزی در بزرگسالان افزایش سطح بیان آن توسط آستروسیتها اتفاق میافتد. علاوه بر این لامینین نقش مهمی در ساخت و ترمیم سد خونی مغزی دارد (15). از آنجایی که ECM حاوی ترکیباتی است که میتواند روی رفتارهای سلولی اثر بگذارد، فرایندی تحت عنوان سلولزدایی تعریف میشود که طی آن سلولهای ساکن در ECM یک بافت یا اندام از آن جداشده و تنها ECM آن باقی بماند که بهعنوان یک بستر و داربست میتواند در شرایط آزمایشگاهی و در بدن، در بازسازی بافت و اندامها کاربرد داشته باشد.
روشهای سلولزدایی
در سلولزدایی حفظ معماری بافت، ساختار و ترکیب ECM از اهمیت بالایی برخوردار است (16). در فرآیند سلولزدایی بافت یا اندام، از روشهای فیزیکی، شیمیایی و زیستی برای حذف سلولها و سپس شستشو با آب یا محلول نمک فسفات (PhosphateBuffered Saline) برای حذف بقایای سلولی استفاده میشود.
روشهای شیمیایی
برای حذف سلولها میتوان از مواد شیمیایی استفاده کرد، ازجمله: اسیدها و بازها، محلولهای هایپو و هایپرتونیک، الکل، دترجنتها و مواد دیگری مانند استون (16). از بین این مواد، دترجنتهای یونی و غیریونی مانند تریتون X-100، سدیم دئوکسی کولات (Sodium Deoxycolate, SDC) و سدیم دودسیل سولفات (Sodium Dodecyl Sulfate, SDS) بهطور موثرتری در فرایند سلولزدایی بافت کاربرد دارند (16).
روشهای زیستی
استفاده از مواد زیستی جهت حذف سلولها در فناوری سلولزدایی بافت به دو دسته آنزیم و غیر آنزیم تقسیم میشوند (16). آنزیمها شامل نوکلئازها (DNase و RNase) و تریپسین هستند. آنزیمDNase رایجترین نوکلئازی است که بسته به نیاز با غلظتهای مختلف در سلولزدایی بافت مورد استفاده بوده و باعث کاهش میزان 95 درصدی غلظت DNA در بافت مغز میشود (17). آنزیم تریپسین متداولترین پروتئازی است که اغلب با EDTA (Ethylenediaminetetraacetic acid) مورد استفاده قرار میگیرد. تریپسین با اثر روی آرژنین و لیزین باعث شکستن پیوند پپتیدی میشود، از اینرو تیمار طولانیمدت با این آنزیم میتواند سبب تخریب کلاژن، لامینین و فیبرونکتین ماتریکس خارج سلولی شود (18).
روشهای فیزیکی
سلولزدایی با روشهای فیزیکی مانند پرتوافکنی و تکرار چرخههای فریز و ذوب میتواند باعث سست شدن بافت و از بین رفتن گسستگی سلولها شود اما نمیتواند سلولهای مرده بافت را حذف کند از اینرو به شستشو و استفاده از نیروهایی که خود جزئی از عوامل فیزیکی بهحساب میآیند، مانند نیروی حاصل از سانتریفیوژ نیاز دارند (18).
کاربرد بافت سلولزدایی شده در مهندسی بافت
داربستهای سلولی در مهندسی بافت و پزشکی بازساختی به دو دسته پلیمرهای مصنوعی و داربستهای طبیعی تقسیمبندی میشوند. در داربستهای مصنوعی از پلیمرهای مصنوعی در ساخت داربست استفاده میشود که شامل گروه بزرگی از پلیمرهای تخریبپذیر هستند. این داربستها به دلیل خاصیت منحصربهفرد خود از جمله نسبت سطح به حجم زیاد، تخلخل زیاد با اندازه منافذ کوچک و خاصیت مکانیکی خوبی که دارند مورد توجه محققین قرار گرفتهاند. آنها مزایای دیگری مانند زیستسازگاری و خصوصیات بیولوژیکی دارند که در مهندسی بافت و بازسازی اندام کاربرد دارد. مواد داربست بسته به کاربرد مورد نظر میتوانند مصنوعی یا زیستی، قابل تجزیه یا غیر قابل تجزیه باشند. خواص پلیمرها به ترکیب، ساختار و ترتیب ماکرومولکولهای تشکیل دهنده آنها بستگیدارد. از نظر خصوصیات ساختاری، شیمیایی و بیولوژیکی میتوان آنها را در انواع مختلفی مانند سرامیک، شیشه، پلیمر و غیره طبقهبندی کرد. کوپلیمرهای Polylactic acid PLA) )، (PGA) poly glycolic acid و poly lactic-co-glycolic acid PLGA)) از متداولترین پلیمرهای مصنوعی در مهندسی بافت هستند. مواد طبیعی بهدلیل خاصیت فعال زیستی، تعامل بهتری با سلولها دارند و این به آنها این امکان را میدهد تا عملکرد سلولها را در سیستم بیولوژیکی افزایش دهند. پلیمرهای طبیعی را میتوان بهعنوان پروتئینها (کلاژن، ژلاتین، فیبرینوژن، الاستین، کراتین، اکتین و میوزین)، پلیساکاریدها (سلولز، آمیلوز، دکستران، کیتین و گلیکوزآمینوگلیکانها) یا پلیریبونوکلئوتیدها (DNA، RNA) طبقهبندی کرد (19). از طرفی استفاده از بافتهای سلولزدایی شده دارای مزیتهایی است که نسبت بهپلیمرهای مصنوعی کاربرد آنها را در پزشکی بازساختی گستردهتر نموده است زیرا این ساختار دقیق مشابه بدن بوده و زیستسازگار است و حتی ممکن است برخی از سیگنالهای شیمیایی و مکانیکی را نیز درپی داشته باشد که این باعث میشود سلولها بهرفتار فیزیولوژیکی طبیعی خود ادامه دهند. همچنین ECM تهیه شده از بافت سلولزدایی شده علاوه بر کاربرد در مهندسی بافت و پزشکی بازساختی بهعنوان حامل دارویی در حوزههای درمان سرطان نیز کاربرد دارند (20). در سالهای اخیر، استفاده از بافتهای سلولزدایی شده جهت تعویض و ترمیم بافتها و اندامهایی مانند پوست، مثانه، روده کوچک، ماهیچه اسکلتی، قلب، ریه، کلیه و بسیاری از بافتهای دیگر مورد توجه محققین بوده است. در فرآیند سلولزدایی، روش پرفیوژن در مورد بسیاری از بافتها و اندامها جهت حفظ ساختار سهبعدی ECM مورد استفاده قرار گرفته است اینروش در مهندسی بافت از اهمیت بالایی برخوردار است چرا که امکان نگهداری زیرساخت بافت یا اندام را فراهم میکند وECM آن بدون از دست رفتن ساختار و معماری حفظ میشود در اینروش بافت یا اندام به صورت ثابت در محفظهای قرار میگیرد و مواد و محلولهای لازم برای سلولزدایی از طریق عروق به بافت یا اندام اضافه و خارج میشود، اینروش نه تنها امکان سلولزدایی را فراهم میکند بلکه در مراحل بعدی باعث میشود که سلولها بهراحتی در بافت کشت داده شوند (22, 21) که در زیر بهچهار بافت سلولزدایی شده با اینروش اشاره شده است:
الف) پرفیوژن قلب: که از طریق دترجنتهای سدیم دئوکسی کولات 4%، تریتون ایکس 100 و آنزیم تریپسین صورت میگیرد و باعث حفظ ساختار ECM عروق خونی و سهولت انتقال سلول به آن میشود (24, 23).
ب) ریه: حفظ ساختار ریه بهدلیل داشتن غشاء تنفسی که حاوی شبکه عروقی و راههای هوایی حفرهدار میباشد از اهمیت بالایی برخوردار است، لذا پرفیوژن ریه موجب میشود تا اجزای اصلی ECM و ریزساختارهای کلی ریه بعد از پرفیوژن با دترجنتهای سدیم دودسیل سولفات 1% و تریتون ایکس 100 و آنزیم DNase حفظ شوند (24).
ج) کبد: حذف محتوای سلولی از طریق پرفیوژن کبد با دو دترجنت SDS1%، تریتون 100-X صورت گرفته است. عمل سلولزدایی کبد با هدف حذف محتوای سلولی و حفظ ECM از روشهای مختلف پرفیوژن مانند استفاده از فشار جریان ثابت و سرعت جریان ثابت صورت گرفته است که اساس هر روش مبتنی بر پمپ پرستیالتیک-پرفیوژن است. معمولاً پرفیوژن کبد از طریق سیستم عروق وریدی و یا شریانی صورت میگیرد که هر کدام از اینروشها چالشی برای محقیقن بوده است، چرا که استفاده از عروق شریانی باعث حذف DNA بیشتر و حفظ بهتر GAGها میشود در حالیکه عروق وریدی منجر بهحفظ فاکتورهای رشد کبدی (Hepatocyte Growth Factor, HGF) میشود با این حال اصلیترین چالش در پرفیوژن کبد، استفاده از درصدهای دترجنتها و روشهای فیزیکی و آنزیمی بوده است چرا که در سلولزدایی کبد حذف DNA بهصورت کامل انجام نمیشود و همچنین استفاده از SDS 1% منجر به فروپاشی شبکه عروقی در مقایسه با تریتون ایکس 100 در درصدهای 0/5 و 1 میشود. با اینحال نتایج کلی مطالعات نشان میدهد که استفاده از دو دترجنت SDS1% و تریتون ایکس 100 منجر بهحذف بهتر سلولها و حفظ میزان بالاتری از کلاژن و GAGها میشود (26, 25).
د) کلیه: پرفیوژن کلیه از طریق شریان کلیوی و دترجنتهای SDS و تریتون ایکس 100 و آنزیم DNase % 0/025 صورت پذیرفته است. در اینروش علاوه بر حفظ مؤلفههای ECM غلظتهای زیادی از سایتوکینها نیز حفظ میشوند که در تکثیر سلولهای پیشساز کلیوی و همچنین ترمیم بافت کلیه موثر بودهاند (28, 27). هدف از سلولزدایی بافت یا اندام، بهدست آوردن ساختار طبیعی یک بافت برای میزبان بودن سلولهای مختص به آن بافت یا اندام است. بالطبع حضور فاکتورهای رشد و تمایزی در یک ECM میتواند فرایند تمایز و رشد سلولها را بهصورت طبیعی پیش ببرد با این حال در روشهای نوین از ECM به همراه ترکیبات دیگری مانند پلیمرهای طبیعی یا مصنوعی بهعنوان القاکننده در ساختار داربستهای مهندسیشده جهت کشت سلول و تمایز بهبافت هدف استفاده می شود. این پلیمرها بهعنوان یک القا کننده در ساختار داربستهای ECM ترکیب شده و ECM مهندسی شدهای را بهوجود میآورند که میتواند در کشت سلول و تمایز بهبافت هدف نقش ایفا کند بهعنوان مثال با ایجاد عاملهای پیوندی در ECM با استفاده از گلوتارآلدئید میتوان علیرغم حفظ ساختارهای فیبری باعث افزایش چسبندگی سلولها به داربست نهایی نیز شد (29). ECM بهعنوان یک داربست جهت ترمیم و بهبود فعالیتهای بیولوژیکی در نظر گرفته میشود، که در نهایت بسته به نوع استفاده از آن در شرایط آزمایشگاهی و در بدن (in vivo) بهصورت پودر، ورق و هیدروژل در دسترس قرار میگیرد (30). اگرچه تهیه داربست از بافتهای سلولزدایی شده برای ترمیم بافتهای مختلفی کاربرد دارد و روشهای متعددی برای سلولزدایی این بافتها وجود دارد اما در مورد سلولزدایی سیستم عصبی مرکزی به مطالعات گستردهتری نیاز است. بااینحال چندین روش برای سلولزدایی از بافتهای سیستم عصبی مرکزی مانند مغز، نخاع و مخچه بهکار گرفته شدهاند که توانستهاند داربست مناسبی برای رفتار و عملکرد سلولها (32, 31) و رگزایی فراهم کرده و پروتیئنها و عوامل رشد را بعد از سلولزدایی در ECM حفظ کنند (33). از ECM بافت مغز میتوان جهت پوشش کف ظرف کشت (Coating) (17)، اضافهکردن بهمحیط کشت و تهیه هیدروژل (32) استفاده کرد. آزمایشات بسیاری در شرایط آزمایشگاهی صورت گرفته که ثابت میکند ECM سلولزدایی شده از بافتهای مربوط بهسیستم عصبی مرکزی ازجمله مغز میتواند ریزمحیط مناسبی برای رشد، مهاجرت، تکثیر و تمایز سلولهای بنیادی عصبی فراهم کند (34, 32, 31). به این ترتیب داربستهای سلولزدایی شده نقش مهمی در بازسازی بافت ایفا میکنند و نتایج مقدماتی بهدست آمده از آزمایشات درونتنی این موضوع را تایید میکند که کشت سلولهای مختص یک بافت در ECM سلولزدایی شده همان بافت میتواند امکان رد پیوند را تا حدود زیادی کاهش دهد (33،34). بهعنوان مثال گزارشاتی مبنی بر امکان کاربرد موثر این داربستها در بازسازی و درمان بیماریهای عصبی مانند پارکینسون وجود دارد (34,32,31).
سلولزدایی بافت مغز
هر بافت دارای ترکیباتی است که روی رفتار سلولهای آن بافت اثر متفاوتی نسبت به بافتهای دیگر میگذارد، از اینرو ECM هر بافت خاص در فرآیندهای سلولی، نقشهای متفاوتی را ایفا میکنند؛ بافت مغز بهدلیل شکننده بودن آن دارای ECM منحصربهفردی است بنابراینروشهای سلولزدایی آن نیز قابل تأمل است.
روشهای سلولزدایی بافت مغز
در خصوص سلولزدایی بافت مغز چندین مقاله چاپ شده است که در آنها عمدتاً سلولزدایی به سه صورت: روش دترجنت، روش دترجنت-آنزیم و روش فیزیکوشیمیایی-آنزیم بهکار گرفته شدهاند. ما در این مطالعه بافت مغز سلولزدایی شده را به اختصار با BEM (Brain Extracellular Matrix) نشان میدهیم. شکل 1، تصویر شماتیک هر سه روش سلولزدایی را نشان می دهد.
روش دترجنت: از یک یا چند دترجنت برای حذف سلولها استفاده میشود و بعد از شستشو با آب یا PBS بافت مقدار کمتری از سلولهای خود را با اینروش از دست میدهد.
روش دترجنت – آنزیم: علاوه بر دترجنت از آنزیم هم برای سلولزدایی استفاده میشود که بعد از هر بار شستشو با آب یا PBS نسبت به روش دترجنت بافت مقدار زیادی از سلول خود را از دست میدهد و شفافتر میشود.
روش فیزیکوشیمیایی – آنزیم: در اینروش از روشهای فیزیکی مانند فریز و ذوب بافت، از روشهای شیمیایی مثل استفاده از دترجنتها و از مواد آنزیمی برای حذف سلولها استفاده میشود که در هر مرحله بعد از شستشو بافت مقدار زیادی از سلولهای خود را از دست میدهد و نسبت بهروشهای قبلی شفافتر و سفیدتر میشود.
روش دترجنت: مطالعات انجام شده در راستای سلولزدایی بافت مغز با استفاده از روش شیمیایی در جدول 1 خلاصه شده است دکواچ و همکارانش مغز خوک سلولزدایی شده را با استفاده از محلول SDS 1% تهیه کردند. آنها بافت را در این دترجنت غوطهور کرده و هر 24 ساعت یکبار به مدت 3 الی 4 روز محلول را جهت حذف سلولهای جداشده از ECM تعویض کردند. در نهایت برای حذف SDS باقیمانده، بافت را 10 تا 12 بار با آب مقطر شستشو داده و در دور (دور در دقیقه)rpm 10000 به مدت 5 دقیقه سانتریفیوژ کردند (17). ژااو و همکاران (35)، کیان لین (36) و شو و همکاران (37) از دو دترجنت SDC 4 % و تریتون ایکس 100 با دور سانترفیوژ 120 در کمتر از سه روز بافت مغز را سلولزدایی کردند. در مقایسه با بافت طبیعی، شکل مغز بعد از سلولزدایی با دترجنتها به صورت شفاف و سفید در میآید که این نشاندهنده حذف سلولها و باقی ماندن ماتریکس خارج سلولی بافت است (36, 17). علاوه بر این رنگآمیزی با رنگهای DAPI (4′,6-diamidino-2-phenylindole) و هماتوکسین-ائوزین (H&E) از BEM نشاندهنده عدم حضور سلولها و بقایای هستهای است. همچنین نتایج تصویربرداری با میکروسکوپ الکترونی SEM، منافذ و ساختار شبکه سهبعدی BEM را نشان میدهد (36, 17). حفظ GAGها و پروتئینهای فیبری، یکی از اهداف مهم در روش سلولزدایی بافت یا اندام است از اینرو کیان لین و همکاران حضور پروتئینهای کلاژن نوع4، فیبرونکتین و لامینین را با استفاده از روش رنگآمیزی ایمونوهیستوشیمی و همچنین حضور گلیکوزآمینوگلیکانها را با استفاده از روش رنگآمیزی اسیدشیف (Acid-schiff staining) در BEM اثبات کردند (36). از آنجاییکه سیگنالهای ECM در رفتارهای سلولی نقش دارند لذا میتوان از ECM بافتهای سلولزدایی شده در کشت سلولها و تأثیر آن در رفتارهای سلولی در شرایط آزمایشگاهی و در بدن استفاده نمود. از اینرو دکواچ و همکاران در مطالعه خود قابلیت کشت سلولهای بنیادی پرتوان القا شده (induced Pluripotent Stem Cells, iPSCs) و نورونها را روی هیدروژل BEM تهیه شده در مقایسه با ماتریژل گزارش کردند (17). آنها در مطالعهشان تمایز iPSCs روی بستر ECM بهسلولهای عصبی را با افزایش زوائد عصبی و افزایش بیان گاما-آمینوبوتریک اسید (γ-Amino Butyric Acid :GABA) در روز هشتم نشان دادند. علاوه بر این بیان مارکر عصبی پروتئین2 مرتبط با میکروتوبول (microtubule associated protein II: MAP2) در هفته اول و بیان سیناپسین بهعنوان یک نشانگر بلوغ نورونها در هفته دوم کشت نورونها روی بستر BEM نیز توسط آنها تایید شد. علاوه بر تمایز، قابلیت بقاء و رشد سلولها یکی دیگر از رفتارهای سلولی است که ECM در آن نیز دخیل است از اینرو شو و همکاران اثر BEM را در بقاء سلولهای C6 گلیوما در 24 ساعت بعد از کشت روی ECM مغز تا 90% گزارش کردند (37). اثر BEM در شرایط بدن نیز در مطالعه دکواچ مورد بررسی قرار گرفته است. نتایج ایمونوهیستوشیمی بهدست آمده از مقاطع بافتی پس از تزریق ژلهای ماتریکس مغزی وجود پروتئینهای فیبری را در داخل بدن نشان میدهد. بهطورکلی نتایج بهدستآمده در این مطالعات نشان میدهد که استفاده از دترجنتهای یونی و غیریونی در سلولزدایی بافت مغز نتایج مطلوبی بههمراه داشته است.

شکل1: شکل شماتیک از روشهای سلولزدایی بافت مغز. در شکل سه روش نشان داده شده است
جدول 1: مطالعات موجود با روش دترجنت برای سلولزدایی بافت مغز

چهار مطالعه در خصوص سلولزدایی بافت مغز با روش دترجنت وجود دارد که از دترجنت های SDS و ترتیون X-100 برای سلولزدایی
بافت مغز استفاده کردهاند و نهایتاً کمتر از چهار روز به بافت سلولزدایی شده مغز دست یافتهاند.
جدول2: مطالعات موجود با روش دترجنت-آنزیم برای سلولزدایی بافت مغز.

سه مطالعه در خصوص سلولزدایی بافت مغز با روش دترجنت-آنزیم وجود دارد که از دترجنت های SDS و ترتیون X-100 و از آنزیم های DNase و تریپسین برای سلولزدایی بافت مغز استفاده کردهاند.
روش دترجنت-آنزیم
چندین مطالعه با استفاده از روش دترجنت-آنزیم مورد بررسی قرار گرفته که بهطور خلاصه در جدول2 ذکر شده است. در سال 2014 دوایل و همکاران جهت کشت سهبعدی سلولهای بنیادی عصبی روی بستر BEM، قطعات 5/1 میلیمتر مغز موش را با استفاده از دترجنتهای SDC 4% و %3تریتون ایکس 100 و آنزیمDNaseI با غلظت 40 کیلو واحد بر میلیلیتر و با دور سانتریفیوژ 150 در دقیقه طی کمتر از سه روز سلولزدایی کردند. آنها در مطالعه شان ثابت کردند که BEM تهیه شده به این روش میتواند بستر مناسبی برای رشد سلولهای بنیادی عصبی تمایز نیافته فراهم کند (38). سود و همکاران با استفاده از آنزیمهای تریپسین با غلظت 05/0% و DNaseI با غلظت40 کیلو واحد بر میلیلیتر و دترجنتهایSDC 4% و 3% تریتون ایکس 100 در کمتر از 24 ساعت به BEM جنین و بزرگسال خوک دست یافتند. آنها در مطالعاشان به این نتیجه رسیدند که حضور برخی از ترکیبات ECM و مقدار DNA حذفشده در بافت سلولزدایی شده به سن و موقعیت بافتهای سیستم عصبی مرکزی بستگی دارد (3). ژو و همکاران نیز از اینروش برای سلولزدایی بافتمخچه استفاده کردند. آنها در ابتدا ذکر کردند که مخچه بهآسانی در زمان شستشو و تیمار با دترجنتها و آنزیم متلاشی میشود، بههمین دلیل از درصدهای کمتر دترجنتها و با آنزیم تریپسین 05/0% در 60 و 100 دور در دقیقه از سانتریفیوژ استفاده کردند و نهایتاً با اینروش در کمتر از 4 روز به بافت سلولزدایی شده دست یافتند (34). در مقایسه با بافت طبیعی، مقاطع مغز بعد از سلولزدایی با دترجنت و آنزیم، به شکل کوچکتر، نازکتر، سفیدتر و شفاف تر در میآیند (38). این در حالی است که انسجام داربستی بافت مغز تقریباً حفظ میشود. رنگآمیزی مقاطع مغز و مخچه سلولزدایی شده با استفاده از DAPI و H&E حضور حداقلی مواد سلولی بعد از سلولزدایی را نشان داد. (38, 34, 3). از طرف دیگر نتایج الکتروفورز DNA باقیمانده از مخچه سلولزدایی شده نشان میدهد که تقریباً 95% از مواد هستهای از بین رفته است (34). علاوه بر این تعیین غلظت DNA در مغز جنین و بزرگسال خوک سلولزدایی شده تأیید میکند که با در نظر گرفتن وزن خشک BEM، هنوز مقدار 30 نانوگرم بر میلیلیتر از DNA در ECM لیوفیلیزه شده وجود دارد. با توجه به اینکه آستانه قابل قبول غلظت DNA به جا مانده بعد از سلولزدایی کمتر از 50 نانوگرم بر میلیلیتر است لذا این مقدار ثابت میکند که سلولزدایی بهخوبی انجام شده است (3). PCR برای ژن بتا دو میکروگلوبولین (Beta-2-Microglobulin: B2M) در ابتدا و انتهای مراحل سلولزدایی از مقاطع مغز نشان میدهد که در همان ابتدای سلولزدایی فرآیند حذف مواد هستهای آغاز میشود (38). سود و همکاران در مطالعهشان میزان بیان پروتئینهای BEM جنین و بزرگسال خوک را با بارگذاری پروتئینها در چاهکهای الکتروفورز و بررسی نتایج باندها بهدست آوردند که حاکی از تفاوت بیان پروتئینهای ECM در بین گروههایشان بود. آنها به این نتیجه رسیدند که بیان پروتئینها به سن بستگی دارد، برای مثال، شدت باند کلاژن در ECM جنین نسبت به ECM بزرگسالان بیشتر بود (3). آنها علاوه بر الکتروفورز از رنگآمیزی ایمنوهیستوشیمیایی برای تشخیص پروتئینها در BEM نیز استفاده کردند. نتایج رنگآمیزی علیه پروتئینهای ECM طی اینروش نشان داد که در مخچه سلولزدایی شده در مقایسه با بافت طبیعی کلاژن و گلیکوزآمینوگلیکانها باقی میمانند اما میلین از بین میرود (34). رنگآمیزی پروتیئن لامینین در مقاطع BEM نیز نشاندهنده حضور پروتئینهای ضروری در مغز بعد از سلولزدایی بود (38). ECM در رفتارهای سلولی از جمله قابلیت بقاء، تمایز و رفتارهای دیگر نقش بسزایی دارد از اینرو نقش ECMهای بهدست آمده از روش دترجنت- آنزیم روی سلولهای کشت یافته نیز در مطالعات حاضر بررسی شده است. بر این اساس دوایل و همکاران در مطالعهشان قابلیت تکثیر سلولهای بنیادی عصبی را با کشت در BEM در حالتهای دو و سه بعدی بررسی کردند. نتایج حاصل از مطالعهشان نشان داد که این سلولها ضمن حفظ بنیادینگی خود در خارج از بدن و در حضور عوامل میتوژنیک و BEM، میتوانند تکثیر یابند (38). سود و همکاران جهت بررسی رشد و تمایز نورونهای اولیه موشی این سلولها را در ژلهای BEM مهندسی شده کشت دادند و به این نتیجه رسیدند که BEM میتواند رشد و تمایز به سلولهای گلیا و تشکیل شبکه آکسونی را در سلولهای تمایز یافته افزایش دهد. از آنجاییکه آستروسیتها نقش مهمی در تعاملات ECM و نورونها دارند، اثر BEMروی تمایز به آستروسیتها و رفتار آستروسیتها در برابر تمایز عصبی نیز مورد بررسی قرار گرفته است، نتایج نشان میدهد که این سلولها بهوسیله پروتئین های موجود در BEM میتوانند در روند تشکیل شبکه عصبی نقش ایفا کنند. بافت سلولزدایی شده مغز جنین نیز میتواند به عنوان ریز محیط مناسبی جهت رشد سلولهای عصبی جنین مورد استفاده باشد، و نیز احتمالاً دارای پروتیئنهایی است که میتواند تعاملات ECM و نورون را تسهیل نماید (3). ECM مخچه نیز حاوی پروتئینهایی مانند پروتئینهای حمایتگر نورونها و عوامل رشد است که باعث تکثیر، مهاجرت و تمایز سلولهای بنیادی عصبی به نورون ها و آستروسیتها میشود. این یافتهها با توجه به رنگآمیزی بتاتوبولین3 در شرایط آزمایشگاهی و تزریق زیرپوستی و داخل جمجهای ECM مخچه تأیید شده است (34). یانگ هانگ و همکاران نیز اخیراً برای افزایش بقای عصبی، رشد عصبی و کاهش پاسخهای التهابی از ECM بافت مغز خوک استفاده کردند آنها بافت مغز را بهمدت یک شبانهروز در آب و در دمای 4 درجه سانتیگراد نگهداری کردند و پس از آن از آنزیم تریپسین 02/0% در دمای 37 درجه سانتیگراد به مدت یک ساعت استفاده کردند، پس از تیمار با SDC4%، سوکروز 1 مولار برای سلولزدایی استفاده کردند و بین هر مرحله از PBS و آب برای شستشوی ECM استفاده کردند. بررسی میزان DNA باقیمانده، GAG و کلاژن حفظ شده در این مطالعه نشان داد که سلولزدایی بهخوبی اتفاق افتاده است، علاوه بر این آنها نشان دادند که ECM بهدست آمده با اینروش بهدلیل داشتن فاکتورهای زیادی از جمله FGF1 و FGF2 توانسته است باعث افزایش تکثیر و تمایز سلولهای عصبی شود (39). بهطور کلی نتایج بهدست آمده در این مطالعات نشان میدهد که استفاده از دترجنت-آنزیم میتواند ساختار سه بعدی بافت مغز را تا حدودی حفظ کرده و معماری بافت کمتر دستخوش تغییر قرار گیرد. ECM سلولزدایی شده مغز و مخچه میتوانند بهعنوان یک بستر برای رشد، تکثیر، مهاجرت و تمایز سلولها در شرایط آزمایشگاهی در نظر گرفته شود، در حالیکه مطالعات بیشتری برای قابلیت استفاده از آن در بدن لازم است.
روش فیزیکوشیمیایی-آنزیم
علیرغم اینکه روشهای سلولزدایی با مواد شیمیایی و آنزیمی میتوانند تا حدودی ساختارهای بافت را حفظ کنند اما محققان دریافتند که استفاده از عوامل فیزیکی بههمراه این مواد ضمن آسیب کمتر باعث تسهیل در حذف سلولهای بافت میشوند. از جمله عوامل فیزیکی که در سلولزدایی بافت مغز استفاده شده است میتوان به نوسآنهای مکانیکی، سانتریفیوژ و شوکهای اسمتیک و دمایی به بافت اشاره کرد. بسته به نوع بافت و شدت روشهای فیزیکی، این عوامل می توانند باعث از بین رفتن سلولها و تسهیل در مرگ سلولی شوند. یین و همکاران در مطالعه خود نشان دادند که 120 دور در دقیقه طی سانتریفیوژ میتواند برای سلولزدایی نخاع مورد استفاده قرار گیرد (40). علاوه بر آن بایگورا و همکاران و ریباتی و همکاران در مطالعهشان برای سلولزدایی بافت مغز از تکرار چهار چرخه فریز و ذوب استفاده کردند (41, 33). روشهای فیزیکی بهتنهایی نمیتوانند برای سلولزدایی بافت مورد استفاده باشند و نقشی در حذف سلولهای مرده درون بافت ندارند. اینروشها می توانند بههمراه روشهای شیمیایی و آنزیمی در تسهیل سلولزدایی بافت نقش داشته باشند (18). مطالعات در دسترس برای سلولزدایی بافت مغز با استفاده از روشهای فیزیکی، شیمیایی و آنزیمی در جدول 3 خلاصه شده است.
جدول 3: مطالعات موجود با روش فیزیکوشیمیایی-آنزیم برای سلولزدایی بافت مغز.
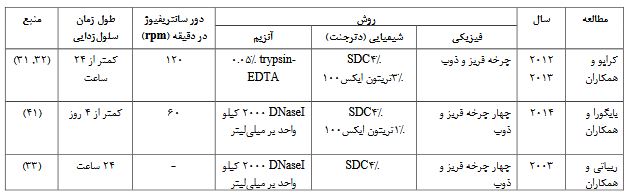
سه مطالعه در خصوص سلولزدایی بافت مغز با روش فیزیکوشیمیایی-آنزیم وجود دارد که از چند مرحله ذوب و فریز بافت به عنوان روش فیزیکی و از دترجنت های SDS و ترتیون X-100 و از آنزیم های DNase و تریپسین برای سلولزدایی بافت مغز استفاده کرده اند.
علیرغم دستهبندی روشهای سلولزدایی بافت مغز به سه صورت ذکر شده، اخیراً گراناتو و همکاران مطالعهای را روی روش جدیدی از سلولزدایی با مدغوم کردن روش فیزیکی و دترجنت انجام دادهاند، آنها از تکرارهای فریز و ذوب و شستشوی 24 ساعته بافت مغز در SDC 4% به ECM بافت مغز دست یافتند که اینروش علیرغم اینکه یک روش سریع و آسانی است اما جهت تایید تکرارپذیری به مطالعات بیشتری نیاز دارد (42). همانطور که در بالا ذکر شد، بافت مغز بعد از سلولزدایی بهدلیل حذف سلولها کوچکتر و شفافتر میشود. کراپو و همکاران نیز در مطالعه خود کوچکتر شدن سه بافت از سیستم عصبی مرکزی از جمله بافت مغز را بعد از سلولزدایی با روشهای فیزیکی، شیمیایی و آنزیمی گزارش کردند (31,41). بهطورکلی استفاده از روشهای فیزیکی مانند تکرار چرخه فریز و ذوب میتواند سبب از بین بردن محتوای هستهای میشود که نتیجه آن به وسیله رنگآمیزی با روشهای H&E و DAPI بهدست آمده است (42, 32, 31). این دادهها نشان میهند که 91% از DNA حذف شده (41) و غلظت کمتر از 50 نانوگرم از DNA در هر گرم از بافت باقیمانده است (31). علیرغم اینکه چرخههای فریز و ذوب بهدلیل ایجاد کریستالهایی در آب بافت سبب برهم خوردن ساختار و معماری بافت میشوند اما بایگورا و همکاران در مطالعهشان با استفاده از تصویربرداری SEM از BEM حضور الاستین و گلیکوزآمینوگلیکانهای سولفیده شده را نشان دادند و به این نتیجه رسیدند که ساختار سهبعدی مغز بعد از سلولزدایی بدون شکستگی در ماتریکس حفظ می شود و معماری بافت تغییر نمیکند (41). علاوه بر الاستین، پروتئینهای دیگری از جمله لامینین و میلین در BEM قابل شناسایی بوده است (31). با استناد بر این نتایج، علیرغم اینکه ساختار و ترکیبات ECM در مغزهای سلولزدایی شده با روش فیزیکوشیمیایی-آنزیم حفظ میشوند اما مواد هستهای بهطور کامل حذف نمیشوند. از آنجایی که فاکتورهای رشد در ECM سایر بافتها نقش مهمی در رفتار سلولها دارند حضور آنها در BEM نیز از اهمیت بالایی برخوردار است از اینرو کراپو و همکاران با تأیید حضور فاکتور رشد عروقی اندوتلیال (Vascular Endothelial Growth Factor, VEGF)، فاکتور رشد فیبروبلاست (basic Fibroblast Growth Fact, bFGF) و فاکتور رشد عصبی (Nerve Growth Factor, NGF ) در بافتهای سلولزدایی شده سیستم عصبی مرکزی نشان دادند که بعد از سلولزدایی عوامل رشد باقی میمانند (31). ریباتی و همکاران نیز در مطالعهشان نقش bFGF و VEGF باقیمانده بعد از سلولزدایی را عاملی در رگزایی بعد از پیوند دانستند (33). با توجه به عملکرد ECM در رفتارهای سلولی نقش BEMهای بهدست آمده از روش فیزیکوشیمیایی-آنزیمی در مطالعات حاضر بررسی شده است. بایگورا و همکاران سلولهای بنیادی مزانشیمی (Mesenchymal Stem Cells, MSCs) را روی BEM کشت دادند و در پی نتایج بهدست آمده از مقاطع بافتی رنگآمیزی شده با روش DAPI و H&E مشاهده کردند که سلولها نه تنها در سطح خارجی ECM رشد می کنند بلکه در داخل آن نیز وجود دارند. آنها همچنین گزارش کردند که BEM میتواند در چسبندگی، رشد و تکثیر سلولها مؤثر باشد (41). کراپو و همکاران در مطالعهای که در سال 2012 چاپ کردند، گزارش کردند که غلظتهای متفاوتی از BEM میتواند در هر یک از رفتارهای سلولی نقش داشته باشد. بهطور مثال: تکثیر، مهاجرت و تمایز سلولهای PC12 (Phaeochromocytoma) بهترتیب با غلظتهای 5/2، 10و 100 میکروگرم بر میلیلیتر از BEM امکانپذیر است. علاوه بر این نشان دادند که اثر این غلظتها در تغییر رفتار سلولهای مختلف متفاوت است (32). این نشان میدهد که غلظتهای متفاوت BEM اثر مثبتی روی رفتارهای سلولی میگذارد و پاسخ سلولهای بنیادی بهطیف غلظتهای 5/2 تا 100میکروگرم بر میلیلیتر از BEM بیشتر است. نتایج حاصل از مطالعات در مورد سلولزدایی بافت مغز بهروش فیزیکوشیمایی-آنزیم، اهمیت روش فیزیکی خصوصاً استفاده از چرخههای مکرر فریز و ذوب را بههمراه روشهای دترجنت و آنزیم جهت تسهیل در سلولزدایی نشان میدهد.
نتیجهگیری
از میان دترجنتهای موجود، تریتون ایکس 100 با غلظتهای 1% و 3% ، سدیم دئوکسی کولات با غلظت 4% و سدیم دودسیل سولفات با غلظت 4% بیشترین کاربرد را در سلولزدایی بافت مغز را دارند. از بین آنزیمها، تریپسین با هدف حذف سلولهای موجود در ECM بافت مغز کاربرد بیشتری نسبت بهآنزیمهای دیگر دارد. با این حال آنزیم DNaseI با غلظتهای 40 و 100 کیلو واحد بر میلیلیتر نیز مورد استفاده قرار گرفته است. از طرفی تکرار چرخههای فریز و ذوب قبل از سلولزدایی میتواند سلولزدایی را تسهیل کند. با توجه به سهروش سلولزدایی بافت مغز تعریف شده در این مطالعه، نیروی گریز از مرکز حاصل از دستگاه سانتریفیوژ با 60 تا 120 دور در دقیقه امری ضروری برای حذف سلولهای جدا شده از ECM باقیمانده بافت خواهد بود. اگرچه DNAبهطور کامل در سلولزدایی حذف نمیشود اما ترکیبات ECM حفظ میشوند و میتوان از این ترکیبات بهعنوان بستر مناسبی برای تکثیر، مهاجرت و تمایز دو بعدی و سه بعدی برای سلولهای بنیادی با غلظتهای 2/5 تا 100 میکروگرم بر میلیلیتر در شرایط آزمایشگاهی استفاده نمود. در نهایت ECM مغز میتواند گزینه مناسبی برای کاربردهای پزشکی بازساختی و مهندسی بافت در آینده باشد.
تعارض در منافع: وجود ندارد.
لامینین: این پروتیئن توسط سلولهای آستروسیت بیان میشود و همچنین متعاقب آسیب مغزی در بزرگسالان افزایش سطح بیان آن توسط آستروسیتها اتفاق میافتد. علاوه بر این لامینین نقش مهمی در ساخت و ترمیم سد خونی مغزی دارد (15). از آنجایی که ECM حاوی ترکیباتی است که میتواند روی رفتارهای سلولی اثر بگذارد، فرایندی تحت عنوان سلولزدایی تعریف میشود که طی آن سلولهای ساکن در ECM یک بافت یا اندام از آن جداشده و تنها ECM آن باقی بماند که بهعنوان یک بستر و داربست میتواند در شرایط آزمایشگاهی و در بدن، در بازسازی بافت و اندامها کاربرد داشته باشد.
روشهای سلولزدایی
در سلولزدایی حفظ معماری بافت، ساختار و ترکیب ECM از اهمیت بالایی برخوردار است (16). در فرآیند سلولزدایی بافت یا اندام، از روشهای فیزیکی، شیمیایی و زیستی برای حذف سلولها و سپس شستشو با آب یا محلول نمک فسفات (PhosphateBuffered Saline) برای حذف بقایای سلولی استفاده میشود.
روشهای شیمیایی
برای حذف سلولها میتوان از مواد شیمیایی استفاده کرد، ازجمله: اسیدها و بازها، محلولهای هایپو و هایپرتونیک، الکل، دترجنتها و مواد دیگری مانند استون (16). از بین این مواد، دترجنتهای یونی و غیریونی مانند تریتون X-100، سدیم دئوکسی کولات (Sodium Deoxycolate, SDC) و سدیم دودسیل سولفات (Sodium Dodecyl Sulfate, SDS) بهطور موثرتری در فرایند سلولزدایی بافت کاربرد دارند (16).
روشهای زیستی
استفاده از مواد زیستی جهت حذف سلولها در فناوری سلولزدایی بافت به دو دسته آنزیم و غیر آنزیم تقسیم میشوند (16). آنزیمها شامل نوکلئازها (DNase و RNase) و تریپسین هستند. آنزیمDNase رایجترین نوکلئازی است که بسته به نیاز با غلظتهای مختلف در سلولزدایی بافت مورد استفاده بوده و باعث کاهش میزان 95 درصدی غلظت DNA در بافت مغز میشود (17). آنزیم تریپسین متداولترین پروتئازی است که اغلب با EDTA (Ethylenediaminetetraacetic acid) مورد استفاده قرار میگیرد. تریپسین با اثر روی آرژنین و لیزین باعث شکستن پیوند پپتیدی میشود، از اینرو تیمار طولانیمدت با این آنزیم میتواند سبب تخریب کلاژن، لامینین و فیبرونکتین ماتریکس خارج سلولی شود (18).
روشهای فیزیکی
سلولزدایی با روشهای فیزیکی مانند پرتوافکنی و تکرار چرخههای فریز و ذوب میتواند باعث سست شدن بافت و از بین رفتن گسستگی سلولها شود اما نمیتواند سلولهای مرده بافت را حذف کند از اینرو به شستشو و استفاده از نیروهایی که خود جزئی از عوامل فیزیکی بهحساب میآیند، مانند نیروی حاصل از سانتریفیوژ نیاز دارند (18).
کاربرد بافت سلولزدایی شده در مهندسی بافت
داربستهای سلولی در مهندسی بافت و پزشکی بازساختی به دو دسته پلیمرهای مصنوعی و داربستهای طبیعی تقسیمبندی میشوند. در داربستهای مصنوعی از پلیمرهای مصنوعی در ساخت داربست استفاده میشود که شامل گروه بزرگی از پلیمرهای تخریبپذیر هستند. این داربستها به دلیل خاصیت منحصربهفرد خود از جمله نسبت سطح به حجم زیاد، تخلخل زیاد با اندازه منافذ کوچک و خاصیت مکانیکی خوبی که دارند مورد توجه محققین قرار گرفتهاند. آنها مزایای دیگری مانند زیستسازگاری و خصوصیات بیولوژیکی دارند که در مهندسی بافت و بازسازی اندام کاربرد دارد. مواد داربست بسته به کاربرد مورد نظر میتوانند مصنوعی یا زیستی، قابل تجزیه یا غیر قابل تجزیه باشند. خواص پلیمرها به ترکیب، ساختار و ترتیب ماکرومولکولهای تشکیل دهنده آنها بستگیدارد. از نظر خصوصیات ساختاری، شیمیایی و بیولوژیکی میتوان آنها را در انواع مختلفی مانند سرامیک، شیشه، پلیمر و غیره طبقهبندی کرد. کوپلیمرهای Polylactic acid PLA) )، (PGA) poly glycolic acid و poly lactic-co-glycolic acid PLGA)) از متداولترین پلیمرهای مصنوعی در مهندسی بافت هستند. مواد طبیعی بهدلیل خاصیت فعال زیستی، تعامل بهتری با سلولها دارند و این به آنها این امکان را میدهد تا عملکرد سلولها را در سیستم بیولوژیکی افزایش دهند. پلیمرهای طبیعی را میتوان بهعنوان پروتئینها (کلاژن، ژلاتین، فیبرینوژن، الاستین، کراتین، اکتین و میوزین)، پلیساکاریدها (سلولز، آمیلوز، دکستران، کیتین و گلیکوزآمینوگلیکانها) یا پلیریبونوکلئوتیدها (DNA، RNA) طبقهبندی کرد (19). از طرفی استفاده از بافتهای سلولزدایی شده دارای مزیتهایی است که نسبت بهپلیمرهای مصنوعی کاربرد آنها را در پزشکی بازساختی گستردهتر نموده است زیرا این ساختار دقیق مشابه بدن بوده و زیستسازگار است و حتی ممکن است برخی از سیگنالهای شیمیایی و مکانیکی را نیز درپی داشته باشد که این باعث میشود سلولها بهرفتار فیزیولوژیکی طبیعی خود ادامه دهند. همچنین ECM تهیه شده از بافت سلولزدایی شده علاوه بر کاربرد در مهندسی بافت و پزشکی بازساختی بهعنوان حامل دارویی در حوزههای درمان سرطان نیز کاربرد دارند (20). در سالهای اخیر، استفاده از بافتهای سلولزدایی شده جهت تعویض و ترمیم بافتها و اندامهایی مانند پوست، مثانه، روده کوچک، ماهیچه اسکلتی، قلب، ریه، کلیه و بسیاری از بافتهای دیگر مورد توجه محققین بوده است. در فرآیند سلولزدایی، روش پرفیوژن در مورد بسیاری از بافتها و اندامها جهت حفظ ساختار سهبعدی ECM مورد استفاده قرار گرفته است اینروش در مهندسی بافت از اهمیت بالایی برخوردار است چرا که امکان نگهداری زیرساخت بافت یا اندام را فراهم میکند وECM آن بدون از دست رفتن ساختار و معماری حفظ میشود در اینروش بافت یا اندام به صورت ثابت در محفظهای قرار میگیرد و مواد و محلولهای لازم برای سلولزدایی از طریق عروق به بافت یا اندام اضافه و خارج میشود، اینروش نه تنها امکان سلولزدایی را فراهم میکند بلکه در مراحل بعدی باعث میشود که سلولها بهراحتی در بافت کشت داده شوند (22, 21) که در زیر بهچهار بافت سلولزدایی شده با اینروش اشاره شده است:
الف) پرفیوژن قلب: که از طریق دترجنتهای سدیم دئوکسی کولات 4%، تریتون ایکس 100 و آنزیم تریپسین صورت میگیرد و باعث حفظ ساختار ECM عروق خونی و سهولت انتقال سلول به آن میشود (24, 23).
ب) ریه: حفظ ساختار ریه بهدلیل داشتن غشاء تنفسی که حاوی شبکه عروقی و راههای هوایی حفرهدار میباشد از اهمیت بالایی برخوردار است، لذا پرفیوژن ریه موجب میشود تا اجزای اصلی ECM و ریزساختارهای کلی ریه بعد از پرفیوژن با دترجنتهای سدیم دودسیل سولفات 1% و تریتون ایکس 100 و آنزیم DNase حفظ شوند (24).
ج) کبد: حذف محتوای سلولی از طریق پرفیوژن کبد با دو دترجنت SDS1%، تریتون 100-X صورت گرفته است. عمل سلولزدایی کبد با هدف حذف محتوای سلولی و حفظ ECM از روشهای مختلف پرفیوژن مانند استفاده از فشار جریان ثابت و سرعت جریان ثابت صورت گرفته است که اساس هر روش مبتنی بر پمپ پرستیالتیک-پرفیوژن است. معمولاً پرفیوژن کبد از طریق سیستم عروق وریدی و یا شریانی صورت میگیرد که هر کدام از اینروشها چالشی برای محقیقن بوده است، چرا که استفاده از عروق شریانی باعث حذف DNA بیشتر و حفظ بهتر GAGها میشود در حالیکه عروق وریدی منجر بهحفظ فاکتورهای رشد کبدی (Hepatocyte Growth Factor, HGF) میشود با این حال اصلیترین چالش در پرفیوژن کبد، استفاده از درصدهای دترجنتها و روشهای فیزیکی و آنزیمی بوده است چرا که در سلولزدایی کبد حذف DNA بهصورت کامل انجام نمیشود و همچنین استفاده از SDS 1% منجر به فروپاشی شبکه عروقی در مقایسه با تریتون ایکس 100 در درصدهای 0/5 و 1 میشود. با اینحال نتایج کلی مطالعات نشان میدهد که استفاده از دو دترجنت SDS1% و تریتون ایکس 100 منجر بهحذف بهتر سلولها و حفظ میزان بالاتری از کلاژن و GAGها میشود (26, 25).
د) کلیه: پرفیوژن کلیه از طریق شریان کلیوی و دترجنتهای SDS و تریتون ایکس 100 و آنزیم DNase % 0/025 صورت پذیرفته است. در اینروش علاوه بر حفظ مؤلفههای ECM غلظتهای زیادی از سایتوکینها نیز حفظ میشوند که در تکثیر سلولهای پیشساز کلیوی و همچنین ترمیم بافت کلیه موثر بودهاند (28, 27). هدف از سلولزدایی بافت یا اندام، بهدست آوردن ساختار طبیعی یک بافت برای میزبان بودن سلولهای مختص به آن بافت یا اندام است. بالطبع حضور فاکتورهای رشد و تمایزی در یک ECM میتواند فرایند تمایز و رشد سلولها را بهصورت طبیعی پیش ببرد با این حال در روشهای نوین از ECM به همراه ترکیبات دیگری مانند پلیمرهای طبیعی یا مصنوعی بهعنوان القاکننده در ساختار داربستهای مهندسیشده جهت کشت سلول و تمایز بهبافت هدف استفاده می شود. این پلیمرها بهعنوان یک القا کننده در ساختار داربستهای ECM ترکیب شده و ECM مهندسی شدهای را بهوجود میآورند که میتواند در کشت سلول و تمایز بهبافت هدف نقش ایفا کند بهعنوان مثال با ایجاد عاملهای پیوندی در ECM با استفاده از گلوتارآلدئید میتوان علیرغم حفظ ساختارهای فیبری باعث افزایش چسبندگی سلولها به داربست نهایی نیز شد (29). ECM بهعنوان یک داربست جهت ترمیم و بهبود فعالیتهای بیولوژیکی در نظر گرفته میشود، که در نهایت بسته به نوع استفاده از آن در شرایط آزمایشگاهی و در بدن (in vivo) بهصورت پودر، ورق و هیدروژل در دسترس قرار میگیرد (30). اگرچه تهیه داربست از بافتهای سلولزدایی شده برای ترمیم بافتهای مختلفی کاربرد دارد و روشهای متعددی برای سلولزدایی این بافتها وجود دارد اما در مورد سلولزدایی سیستم عصبی مرکزی به مطالعات گستردهتری نیاز است. بااینحال چندین روش برای سلولزدایی از بافتهای سیستم عصبی مرکزی مانند مغز، نخاع و مخچه بهکار گرفته شدهاند که توانستهاند داربست مناسبی برای رفتار و عملکرد سلولها (32, 31) و رگزایی فراهم کرده و پروتیئنها و عوامل رشد را بعد از سلولزدایی در ECM حفظ کنند (33). از ECM بافت مغز میتوان جهت پوشش کف ظرف کشت (Coating) (17)، اضافهکردن بهمحیط کشت و تهیه هیدروژل (32) استفاده کرد. آزمایشات بسیاری در شرایط آزمایشگاهی صورت گرفته که ثابت میکند ECM سلولزدایی شده از بافتهای مربوط بهسیستم عصبی مرکزی ازجمله مغز میتواند ریزمحیط مناسبی برای رشد، مهاجرت، تکثیر و تمایز سلولهای بنیادی عصبی فراهم کند (34, 32, 31). به این ترتیب داربستهای سلولزدایی شده نقش مهمی در بازسازی بافت ایفا میکنند و نتایج مقدماتی بهدست آمده از آزمایشات درونتنی این موضوع را تایید میکند که کشت سلولهای مختص یک بافت در ECM سلولزدایی شده همان بافت میتواند امکان رد پیوند را تا حدود زیادی کاهش دهد (33،34). بهعنوان مثال گزارشاتی مبنی بر امکان کاربرد موثر این داربستها در بازسازی و درمان بیماریهای عصبی مانند پارکینسون وجود دارد (34,32,31).
سلولزدایی بافت مغز
هر بافت دارای ترکیباتی است که روی رفتار سلولهای آن بافت اثر متفاوتی نسبت به بافتهای دیگر میگذارد، از اینرو ECM هر بافت خاص در فرآیندهای سلولی، نقشهای متفاوتی را ایفا میکنند؛ بافت مغز بهدلیل شکننده بودن آن دارای ECM منحصربهفردی است بنابراینروشهای سلولزدایی آن نیز قابل تأمل است.
روشهای سلولزدایی بافت مغز
در خصوص سلولزدایی بافت مغز چندین مقاله چاپ شده است که در آنها عمدتاً سلولزدایی به سه صورت: روش دترجنت، روش دترجنت-آنزیم و روش فیزیکوشیمیایی-آنزیم بهکار گرفته شدهاند. ما در این مطالعه بافت مغز سلولزدایی شده را به اختصار با BEM (Brain Extracellular Matrix) نشان میدهیم. شکل 1، تصویر شماتیک هر سه روش سلولزدایی را نشان می دهد.
روش دترجنت: از یک یا چند دترجنت برای حذف سلولها استفاده میشود و بعد از شستشو با آب یا PBS بافت مقدار کمتری از سلولهای خود را با اینروش از دست میدهد.
روش دترجنت – آنزیم: علاوه بر دترجنت از آنزیم هم برای سلولزدایی استفاده میشود که بعد از هر بار شستشو با آب یا PBS نسبت به روش دترجنت بافت مقدار زیادی از سلول خود را از دست میدهد و شفافتر میشود.
روش فیزیکوشیمیایی – آنزیم: در اینروش از روشهای فیزیکی مانند فریز و ذوب بافت، از روشهای شیمیایی مثل استفاده از دترجنتها و از مواد آنزیمی برای حذف سلولها استفاده میشود که در هر مرحله بعد از شستشو بافت مقدار زیادی از سلولهای خود را از دست میدهد و نسبت بهروشهای قبلی شفافتر و سفیدتر میشود.
روش دترجنت: مطالعات انجام شده در راستای سلولزدایی بافت مغز با استفاده از روش شیمیایی در جدول 1 خلاصه شده است دکواچ و همکارانش مغز خوک سلولزدایی شده را با استفاده از محلول SDS 1% تهیه کردند. آنها بافت را در این دترجنت غوطهور کرده و هر 24 ساعت یکبار به مدت 3 الی 4 روز محلول را جهت حذف سلولهای جداشده از ECM تعویض کردند. در نهایت برای حذف SDS باقیمانده، بافت را 10 تا 12 بار با آب مقطر شستشو داده و در دور (دور در دقیقه)rpm 10000 به مدت 5 دقیقه سانتریفیوژ کردند (17). ژااو و همکاران (35)، کیان لین (36) و شو و همکاران (37) از دو دترجنت SDC 4 % و تریتون ایکس 100 با دور سانترفیوژ 120 در کمتر از سه روز بافت مغز را سلولزدایی کردند. در مقایسه با بافت طبیعی، شکل مغز بعد از سلولزدایی با دترجنتها به صورت شفاف و سفید در میآید که این نشاندهنده حذف سلولها و باقی ماندن ماتریکس خارج سلولی بافت است (36, 17). علاوه بر این رنگآمیزی با رنگهای DAPI (4′,6-diamidino-2-phenylindole) و هماتوکسین-ائوزین (H&E) از BEM نشاندهنده عدم حضور سلولها و بقایای هستهای است. همچنین نتایج تصویربرداری با میکروسکوپ الکترونی SEM، منافذ و ساختار شبکه سهبعدی BEM را نشان میدهد (36, 17). حفظ GAGها و پروتئینهای فیبری، یکی از اهداف مهم در روش سلولزدایی بافت یا اندام است از اینرو کیان لین و همکاران حضور پروتئینهای کلاژن نوع4، فیبرونکتین و لامینین را با استفاده از روش رنگآمیزی ایمونوهیستوشیمی و همچنین حضور گلیکوزآمینوگلیکانها را با استفاده از روش رنگآمیزی اسیدشیف (Acid-schiff staining) در BEM اثبات کردند (36). از آنجاییکه سیگنالهای ECM در رفتارهای سلولی نقش دارند لذا میتوان از ECM بافتهای سلولزدایی شده در کشت سلولها و تأثیر آن در رفتارهای سلولی در شرایط آزمایشگاهی و در بدن استفاده نمود. از اینرو دکواچ و همکاران در مطالعه خود قابلیت کشت سلولهای بنیادی پرتوان القا شده (induced Pluripotent Stem Cells, iPSCs) و نورونها را روی هیدروژل BEM تهیه شده در مقایسه با ماتریژل گزارش کردند (17). آنها در مطالعهشان تمایز iPSCs روی بستر ECM بهسلولهای عصبی را با افزایش زوائد عصبی و افزایش بیان گاما-آمینوبوتریک اسید (γ-Amino Butyric Acid :GABA) در روز هشتم نشان دادند. علاوه بر این بیان مارکر عصبی پروتئین2 مرتبط با میکروتوبول (microtubule associated protein II: MAP2) در هفته اول و بیان سیناپسین بهعنوان یک نشانگر بلوغ نورونها در هفته دوم کشت نورونها روی بستر BEM نیز توسط آنها تایید شد. علاوه بر تمایز، قابلیت بقاء و رشد سلولها یکی دیگر از رفتارهای سلولی است که ECM در آن نیز دخیل است از اینرو شو و همکاران اثر BEM را در بقاء سلولهای C6 گلیوما در 24 ساعت بعد از کشت روی ECM مغز تا 90% گزارش کردند (37). اثر BEM در شرایط بدن نیز در مطالعه دکواچ مورد بررسی قرار گرفته است. نتایج ایمونوهیستوشیمی بهدست آمده از مقاطع بافتی پس از تزریق ژلهای ماتریکس مغزی وجود پروتئینهای فیبری را در داخل بدن نشان میدهد. بهطورکلی نتایج بهدستآمده در این مطالعات نشان میدهد که استفاده از دترجنتهای یونی و غیریونی در سلولزدایی بافت مغز نتایج مطلوبی بههمراه داشته است.

شکل1: شکل شماتیک از روشهای سلولزدایی بافت مغز. در شکل سه روش نشان داده شده است
جدول 1: مطالعات موجود با روش دترجنت برای سلولزدایی بافت مغز

چهار مطالعه در خصوص سلولزدایی بافت مغز با روش دترجنت وجود دارد که از دترجنت های SDS و ترتیون X-100 برای سلولزدایی
بافت مغز استفاده کردهاند و نهایتاً کمتر از چهار روز به بافت سلولزدایی شده مغز دست یافتهاند.
جدول2: مطالعات موجود با روش دترجنت-آنزیم برای سلولزدایی بافت مغز.

سه مطالعه در خصوص سلولزدایی بافت مغز با روش دترجنت-آنزیم وجود دارد که از دترجنت های SDS و ترتیون X-100 و از آنزیم های DNase و تریپسین برای سلولزدایی بافت مغز استفاده کردهاند.
روش دترجنت-آنزیم
چندین مطالعه با استفاده از روش دترجنت-آنزیم مورد بررسی قرار گرفته که بهطور خلاصه در جدول2 ذکر شده است. در سال 2014 دوایل و همکاران جهت کشت سهبعدی سلولهای بنیادی عصبی روی بستر BEM، قطعات 5/1 میلیمتر مغز موش را با استفاده از دترجنتهای SDC 4% و %3تریتون ایکس 100 و آنزیمDNaseI با غلظت 40 کیلو واحد بر میلیلیتر و با دور سانتریفیوژ 150 در دقیقه طی کمتر از سه روز سلولزدایی کردند. آنها در مطالعه شان ثابت کردند که BEM تهیه شده به این روش میتواند بستر مناسبی برای رشد سلولهای بنیادی عصبی تمایز نیافته فراهم کند (38). سود و همکاران با استفاده از آنزیمهای تریپسین با غلظت 05/0% و DNaseI با غلظت40 کیلو واحد بر میلیلیتر و دترجنتهایSDC 4% و 3% تریتون ایکس 100 در کمتر از 24 ساعت به BEM جنین و بزرگسال خوک دست یافتند. آنها در مطالعاشان به این نتیجه رسیدند که حضور برخی از ترکیبات ECM و مقدار DNA حذفشده در بافت سلولزدایی شده به سن و موقعیت بافتهای سیستم عصبی مرکزی بستگی دارد (3). ژو و همکاران نیز از اینروش برای سلولزدایی بافتمخچه استفاده کردند. آنها در ابتدا ذکر کردند که مخچه بهآسانی در زمان شستشو و تیمار با دترجنتها و آنزیم متلاشی میشود، بههمین دلیل از درصدهای کمتر دترجنتها و با آنزیم تریپسین 05/0% در 60 و 100 دور در دقیقه از سانتریفیوژ استفاده کردند و نهایتاً با اینروش در کمتر از 4 روز به بافت سلولزدایی شده دست یافتند (34). در مقایسه با بافت طبیعی، مقاطع مغز بعد از سلولزدایی با دترجنت و آنزیم، به شکل کوچکتر، نازکتر، سفیدتر و شفاف تر در میآیند (38). این در حالی است که انسجام داربستی بافت مغز تقریباً حفظ میشود. رنگآمیزی مقاطع مغز و مخچه سلولزدایی شده با استفاده از DAPI و H&E حضور حداقلی مواد سلولی بعد از سلولزدایی را نشان داد. (38, 34, 3). از طرف دیگر نتایج الکتروفورز DNA باقیمانده از مخچه سلولزدایی شده نشان میدهد که تقریباً 95% از مواد هستهای از بین رفته است (34). علاوه بر این تعیین غلظت DNA در مغز جنین و بزرگسال خوک سلولزدایی شده تأیید میکند که با در نظر گرفتن وزن خشک BEM، هنوز مقدار 30 نانوگرم بر میلیلیتر از DNA در ECM لیوفیلیزه شده وجود دارد. با توجه به اینکه آستانه قابل قبول غلظت DNA به جا مانده بعد از سلولزدایی کمتر از 50 نانوگرم بر میلیلیتر است لذا این مقدار ثابت میکند که سلولزدایی بهخوبی انجام شده است (3). PCR برای ژن بتا دو میکروگلوبولین (Beta-2-Microglobulin: B2M) در ابتدا و انتهای مراحل سلولزدایی از مقاطع مغز نشان میدهد که در همان ابتدای سلولزدایی فرآیند حذف مواد هستهای آغاز میشود (38). سود و همکاران در مطالعهشان میزان بیان پروتئینهای BEM جنین و بزرگسال خوک را با بارگذاری پروتئینها در چاهکهای الکتروفورز و بررسی نتایج باندها بهدست آوردند که حاکی از تفاوت بیان پروتئینهای ECM در بین گروههایشان بود. آنها به این نتیجه رسیدند که بیان پروتئینها به سن بستگی دارد، برای مثال، شدت باند کلاژن در ECM جنین نسبت به ECM بزرگسالان بیشتر بود (3). آنها علاوه بر الکتروفورز از رنگآمیزی ایمنوهیستوشیمیایی برای تشخیص پروتئینها در BEM نیز استفاده کردند. نتایج رنگآمیزی علیه پروتئینهای ECM طی اینروش نشان داد که در مخچه سلولزدایی شده در مقایسه با بافت طبیعی کلاژن و گلیکوزآمینوگلیکانها باقی میمانند اما میلین از بین میرود (34). رنگآمیزی پروتیئن لامینین در مقاطع BEM نیز نشاندهنده حضور پروتئینهای ضروری در مغز بعد از سلولزدایی بود (38). ECM در رفتارهای سلولی از جمله قابلیت بقاء، تمایز و رفتارهای دیگر نقش بسزایی دارد از اینرو نقش ECMهای بهدست آمده از روش دترجنت- آنزیم روی سلولهای کشت یافته نیز در مطالعات حاضر بررسی شده است. بر این اساس دوایل و همکاران در مطالعهشان قابلیت تکثیر سلولهای بنیادی عصبی را با کشت در BEM در حالتهای دو و سه بعدی بررسی کردند. نتایج حاصل از مطالعهشان نشان داد که این سلولها ضمن حفظ بنیادینگی خود در خارج از بدن و در حضور عوامل میتوژنیک و BEM، میتوانند تکثیر یابند (38). سود و همکاران جهت بررسی رشد و تمایز نورونهای اولیه موشی این سلولها را در ژلهای BEM مهندسی شده کشت دادند و به این نتیجه رسیدند که BEM میتواند رشد و تمایز به سلولهای گلیا و تشکیل شبکه آکسونی را در سلولهای تمایز یافته افزایش دهد. از آنجاییکه آستروسیتها نقش مهمی در تعاملات ECM و نورونها دارند، اثر BEMروی تمایز به آستروسیتها و رفتار آستروسیتها در برابر تمایز عصبی نیز مورد بررسی قرار گرفته است، نتایج نشان میدهد که این سلولها بهوسیله پروتئین های موجود در BEM میتوانند در روند تشکیل شبکه عصبی نقش ایفا کنند. بافت سلولزدایی شده مغز جنین نیز میتواند به عنوان ریز محیط مناسبی جهت رشد سلولهای عصبی جنین مورد استفاده باشد، و نیز احتمالاً دارای پروتیئنهایی است که میتواند تعاملات ECM و نورون را تسهیل نماید (3). ECM مخچه نیز حاوی پروتئینهایی مانند پروتئینهای حمایتگر نورونها و عوامل رشد است که باعث تکثیر، مهاجرت و تمایز سلولهای بنیادی عصبی به نورون ها و آستروسیتها میشود. این یافتهها با توجه به رنگآمیزی بتاتوبولین3 در شرایط آزمایشگاهی و تزریق زیرپوستی و داخل جمجهای ECM مخچه تأیید شده است (34). یانگ هانگ و همکاران نیز اخیراً برای افزایش بقای عصبی، رشد عصبی و کاهش پاسخهای التهابی از ECM بافت مغز خوک استفاده کردند آنها بافت مغز را بهمدت یک شبانهروز در آب و در دمای 4 درجه سانتیگراد نگهداری کردند و پس از آن از آنزیم تریپسین 02/0% در دمای 37 درجه سانتیگراد به مدت یک ساعت استفاده کردند، پس از تیمار با SDC4%، سوکروز 1 مولار برای سلولزدایی استفاده کردند و بین هر مرحله از PBS و آب برای شستشوی ECM استفاده کردند. بررسی میزان DNA باقیمانده، GAG و کلاژن حفظ شده در این مطالعه نشان داد که سلولزدایی بهخوبی اتفاق افتاده است، علاوه بر این آنها نشان دادند که ECM بهدست آمده با اینروش بهدلیل داشتن فاکتورهای زیادی از جمله FGF1 و FGF2 توانسته است باعث افزایش تکثیر و تمایز سلولهای عصبی شود (39). بهطور کلی نتایج بهدست آمده در این مطالعات نشان میدهد که استفاده از دترجنت-آنزیم میتواند ساختار سه بعدی بافت مغز را تا حدودی حفظ کرده و معماری بافت کمتر دستخوش تغییر قرار گیرد. ECM سلولزدایی شده مغز و مخچه میتوانند بهعنوان یک بستر برای رشد، تکثیر، مهاجرت و تمایز سلولها در شرایط آزمایشگاهی در نظر گرفته شود، در حالیکه مطالعات بیشتری برای قابلیت استفاده از آن در بدن لازم است.
روش فیزیکوشیمیایی-آنزیم
علیرغم اینکه روشهای سلولزدایی با مواد شیمیایی و آنزیمی میتوانند تا حدودی ساختارهای بافت را حفظ کنند اما محققان دریافتند که استفاده از عوامل فیزیکی بههمراه این مواد ضمن آسیب کمتر باعث تسهیل در حذف سلولهای بافت میشوند. از جمله عوامل فیزیکی که در سلولزدایی بافت مغز استفاده شده است میتوان به نوسآنهای مکانیکی، سانتریفیوژ و شوکهای اسمتیک و دمایی به بافت اشاره کرد. بسته به نوع بافت و شدت روشهای فیزیکی، این عوامل می توانند باعث از بین رفتن سلولها و تسهیل در مرگ سلولی شوند. یین و همکاران در مطالعه خود نشان دادند که 120 دور در دقیقه طی سانتریفیوژ میتواند برای سلولزدایی نخاع مورد استفاده قرار گیرد (40). علاوه بر آن بایگورا و همکاران و ریباتی و همکاران در مطالعهشان برای سلولزدایی بافت مغز از تکرار چهار چرخه فریز و ذوب استفاده کردند (41, 33). روشهای فیزیکی بهتنهایی نمیتوانند برای سلولزدایی بافت مورد استفاده باشند و نقشی در حذف سلولهای مرده درون بافت ندارند. اینروشها می توانند بههمراه روشهای شیمیایی و آنزیمی در تسهیل سلولزدایی بافت نقش داشته باشند (18). مطالعات در دسترس برای سلولزدایی بافت مغز با استفاده از روشهای فیزیکی، شیمیایی و آنزیمی در جدول 3 خلاصه شده است.
جدول 3: مطالعات موجود با روش فیزیکوشیمیایی-آنزیم برای سلولزدایی بافت مغز.

سه مطالعه در خصوص سلولزدایی بافت مغز با روش فیزیکوشیمیایی-آنزیم وجود دارد که از چند مرحله ذوب و فریز بافت به عنوان روش فیزیکی و از دترجنت های SDS و ترتیون X-100 و از آنزیم های DNase و تریپسین برای سلولزدایی بافت مغز استفاده کرده اند.
علیرغم دستهبندی روشهای سلولزدایی بافت مغز به سه صورت ذکر شده، اخیراً گراناتو و همکاران مطالعهای را روی روش جدیدی از سلولزدایی با مدغوم کردن روش فیزیکی و دترجنت انجام دادهاند، آنها از تکرارهای فریز و ذوب و شستشوی 24 ساعته بافت مغز در SDC 4% به ECM بافت مغز دست یافتند که اینروش علیرغم اینکه یک روش سریع و آسانی است اما جهت تایید تکرارپذیری به مطالعات بیشتری نیاز دارد (42). همانطور که در بالا ذکر شد، بافت مغز بعد از سلولزدایی بهدلیل حذف سلولها کوچکتر و شفافتر میشود. کراپو و همکاران نیز در مطالعه خود کوچکتر شدن سه بافت از سیستم عصبی مرکزی از جمله بافت مغز را بعد از سلولزدایی با روشهای فیزیکی، شیمیایی و آنزیمی گزارش کردند (31,41). بهطورکلی استفاده از روشهای فیزیکی مانند تکرار چرخه فریز و ذوب میتواند سبب از بین بردن محتوای هستهای میشود که نتیجه آن به وسیله رنگآمیزی با روشهای H&E و DAPI بهدست آمده است (42, 32, 31). این دادهها نشان میهند که 91% از DNA حذف شده (41) و غلظت کمتر از 50 نانوگرم از DNA در هر گرم از بافت باقیمانده است (31). علیرغم اینکه چرخههای فریز و ذوب بهدلیل ایجاد کریستالهایی در آب بافت سبب برهم خوردن ساختار و معماری بافت میشوند اما بایگورا و همکاران در مطالعهشان با استفاده از تصویربرداری SEM از BEM حضور الاستین و گلیکوزآمینوگلیکانهای سولفیده شده را نشان دادند و به این نتیجه رسیدند که ساختار سهبعدی مغز بعد از سلولزدایی بدون شکستگی در ماتریکس حفظ می شود و معماری بافت تغییر نمیکند (41). علاوه بر الاستین، پروتئینهای دیگری از جمله لامینین و میلین در BEM قابل شناسایی بوده است (31). با استناد بر این نتایج، علیرغم اینکه ساختار و ترکیبات ECM در مغزهای سلولزدایی شده با روش فیزیکوشیمیایی-آنزیم حفظ میشوند اما مواد هستهای بهطور کامل حذف نمیشوند. از آنجایی که فاکتورهای رشد در ECM سایر بافتها نقش مهمی در رفتار سلولها دارند حضور آنها در BEM نیز از اهمیت بالایی برخوردار است از اینرو کراپو و همکاران با تأیید حضور فاکتور رشد عروقی اندوتلیال (Vascular Endothelial Growth Factor, VEGF)، فاکتور رشد فیبروبلاست (basic Fibroblast Growth Fact, bFGF) و فاکتور رشد عصبی (Nerve Growth Factor, NGF ) در بافتهای سلولزدایی شده سیستم عصبی مرکزی نشان دادند که بعد از سلولزدایی عوامل رشد باقی میمانند (31). ریباتی و همکاران نیز در مطالعهشان نقش bFGF و VEGF باقیمانده بعد از سلولزدایی را عاملی در رگزایی بعد از پیوند دانستند (33). با توجه به عملکرد ECM در رفتارهای سلولی نقش BEMهای بهدست آمده از روش فیزیکوشیمیایی-آنزیمی در مطالعات حاضر بررسی شده است. بایگورا و همکاران سلولهای بنیادی مزانشیمی (Mesenchymal Stem Cells, MSCs) را روی BEM کشت دادند و در پی نتایج بهدست آمده از مقاطع بافتی رنگآمیزی شده با روش DAPI و H&E مشاهده کردند که سلولها نه تنها در سطح خارجی ECM رشد می کنند بلکه در داخل آن نیز وجود دارند. آنها همچنین گزارش کردند که BEM میتواند در چسبندگی، رشد و تکثیر سلولها مؤثر باشد (41). کراپو و همکاران در مطالعهای که در سال 2012 چاپ کردند، گزارش کردند که غلظتهای متفاوتی از BEM میتواند در هر یک از رفتارهای سلولی نقش داشته باشد. بهطور مثال: تکثیر، مهاجرت و تمایز سلولهای PC12 (Phaeochromocytoma) بهترتیب با غلظتهای 5/2، 10و 100 میکروگرم بر میلیلیتر از BEM امکانپذیر است. علاوه بر این نشان دادند که اثر این غلظتها در تغییر رفتار سلولهای مختلف متفاوت است (32). این نشان میدهد که غلظتهای متفاوت BEM اثر مثبتی روی رفتارهای سلولی میگذارد و پاسخ سلولهای بنیادی بهطیف غلظتهای 5/2 تا 100میکروگرم بر میلیلیتر از BEM بیشتر است. نتایج حاصل از مطالعات در مورد سلولزدایی بافت مغز بهروش فیزیکوشیمایی-آنزیم، اهمیت روش فیزیکی خصوصاً استفاده از چرخههای مکرر فریز و ذوب را بههمراه روشهای دترجنت و آنزیم جهت تسهیل در سلولزدایی نشان میدهد.
نتیجهگیری
از میان دترجنتهای موجود، تریتون ایکس 100 با غلظتهای 1% و 3% ، سدیم دئوکسی کولات با غلظت 4% و سدیم دودسیل سولفات با غلظت 4% بیشترین کاربرد را در سلولزدایی بافت مغز را دارند. از بین آنزیمها، تریپسین با هدف حذف سلولهای موجود در ECM بافت مغز کاربرد بیشتری نسبت بهآنزیمهای دیگر دارد. با این حال آنزیم DNaseI با غلظتهای 40 و 100 کیلو واحد بر میلیلیتر نیز مورد استفاده قرار گرفته است. از طرفی تکرار چرخههای فریز و ذوب قبل از سلولزدایی میتواند سلولزدایی را تسهیل کند. با توجه به سهروش سلولزدایی بافت مغز تعریف شده در این مطالعه، نیروی گریز از مرکز حاصل از دستگاه سانتریفیوژ با 60 تا 120 دور در دقیقه امری ضروری برای حذف سلولهای جدا شده از ECM باقیمانده بافت خواهد بود. اگرچه DNAبهطور کامل در سلولزدایی حذف نمیشود اما ترکیبات ECM حفظ میشوند و میتوان از این ترکیبات بهعنوان بستر مناسبی برای تکثیر، مهاجرت و تمایز دو بعدی و سه بعدی برای سلولهای بنیادی با غلظتهای 2/5 تا 100 میکروگرم بر میلیلیتر در شرایط آزمایشگاهی استفاده نمود. در نهایت ECM مغز میتواند گزینه مناسبی برای کاربردهای پزشکی بازساختی و مهندسی بافت در آینده باشد.
تعارض در منافع: وجود ندارد.
References:
1-Schenke-Layland K. Special Issue" Extracellular Matrix Proteins and Mimics". Acta Biomaterialia 2017; 52: Iv.
2-Teti A. Regulation of Cellular Functions by Extracellular Matrix. J the American Society Nephrology 1992; 2(10): S83.
3-Sood D, Chwalek K, Stuntz E, Pouli D, Du C, Tang-Schomer M, et al. Fetal Brain Extracellular Matrix Boosts Neuronal Network Formation in 3d Bioengineered Model of Cortical Brain Tissue. ACS Biomaterials Science & Engineering 2015; 2(1): 131-40.
4-Ruoslahti E. Brain Extracellular Matrix. Glycobiology 1996; 6(5): 489-92.
5-Yamagata M, Sanes JR. Versican in the Developing Brain: Lamina-Specific Expression in Interneuronal Subsets and Role in Presynaptic Maturation. J Neuroscience 2005; 25(37): 8457-67.
6-Xiang Y-Y, Dong H, Wan Y, Li J, Yee A, Yang BB, et al. Versican G3 Domain Regulates Neurite Growth And Synaptic Transmission of Hippocampal Neurons by Activation of Epidermal Growth Factor Receptor. J Biological Chemistry 2006; 281(28): 19358-68.
7-Morawski M, Brückner G, Arendt T, Matthews R. Aggrecan: Beyond Cartilage and into the Brain. International J Biochemistry & Cell Biology 2012; 44(5): 690-3.
8-Zhou X-H, Brakebusch C, Matthies H, Oohashi T, Hirsch E, Moser M, et al. Neurocan is Dispensable for Brain Development. Mol Cell Biol 2001; 21(17): 5970-8.
9-Frischknecht R, Seidenbecher CI. Brevican: A Key Proteoglycan in the Perisynaptic Extracellular Matrix of the Brain. The International J Biochemistry & Cell Biology 2012; 44(7): 1051-4.
10-Donahue JE, Berzin TM, Rafii MS, Glass DJ, Yancopoulos GD, Fallon JR, et al. Agrin in Alzheimer’s Disease: Altered Solubility and Abnormal Distribution with in Microvasculature and Brain Parenchyma. Proc Nati Acad Sci 1999; 96(11): 6468-72.
11-Garwood J, Heck N, Reichardt F, Faissner A. Phosphacan Short Isoform, A Novel Non-Proteoglycan Variant of Phosphacan/Receptor Protein Tyrosine Phosphatase-Β, Interacts with Neuronal Receptors and Promotes Neurite Outgrowth. J Biological Chemistry 2003; 278(26): 24164-73.
12-Rutka JT, Apodaca G, Stern R, Rosenblum M. The Extracellular Matrix of the Central and Peripheral Nervous Systems: Structure and Function. J Neurosurgery 1988; 69(2): 70-155.
13-Tonge DA, De Burgh HT, Docherty R, Humphries MJ, Craig SE, Pizzey J. Fibronectin Supports Neurite Outgrowth and Axonal Regeneration of Adult Brain Neurons in Vitro. Brain Res 2012; 1453: 8-16.
14-Tate CC, Tate MC, Laplaca MC. Fibronectin and Laminin Increase in the Mouse Brain after Controlled Cortical Impact Injury. J Neurotrauma 2007; 24(1): 226-30.
15-Uhm JH, Dooley NP, Kyritsis AP, Rao JS, Gladson CL. Vitronectin, A Glioma-Derived Extracellular Matrix Protein, Protects Tumor Cells from Apoptotic Death. Clinical Cancer Res 1999; 5(6): 1587-94.
16-Crapo PM, Gilbert TW, Badylak SF. An Overview of Tissue and whole Organ Decellularization Processes. Biomaterials 2011; 32(12): 3233-43.
17-Dequach JA, Yuan SH, Goldstein LS, Christman KL. Decellularized Porcine Brain Matrix for Cell Culture and Tissue Engineering Scaffolds. Tissue Engineering Part A 2011; 17(21-22): 2583-92.
18-Wang H, Lin X-F, Wang L-R, Lin Y-Q, Wang J-T, Liu W-Y, et al. Decellularization Technology in CNS Tissue Repair. Expert Review of Neuro therapeutics 2015; 15(5): 493-500.
19-Dhandayuthapani B, Yoshida Y, Maekawa T, Kumar DS. Polymeric Scaffolds in Tissue Engineering Application: A Review. International J Polymer Science 2011; 2011.
20- Hinderer S, Layland SL, Schenke-Layland K. ECM and ECM-Like Materials—Biomaterials for Applications in Regenerative Medicine and Cancer Therapy. Advanced Drug Delivery Rev 2016; 97: 260-9.
21-Wu Q, Bao J, Zhou Y-J, Wang Y-J, Du Z-G, Shi Y-J, et al. Optimizing Perfusion-Decellularization Methods of Porcine Livers for Clinical-Scale Whole-Organ Bioengineering. Biomed Res International 2015; 2015: 785474.
22-Gilpin A, Yang Y. Decellularization Strategies for Regenerative Medicine: From Processing Techniques to Applications. Biomed Res Int 2017; 2017: 9831534.
23-Ott HC, Matthiesen TS, Goh S-K, Black LD, Kren SM, Netoff TI, et al. Perfusion-Decellularized Matrix: Using Nature's Platform to Engineer a Bioartificial Heart. Nature Medicine 2008; 14(2): 213-21.
24-Ott HC, Clippinger B, Conrad C, Schuetz C, Pomerantseva I, Ikonomou L, et al. Regeneration and Orthotopic Transplantation of a Bioartificial Lung. Nature Medicine 2010; 16(8): 927-34.
25-Shupe T, Williams M, Brown A, Willenberg B, Petersen BE. Method for the Decellularization of Intact Rat Liver. Organogenesis 2010; 6(2): 134-6.
26-Fathi I, Eltawila A. Whole-Liver Decellularization: Advances and Insights into Current Understanding. Xenotransplantation: New Insights; 2017: 139.
27-Ross EA, Williams MJ, Hamazaki T, Terada N, Clapp WL, Adin C, et al. Embryonic Stem Cells Proliferate and Differentiate when Seeded into Kidney Scaffolds. J Am Soc Nephrol 2009; 20(11): 2338-47.
28-Yu Y, Shao Y, Ding Y, Lin K, Chen B, Zhang H, et al. Decellularized Kidney Scaffold-Mediated Renal Regeneration. Biomaterials 2014; 35(25): 6822-8.
29-Jiang T, Ren X-J, Tang J-L, Yin H, Wang K-J, Zhou C-L. Preparation and Characterization of Genipin-Crosslinked Rat Acellular Spinal Cord Scaffolds. Materials Science and Engineering: C 2013; 33(6): 3514-21.
30-Wolf MT, Daly KA, Brennan-Pierce EP, Johnson SA, Carruthers CA, D'Amore A, et al. A Hydrogel Derived from Decellularized Dermal Extracellular Matrix. Biomaterials 2012; 33(29): 7028-38.
31-Crapo PM, Medberry CJ, Reing JE, Tottey S, Van Der Merwe Y, Jones KE, et al. Biologic Scaffolds Composed of Central Nervous System Extracellular Matrix. Biomaterials 2012; 33(13): 3539-47.
32-Crapo PM, Tottey S, Slivka PF, Badylak SF. Effects of Biologic Scaffolds on Human Stem Cells and Implications for CNS Tissue Engineering. Tissue Engineering Part A 2013; 20(1-2): 313-23.
33-Ribatti D, Conconi MT, Nico B, Baiguera S, Corsi P, Parnigotto PP, et al. Angiogenic Response Induced by Acellular Brain Scaffolds Grafted on to the Chick Embryo Chorioallantoic Membrane. Brain Res 2003; 989(1): 9-15.
34-Zhu T, Tang Q, Shen Y, Tang H, Chen L, Zhu J. An Acellular Cerebellar Biological Scaffold: Preparation, Characterization, Biocompatibility and Effects on Neural Stem Cells. Brain Res Bulletin 2015; 113: 48-57.
35-Zhao Z, Wang Y, Peng J, Ren Z, Zhang L, Guo Q, et al. Improvement in Nerve Regeneration through a Decellularized Nerve Graft by Supplementation with Bone Marrow Stromal Cells in Fibrin. Cell Transplant 2014; 23(1): 97-110.
36-Lin Q, Wong HL, Tian F-R, Huang Y-D, Xu J, Yang J-J, et al. Enhanced Neuroprotection with Decellularized Brain Extracellular Matrix Containing Bfgf after Intracerebral Transplantation in Parkinson’s Disease Rat Model. Int J Pharm 2017; 517(1): 383-94.
37-Xu H-L, Mao K-L, Lu C-T, Fan Z-L, Yang J-J, Xu J, et al. An Injectable Acellular Matrix Scaffold with Absorbable Permeable Nanoparticles Improves the Therapeutic Effects of Docetaxel on Glioblastoma. Biomaterials 2016; 107: 44-60.
38-De Waele J, Reekmans K, Daans J, Goossens H, Berneman Z, Ponsaerts P. 3D Culture of Murine Neural Stem Cells on Decellularized Mouse Brain Sections. Biomaterials 2015; 41: 122-31.
39-Hong JY, Seo Y, Davaa G, Kim H-W, Kim SH, Hyun JK. Decellularized Brain Matrix Enhances Macrophage Polarization and Functional Improvements in Rat Spinal Cord Injury. Acta Biomater 2020; 101: 357-71.
40-Yin W, Jin D, Deng X, Lu K. Effects of Mechanical Vibration on the Morphology of the Acellular Scaffold for the Spinal Cord. Nan Fang Yi Ke Da Xue Xue Bao. Nan Fang Yi Ke Da Xue Xue Bao 2008; 28(10): 1748-51.
41-Baiguera S, Del Gaudio C, Lucatelli E, Kuevda E, Boieri M, Mazzanti B, et al. Electrospun Gelatin Scaffolds Incorporating Rat Decellularized Brain Extracellular Matrix for Neural Tissue Engineering. Biomaterials 2014; 35(4): 1205-14.
42-Granato AE, Da Cruz EF, Rodrigues-Junior DM, Mosini AC, Ulrich H, Cheffer A, et al. A Novel Decellularization Method to Produce Brain Scaffolds. Tissue and Cell 2020; 67; 101412.
1-Schenke-Layland K. Special Issue" Extracellular Matrix Proteins and Mimics". Acta Biomaterialia 2017; 52: Iv.
2-Teti A. Regulation of Cellular Functions by Extracellular Matrix. J the American Society Nephrology 1992; 2(10): S83.
3-Sood D, Chwalek K, Stuntz E, Pouli D, Du C, Tang-Schomer M, et al. Fetal Brain Extracellular Matrix Boosts Neuronal Network Formation in 3d Bioengineered Model of Cortical Brain Tissue. ACS Biomaterials Science & Engineering 2015; 2(1): 131-40.
4-Ruoslahti E. Brain Extracellular Matrix. Glycobiology 1996; 6(5): 489-92.
5-Yamagata M, Sanes JR. Versican in the Developing Brain: Lamina-Specific Expression in Interneuronal Subsets and Role in Presynaptic Maturation. J Neuroscience 2005; 25(37): 8457-67.
6-Xiang Y-Y, Dong H, Wan Y, Li J, Yee A, Yang BB, et al. Versican G3 Domain Regulates Neurite Growth And Synaptic Transmission of Hippocampal Neurons by Activation of Epidermal Growth Factor Receptor. J Biological Chemistry 2006; 281(28): 19358-68.
7-Morawski M, Brückner G, Arendt T, Matthews R. Aggrecan: Beyond Cartilage and into the Brain. International J Biochemistry & Cell Biology 2012; 44(5): 690-3.
8-Zhou X-H, Brakebusch C, Matthies H, Oohashi T, Hirsch E, Moser M, et al. Neurocan is Dispensable for Brain Development. Mol Cell Biol 2001; 21(17): 5970-8.
9-Frischknecht R, Seidenbecher CI. Brevican: A Key Proteoglycan in the Perisynaptic Extracellular Matrix of the Brain. The International J Biochemistry & Cell Biology 2012; 44(7): 1051-4.
10-Donahue JE, Berzin TM, Rafii MS, Glass DJ, Yancopoulos GD, Fallon JR, et al. Agrin in Alzheimer’s Disease: Altered Solubility and Abnormal Distribution with in Microvasculature and Brain Parenchyma. Proc Nati Acad Sci 1999; 96(11): 6468-72.
11-Garwood J, Heck N, Reichardt F, Faissner A. Phosphacan Short Isoform, A Novel Non-Proteoglycan Variant of Phosphacan/Receptor Protein Tyrosine Phosphatase-Β, Interacts with Neuronal Receptors and Promotes Neurite Outgrowth. J Biological Chemistry 2003; 278(26): 24164-73.
12-Rutka JT, Apodaca G, Stern R, Rosenblum M. The Extracellular Matrix of the Central and Peripheral Nervous Systems: Structure and Function. J Neurosurgery 1988; 69(2): 70-155.
13-Tonge DA, De Burgh HT, Docherty R, Humphries MJ, Craig SE, Pizzey J. Fibronectin Supports Neurite Outgrowth and Axonal Regeneration of Adult Brain Neurons in Vitro. Brain Res 2012; 1453: 8-16.
14-Tate CC, Tate MC, Laplaca MC. Fibronectin and Laminin Increase in the Mouse Brain after Controlled Cortical Impact Injury. J Neurotrauma 2007; 24(1): 226-30.
15-Uhm JH, Dooley NP, Kyritsis AP, Rao JS, Gladson CL. Vitronectin, A Glioma-Derived Extracellular Matrix Protein, Protects Tumor Cells from Apoptotic Death. Clinical Cancer Res 1999; 5(6): 1587-94.
16-Crapo PM, Gilbert TW, Badylak SF. An Overview of Tissue and whole Organ Decellularization Processes. Biomaterials 2011; 32(12): 3233-43.
17-Dequach JA, Yuan SH, Goldstein LS, Christman KL. Decellularized Porcine Brain Matrix for Cell Culture and Tissue Engineering Scaffolds. Tissue Engineering Part A 2011; 17(21-22): 2583-92.
18-Wang H, Lin X-F, Wang L-R, Lin Y-Q, Wang J-T, Liu W-Y, et al. Decellularization Technology in CNS Tissue Repair. Expert Review of Neuro therapeutics 2015; 15(5): 493-500.
19-Dhandayuthapani B, Yoshida Y, Maekawa T, Kumar DS. Polymeric Scaffolds in Tissue Engineering Application: A Review. International J Polymer Science 2011; 2011.
20- Hinderer S, Layland SL, Schenke-Layland K. ECM and ECM-Like Materials—Biomaterials for Applications in Regenerative Medicine and Cancer Therapy. Advanced Drug Delivery Rev 2016; 97: 260-9.
21-Wu Q, Bao J, Zhou Y-J, Wang Y-J, Du Z-G, Shi Y-J, et al. Optimizing Perfusion-Decellularization Methods of Porcine Livers for Clinical-Scale Whole-Organ Bioengineering. Biomed Res International 2015; 2015: 785474.
22-Gilpin A, Yang Y. Decellularization Strategies for Regenerative Medicine: From Processing Techniques to Applications. Biomed Res Int 2017; 2017: 9831534.
23-Ott HC, Matthiesen TS, Goh S-K, Black LD, Kren SM, Netoff TI, et al. Perfusion-Decellularized Matrix: Using Nature's Platform to Engineer a Bioartificial Heart. Nature Medicine 2008; 14(2): 213-21.
24-Ott HC, Clippinger B, Conrad C, Schuetz C, Pomerantseva I, Ikonomou L, et al. Regeneration and Orthotopic Transplantation of a Bioartificial Lung. Nature Medicine 2010; 16(8): 927-34.
25-Shupe T, Williams M, Brown A, Willenberg B, Petersen BE. Method for the Decellularization of Intact Rat Liver. Organogenesis 2010; 6(2): 134-6.
26-Fathi I, Eltawila A. Whole-Liver Decellularization: Advances and Insights into Current Understanding. Xenotransplantation: New Insights; 2017: 139.
27-Ross EA, Williams MJ, Hamazaki T, Terada N, Clapp WL, Adin C, et al. Embryonic Stem Cells Proliferate and Differentiate when Seeded into Kidney Scaffolds. J Am Soc Nephrol 2009; 20(11): 2338-47.
28-Yu Y, Shao Y, Ding Y, Lin K, Chen B, Zhang H, et al. Decellularized Kidney Scaffold-Mediated Renal Regeneration. Biomaterials 2014; 35(25): 6822-8.
29-Jiang T, Ren X-J, Tang J-L, Yin H, Wang K-J, Zhou C-L. Preparation and Characterization of Genipin-Crosslinked Rat Acellular Spinal Cord Scaffolds. Materials Science and Engineering: C 2013; 33(6): 3514-21.
30-Wolf MT, Daly KA, Brennan-Pierce EP, Johnson SA, Carruthers CA, D'Amore A, et al. A Hydrogel Derived from Decellularized Dermal Extracellular Matrix. Biomaterials 2012; 33(29): 7028-38.
31-Crapo PM, Medberry CJ, Reing JE, Tottey S, Van Der Merwe Y, Jones KE, et al. Biologic Scaffolds Composed of Central Nervous System Extracellular Matrix. Biomaterials 2012; 33(13): 3539-47.
32-Crapo PM, Tottey S, Slivka PF, Badylak SF. Effects of Biologic Scaffolds on Human Stem Cells and Implications for CNS Tissue Engineering. Tissue Engineering Part A 2013; 20(1-2): 313-23.
33-Ribatti D, Conconi MT, Nico B, Baiguera S, Corsi P, Parnigotto PP, et al. Angiogenic Response Induced by Acellular Brain Scaffolds Grafted on to the Chick Embryo Chorioallantoic Membrane. Brain Res 2003; 989(1): 9-15.
34-Zhu T, Tang Q, Shen Y, Tang H, Chen L, Zhu J. An Acellular Cerebellar Biological Scaffold: Preparation, Characterization, Biocompatibility and Effects on Neural Stem Cells. Brain Res Bulletin 2015; 113: 48-57.
35-Zhao Z, Wang Y, Peng J, Ren Z, Zhang L, Guo Q, et al. Improvement in Nerve Regeneration through a Decellularized Nerve Graft by Supplementation with Bone Marrow Stromal Cells in Fibrin. Cell Transplant 2014; 23(1): 97-110.
36-Lin Q, Wong HL, Tian F-R, Huang Y-D, Xu J, Yang J-J, et al. Enhanced Neuroprotection with Decellularized Brain Extracellular Matrix Containing Bfgf after Intracerebral Transplantation in Parkinson’s Disease Rat Model. Int J Pharm 2017; 517(1): 383-94.
37-Xu H-L, Mao K-L, Lu C-T, Fan Z-L, Yang J-J, Xu J, et al. An Injectable Acellular Matrix Scaffold with Absorbable Permeable Nanoparticles Improves the Therapeutic Effects of Docetaxel on Glioblastoma. Biomaterials 2016; 107: 44-60.
38-De Waele J, Reekmans K, Daans J, Goossens H, Berneman Z, Ponsaerts P. 3D Culture of Murine Neural Stem Cells on Decellularized Mouse Brain Sections. Biomaterials 2015; 41: 122-31.
39-Hong JY, Seo Y, Davaa G, Kim H-W, Kim SH, Hyun JK. Decellularized Brain Matrix Enhances Macrophage Polarization and Functional Improvements in Rat Spinal Cord Injury. Acta Biomater 2020; 101: 357-71.
40-Yin W, Jin D, Deng X, Lu K. Effects of Mechanical Vibration on the Morphology of the Acellular Scaffold for the Spinal Cord. Nan Fang Yi Ke Da Xue Xue Bao. Nan Fang Yi Ke Da Xue Xue Bao 2008; 28(10): 1748-51.
41-Baiguera S, Del Gaudio C, Lucatelli E, Kuevda E, Boieri M, Mazzanti B, et al. Electrospun Gelatin Scaffolds Incorporating Rat Decellularized Brain Extracellular Matrix for Neural Tissue Engineering. Biomaterials 2014; 35(4): 1205-14.
42-Granato AE, Da Cruz EF, Rodrigues-Junior DM, Mosini AC, Ulrich H, Cheffer A, et al. A Novel Decellularization Method to Produce Brain Scaffolds. Tissue and Cell 2020; 67; 101412.
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |







