دوره 28، شماره 2 - ( اردیبهشت 1399 )
جلد 28 شماره 2 صفحات 2333-2324 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Heydari khormizi N, Kavussi H R, Miresmaeili S M, Nikoonahad Lotfabadi N. Niosomes from Preparation to Application in Drug Delivery. JSSU 2020; 28 (2) :2324-2333
URL: http://jssu.ssu.ac.ir/article-1-4914-fa.html
URL: http://jssu.ssu.ac.ir/article-1-4914-fa.html
حیدری خورمیزی نسرین، کاووسی حمیدرضا، میراسمعیلی سیدمحسن، نیکونهاد لطفآبادی نرگس. نیوزومها از آمادهسازی تا کاربرد در دارورسانی. مجله علمي پژوهشي دانشگاه علوم پزشكي شهید صدوقی يزد. 1399; 28 (2) :2324-2333
متن کامل [PDF 686 kb]
(2851 دریافت)
| چکیده (HTML) (3672 مشاهده)
متن کامل: (15386 مشاهده)
مقدمه
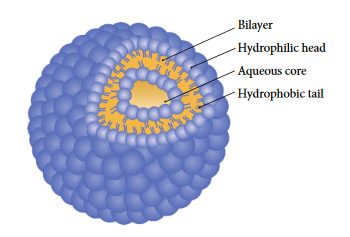
بیوتکنولوژِی و نانوبیوتکنولوژی دو فناوری امیدوار کننده قرن 21 هستند. نانوبیوتکنولوژی بهعنوان طراحی، توسعه و کاربرد مواد و دستگاهها در مقیاس نانومتر تعریف شده است. نانوتکنولوژی سر و کار داشتن یا توسعه دادن مواد، دستگاهها یا دیگر ساختارهای دارای حداقل اندازه بین 100-0 نانومتر میباشد (1). نانوتکنولوژی یک رویداد برای تحویل هدفمند دارو، ژن و پروتئین به بافتهای توموری را فراهم میکند، بنابراین سمیت عوامل ضد سرطان در بافتهای سالم کاهش مییابد. سرطان علت برجسته ی مرگ و میر در جهان، بهخصوص کشورهای در حال توسعه میباشد، به گفته موسسه ملی سرطان آمریکا (NCI) فناوری نانو پایههای مهم تشخیص، درمان و پیشگیری سرطان را تغییر خواهد داد (2). استفاده از مواد مهندسی در مقیاس نانو جهت درمان سرطان، حذف ترجیحی سلولهای سرطانی بدون آسیب جدی به سلولهای طبیعی را فراهم میکند (3). نیوزوم برای اولین بار در سال 1970 بهعنوان یک فاکتور برای صنعت آرایشی معرفی شد و سپس برنامههای بالقوه برای تحویل دارو مورد بررسی قرار گرفت. نیوزومها یکی از برجستهترین وزیکولها در سیستم دارورسانی هستند، که توجه زیادی را به جهت تحویل دارو به خود جلب کردهاند (5, 4). این ساختارها وزیکولهای یک یا چند لایه بر پایه سورفکتانتهای غیریونیاند، که بهعنوان حامل داروهای چربیدوست و آبدوست استفاده میشوند (6). در بسیاری از موارد برای تهیه نیوزوم از کلسترول و مشتقات آن استفاده میشود (4). آنها توسط خود تجمعی سورفکتانتهای غیریونی در محیط آبی تشکیل میشوند و وزیکولهای دو لایه هم مرکز را تشکیل میدهندکه ساختاری شبیه لیپوزوم دارند (5).
بیوتکنولوژِی و نانوبیوتکنولوژی دو فناوری امیدوار کننده قرن 21 هستند. نانوبیوتکنولوژی بهعنوان طراحی، توسعه و کاربرد مواد و دستگاهها در مقیاس نانومتر تعریف شده است. نانوتکنولوژی سر و کار داشتن یا توسعه دادن مواد، دستگاهها یا دیگر ساختارهای دارای حداقل اندازه بین 100-0 نانومتر میباشد (1). نانوتکنولوژی یک رویداد برای تحویل هدفمند دارو، ژن و پروتئین به بافتهای توموری را فراهم میکند، بنابراین سمیت عوامل ضد سرطان در بافتهای سالم کاهش مییابد. سرطان علت برجسته ی مرگ و میر در جهان، بهخصوص کشورهای در حال توسعه میباشد، به گفته موسسه ملی سرطان آمریکا (NCI) فناوری نانو پایههای مهم تشخیص، درمان و پیشگیری سرطان را تغییر خواهد داد (2). استفاده از مواد مهندسی در مقیاس نانو جهت درمان سرطان، حذف ترجیحی سلولهای سرطانی بدون آسیب جدی به سلولهای طبیعی را فراهم میکند (3). نیوزوم برای اولین بار در سال 1970 بهعنوان یک فاکتور برای صنعت آرایشی معرفی شد و سپس برنامههای بالقوه برای تحویل دارو مورد بررسی قرار گرفت. نیوزومها یکی از برجستهترین وزیکولها در سیستم دارورسانی هستند، که توجه زیادی را به جهت تحویل دارو به خود جلب کردهاند (5, 4). این ساختارها وزیکولهای یک یا چند لایه بر پایه سورفکتانتهای غیریونیاند، که بهعنوان حامل داروهای چربیدوست و آبدوست استفاده میشوند (6). در بسیاری از موارد برای تهیه نیوزوم از کلسترول و مشتقات آن استفاده میشود (4). آنها توسط خود تجمعی سورفکتانتهای غیریونی در محیط آبی تشکیل میشوند و وزیکولهای دو لایه هم مرکز را تشکیل میدهندکه ساختاری شبیه لیپوزوم دارند (5).

ساختار نیوزوم (7)
نیوزومها یک سیتم تحویل دارویی جدید
تحقیقات زیادی در مورد استفاده از نیوزومها به عنوان حاملهای دارویی انجام شده است، که به ذکر چند مورد میپردازیم.
• Parthasarthi و همکاران، نیوزومهای حاوی وینکریستین سولفات تهیه کردند، که دارای سمیت کمتر و بهبود فعالیت ضد سرطان بودند (8).
• Paolino و همکاران، یک سیستم نیوزومی متشکل از span80 و کلسترول حاوی fluorouracil برای درمان سرطان پوست تهیه کردند، که در ارزیابی فعالیت سیتوتوکسیک نسبت به داروی آزاد سمیت بیشتری برای سلول سرطانی داشت (9).
• ترکیبات فیتوشیمیایی نظیر lawsone حلالیت کمی در آب دارند که موجب نفوذپذیری کم و بیثباتی آن میشود. بارانی و همکاران، در سال 2018، در مطالعهای نیوزومهایی حاوی lawsone سنتز کردند، که نسبت به داروی آزاد در رده سلولی MCF7 فعالیت سیتوتوکسیک بیشتری نشان دادند (10).
• Asgharkhani و همکاران، در سال 2018، آرتمیزین را در نیوزوم و نیوزومهای پگیله با دو تکنیک متفاوت بارگذاری کردند. پگیله شدن نیوزوم باعث رهایش کندتر، افزایش ثبات و تاثیر بیشتر آرتمیزین میشود. نتایج نشان داد نیوزومهای پگیله دارای مزایای زیادی در رابطه با تعامل با غشای سلولهای MCF7 میباشد (11).
• عسکری و همکاران، نانو حامل نیوزومی حاوی عصاره پوست انار به ترتیب راندمان کپسولاسیون، اندازه و شارژ سطحی 61/861 درصد و143/6 نانومتر و 40/9- سنتز و تاثیر آنها را بر رده سلولی MCF7 مورد ارزیابی قرار دادند. نتایج حاصل از سمیت سلولی نشان داد سمیت عصاره آزاد و نیوزومه وابسته به غلظت و زمان است. همچنین نیوزومهای حاوی عصاره پوست انار در مقایسه با عصاره آزاد سمیت بیشتری ایجاد کردند (12).
• نیکونهاد و همکاران با استفاده از لیپیدهای کاتیونی DOTAP، DOTIMA، DOABو DDAB به همراه مقادیر فسفولیپید colesterol، dppc و dspe-Mpeg فرمولاسیونهای لیپوزومی کاتیونی سنتز و سمیت سلولی آنها را در دو رده سلولی در 48 و 72 ساعت مورد ارزیابی قرار دادند. بر اساس نتایج حاصل شده لیپوزومهای کاتیونی بر پایه dotap میتوانند بهطور موثری در فرآیند ژن درمانی خصوصا جهت انتقال miRNA بهعنوان یک عامل درمانی نوین بهویژه در درمان انواع سرطان مورد استفاده واقع شوند (13).
• نیکونهاد و همکاران در مطالعهای از لیپوفکتامین 2000 بهعنوان لیپوزوم کاتیونی جهت ترانسفکشن miR-101 بهمنظور بررسی سمیت سلولی و تاثیرش بر بیان یوبیکوئتین لیگاز در سلولهای لوسمی میلوئیدی حاد (AML) استفاده کردند. نتایج نشان داد لیپوفکتامین بهعنوان یک لیپوزوم کاتیونی میتواند بهطور موثری ترانسقکشن miR-101 به درون سلول را انجام دهد و همچنین با افزایش بیان HECTH9 اثرات ضد توموری خود را اعمال نماید (14).
بر اساس اندازه وزیکولها، نیوزوم را میتوان به سه گروه تقسیم کرد.
1. وزیکولهای تک لایه کوچک suv(small unilamellar vesicle) (اندازه بین 0/25-0/5)
تحقیقات زیادی در مورد استفاده از نیوزومها به عنوان حاملهای دارویی انجام شده است، که به ذکر چند مورد میپردازیم.
• Parthasarthi و همکاران، نیوزومهای حاوی وینکریستین سولفات تهیه کردند، که دارای سمیت کمتر و بهبود فعالیت ضد سرطان بودند (8).
• Paolino و همکاران، یک سیستم نیوزومی متشکل از span80 و کلسترول حاوی fluorouracil برای درمان سرطان پوست تهیه کردند، که در ارزیابی فعالیت سیتوتوکسیک نسبت به داروی آزاد سمیت بیشتری برای سلول سرطانی داشت (9).
• ترکیبات فیتوشیمیایی نظیر lawsone حلالیت کمی در آب دارند که موجب نفوذپذیری کم و بیثباتی آن میشود. بارانی و همکاران، در سال 2018، در مطالعهای نیوزومهایی حاوی lawsone سنتز کردند، که نسبت به داروی آزاد در رده سلولی MCF7 فعالیت سیتوتوکسیک بیشتری نشان دادند (10).
• Asgharkhani و همکاران، در سال 2018، آرتمیزین را در نیوزوم و نیوزومهای پگیله با دو تکنیک متفاوت بارگذاری کردند. پگیله شدن نیوزوم باعث رهایش کندتر، افزایش ثبات و تاثیر بیشتر آرتمیزین میشود. نتایج نشان داد نیوزومهای پگیله دارای مزایای زیادی در رابطه با تعامل با غشای سلولهای MCF7 میباشد (11).
• عسکری و همکاران، نانو حامل نیوزومی حاوی عصاره پوست انار به ترتیب راندمان کپسولاسیون، اندازه و شارژ سطحی 61/861 درصد و143/6 نانومتر و 40/9- سنتز و تاثیر آنها را بر رده سلولی MCF7 مورد ارزیابی قرار دادند. نتایج حاصل از سمیت سلولی نشان داد سمیت عصاره آزاد و نیوزومه وابسته به غلظت و زمان است. همچنین نیوزومهای حاوی عصاره پوست انار در مقایسه با عصاره آزاد سمیت بیشتری ایجاد کردند (12).
• نیکونهاد و همکاران با استفاده از لیپیدهای کاتیونی DOTAP، DOTIMA، DOABو DDAB به همراه مقادیر فسفولیپید colesterol، dppc و dspe-Mpeg فرمولاسیونهای لیپوزومی کاتیونی سنتز و سمیت سلولی آنها را در دو رده سلولی در 48 و 72 ساعت مورد ارزیابی قرار دادند. بر اساس نتایج حاصل شده لیپوزومهای کاتیونی بر پایه dotap میتوانند بهطور موثری در فرآیند ژن درمانی خصوصا جهت انتقال miRNA بهعنوان یک عامل درمانی نوین بهویژه در درمان انواع سرطان مورد استفاده واقع شوند (13).
• نیکونهاد و همکاران در مطالعهای از لیپوفکتامین 2000 بهعنوان لیپوزوم کاتیونی جهت ترانسفکشن miR-101 بهمنظور بررسی سمیت سلولی و تاثیرش بر بیان یوبیکوئتین لیگاز در سلولهای لوسمی میلوئیدی حاد (AML) استفاده کردند. نتایج نشان داد لیپوفکتامین بهعنوان یک لیپوزوم کاتیونی میتواند بهطور موثری ترانسقکشن miR-101 به درون سلول را انجام دهد و همچنین با افزایش بیان HECTH9 اثرات ضد توموری خود را اعمال نماید (14).
بر اساس اندازه وزیکولها، نیوزوم را میتوان به سه گروه تقسیم کرد.
1. وزیکولهای تک لایه کوچک suv(small unilamellar vesicle) (اندازه بین 0/25-0/5)
2. وزیکولهای چند لایه mlv (multi lamellar vesicle) (0/5< اندازه)
3. وزیکولهای تک لایه بزرگ luv(large unilamellar vesicle) (0/1<= اندازه) (15).
روشهای آماده سازی نیوزوم
روشهای آمادهسازی نیوزوم شامل: هیدراسیون فیلم نازک،Freeze-drying ، تبخیر فاز معکوس، تزریق اتر، سونیکاسیون،Microfluidization ، bubble و غیره میباشد که در ادامه به توضیح چند روش میپردازیم (16).
1. Sonication: در این روش مقداری از دارو در بافر حل شده و به مخلوط سورفکتانت و کلسترول در یک ویال اضافه میشود. این مخلوط با استفاده از پروب صوتی با دمای 60 درجه سانتیگراد برای 3 دقیقه همگن میشود. در نتیجه وزیکولهای همگن و یکنواختی تشکیل میشوند (17).
2. تکنیک تبخیر فاز معکوس (Reverse Phase Evaporation Technique) در این روش کلسترول و سورفکتانت در مخلوطی از اتر و کلروفرم حل میشود. فاز آبی حاوی دارو به این مواد اضافه و دو فاز حاصل در دمای 5-4 درجه سانتیگراد همگن میشود. به ژل زلال تشکیل شده مقدار کمی نمک بافر فسفات اضافه میشود. فاز آلی در دمای 60-40 درجه سانتیگراد و فشار کم حذف میشود. در نتیجه سوسپانسیون چسبناک نیوزوم با نمک فسفات رقیق شده و در حمام آبی در دمای 60 درجه به مدت 10 دقیقه حرارت داده می شود تا نیوزوم ها تشکیل شود (18).
3. روش تزریق اتر (Ether Injection Method): ابتدا به آرامی مقدار مشخص از سورفکتانت در دیاتیلاتر حل شده و در حمام آب گرم در دمای 60 درجه قرار داده میشود. مخلوط سورفکتانت توسط سوزن 14 درجهای به یک محلول آبی تزریق میشود. تبخیر اتر منجر به تشکیل وزیکولهای تک لایه میشود. بسته به شرایط مورد استفاده، وزیکولهایی با قطر 1000-50 نانومتر تشکیل میگردد (19).
4. تکنیک آبدهی فیلم نازک (Thin Film HydrationTechnique ) ابتدا تمام مولکولهای تشکیل دهنده وزیکول از قبیل سورفکتانتها، کلسترول و القا کنندههای شارژ در یک حلال آلی فرار مانند: دیاتیلاتر، متانول، کلروفرم و غیره در یک بالن ته گرد حل شده و با استفاده از یک دستگاه تبخیر کننده دوار حلالهای آلی در دمای اتاق تبخیر میشود و یک فیلم خشک و نازک از اجزای محلول تشکیل میشود. فیلم نازک خشک شده با فاز آبی با تحریک ملایم هیدراته شده که منجر به تشکیل نیوزوم میشود (20). در این روش نیوزومهای چند لایه ایجاد میشوند (7).
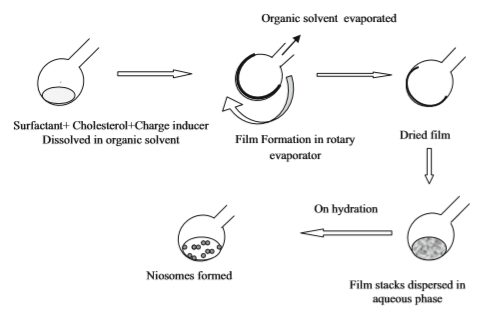
روش آبدهی فیلم نازک(17)
فرموله کردن نیوزوم: فرموله کردن نیوزوم مهمترین پارامتر است که میتواند روی ویژگیهای نیوزوم تاثیر بگذارد (21).
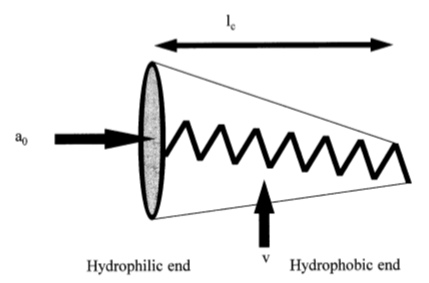
سورفکتانتها: سورفکتانتها یک کلاس منحصر به فرد از ترکیبات شیمیایی را تشکیل میدهند. آنها مولکولهای آمفیفیلیک هستند با دو ناحیه مجزا که قابلیت حل شدن بسیار متفاوتی دارند، یک انتهای آبدوست و یک انتهای چربیدوست که آبگریز میباشد. سورفکتانتها را میتوان به چهار گروه آنیونی، کاتیونی، آمفوتریک و غیر یونی طبقهبندی کرد (22). اگر قسمت سر یک سورفکتانت دارای بار منفی باشد به آن آنیونی گفته میشود، شامل: نمکهای اسید چرب (صابون)، سولفاتها، اتر سولفاتها و فسفات استرها میشود. اگر قسمت سر دارای بار مثبت باشد سورفکتانت کاتیونی و اگر سر حاوی هر دو بار مثبت و منفی باشد به آن آمفوتریک گفته میشود. انواع کاتیونی اغلب باعث تحریکپذیری و گاهی حتی باعث سمیت میشوند، بنابراین استفاده از آنها محدود است. سورفکتانتهای غیر یونی در سرشان هیچ باری ندارند. بنابراین در محلولها ساختارهایی ایجاد میکنند که در آن سرهای آبدوست در مقابل محلول آبی و دمهای آبگریز در مقابل محلولهای آلی قرار میگیرند. آمفی فیلهای غیر یونی که در نیوزومها استفاده میشود در چهار دسته آلکیلاسترها، آلکیلآمیدها، آلکیلاترها و استرهای اسیدچرب طبقهبندی میشوند. اغلب سورفکتانتهای مورد استفاده در نیوزوم براساس تعادل هیدروفیلیک-لیپوفیلیک در زیر آمده است، انتخاب نوع سورفکتانت به تعادل هیدروفیلیک-لیپوفیلیک (HLB) و پارامترهای بستهبندی بحرانی (CPP) بستگی دارد (23). تعادل هیدروفیلی- لیپوفیلی (Hydrophillic-Lipophillic Balance) یک راهنما برای انتخاب سورفکتانت بوده و مقدار آن نقش مهمی در کنترل بازده کپسولاسیون دارو دارد. تا به حال، بسته به مدیریت نیوزوم، تعداد زیادی از سورفکتانتهای غیر یونی با ارزش HLB مختلف ازقبیل پلیگلیسرول آلکیلاترها، گلوکوزیل دیآلکیلاترها، پلیاکسیاتیلناترها و استرها از جمله سری Brij،Tween ، Spanاستفاده شده است. سورفکتانتهای با HLB بین 8-3 با آماده سازی سطوح دو لایه سازگار است (4). مقیاس HLBبین مقادیر20-0 میباشد.HLB پایینتر به سورفاکتانت لیپوفیلی و HLB بالاتر به سورفاکتانت هیدروفیلی بیشتر اشاره دارد (15). سورفاکتانتهای هیدروفیلی با ارزش HLB بین 14 تا 17 به علت حلالیت بالا در آب برای تشکیل وزیکولهای دو لایه مناسب نیستند (24). پارامترهای بستهبندی بحرانی ( Critical Packing Parameter) علاوه بر HLB، برای پیشبینی توانایی تشکیل وزیکول، عوامل مختلف دیگر هم نقش اساس دارند. CPP یک مقیاس بدون بعد برای سورفکتانتها میباشد که به صورت زیرتعریف شده است.
Cpp=V/Lca0
V = حجم گروه هیدروفوب
LC= طول گروه هیدروفوب بحرانی
a0= منطقه سر گروه هیدروفیل
3. وزیکولهای تک لایه بزرگ luv(large unilamellar vesicle) (0/1<= اندازه) (15).
روشهای آماده سازی نیوزوم
روشهای آمادهسازی نیوزوم شامل: هیدراسیون فیلم نازک،Freeze-drying ، تبخیر فاز معکوس، تزریق اتر، سونیکاسیون،Microfluidization ، bubble و غیره میباشد که در ادامه به توضیح چند روش میپردازیم (16).
1. Sonication: در این روش مقداری از دارو در بافر حل شده و به مخلوط سورفکتانت و کلسترول در یک ویال اضافه میشود. این مخلوط با استفاده از پروب صوتی با دمای 60 درجه سانتیگراد برای 3 دقیقه همگن میشود. در نتیجه وزیکولهای همگن و یکنواختی تشکیل میشوند (17).
2. تکنیک تبخیر فاز معکوس (Reverse Phase Evaporation Technique) در این روش کلسترول و سورفکتانت در مخلوطی از اتر و کلروفرم حل میشود. فاز آبی حاوی دارو به این مواد اضافه و دو فاز حاصل در دمای 5-4 درجه سانتیگراد همگن میشود. به ژل زلال تشکیل شده مقدار کمی نمک بافر فسفات اضافه میشود. فاز آلی در دمای 60-40 درجه سانتیگراد و فشار کم حذف میشود. در نتیجه سوسپانسیون چسبناک نیوزوم با نمک فسفات رقیق شده و در حمام آبی در دمای 60 درجه به مدت 10 دقیقه حرارت داده می شود تا نیوزوم ها تشکیل شود (18).
3. روش تزریق اتر (Ether Injection Method): ابتدا به آرامی مقدار مشخص از سورفکتانت در دیاتیلاتر حل شده و در حمام آب گرم در دمای 60 درجه قرار داده میشود. مخلوط سورفکتانت توسط سوزن 14 درجهای به یک محلول آبی تزریق میشود. تبخیر اتر منجر به تشکیل وزیکولهای تک لایه میشود. بسته به شرایط مورد استفاده، وزیکولهایی با قطر 1000-50 نانومتر تشکیل میگردد (19).
4. تکنیک آبدهی فیلم نازک (Thin Film HydrationTechnique ) ابتدا تمام مولکولهای تشکیل دهنده وزیکول از قبیل سورفکتانتها، کلسترول و القا کنندههای شارژ در یک حلال آلی فرار مانند: دیاتیلاتر، متانول، کلروفرم و غیره در یک بالن ته گرد حل شده و با استفاده از یک دستگاه تبخیر کننده دوار حلالهای آلی در دمای اتاق تبخیر میشود و یک فیلم خشک و نازک از اجزای محلول تشکیل میشود. فیلم نازک خشک شده با فاز آبی با تحریک ملایم هیدراته شده که منجر به تشکیل نیوزوم میشود (20). در این روش نیوزومهای چند لایه ایجاد میشوند (7).

روش آبدهی فیلم نازک(17)
فرموله کردن نیوزوم: فرموله کردن نیوزوم مهمترین پارامتر است که میتواند روی ویژگیهای نیوزوم تاثیر بگذارد (21).
سورفکتانتها: سورفکتانتها یک کلاس منحصر به فرد از ترکیبات شیمیایی را تشکیل میدهند. آنها مولکولهای آمفیفیلیک هستند با دو ناحیه مجزا که قابلیت حل شدن بسیار متفاوتی دارند، یک انتهای آبدوست و یک انتهای چربیدوست که آبگریز میباشد. سورفکتانتها را میتوان به چهار گروه آنیونی، کاتیونی، آمفوتریک و غیر یونی طبقهبندی کرد (22). اگر قسمت سر یک سورفکتانت دارای بار منفی باشد به آن آنیونی گفته میشود، شامل: نمکهای اسید چرب (صابون)، سولفاتها، اتر سولفاتها و فسفات استرها میشود. اگر قسمت سر دارای بار مثبت باشد سورفکتانت کاتیونی و اگر سر حاوی هر دو بار مثبت و منفی باشد به آن آمفوتریک گفته میشود. انواع کاتیونی اغلب باعث تحریکپذیری و گاهی حتی باعث سمیت میشوند، بنابراین استفاده از آنها محدود است. سورفکتانتهای غیر یونی در سرشان هیچ باری ندارند. بنابراین در محلولها ساختارهایی ایجاد میکنند که در آن سرهای آبدوست در مقابل محلول آبی و دمهای آبگریز در مقابل محلولهای آلی قرار میگیرند. آمفی فیلهای غیر یونی که در نیوزومها استفاده میشود در چهار دسته آلکیلاسترها، آلکیلآمیدها، آلکیلاترها و استرهای اسیدچرب طبقهبندی میشوند. اغلب سورفکتانتهای مورد استفاده در نیوزوم براساس تعادل هیدروفیلیک-لیپوفیلیک در زیر آمده است، انتخاب نوع سورفکتانت به تعادل هیدروفیلیک-لیپوفیلیک (HLB) و پارامترهای بستهبندی بحرانی (CPP) بستگی دارد (23). تعادل هیدروفیلی- لیپوفیلی (Hydrophillic-Lipophillic Balance) یک راهنما برای انتخاب سورفکتانت بوده و مقدار آن نقش مهمی در کنترل بازده کپسولاسیون دارو دارد. تا به حال، بسته به مدیریت نیوزوم، تعداد زیادی از سورفکتانتهای غیر یونی با ارزش HLB مختلف ازقبیل پلیگلیسرول آلکیلاترها، گلوکوزیل دیآلکیلاترها، پلیاکسیاتیلناترها و استرها از جمله سری Brij،Tween ، Spanاستفاده شده است. سورفکتانتهای با HLB بین 8-3 با آماده سازی سطوح دو لایه سازگار است (4). مقیاس HLBبین مقادیر20-0 میباشد.HLB پایینتر به سورفاکتانت لیپوفیلی و HLB بالاتر به سورفاکتانت هیدروفیلی بیشتر اشاره دارد (15). سورفاکتانتهای هیدروفیلی با ارزش HLB بین 14 تا 17 به علت حلالیت بالا در آب برای تشکیل وزیکولهای دو لایه مناسب نیستند (24). پارامترهای بستهبندی بحرانی ( Critical Packing Parameter) علاوه بر HLB، برای پیشبینی توانایی تشکیل وزیکول، عوامل مختلف دیگر هم نقش اساس دارند. CPP یک مقیاس بدون بعد برای سورفکتانتها میباشد که به صورت زیرتعریف شده است.
Cpp=V/Lca0
V = حجم گروه هیدروفوب
LC= طول گروه هیدروفوب بحرانی
a0= منطقه سر گروه هیدروفیل

پارامتر بحرانی بسته بندی یک آمفی فیل(26)
نوع وزیکول را میتوان از طریق ارزش CPP سورفکتانت پیشبینی کرد. CPP بین 1/5-1 نشان دهنده این است، که احتمالاً سورفکتانت بهشکل وزیکول است. CPPکمتر از 0/5 نشان میدهد به علت بزرگی سر آبدوست میسلها کروی هستند و CPP بیشتر از 1 به دلیل مقدار زیاد گروه آبگریز میسلهای معکوس تولید میکند، که احتمالاً فقط بر روی فاز چربی یا رسوب اتفاق میافتد (25).
دمای انتقال فاز(TC)
دمای انتقال فاز تاثیر مستقیمی بر راندمان کپسولاسیون سورفکتانت دارد. بهعنوان مثال Span60 یک سورفکتانت با دمای انتقال فاز بالاست که بالاترین بازده کپسولاسیون را نشان میدهد (26).
عوامل افزودنی(Additive agants)
علاوه بر ماهیت سورفکتانتها، کپسولاسیون و روش تهیه نیوزوم، یک عامل افزودنی میتواند پارامتر موثری در خود تجمعی سورفکتانتها باشد. تاکنون افزودنیهای مختلفی برای نیوزومها استفاده شده که در میان آنها شایعترین و مهم ترین کلسترول است. محتوای کلسترول روی خواص وزیکولها از قبیل بازده کپسولاسیون، زمان نگهداری، رهایش و پایداری تاثیر میگذارد (27).
القا کننده های شارژ
القا کنندههای شارژ یکی دیگر از افزودنیهای غشایی هستند که اغلب در نیوزومها یافت میشود، زیرا باعث افزایش تراکم شارژ سطحی و جلوگیری از انحلال، تجمع و همجوشی میشود. مولکولهایی با بار منفی و مثبت برای ایجاد القای بار در نیوزم استفاده میشود. دیستیلفسفات(Dicetyl phosphate) و استاریلآمین (Stearyl amine)که منجر به شارژ منفی یا مثبت میشود، نمونههایی از این افزودنیهای غشایی هستند (6).
ویژگیهای نیوزوم
اندازه و پتانسیل زتا برای حرکت وزیکول در بدن، توزیع زیستی، سمیت و پایداری نیوزومها بسیار مهم هستند (28). شکل وزیکول نیوزوم به صورت کروی فرض میشود و برای تعیین قطر متوسط و شکل آنها از روشهایی مانند پراکندگی نور لیزر، میکروسکوپ الکترونی، کروماتوگرافی غربالی مولکولی استفاده میشود (29).
تشکیل دو لایه، سفتی غشا و تعداد لایهها
تشکیل دو لایه بوسیله سورفکتانتهای غیر یونی توسط X-cross در میکروسکوپ پلاریزاسیون نوری مشخص میشود و با استفاده ازابزار پروب فلورسانس میتوان آن را اندازهگیری کرد. طیفسنجی NMR، پراکندگی اشعه X و میکروسکوپ الکترونی برای تعیین تعداد لایه استفاده میشود (30).
راندمان داروی بارگذاری شده
داروی آزاد موجود در سوسپانسیون نیوزومی توسط کیسه دیالیز، ژل فیلتراسیون یا سانتریفیوژ جدا میشوند. مقدار داروی بارگذاری شده در آنها توسط لیز کردن وزیکولها با استفاده ازپروپانول 50 درصد یا تریتون x-100، محاسبه میشود. برای تعین درصد بارگزاری دارو، سوسپانسیون نیوزومی لیز شده سانتریفوژ میشود، محلول رویی حذف شده و رسوب دو بار توسط آب مقطر شسته میشود تا داروی بارگذاری شده حذف شود. راندمان بارگذاری با استفاده از فرمول زیر محاسبه میشود (31).
100* (مقدار کل دارو/مقدار داروی موجود در نیوزوم) =درصد بارگذاری
جداسازی داروی بارگذاری نشده از محلول نیوزوم
• ژل فیلتراسیون
داروی بارگذاری نشده در نیوزوم توسط ستون Sephadex-G-50 و شستشو با بافر فسفات سالین یا نمک معمولی جدا میشوند.
• کیسه دیالیز
محلول آبی اطراف نیوزوم توسط کیسه دیالیز در بافر نمکی فسفات یا محلول گلوکز یا نمک طبیعی دیالیز میشود.
• سانتریفیوژ
سوسپانسیون نیوزومها سانتریفیوژ شده، رسوب حاصله شسته میشود تا یک محلول نیوزومی بدون داروی آزاد بهدست بیاید (32).
رهایش
اندازهگیری میزان رهایش دارو از نیووزم
• کیسه دیالیز: انتشار دارو از سوسپانسیون نیوزوم تحت تاثیر عوامل متعددی از جمله غلظت دارو و حجم هیدراسیون قرار میگیرد. در این روش نیوزوم در کیسه دیالیز پرورده قرار میگیرد، اطراف آن را (100-300، 7/5= PH) بافر نمکی فسفات قرار داده در دمای37 درجه و بر روی همزن مغناطیسی دیالیز میشود. از اطراف کیسه دیالیز نمونهها در فواصل زمانی مشخص خارج و سانتریفوژ شده، سپس با استفاده از روشهای متداول طیفسنجی مانند UV،HPLC مورد بررسی قرار میگیرند (33).
• دیالیز معکوس: در این روش، تعدادی کیسه دیالیز کوچک که حاوی 1 میلیلیتر از بافر فسفات هستند، در محلول نیوزوم قرار میگیرند. رقیقسازی مستقیم نیوزومها با این روش امکانپذیر است؛ با این وجود انتشار سریع آن با استفاده از این روش قابل اندازهگیری نیست (18).
مزایای نیوزوم
1.این وزیکولها حاملهای مبتنی بر آب هستند،که در مقایسه با فرمهای دارویی روغنی، رضایت بیمار را بالا میبرد.
2.آنها دارای یک زیر ساخت متشکل از اجزای هیدروفیلی، آمفیفیلی و لیپوفیلی هستند و در نتیجه میتوانند مولکولهای دارویی با یک رنج وسیعی از حلالیت را در خود جای دهند.
3. خصوصیات فرمولاسیون وزیکول قابل تغییر و کنترل است. با تغییر ترکیبات وزیکول اندازه، لاملاریته، بارسطحی وغلظت وزیکول را میتوان کنترل کرد.
4. این وزیکولها میتوانند به عنوان مخزن عمل کنند و دارو را به صورت کنترل شده آزاد کنند.
5. از لحاظ اسمزی فعال و پایدار هستند و همچنین ثبات دارو را افزایش میدهند (33).
6. اداره و نگهداری سورفکتانتها نیاز به شرایط خاصی ندارد.
7.آنها توانایی زیستی و جذب ناچیز داروهای خوراکی را بهبود میبخشند و نفوذ دارو به پوست را بالا می برند.
8. نیوزوم ها میتوانند از طریق مسیر خوراکی، موضعی و تزریقی به محل مورد نظر برسند.
9. سورفکتانتها زیست سازگار و بیولوژیک هستند و پاسخ ایمنی تولید نمیکنند.
10. عملکرد درمانی مولکولهای دارویی را با به تاخیر انداختن ترخیص دارو از گردش خون، محافظت از دارو در محیط بیولوژیک و محدود کردن اثر دارو به سلولهای هدف بهبود میبخشند (34).
نتیجهگیری
نوع وزیکول را میتوان از طریق ارزش CPP سورفکتانت پیشبینی کرد. CPP بین 1/5-1 نشان دهنده این است، که احتمالاً سورفکتانت بهشکل وزیکول است. CPPکمتر از 0/5 نشان میدهد به علت بزرگی سر آبدوست میسلها کروی هستند و CPP بیشتر از 1 به دلیل مقدار زیاد گروه آبگریز میسلهای معکوس تولید میکند، که احتمالاً فقط بر روی فاز چربی یا رسوب اتفاق میافتد (25).
دمای انتقال فاز(TC)
دمای انتقال فاز تاثیر مستقیمی بر راندمان کپسولاسیون سورفکتانت دارد. بهعنوان مثال Span60 یک سورفکتانت با دمای انتقال فاز بالاست که بالاترین بازده کپسولاسیون را نشان میدهد (26).
عوامل افزودنی(Additive agants)
علاوه بر ماهیت سورفکتانتها، کپسولاسیون و روش تهیه نیوزوم، یک عامل افزودنی میتواند پارامتر موثری در خود تجمعی سورفکتانتها باشد. تاکنون افزودنیهای مختلفی برای نیوزومها استفاده شده که در میان آنها شایعترین و مهم ترین کلسترول است. محتوای کلسترول روی خواص وزیکولها از قبیل بازده کپسولاسیون، زمان نگهداری، رهایش و پایداری تاثیر میگذارد (27).
القا کننده های شارژ
القا کنندههای شارژ یکی دیگر از افزودنیهای غشایی هستند که اغلب در نیوزومها یافت میشود، زیرا باعث افزایش تراکم شارژ سطحی و جلوگیری از انحلال، تجمع و همجوشی میشود. مولکولهایی با بار منفی و مثبت برای ایجاد القای بار در نیوزم استفاده میشود. دیستیلفسفات(Dicetyl phosphate) و استاریلآمین (Stearyl amine)که منجر به شارژ منفی یا مثبت میشود، نمونههایی از این افزودنیهای غشایی هستند (6).
ویژگیهای نیوزوم
اندازه و پتانسیل زتا برای حرکت وزیکول در بدن، توزیع زیستی، سمیت و پایداری نیوزومها بسیار مهم هستند (28). شکل وزیکول نیوزوم به صورت کروی فرض میشود و برای تعیین قطر متوسط و شکل آنها از روشهایی مانند پراکندگی نور لیزر، میکروسکوپ الکترونی، کروماتوگرافی غربالی مولکولی استفاده میشود (29).
تشکیل دو لایه، سفتی غشا و تعداد لایهها
تشکیل دو لایه بوسیله سورفکتانتهای غیر یونی توسط X-cross در میکروسکوپ پلاریزاسیون نوری مشخص میشود و با استفاده ازابزار پروب فلورسانس میتوان آن را اندازهگیری کرد. طیفسنجی NMR، پراکندگی اشعه X و میکروسکوپ الکترونی برای تعیین تعداد لایه استفاده میشود (30).
راندمان داروی بارگذاری شده
داروی آزاد موجود در سوسپانسیون نیوزومی توسط کیسه دیالیز، ژل فیلتراسیون یا سانتریفیوژ جدا میشوند. مقدار داروی بارگذاری شده در آنها توسط لیز کردن وزیکولها با استفاده ازپروپانول 50 درصد یا تریتون x-100، محاسبه میشود. برای تعین درصد بارگزاری دارو، سوسپانسیون نیوزومی لیز شده سانتریفوژ میشود، محلول رویی حذف شده و رسوب دو بار توسط آب مقطر شسته میشود تا داروی بارگذاری شده حذف شود. راندمان بارگذاری با استفاده از فرمول زیر محاسبه میشود (31).
100* (مقدار کل دارو/مقدار داروی موجود در نیوزوم) =درصد بارگذاری
جداسازی داروی بارگذاری نشده از محلول نیوزوم
• ژل فیلتراسیون
داروی بارگذاری نشده در نیوزوم توسط ستون Sephadex-G-50 و شستشو با بافر فسفات سالین یا نمک معمولی جدا میشوند.
• کیسه دیالیز
محلول آبی اطراف نیوزوم توسط کیسه دیالیز در بافر نمکی فسفات یا محلول گلوکز یا نمک طبیعی دیالیز میشود.
• سانتریفیوژ
سوسپانسیون نیوزومها سانتریفیوژ شده، رسوب حاصله شسته میشود تا یک محلول نیوزومی بدون داروی آزاد بهدست بیاید (32).
رهایش
اندازهگیری میزان رهایش دارو از نیووزم
• کیسه دیالیز: انتشار دارو از سوسپانسیون نیوزوم تحت تاثیر عوامل متعددی از جمله غلظت دارو و حجم هیدراسیون قرار میگیرد. در این روش نیوزوم در کیسه دیالیز پرورده قرار میگیرد، اطراف آن را (100-300، 7/5= PH) بافر نمکی فسفات قرار داده در دمای37 درجه و بر روی همزن مغناطیسی دیالیز میشود. از اطراف کیسه دیالیز نمونهها در فواصل زمانی مشخص خارج و سانتریفوژ شده، سپس با استفاده از روشهای متداول طیفسنجی مانند UV،HPLC مورد بررسی قرار میگیرند (33).
• دیالیز معکوس: در این روش، تعدادی کیسه دیالیز کوچک که حاوی 1 میلیلیتر از بافر فسفات هستند، در محلول نیوزوم قرار میگیرند. رقیقسازی مستقیم نیوزومها با این روش امکانپذیر است؛ با این وجود انتشار سریع آن با استفاده از این روش قابل اندازهگیری نیست (18).
مزایای نیوزوم
1.این وزیکولها حاملهای مبتنی بر آب هستند،که در مقایسه با فرمهای دارویی روغنی، رضایت بیمار را بالا میبرد.
2.آنها دارای یک زیر ساخت متشکل از اجزای هیدروفیلی، آمفیفیلی و لیپوفیلی هستند و در نتیجه میتوانند مولکولهای دارویی با یک رنج وسیعی از حلالیت را در خود جای دهند.
3. خصوصیات فرمولاسیون وزیکول قابل تغییر و کنترل است. با تغییر ترکیبات وزیکول اندازه، لاملاریته، بارسطحی وغلظت وزیکول را میتوان کنترل کرد.
4. این وزیکولها میتوانند به عنوان مخزن عمل کنند و دارو را به صورت کنترل شده آزاد کنند.
5. از لحاظ اسمزی فعال و پایدار هستند و همچنین ثبات دارو را افزایش میدهند (33).
6. اداره و نگهداری سورفکتانتها نیاز به شرایط خاصی ندارد.
7.آنها توانایی زیستی و جذب ناچیز داروهای خوراکی را بهبود میبخشند و نفوذ دارو به پوست را بالا می برند.
8. نیوزوم ها میتوانند از طریق مسیر خوراکی، موضعی و تزریقی به محل مورد نظر برسند.
9. سورفکتانتها زیست سازگار و بیولوژیک هستند و پاسخ ایمنی تولید نمیکنند.
10. عملکرد درمانی مولکولهای دارویی را با به تاخیر انداختن ترخیص دارو از گردش خون، محافظت از دارو در محیط بیولوژیک و محدود کردن اثر دارو به سلولهای هدف بهبود میبخشند (34).
نتیجهگیری
در سالهای اخیر، سیستمهای وزیکولی تحویل دارو توجه زیادی را به خود جلب کردهاند. نیوزومها یک سیستم تحویل دارویی مناسب، هدفمند و موثر با توانایی بارگیری هر دو داروی آبدوست و آبگریز هستند. سورفکتانتها بهعنوان اجزای ساختمانی نیوزومها نقش مهمی در شکلگیری و خواص این نانو حاملها دارند، بنابراین هرگونه پیشرفت در سنتز سورفکتانتهای جدید که غیر سمی، کمهزینه، زیست سازگار و زیست تخریبپذیر باشند، باعث افزایش راندمان نیوزومها خواهد شد .بهطور خلاصه، نیوزمها یک ابزار بسیار مؤثر برای تحویل دارو در درمان بیماریهای متعدد هستند و دارای قابلیت بالاتری نسبت به درمانهای دارویی معمولی میباشند.
تعارض در منافع: وجود ندارد.
References:
1- Fakruddin M, Hossain Z, Afroz H. Prospects and Applications of Nanobiotechnology: A Medical Perspective. J Nanobiotechnol 2012; 10(1): 1-8.
2-Telrandhe R. Nanotechnology for Cancer Therapy: Recent Developments. EJPMR 2016; 3(11): 284-94.
3- Misra R, Acharya S, Sahoo SK. Cancer Nanotechnology: Application of Nanotechnology in Cancer Therapy. Drug Discovery Today 2010; 15(19-20): 842-50.
4-Moghassemi S, Hadjizadeh A. Nano-Niosomes as Nanoscale Drug Delivery Systems: An Illustrated Review. Journal of Controlled Release 2014; 185: 22-36.
5-Waddad AY, Abbad S, Yu F, Munyendo WL, Wang J, Lv H, et al. Formulation, Characterization and Pharmacokinetics of Morin Hydrate Niosomes Prepared from Various Non-Ionic Surfactants. Int J Pharma 2013; 456(2): 446-58.
6- Nasir A, Harikumar S, Amanpreet K. Niosomes: An Excellent Tool for Drug Delivery. IJRPC 2012; 2(2): 479-87.
7-Seleci DA, Seleci M, Walter J-G, Stahl F, Scheper T. Niosomes as Nanoparticular Drug Carriers: Fundamentals and Recent Applications. Journal of Nanomaterials 2016; 2016: 2-13.
8-Parthasarathi G, Udupa N, Umadevi P, Pillai G. Niosome Encapsulated of Vincristine Sulfate: Improved Anticancer Activity with Reduced Toxicity in Mice. Journal of Drug Targeting 1994; 2(2): 173-82.
9-Paolino D, Cosco D, Muzzalupo R, Trapasso E, Picci N, Fresta M. Innovative Bola-Surfactant Niosomes as Topical Delivery Systems of 5-Fluorouracil for the Treatment of Skin Cancer. Int J Pharm 2008; 353(1-2): 233-42.
10-Barani M, Mirzaei M, Torkzadeh-Mahani M, Nematollahi MH. Lawsone-Loaded Niosome and its Antitumor Activity in MCF-7 Breast Cancer Cell Line: A Nano-Herbal Treatment for Cancer. DARU 2018; 26(1): 11-17.
11-Asgharkhani E, Azarbayjani AF, Irani S, Chiani M, Saffari Z, Norouzian D, et al. Artemisinin-Loaded Niosome and Pegylated Niosome: Physico-Chemical Characterization and Effects on MCF-7 Cell Proliferation. J Pharm Investig 2018; 48: 251-6.
12-Askari M, Nikoonahad Lotfabadi N. Evaluation of Niosomal Nano-Carriers Capabilities on Toxicity Preservation and Delivery of Pomegranate Peel Extract in Cell Culture Conditions (MCF-7 Cell Line of Breast Cancer). DMed 2018; 26(5): 9-20. [Persian]
13-Nikoonahad Lotfabadi N, Mohseni Kouchesfehani H, Sheikhha MH, Kalantar SM. Evaluation and Comparison of Physicochemical Properties, Cytotoxicity and the Ability of Mirna Loading of Different Cationic Liposomes for Gene Therapy Application. JSSU 2017; 25(6): 444-56. [Persian]
14-Nikoonahad Lotfabadi N, Mohseni Kouchesfehani H, Sheikhha MH, Kalantar SM. Mirna -101 Transfection and its Effect on the Cytotoxicity Induction and Expression of Ubiquitin Ligase HECTH9 in Acute Myeloid Leukemia Cells (AML). JSSU 2018; 26(1): 64-76. [Persian]
15-Kazi KM, Mandal AS, Biswas N, Guha A, Chatterjee S, Behera M, et al. Niosome: A Future of Targeted Drug Delivery Systems. J Adv Pharm Technol Res 2010; 1(4): 374-80.
16-Amoabediny G, Haghiralsadat F, Naderinezhad S, Helder MN, Akhoundi Kharanaghi E, Mohammadnejad Arough J. Overview of Preparation Methods of Polymeric And Lipid-Based (Niosome, Solid Lipid, Liposome) Nanoparticles: A Comprehensive Review. International Journal of Polymeric Materials and Polymeric Biomaterials 2018; 67(6): 383-400.
17-Baillie A, Florence A, Hume L, Muirhead G, Rogerson A. The Preparation and Properties of Niosomes—Non‐Ionic Surfactant Vesicles. Journal of Pharmacy and Pharmacology 1985; 37(12): 863-8.
18-Goswami, Swarnali. Niosomes- A Review of Current Status and Application. World Journal of Pharmacy and Pharmaceutical Sciences 2017; 594-615.
19-Baillie A, Coombs G, Dolan T, Laurie J. Non‐Ionic Surfactant Vesicles, Niosomes, as a Delivery System for the Anti‐Leishmanial Drug, Sodium Stibogluconate. Journal of Pharmacy and Pharmacology 1986; 38(7): 502-5.
20-Khan R, Irchhaiya R. Niosomes: A Potential Tool for Novel Drug Delivery. Journal of Pharmaceutical Investigation 2016; 46(3): 195-204.
21-Mahale N, Thakkar P, Mali R, Walunj D, Chaudhari S. Niosomes: Novel Sustained Release Nonionic Stable Vesicular Systems—An Overview. Advances in Colloid and Interface Science 2012; 183: 46-54.
22-Guertechin D, Oldenhove L. Classification of Surfactants. Handbook of Cosmetic Science and Technology 2001; 431-32.
23-Schramm LL, Stasiuk EN, Marangoni DG. Surfactants and their Applications. Annu Rep Prog Chem Sect 2003; 99: 3-48.
24-Shahiwala A, Misra A. Studies in Topical Application of Niosomally Entrapped Nimesulide. J Pharm Pharm Sci 2002; 5(3): 220-5.
25-Uchegbu IF, Vyas SP. Non-Ionic Surfactant Based Vesicles (Niosomes) in Drug Delivery. International Journal of Pharmaceutics 1998; 172(1-2): 33-70.
26-Kumar GP, Rajeshwarrao P. Nonionic Surfactant Vesicular Systems for Effective Drug Delivery—An Overview. Acta Pharmaceutica Sinica B 2011; 1(4): 208-19.
27-Yeo PL, Lim CL, Chye SM, Ling APK, Koh RY. Niosomes: A Review of their Structure, Properties, Methods of Preparation, and Medical Applications. Asian Biomedicine(Res Rev News) 2017; 11(4): 301-14.
28-Ge X, Wei M, He S, Yuan WE. Advances of Non-Ionic Surfactant Vesicles (Niosomes) and their Application in Drug Delivery. Pharmaceutics 2019; 11(2): 55.
29-Lohumi A. A Novel Drug Delivery System: Niosomes Review. Journal of Drug Delivery and Therapeutics 2012; 2(5): 129-35.
30-Azmin M, Florence A, Handjani‐Vila R, Stuart J, Vanlerberghe G, Whittaker J. The Effect of Non‐Ionic Surfactant Vesicle (Niosome) Entrapment on the Absorption and Distribution of Methotrexate In Mice. J Pharm Pharmacol 1985; 37(4): 237-42.
31-Makeshwar KB, Wasankar SR. Niosome: A Novel Drug Delivery System. Asian J Pharm Res 2013; 3(1): 16-20.
32-Shah C, Kela M, Ganesh N, Chandy V. Niosomes as Promising Vehicle for Novel Drug Delivery System: Recent Review. Pharma Science Monitor 2017; 8(4): 717-31.
33-Khoee S, Yaghoobian M. Niosomes: A Novel Approach in Modern Drug Delivery Systems. Nanostructures for Drug Delivery 2017: 207-37.
34-Tarekegn A, Joseph NM, Palani S, Zacharia A, Ayenew Z. Niosomes in Targeted Drug Delivery: Some Recent Advances. IJPSR 2010; 1(9): 1-8.
2-Telrandhe R. Nanotechnology for Cancer Therapy: Recent Developments. EJPMR 2016; 3(11): 284-94.
3- Misra R, Acharya S, Sahoo SK. Cancer Nanotechnology: Application of Nanotechnology in Cancer Therapy. Drug Discovery Today 2010; 15(19-20): 842-50.
4-Moghassemi S, Hadjizadeh A. Nano-Niosomes as Nanoscale Drug Delivery Systems: An Illustrated Review. Journal of Controlled Release 2014; 185: 22-36.
5-Waddad AY, Abbad S, Yu F, Munyendo WL, Wang J, Lv H, et al. Formulation, Characterization and Pharmacokinetics of Morin Hydrate Niosomes Prepared from Various Non-Ionic Surfactants. Int J Pharma 2013; 456(2): 446-58.
6- Nasir A, Harikumar S, Amanpreet K. Niosomes: An Excellent Tool for Drug Delivery. IJRPC 2012; 2(2): 479-87.
7-Seleci DA, Seleci M, Walter J-G, Stahl F, Scheper T. Niosomes as Nanoparticular Drug Carriers: Fundamentals and Recent Applications. Journal of Nanomaterials 2016; 2016: 2-13.
8-Parthasarathi G, Udupa N, Umadevi P, Pillai G. Niosome Encapsulated of Vincristine Sulfate: Improved Anticancer Activity with Reduced Toxicity in Mice. Journal of Drug Targeting 1994; 2(2): 173-82.
9-Paolino D, Cosco D, Muzzalupo R, Trapasso E, Picci N, Fresta M. Innovative Bola-Surfactant Niosomes as Topical Delivery Systems of 5-Fluorouracil for the Treatment of Skin Cancer. Int J Pharm 2008; 353(1-2): 233-42.
10-Barani M, Mirzaei M, Torkzadeh-Mahani M, Nematollahi MH. Lawsone-Loaded Niosome and its Antitumor Activity in MCF-7 Breast Cancer Cell Line: A Nano-Herbal Treatment for Cancer. DARU 2018; 26(1): 11-17.
11-Asgharkhani E, Azarbayjani AF, Irani S, Chiani M, Saffari Z, Norouzian D, et al. Artemisinin-Loaded Niosome and Pegylated Niosome: Physico-Chemical Characterization and Effects on MCF-7 Cell Proliferation. J Pharm Investig 2018; 48: 251-6.
12-Askari M, Nikoonahad Lotfabadi N. Evaluation of Niosomal Nano-Carriers Capabilities on Toxicity Preservation and Delivery of Pomegranate Peel Extract in Cell Culture Conditions (MCF-7 Cell Line of Breast Cancer). DMed 2018; 26(5): 9-20. [Persian]
13-Nikoonahad Lotfabadi N, Mohseni Kouchesfehani H, Sheikhha MH, Kalantar SM. Evaluation and Comparison of Physicochemical Properties, Cytotoxicity and the Ability of Mirna Loading of Different Cationic Liposomes for Gene Therapy Application. JSSU 2017; 25(6): 444-56. [Persian]
14-Nikoonahad Lotfabadi N, Mohseni Kouchesfehani H, Sheikhha MH, Kalantar SM. Mirna -101 Transfection and its Effect on the Cytotoxicity Induction and Expression of Ubiquitin Ligase HECTH9 in Acute Myeloid Leukemia Cells (AML). JSSU 2018; 26(1): 64-76. [Persian]
15-Kazi KM, Mandal AS, Biswas N, Guha A, Chatterjee S, Behera M, et al. Niosome: A Future of Targeted Drug Delivery Systems. J Adv Pharm Technol Res 2010; 1(4): 374-80.
16-Amoabediny G, Haghiralsadat F, Naderinezhad S, Helder MN, Akhoundi Kharanaghi E, Mohammadnejad Arough J. Overview of Preparation Methods of Polymeric And Lipid-Based (Niosome, Solid Lipid, Liposome) Nanoparticles: A Comprehensive Review. International Journal of Polymeric Materials and Polymeric Biomaterials 2018; 67(6): 383-400.
17-Baillie A, Florence A, Hume L, Muirhead G, Rogerson A. The Preparation and Properties of Niosomes—Non‐Ionic Surfactant Vesicles. Journal of Pharmacy and Pharmacology 1985; 37(12): 863-8.
18-Goswami, Swarnali. Niosomes- A Review of Current Status and Application. World Journal of Pharmacy and Pharmaceutical Sciences 2017; 594-615.
19-Baillie A, Coombs G, Dolan T, Laurie J. Non‐Ionic Surfactant Vesicles, Niosomes, as a Delivery System for the Anti‐Leishmanial Drug, Sodium Stibogluconate. Journal of Pharmacy and Pharmacology 1986; 38(7): 502-5.
20-Khan R, Irchhaiya R. Niosomes: A Potential Tool for Novel Drug Delivery. Journal of Pharmaceutical Investigation 2016; 46(3): 195-204.
21-Mahale N, Thakkar P, Mali R, Walunj D, Chaudhari S. Niosomes: Novel Sustained Release Nonionic Stable Vesicular Systems—An Overview. Advances in Colloid and Interface Science 2012; 183: 46-54.
22-Guertechin D, Oldenhove L. Classification of Surfactants. Handbook of Cosmetic Science and Technology 2001; 431-32.
23-Schramm LL, Stasiuk EN, Marangoni DG. Surfactants and their Applications. Annu Rep Prog Chem Sect 2003; 99: 3-48.
24-Shahiwala A, Misra A. Studies in Topical Application of Niosomally Entrapped Nimesulide. J Pharm Pharm Sci 2002; 5(3): 220-5.
25-Uchegbu IF, Vyas SP. Non-Ionic Surfactant Based Vesicles (Niosomes) in Drug Delivery. International Journal of Pharmaceutics 1998; 172(1-2): 33-70.
26-Kumar GP, Rajeshwarrao P. Nonionic Surfactant Vesicular Systems for Effective Drug Delivery—An Overview. Acta Pharmaceutica Sinica B 2011; 1(4): 208-19.
27-Yeo PL, Lim CL, Chye SM, Ling APK, Koh RY. Niosomes: A Review of their Structure, Properties, Methods of Preparation, and Medical Applications. Asian Biomedicine(Res Rev News) 2017; 11(4): 301-14.
28-Ge X, Wei M, He S, Yuan WE. Advances of Non-Ionic Surfactant Vesicles (Niosomes) and their Application in Drug Delivery. Pharmaceutics 2019; 11(2): 55.
29-Lohumi A. A Novel Drug Delivery System: Niosomes Review. Journal of Drug Delivery and Therapeutics 2012; 2(5): 129-35.
30-Azmin M, Florence A, Handjani‐Vila R, Stuart J, Vanlerberghe G, Whittaker J. The Effect of Non‐Ionic Surfactant Vesicle (Niosome) Entrapment on the Absorption and Distribution of Methotrexate In Mice. J Pharm Pharmacol 1985; 37(4): 237-42.
31-Makeshwar KB, Wasankar SR. Niosome: A Novel Drug Delivery System. Asian J Pharm Res 2013; 3(1): 16-20.
32-Shah C, Kela M, Ganesh N, Chandy V. Niosomes as Promising Vehicle for Novel Drug Delivery System: Recent Review. Pharma Science Monitor 2017; 8(4): 717-31.
33-Khoee S, Yaghoobian M. Niosomes: A Novel Approach in Modern Drug Delivery Systems. Nanostructures for Drug Delivery 2017: 207-37.
34-Tarekegn A, Joseph NM, Palani S, Zacharia A, Ayenew Z. Niosomes in Targeted Drug Delivery: Some Recent Advances. IJPSR 2010; 1(9): 1-8.
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |







