دوره 30، شماره 2 - ( اردیبهشت 1401 )
جلد 30 شماره 2 صفحات 4606-4593 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Fatemi S A, Frzaneh Hesari A, Dadban shahamat M. NLRP-3 Expression in Pancreatic Tissue Following Moderate and High Intensity Interval Training with Liposomal Alpha-Lipoic Acid Supplement in Diabetic Rats. JSSU 2022; 30 (2) :4593-4606
URL: http://jssu.ssu.ac.ir/article-1-5517-fa.html
URL: http://jssu.ssu.ac.ir/article-1-5517-fa.html
فاطمی سید عبدالله، فرزانه حصاری امین، دادبان شهامت مینو. تغییرات بیان ژن NLRP3 بافت پانکراس به دنبال تمرین تناوبی با شدت متوسط و شدید به همراه مکمل آلفالیپوئیک اسید لیپوزومال در موشهای دیابتی. مجله علمي پژوهشي دانشگاه علوم پزشكي شهید صدوقی يزد. 1401; 30 (2) :4593-4606
متن کامل [PDF 878 kb]
(380 دریافت)
| چکیده (HTML) (893 مشاهده)
References:
1- Sproston NR, Ashworth JJ. Role of C - reactive protein at Sites of Inflammation and Infection. Front Immunol 2018; 9: 754.
2- Groslambert M, Py BF. Spotlight on the NLRP3 Inflammasome Pathway. Inflamm Res 2018; 11: 359-74.
3- Vandanmagsar B, Youm YH, Ravussin A, Galgani JE, Stadler K, Mynatt RL, et al. The NLRP3 Inflammasome Instigates Obesity-Induced Inflammation And Insulin Resistance. Nat Med 2011; 17(2): 179-88.
4- Dixit VD. Nlrp3 Inflammasome Activation in Type 2 Diabetes: Is it Clinically Relevant? Diabetes 2013; 62(1): 22-4.
5- Golbidi S, Badran M, Laher I. Diabetes and Alpha Lipoic Acid. Front Pharmacol 2011; 2: 69.
6- Rochette L, Ghibu S, Muresan A, Vergely C. Alpha-Lipoic Acid: Molecular Mechanisms and Therapeutic Potential in Diabetes. Can J Physiol. Pharmacol 2015; 93(12): 1021-7.
7- Midaoui A, Fantus G, Boughrous A, Couture R. Beneficial Effects of Alpha-Lipoic Acid on Hypertension, Visceral Obesity, UCP-1 Expression and Oxidative Stress in Zucker Diabetic Fatty Rats. Antioxidants 2019; 8(12): 648.
8- Malin KS, Francois M, Eichner Z, Gilbertson N, He ston E, Fabris C. Impact of Short-Term Exercise Training Intensity on -Cell Function in Older Obese Adults with Prediabetes. J Appl Physiol 2018; 125(6): 1979-86.
9- Heiskanen MA, Motiani KK, Mari A, Saunavaara V, Eskelinen JJ, Virtanen KA, et al. Exercise Training Decreases Pancreatic Fat Content and Improves Beta Cell Function Regardless of Baseline Glucose Tolerance: A Randomised Controlled Trial. Diabetologia 2018; 61(8): 1817-28.
10- Holmes A, Coppey LJ, Davidson EP, Yorek MA. Rat Models of Diet-Induced Obesity and High Fat/Low Dose Streptozotocin Type 2 Diabetes: Effect of Reversal of High Fat Diet Compared to Treatment with Enalapril or Menhaden Oil on Glucose Utilization and Neuropathic Endpoints. J Diabetes Res 2015; 2015: 307285.
11- Lee J, Lee Y, LaVoy E, Umetani M, Hong J, Park Y. Physical Activity Protects NLRP3 Inflammasome-Associated Coronary Vascular Dysfunction in Obese Mice. Physiol Rep 2018; 6(12): 45-58.
12- Abbasi A, Faramarzi M, Ghatreh Samani M, Bbanitalebi E. The Effect of Different Intensities of Endurance Training on NLRP-3 Inflammasome Protein Expression in Visceral Adipose Tissue, Serum Glucose Levels and Insulin in Streptozotocin-Induced Diabetic Rats. Metabolism and Exercise, 2018; 7(1): 1-19. [Persian]
13- Khakroo Abkenar I, Rahmani-nia F, Lombardi G. The Effect of Different Intensities of Acute and Chronic Aerobic Activity on the Signaling Pathway of the Inflammasome NLRP3 Complex and TLR4 and Some Inflammatory Cytokines in Young Men. Practical Studies of Biosciences in Sport 2020; 8(16): 116-120. [Persian]
14- Zaidi H, Byrkjeland R, Njerve I, Akra A, Solheim S, Arnesen H, et al. Effects of Exercise Training on Inflammasome-Related Mediators and Their Associations to Glucometabolic Variables in Patients with Combined Coronary Artery Disease and Type 2 Diabetes Mellitus: Sub-Study of A Randomized Control Trial. Diab Vasc Dis Res 2019; 16(4): 360-8.
15- Zare Damirchi Z, Bashiri J, Narimani Rad MP, Hadi H. The Effect of Eight Weeks of Endurance Training and Olive Oil Supplementation on IL-1ß and NLRP3 Indices in Obese Male Rats. Yafte 2020; 22(3): 95-107. [Persian]
16- Faridnia M, Mohebbi H, Khalafi M, Moghaddami K, Khalafi M. The Effect of Interval and Continuous Training on the Content of Perilipin 1, ATGL and CGI -58 in Visceral Adipose Tissue of Obese Male Rats. SJKU 2019; 24(1): 78-89. [Persian]
17- Dworacka M, Chukanova G, Iskakova S, Kurmambayev Y, Wesołowska A, Frycz B. New Arguments for Beneficial Effects of Alpha-Lipoic Acid on the Cardiovascular System in the Course of Type 2 Diabetes. Eur J Pharm Sci 2018; 117: 41-7.
18- Karimi N, Bohlooli S, Mazani M. Nanoliposomal Formulation of Ecballium Elaterium Extract: Cytotoxic Evaluation Against Human Gastric Adenocarcinoma (AGS) Cell Line. Nanomedicine Research Journal 2016; 1(1): 9-14.
19- Carlos D, Costa FRC, Pereira CA, Rocha FA, Yaochite JN, Oliveira GG, et al. Mitochondrial DNA Activates the NLRP3 Inflammasome and Predisposes to Type 1 Diabetes in Murine Model. Front Immunol 2017; 8: 164.
20- Kim Y, Wang W, Okla M, Kang I, Moreau R, Chung S. Suppression of NLRP3 Inflammasome by Γ-Tocotrienol Ameliorates Type 2 Diabetes. J Lipid Res 2016; 57(1): 66-76.
21- Stienstra R, van Diepen JA, Tack CJ, Zaki MH, van de Veerdonk FL, Perera D, et al. Inflammasome Is a Central Player in the Induction of Obesity and Insulin Resistance. Proc Natl Acad Sci USA 2011; 108(37): 15324-9.
22- Freigang S, Ampenberger F, Weiss A, Kanneganti T-D, Iwakura Y, Hersberger M, et al. Fatty Acid-Induced Mitochondrial Uncoupling Elicits Inflammasome Independent IL-1 [Alpha] And Sterile Vascular Inflammation In Atherosclerosis. Nat Immunol 2013; 14(10): 1045-53.
23- Hong J, Kim K, Kim J-H, Park Y. The Role of Endoplasmic Reticulum Stress in Cardiovascular Disease and Exercise. Int J Vasc Med 2017; 2017: 2049217.
24- Kim Y, Pitriani P, Park G, Lee W. Moderate Intensity Exercise Has More Positive Effects on The Gene Expression of Inflammasome, M1, M2 Macrophage Infiltration and Brown Adipocyte Markers Compared to High Intensity Exercise in Subcutaneous Adipose of Obese Mice Induced by High Fat Diet. Life Science 2019; 29 (3): 303-10.
25- Mardare C, Krüger K, Liebisch G, Seimetz M, Couturier A, Ringseis R, et al. Endurance And Resistance Training Affect High Fat Diet-Induced Increase of Ceramides, Inflammasome Expression, and Systemic Inflammation in Mice. J Diabetes Res 2016; 2016: 4536470.
26- Mejías-Peña Y, Estébanez B, Rodriguez-Miguelez P, Fernandez-Gonzalo R, Almar M, de Paz JA, et al. Impact of Resistance Training on the Autophagyinflammation-Apoptosis Crosstalk in Elderly Subjects. Aging (Albany NY) 2017; 9(2): 408-18.
27- He Y, Franchi L, Núñez G. TLR Agonists Stimulate Nlrp3-Dependent IL-1β Production Independently of the Purinergic P2X7 Receptor in Dendritic Cells and in Vivo. Immunology 2013; 190(1): 334-9.
28- Oliveira AG, Carvalho BM, Tobar N, Ropelle ER, Pauli JR, Bagarolli RA, et al. Physical Exercise Reduces Circulating Lipopolysaccharide and TLR4 Activation and Improves Insulin Signaling in Tissues of DIO Rats. Diabetes 2011; 60(3): 784-96.
29- Goossens GH, Blaak EE, Theunissen R, Duijvestijn AM, Clément K, Tervaert JWC, et al. Expression of NLRP3 Inflammasome and T Cell Population Markers in Adipose Tissue are Associated with Insulin Resistance and Impaired Glucose Metabolism in Humans. Mol Immunol 2012; 50(3): 142-9.
30- Rovira-Llopis S, Apostolova N, Ban-uls S, Muntane J, Rocha M, Victor V. Mitochondria, the NLRP3 Inflammasome, and Sirtuins in Type 2 Diabetes: New Therapeutic Targets. Antioxid & Redox Signal 2018; 29(8): 749-90.
31- Peterson JM, Bryner RW, Sindler A, Frisbee JC, Alway SE. Mitochondrial Apoptotic Signaling is Elevated in Cardiac But Not Skeletal Muscle in the Obese Zucker Rat and is Reduced with Aerobic Exercise. J Appl Physiol 2008; 105(6): 1934-43.
32- Marin-Garcia J, Goldenthal MJ. Mitochondrial Centrality in Heart Failure. Heart Fail Rev 2008; 13(2): 137-50.
33- Pereira RM, Moura LP, Muñoz VR, Silva AS, Gaspar RS, Ropelle ER, et al. Molecular Mechanisms of Glucose Uptake in Skeletal Muscle at Rest and In Response to Exercise. Motriz- Revista De Educação Física 2017; 23: e101609.
34- Sylow L, Kleinert M, Richter EA, Jensen TE. Exercise-Stimulated Glucose Uptake [Mdash] Regulation and Implications for Glycaemic Control. Nat Rev Endocrinol 2017; 13(3): 133-48
35- EL-Sabbagh D, Dawood L, Abdallah AA, Hassan S. Effect of Alpha Lipoic Acid on Apoptotic Mechanisms and Oxidative Stress in Pancreatic Cells of High Fat Diet Induced Type II Diabetes Mellitus in Rats. Med J Cairo Univ 2019; 87(3): 1615-23.
36- Uchendu C. Chronic Co-Exposure to Chlorpyrifos and Deltamethrin Pesticides Induces Alterations in Serum Lipids and Oxidative Stress in Wistar Rats: Mitigating Role of Alpha-Lipoic Acid. Environ Sci Pollut Res 2018; 25(20):19605-11.
37- Kim SJ, Nian C, Widenmaier S, Mcintosh CH. Glucose-Dependent Insulinotropic Polypeptide-Mediated Up-Regulation of Β -Cell Antiapoptotic Bcl-2 Gene Expression is Coordinated by Cyclic AMP (Camp) Response Element Binding Protein (CREB) and Camp-Responsive CREB Coactivator 2. Mol Cell Biol 2008; 28 (5): 1644-56.
38- Mendoza-Núñez VM, García-Martínez BI, Rosado-Pérez J, Santiago-Osorio E, Pedraza-Chaverri J, Hernández-Abad VJ. The Effect of 600 Mg Alpha-Lipoic Acid Supplementation on Oxidative Stress, Inflammation, and RAGE in Older Adults with Type 2 Diabetes Mellitus. Oxidative Medicine and Cellular Longevity 2019; 3276958; 67-79.
39- Gorąca A, Huk-Kolega H, Piechota A, Kleniewska P, Ciejka E, Skibska B. Lipoic Acid-Biological Activity and Therapeutic Potential. Pharmacological Reports 2011; 63: 849-58.
40- Akbari M, Ostadmohammadi V, Tabrizi R, Mobini M, Lankarani KB, Moosazadeh M, et al. The Effects of Alpha-Lipoic Acid Supplementation on Inflammatory Markers among Patients with Metabolic Syndrome and Related Disorders: A Systematic Review and Meta-Analysis of Randomized Controlled Trials. Nutr Metabol 2018; 15(1): 39.
41- Yamawaki H, Kuramoto J, Kameshima S, Usui T, Okada M, Hara Y. Omentin. A Novel Adipocytokine Inhibits Tnf-Induced Vascular Inflammation in Human Endothelial Cells. Biochem Biophys Res Commun 2011; 408(2): 339-43.
42- Liu R, Wang X, Bu P. Omentin-1 Is Associated With Carotid Atherosclerosis In Patients With Metabolic Syndrome. Diabetes Res Clin Pract 2011; 93(1): 21-5.
43- El Midaoui A, de Champlain J. Prevention of Hypertension, Insulin Resistance, and Oxidative Stress by Alpha-Lipoic Acid. Hypertension 2002; 39(2): 303-7.
44- Peth JA, Kinnick TR, Youngblood EB, Tritschler HJ, Henriksen EJ. Effects of a Unique Conjugate of Alpha-Lipoic Acid and Gamma-Linolenic Acid on Insulin Action in Obese Zucker Rats. Am J Physiol Regul Integr Comp Physiol 2000; 278(2): 453-9.
متن کامل: (576 مشاهده)
مقدمه
التهاب مزمن یک عامل کلیدی در ایجاد دیابت است به طوریکه سطح بالاتری از پروتئینهای التهابی مانند اینترلوکین یک بتا (IL-1β) و اینترلوکین شش (IL-6) و پروتئین واکنش پذیر C پیشبینی کننده دیابت هستند (1). مطالعات نشان از آن دارند که سلولهای ایمنی میتوانند با بهکارگیری گیرندههای NLRs (نوعی از گیرندههای تشخیص الگو) الگوهای مولکولی مرتبط با پاتوژن و مرتبط با خطر را شناسایی و به القا پاسخهای التهابی منجر شوند. فعالسازی NLRs منجر به تعامل انفلامازوم NLRP3 با پروتئین تعدیل-کننده ASC میشود. این عمل منجر به فعالسازی پروکاسپاز-1 و تولید کاسپاز-1 میشود که تولید و ترشح IL-1β و IL-18 را به دنبال دارد (2). مطالعات نشان دادهاند فعال شدنNLRP3 یکی از مکانیسمهای کلیدی در مقاومت به انسولین است (3). یکی از مکانیسمهای احتمالی نقش اینفلامازوم در روند دیابت نوع دو این گونه است که اینفلامازومNLRP3 سیگنالهای خطر ایجاد شده در دیابت نوع 2 از جمله پلیپپتیدآمیلوئید جزیرهای،ATP (adenosine triphosphate) خارج سلولی و گونههای فعال اکسیژن را شناسایی کند (4). در افراد دیابتی افزایش تولید رادیکالهای آزاد و کاهش آنتی اکسیدانها باعث استرس اکسایشی میشود که این موضوع منجر به اثرات مخرب متعددی در دیابت میگردد. لذا مصرف آنتیاکسیدانها میتواند نقش بسزایی داشته باشد. مکمل آلفالیپوئیک اسید (ALA) یک آنتیاکسیدان قوی است و به عنوان کوفاکتور در کمپلکس آنزیمی دهیدروژناز میتوکندریایی در متابولیسم فعالیت دارد (5). این ماده از یک طرف میتواند بهطور مستقیم رادیکالهای پروکسیل تولید شده را از بین برده، از طرف دیگر با احیای آسکوربیل و کرومانوکسیل موجب افزایش قدرت سایر آنتیاکسیدانها گردد (5). تحقیقات نشان میدهد ALA با افزایش فسفریلاسیون تیروزین در سوبسترای 1 گیرنده انسولین و به دنبال آن، فعالسازی فسفاتیدیل اینوزیتول 3-کیناز، سرعت جابجایی انتقال دهندههای گلوکز به غشای پلاسمایی را رهبری میکند (6). ازطرف دیگر، در یک مطالعه مشخص گردید ALA می¬تواند باعث بهبود متابولیسم گلوکز در عضلات اسـکلتی در موشهای چاق و مبتلا به مقاومت انسولین نژاد زوکر شود (7). علاوه بر مداخلات تغذیهای، تمرین ورزشی تاثیرات بارزی بر کنترل و درمان دیابت دارد. با این حال، شدت بهینه تمرین در کاهش مسیرهای التهابی و بهبود عملکرد سلولهای بتا در دیابت به روشنی مشخص نیست. در این راستا، بعضی مطالعات گزارش کرده¬اند که شدت متوسط تمرین عملکرد سلولهای بتا را بیشتر از شدت بالای تمرین بهبود میبخشد (8) در حالیکه بعضی مطالعات تفاوتی بین دو شدت تمرینی گزارش نکردند (9،10). علاوه براین، بعضی مطالعات کاهش (13-11) و بعضی مطالعات عدم تغییر (14،15) NLRP3 را در نتیجه تمرینات ورزشی گزارش کردند. بنابراین، شناسایی مکانیسمهای مولکولی حاکم بر سازگاریهای تحریکشده توسط شدتهای مختلف تمرین در بافت پانکراس میتواند برای کنترل و درمان دیابت مفید باشد. از آنجا که شواهدی زیادی مبنی بر بررسی پاسخ NLRP3 بافت پانکراس به شدتهای مختلف تمرین در دسترس نیست و با وجود نتایج متناقض در رابطه با اثر تمرین بر NLRP3، و همچنین، با توجه به نقش آنتیاکسیدانی ALA، بررسی این موضوع که آیا مصرف ALA همراه تمرین ورزشی دارای اثر همافزایی بر کنترل برخی مسیرهای التهابی سلولهای بتا در دیابت است، حایز اهمیت می باشد. بنابراین هدف از این مطالعه بررسی تأثیر شدت تمرین ورزشی به همراه مصرف مکمل آلفالیپوئیک اسید بر بیان ژن NLRP3 پانکراس موشهای دیابتی بود.
روش بررسی
این مطالعه تجربی بر روی 35 سر موش نر نژاد ویستار با سن هشت هفته در مرکز ﭘﺮورش و ﻧﮕﻬﺪاری ﺣﯿﻮاﻧﺎت آزﻣﺎیﺸﮕﺎﻫﯽ هیستوژنوتک تهران انجام شد. معیار ورود به مطالعه شامل وزن 190 تا 220 گرم و سطح گلوکز پلاسمای بالاتر از 250 میلیگرم در دسیلیتر در گروه دیابت بوده و معیارهای خروج از مطالعه شامل مرگ در اواسط مطالعه و یا بیمار شدن حیوان و اجرا نکردن دو جلسه پیاپی تمرین هر موش در گروههای تمرینی بود. موشهای مورد مطالعه به تعداد پنج عدد در هر قفس از جنس پلیکربنات (30 × 15 × 15 سانتیمتر) در یک شرایط آب و هوایی کنترل شده (دمای 2±22 سانتیگراد، رطوبت 5±50 درصد، یک سیکل شب و روز (12:12) و با رژیم غذایی استاندارد و آب مورد نیاز در شرایط آزمایشگاهی نگهداری شدند. پس از آشنایی موشها با پروتکل تمرینی، 5 موش بهصورت تصادفی به عنوان گروه سالم جدا شد و 30 موش باقیمانده دیابتی شدند و بهصورت تصادفی در شش گروه: کنترل دیابت، تمرین تناوبی شدید، تمرین تناوبی متوسط، مکمل، مکمل+ تمرین تناوبی شدید، مکمل+ تمرین تناوبی متوسط قرار گرفتند. در تمام مراحل پژوهش، آب مورد نیاز حیوان به صورت آزاد در بطری 500 میلیلیتری ویژه حیوانات آزمایشگاهی در دسترس آنها بود. در این مطالعه برای دیابتی نمودن موشها از روش استرپتوزوتوسین (Streptozotocin) استفاده شد. به این صورت که با تزریق ml/kg 50 استرپتوزوتوسین به صورت داخل صفاقی، القای دیابت صورت گرفت. به منظور اطمینان از دیابتی شدن موشها، 48 ساعت پس از تزریق قند خون اندازه گیری شد و موشهای با قند خون بالای mg/dl 250 به عنوان موشهای دیابت در نظر گرفته شدند (10). دو هفته بعد از القا دیابت، برنامه تمرینی و مکملدهی انجام شد. گروه-های تمرینی پنج جلسه در هفته، به مدت شش هفته تمرین تناوبی انجام دادند. قبل از شروع پروتکل تمرینی، آزمودنیهای گروههای تمرین به منظور آشنایی با چگونگی فعالیت توسط نوارگردان (مخصوص فعالیت بدنی حیوانات آزمایشگاهی، ساخت ایران)، در یک هفته طی پنج جلسه، به مدت پنج دقیقه با سرعت هشت تا ده متر بر دقیقه با شیب صفر فعالیت داشتند. سپس، سرعت بیشینه دویدن هنگام حداکثر اکسیژن مصرفی برای هر رت و به منظور کنترل شدت تمرین تعیین شد. برای این منظور، بعد از 10 دقیقه گرم کردن با شدت پایین، رتها شروع به دویدن کردند و سرعت نوارگردان هر دو دقیقه یک بار دو متر بر دقیقه افزایش یافت تا حیوانات دیگر قادر به دویدن نباشند و به واماندگی برسند. سرعت نهایی رت به عنوان سرعت بیشینه در زمان رسیدن به حداکثر اکسیژن مصرفی جهت محاسبه شدتهای تمرینی استفاده گردید. از حیوانات هر دو هفته یک بار آزمون واماندهساز گرفته و شدت تمرین با توجه به مقادیر جدید آزمون تعیین میشد. برنامه تمرینی تناوبی با شدت بالا و تمرین تناوبی با شدت متوسط به مدت شش هفته و پنج جلسه در هفته اجرا شد. در هر دو پروتکل تمرینی، موشها ابتدا 5 دقیقه با سرعت کم (30-40 درصد سرعت بیشینه) و با هدف گرم کردن دویدند. هر جلسه تمرینی تناوبی با شدت بالا شامل 10 ست دویدن چهار دقیقهای با شدت 90-85 درصد سرعت بیشینه و دو دقیقه استراحت فعال (50-40 درصد سرعت بیشینه) بین هر مرحله تمرین بود. پروتکل تمرین تناوبی با شدت متوسط شامل 13 ست دویدن چهار دقیقهای با شدت 65-70 درصد سرعت بیشینه و 2 دقیقه استراحت فعال (50-40 درصد سرعت بیشینه) بین ستها بود (16). به منظور مکملدهی به گروههای مکمل، روزانه ﻣﯿﺰان 20 میلیﮔـﺮم به ازای هر کیلوگرم وزن بدن موشها مکمل آلفالیپوئیک اسید لیپوزومال (مکمل آلفالیپولئیک اسید ساخت شرکت Sigma-Aldrich کشور آمریکا) در متیل سلولز حل شده و یک ساعت بعد از تمرین بهصورت گاواژ و یک وعده در روز به موشها داده شد (17). برای لیپوزوم کردن از روش آب¬پوشانی لایه نازک استفاده شد، بدین صورت که ابتدا لسیتین فسفولیپید (L-a-a-phosphatidylcholine) در کلروفرم حل شد و محلول اول به دست آمد. سپس کلسترول در کلروفرم حل شد و محلول دوم به دست آمد. در مرحله بعد، دو محلول به ترتیب با نسبت چهار به یک با هم ترکیب شدند. سپس این ترکیب در دستگاه روتاری ، در دمای 50 درجه و سرعت rmp 150 و تحت خلا تبخیر شد و با تشکیل فیلم نازک لیپیدی، تبخیر حداقل به مدت دو ساعت ادامه یافت. سپس آلفالیپولئیک اسید را در آب مقطر حل کرده و به محلول اضافه کردیم. برای هموژنایز کردن سوسپانسیون و تولید نانو وزیکولها، نمونههای بهدست آمده به مدت 15 دقیقه با همگن ساز اولتراسوند، همگن شدند. سپس سوسپانسیون هموژن شده در مجاورت نیتروژن قرار گرفت و به مدت یک ساعت تحت حرارت انتقال چربی قرار گرفت. سپس محصول تولید شده سانترفیوژ شد و درنهایت یک سوسپانسیون شفاف از نانولیپوزومها تولید شد و تا زمان استفاده در دمای 4درجه سانتیگراد نگهداری شد (18). 48 ساعت پس از آخرین جلسه تمرین، در شرایط استراحت و ناشتا موشها با تزریق درون صفاقی ترکیبی از کتامین (mg/kg 70) و زایلازین (mg/kg 5-3) بیهوش شدند. نمونه خونی مستقیماً از قلب گرفته شد و سپس، قفسه سینه حیوان شکافته شده و بافت پانکراس موشها نمونهبرداری و پس از شستشو در سرم فیزیولوژیک، در نیتروژن مایع نگهداری شد. جهت سنجش بیان ژن NLRP3 مراحل مختلف انجام شد. ابتدا استخراج RNA صورت گرفت. بدین منظور سلول¬ها و بافتهای آماده شده در شرایط کاملاً استریل و روی یخ آماده شدند. میکروتیوبهای حاوی رسوب سلولی و یا بافت لیز شده را روی یخ قرار داده و به ازای هر 1 میلیون سلول و 50 میلی گرم بافت، 300 میکرولیتر ترایزول اضافه شد. 5 تا 10 ثانیه ورتکس کرده و آن را 5 دقیقه در دمای اتاق قرار داده شد. 200 میکرولیتر کلروفرم به آن اضافه و 15 ثانیه به خوبی مخلوط گردید. میکروتیوب را به مدت 5 دقیقه برروی یخ یا دمای 4 درجه سانتیگراد قرار داده و سپس در RPM 1200 در 4 درجه سانتیگراد به مدت 15 دقیقه سانتریفوژ شد. به میکروتیوبهای حاوی مایع شفاف به اندازه برابر با آن ایزوپروپانول اضافه شده و این ترکیب را به آرامی مخلوط کرده و به مدت 15 دقیقه در دمای 4 درجه سانتیگراد ا گردید. مخلوط در RPM 12000 در 4 درجه سانتیگراد، به مدت 15 دقیقه سانتریفوژ شد. فاز رویی را به آرامی و با استفاده از سمپلر زرد دور ریخته باید دقت شود که رسوب به همراه مخلوط رویی دور ریخته نشود. ml 1 اتانول 75 درصد به رسوب اضافه و خیلی کوتاه ورتکس گردید. محلول در RPM 7500 در دمای 4 درجه سانتیگراد، به مدت 8 دقیقه سانتریفوژ شد. فاز رویی را دور ریخته و به مدت 15 دقیقه اجازه میدهیم که رسوب نیمه خشک شود. پس از نیمه خشک شدن رسوب، μl20 تا μl 30 آب DEPC و یا TE به آن اضافه میکنیم. برای حل شدن رسوب میتوان میکروتیوبها را به مدت 15 دقیقه در دمای 55 تا 60 درجه سانتیگراد قرار داد. در ادامه به بررسی کمی استخراج RNA پرداخته شد. غلظت و خلوص RNA استخراج شده توسط اسپکتروفوتومتر نانو دراپ بررسی شد. جذب نوری نمونهها در طول موج 260 و 280 نانومتر اندازهگیری شده و غلظت آن براساس ضریب رقت برحسب ng/μl به دست آمد. بعد از این مرحله سنتز Cdna انجام شد. برای ساخت cDNAبعد از اندازهگیری OD نمونهها، با استفاد فرمول N1V1=N2V2 آنها را به غلظت ng/μl 1 رسانده و برای سنتز cDNA آماده شدند.μl 10 از RNA تیمار شده با Dnase (غلظتng/μl1 ) را درون میکروتیوب 0/2 ریخته و μl 10 از محلول کیت سنتز cDNA به آن اضافه شد، سپس به مدت 5 دقیقه در دمای 25 درجه سانتیگراد و به دنبال آن 60 دقیقه در 60 درجه سانتیگراد درون ترموسایکلر قرار داده شد. میکروتیوبها روی یخ خنک شده و به منظور انجام qPCR در دمای منفی 20 درجه سانتیگراد ذخیره شدند. برای طراحی پرایمرها در تکنیک Real-Time PCR به روش SYBER Green I در این مطالعه، پرایمرها پس از طراحی در نرمافزار آنلاین Primer3، در صفحه Primer BLAST بررسی شدند. جدول1 توالی پرایمرها را نشان میدهد. برای اندازهگیری گلوگز و انسولین پلاسما، بعد از بیهوش کردن موشها، نمونه خونی مستقیما از قلب جمع¬آوری و به لوله آزمایش حاوی EDTA منتقل شد. نمونه¬های بهدست آمده به سرعت به مدت 15 دقیقه و با سرعت 3000 دور در دقیقه سانتریفیوژ گردید و پلاسمای بهدست آمده در دمای 80- سانتیگراد نگهداری شد. سنجش گلوکز پلاسما به روش گلوکزاکسیداز و بهوسیله کیت تشخیص کمی گلوکز پلاسما شرکت پارس آزمون با حساسیت 5 میلیگرم در دسیلیتر انجام شد. انسولین سرم به روش الایزا و مطابق با استانداردهای کیت تجاری (ELIZA Diagnostic insulin Demeditec) ساخت کشور آلمان اندازه¬گیری شد.
تجزیه و تحلیل آماری
جهت بررسی طبیعی بودن توزیع دادهها از آزمون شاپیرو-ویلک وهمگنی واریانس گروهها از آزمون لون استفاده شد. ﺑﻪ ﻣﻨﻈﻮر ﺑﺮرﺳﯽ ﺗﻔﺎوتﻫﺎ از آزﻣﻮن ﺗﺤﻠﯿﻞ واریﺎﻧﺲ یﮏ ﻃﺮﻓﻪ و از آزﻣﻮن ﺗﻌﻘﯿﺒﯽ ﺗﻮﮐﯽ اﺳﺘﻔﺎده ﺷﺪ. ﺳﻄﺢ ﻣﻌﻨﯽداری 0/05 در نظر گرفته شد. تمامی عملیات آماری با نرمافزارversion 16 SPSS انجام گرفت.
ملاحظات اخلاقی
این مطالعه کلیه قوانین و مقررات بینالمللی کار با حیوانات آزمایشگاهی را رعایت و توسط کمیته اخلاق کار با حیوانات دانشکده تایید و کد اخلاق (IR.IAU.SARI.REC.1399.157) برای آن صادر گردید.
جدول 1: توالی پرایمرهای مورد استفاده

نتایج
نتایج مطالعه حاضر نشان داد که گلوگز پلاسما در تمام گروه¬ها به جز گروه دیابت+تمرین شدید+مکمل افزایش معنیداری نسبت به گروه کنترل سالم داشت (P=0/148) در مقایسه با گروه دیابت، تمرین متوسط(P=0/023) و همچنین ترکیب تمرین متوسط+مکمل(P=0/013) و تمرین شدید+مکمل(P=0/001) منجر به کاهش معنادار گلوگز شد. میزان انسولین در تمام گروه¬ها بهجز گروه دیابت+تمرین شدید+ مکمل کاهش معنیداری نسبت به گروه کنترل سالم داشت (P=0/089). در مقایسه با گروه دیابت، تمرین متوسط(P=0/0021) و تمرین متوسط+مکمل (P=0/018) و تمرین شدید+مکمل (P=0/001) منجر به افزایش معنادار انسولین شد (جدول 2). نتایج آزمون تحلیل واریانس یکراهه برای بیان ژن NLRP3 در جدول 3 نشان میدهد که بین گروه¬های مختلف در میزان بیان ژن نسبی NLRP3 تفاوت معناداری وجود دارد (P=0/0001). نتایج آزمون تعقیبی توکی نیز نشان داد که در گروه دیابت (P=0/0001)، دیابتی مکمل (P=0/001)و دیابتی تمرین متوسط (P=0/006) نسبت به گروه کنترل سالم افزایش معناداری در میزان بیان ژن نسبی NLRP3 مشاهده شد. این درحالی است که در گروه¬های مکمل(P=0/021) ، تمرین شدید(P=0/001) ، تمرین متوسط (P=0/009) ، تمرین متوسط+مکمل(P=0/003) و تمرین شدید+مکمل (P=0/0001) نسبت به گروه دیابت کاهش معناداری در میزان بیان ژن نسبی NLRP3 مشاهده شد. نکته جالب توجه در نتایج مشاهده این بود که بین تمرین شدید+مکمل (P=0/103) و تمرین متوسط+مکمل (P=0/089) نسبت به گروه سالم تفاوت معنی داری مشاهده نشد (نمودار 1).
جدول 2: مقایسه (انحراف معیار± میانگین) گلوگز و انسولین پلاسما در گروه سالم و گروههای دیابتی تحت تاثیر تمرین و مکمل
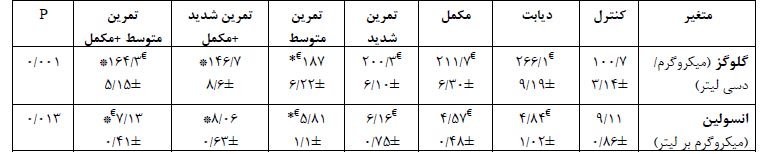
جهت مقایسه از آزمون تحلیل واریانس یکراهه استفاده شد.
* تفاوت معنیدار با دیابت، € تفاوت معنیدار با سالم
جدول 3: نتایج آزمون تحلیل واریانس یکراهه برای بیان ژن NLRP3
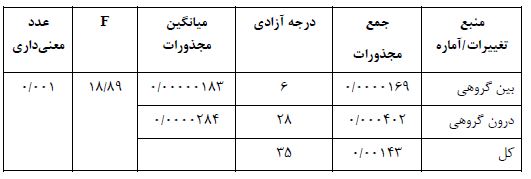
وجود تفاوت معنادار (05/0>p) بین گروه های تحقیق
.jpg)
نمودار 1: مقایسه میانگین و انحراف معیار با استفاده از آزمون توکی برای بیان ژن نسبی NLRP3 mRNA گروههای تحقیق.
a: تغییرات معنادار نسبت به گروه کنترل. b: تعییرات معنادار نسبت به گروه دیابت
بحث
یافتههای پژوهش حاضر نشان داد که دیابت نوع دو سبب افزایش قابل توجه گلوکز پلاسما شد که با افزایش بیان ژن NLRP3 بافت پانکراس نسبت به گروه کنترل سالم همراه بود. همسو با این پژوهش، Carlos و همکاران (2017) نشان دادند القای دیابت با استرپتوزوتوسین در موش ها سبب افزایش بیان ژن NLRP3 می¬گردد (19). Kim و همکاران (2016) گزارش کردند که افزایش بیان ژن NLRP3 پیشرفت دیابت را تسهیل می¬کند (20). مطالعات متعددی نشان دادند سرکوب ژنNLRP3 منجر به بهبود تحمل به گلوکز و حساسیت به انسولین و همچنین کاهش سطوح سایتوکین های التهابی سرم و بافتهای متابولیکی و از طرفی افزایش فعالیت مسیر سیگنالینگ PI3K-AKT انسولین موشهای چاق دیابتی میشود (21). از طرفی، عباسی و همکاران (2018) ارتباط مستقیمی بین اینفلامازومNLRP3 ، التهاب مزمن و مقاومت به انسولین را نشان دادند (12). فعالسازی اینفلامازوم NLRP3 در دیابت نوع دو منجر به تولید IL-1β و IL-18 می¬شود که باعث مقاومت به انسولین و اختلالات متابولیکی در بافت¬هایی از قبیل پانکراس می¬شود (12). مطابق با نتایج بدست آمده، هر دو نوع تمرین تناوبی با شدت متوسط و بالا باعث کاهش معنی¬دار بیان اینفلامازوم NLRP3 بافت پانکراس و همچنین کاهش گلوگز در مقایسه با گروه دیابتی شد بهطوریکه تمرین با شدت بالا منجر به کاهش بیشتر این ژن شد. این نتایج با کاهش سطح گلوگز در گروههای تمرینی در مقایسه با گروه دیابت همراه بود. مطالعات نشان داده¬اند که بلاک ژنهای NLRP3 و کاسپاز-1 منجر به بهبود تحمل به گلوکز و حساسیت به انسولین و همچنین کاهش سطوح سایتوکینهای التهابی سرم و بافتهای متابولیکی در موشهای در معرض رژیمهای پر چرب قرار گرفته میشود (22). علاوه براین، عواملی از قبیل هیپرگلیسمی، عدم تعادل ردوکس و عدم تعادل کلسیمی منجر به القاء استرس¬های شبکه آندوپلاسمی میشوند. استرسهای شبکه سارکوپلاسمی از طریق مسیرهای سیگنالینگ IRE-NF-kB ،CHOP و IRE-TRF2-ASK1 منجر به القاء اثرات التهابی و آپوپتوزی میشود. تنظیم منفی بیان فاکتورهای ذکر شده بهوسیله فعالیت ورزشی منجر به کاهش عوامل التهابی از قبیل اینفلامازوم NLRP3،1β-IL ، کاسپاز-1، پروتئینهای تعاملی تیورودوکسین، گونههای اکسیژنی فعال و دیگر عوامل القاء کننده التهاب می¬شود (23). بنابراین ممکن است کاهش سطح گلوگز بعد از هشت هفته تمرین منجر به کاهش بیان NLRP3 بافت پانکراس شده باشد. در تایید این نتایج، عباسی و همکاران (2018) نشان دادند که فعالیت ورزشی استقامتی با شدت متوسط و بالا باعث کاهش معنیدار بیان اینفلامازوم NLRP3 بافت چربی احشایی و کاهش سطوح گلوگز سرمی در مقایسه با گروه دیابتی شده است. نتایج تحقیق حاضر با نتایج تحقیقات Kim و همکاران (24)، Mardare و همکاران (25) وPea و همکاران (26) همخوانی دارد. Kim و همکاران (2019) گزارش کردند که 16 هفته تمرین هوازی با شدت متوسط (دویدن روی تردمیل با سرعت 10 تا 14 متر در دقیقه) و بالا (دویدن روی تردمیل با سرعت 14 تا 18 متر در دقیقه) منجر به کاهش بیان ژن NLRP3 بافت چربی موشهای چاق شد (24).Mardare و همکاران (2016) کاهش سطوح NLRP3 mRNA بافت چربی موشهای چاق را به دنبال 10 هفته تمرینات هوازی و مقاومتی گزارش کردند. در این مطالعه تمرین هوازی شامل دویدن روی تردمیل با شدت 80 درصد حداکثر اکسیژن مصرفی و تمرین مقاومتی شامل سه ست سه دقیقه¬ای انقباض ایزومتریک بود (25). کاهش بیان اینفلامازوم NLRP3 در افراد سالمند به دنبال هشت هفته تمرینات مقاومتی فزاینده در مطالعهPeña و همکاران (2017) گزارش شد (26). عباسی و همکاران (2018) نشان دادند که هشت هفته تمرین هوازی با شدت متوسط (سرعت 16-14 متر در دقیقه) و بالا (سرعت 22-20 متر در دقیقه) منجر به کاهش سطوح NLRP3 mRNA بافت چربی موشهای دیابتی شد ولی تمرین با شدت پایین (سرعت 8-5 متر در دقیقه) اثری بر آن نداشت (12). در مقابل،Zaidi و همکاران (2019) نتیجه گرفتند که 12 هفته تمرین هوازی اثری بر بیان ژن NLRP3 بافت چربی بیماران دیابتی نداشت (14). زارع و همکاران (2020) گزارش کردند که هشت هفته تمرین استقامتی با شدت 80 درصد حداکثر اکسیژن مصرفی اوج اثری بر NLRP3 موشهای چاق نداشت (15). تفاوت در نتایج مطالعات ذکر شده ممکن است به دلیل تفاوت در نمونه تحقیق، پروتکل تمرینی، آزمودنیها و بافت مورد هدف و روش اندازهگیری NLRP3 باشد. در مطالعهZaidi و همکاران (14) آزمودنیها بیماران مبتلا به بیماری شریان کرونری و دیابت بودند و بیان ژن NLRP3 در بافت چربی و لکوسیتهای در گردش اندازه گیری شد. پروتکل تمرینی سه جلسه در هفته و با شدت متوسط انجام شد که شامل دو جلسه فعایت هوازی و یک جلسه فعالیت مقاومتی بود. دو سوم تمرینات بهصورت گروهی و یک سوم تمرینات را هر آزمودنی در منزل اجرا کرد. با توجه به عدم تغییر وزن بدن بعد از تمرین، به نظر میرسد که شدت تمرین به اندازه کافی نبوده که بر سطوح NLRP3 بافت چربی اثرگذار باشد. در مطالعه زارع و همکاران (15)، موشها چاق و غیردیابتی بودند و NLRP3 به روش الایزا اندازهگیری شد. پروتکل تمرینی به مدت هشت هفته و با شدت 80 درصد اکسیژن مصرفی اوج بهصورت دویدن روی تردمیل اجرا شد. با توجه به اینکه در این مطالعه تمرین منجر به کاهش IL-1 شد، اگر اندازهگیری NLRP3 با بیان ژن یا پروتئین انجام میشد ممکن بود نتایج متفاوتی حاصل شود. تشکیل کمپلکس اینفلامازوم NLRP3 سیتوزولیک در دو مرحله انجام می¬شود: گام اول القاء نسخهبرداری اجزای اینفلامازوم از قبیل NLRP3 ، Pro IL-1β و Pro IL-18 از طریق فعالسازی سیگنالینگ NFkB وساطت شده بهوسیله گیرندههای شبه گذرگاهی (TLRs) است. در گام دوم، الیگومریزاسیون هموتیپیک NLRPها افزایش پیدا میکند و موجب شکلگیری اینفلامازوم فعال میشود که قابلیت تبدیل شکلهای نابالغ IL-1β و IL-18به شکلهای بالغ آن را دارد (27). مشخص نیست که اثرات مهاری تمرینات ورزشی بر فعال سازی اینفلامازوم NLRP3 در کدام یک از مراحل تشکیل این کمپلکس انجام میشود. نشان داده شده است تمرینات ورزشی از طریق کاهش فسفوریلاسیون IKKβ منجر به کاهش فعالسازی TLRs در بافتهای مختلف میشود (28). بنابراین، تمرین ممکن است مسیر اینفلامازوم NLRP3 را درگام اول مهار کند. همچنین گزارش شده است، تمرین گام اولیه فعالسازی اینفلامازوم NLRP3 در موشهای چاق را از طریق کاهش استرسهای شبکه آندوپلاسمی را مهار میکند (29). علاوه براین، محققین نشان دادند عملکرد و محتوای میتوکندریایی سلولهای بتا در بیماران مبتلا به دیابت کاهش پیدا میکند. گزارش شد تخریب میتوکندریایی یکی از علل فعال سازی اینفلامازومNLRP3 است. میتوفاژی از طریق حذف میتوکندری های آسیب دیده موجب بهبود هموستاز سلول میشود و به جلوگیری از افزایش التهاب ناشی از فعالسازی اینفلامازوم NLRP3 منجر میشود (30). مطالعات نشان دادند فعالیتهای ورزشی موجب افزایش چگالی و بهبود عملکرد میتوکندریایی سلولهای بتا پانکراس در افراد دیابتی میشود (31). میتوکندری نقش ممهی در تنظیم آپوپتوز سلولهای بتا ایفا میکند و استرس اکسایشی نیز به عنوان یک آغازگر مهم آپوپتوز در سلول های بتا میباشد (32). چندین سازوکار برای اثرات محافظتی تمرین های ورزشی روی آپوپتوز عضله مطرح شده است که شامل تغییر مستقیم در بیان پروتئنیهای مربوط به آپوپتوز، کاهش آزادسازی عوامل آپوپتوژنیک میتوکندری و تغییرات تولید گونه¬های فعال اکسیژن و وضعیت ضداکسایشی می¬باشد (31). به نظر میرسد در اثر تمرین ورزشی عملکـرد میتوکندریهای سلولهای بتا بهبود یافته و این عامل منجر به افزایش مقادیر عاملهای مهاری و کاهش عوامل تحریکی آپوپتوز شده باشد. این موضوع منجر به تحکیم دیواره میتوکندری، جلوگیری از رهاسازی سیتوکروم c، تنظیم کلسیم رها شده از سارکوپلاسمیک و کـاهش اثـرگونه¬های فعال اکسیژن ناشی از فعالیـت ورزشی، ایمنی سلول بتا را بالا میبرد و از آپوپتوز ناشی از استرس جلوگیری میکند. نتایج مطالعه حاضر نشان داد که مکمل ALA اثر همافزایی بر تمرین دارد و مصرف آن به همراه تمرین منجر به کاهش بیشتر NLRP3 بافت پانکراس و سطوح گلوکز پلاسما نسبت به مکمل یا تمرین به تنهایی شد. به نظرمی-رسد تمرین هوازی با شدت متوسط و بالا توانسته از طریق مکانیسم های سلولی وابسته به فعالیت ورزشی باعث کاهش سطح گلوکز در گروههای تمرینی شده باشد. فعالیت ورزشی باعث میشود GLUT-4 از جایگاههای ذخیرهای درون سلولی خود به جایگاههای غشاء پالسمایی و مجاری عرضی سارکولمایی نقل مکان کند (33). انتقال گلوکز با سیگنالهایی تنظیم میشود که با دوگانه تحریک انقباض ارتباط دارند. مهمترین این سیگنال¬ها افزایش کلسیم شبکه سارکوپلاسمی است. این احتمال وجود دارد که کلسیم رها شده در حین انقباض بهطور مستقیم با پروتئینهای SNARE که در انتقال وزیکول های GLUT-4 به سارکولما درگیرند وارد تعامل شوند. به علاوه، کلسیم از مسیرهای پیامرسانی حساس به کلسیم از قبیل ایزوفرم سنتی پروتئین کیناز C و کیناز وابسته به کلسیم یا کالمودولین عمل می¬کنند (34). در مجموع به نظر می¬رسد این نتایج، فعال شدن پروتئین کینازC در انتقال گلوکز عضلانی ناشی از تحریک انقباضی را نشان میدهند. با توجه به اینکه دیابت با افزایش فشار اکسایشی و آپوپتوز سلولهای بتا همراه است (35)، به نظر می رسد که ALA با ویژگیهای آنتیاکسیدانی خود اثرات تمرین ورزشی را تقویت میکند. در این رابطه، مطالعهUchendu و همکاران (2018) نشان داد که ALA منجر به افزایش سوپراکسید دسموتاز و کاتالاز و کاهش مالوندیآلدهید بافت پانکراس موشهای دیابتی شد، که عملکرد آنتیاکسیدانی ALA و توانایی آن در مهار فعالیت رادیکالهای آزاد و بهبود حالت ردوکس را تأیید میکند (36). نشان داده است که فعالسازی مسیر سیگنالینگ آدنوزین منوفسفات حلقوی (cAMP) بوسیله ALA افزایش می¬یابد که این موضوع منجر به افزایش بیان پروتئینهای آنتیآپوپتوزی BCL-2 و BCL-X1 و مهار فعالسازی کاسپازها می¬شود (37). مطالعات نشان دادهاند در افراد مبتلا به دیابت سطح ALA کاهش مییابد (38). چندین مطالعه هم خاصیت آنتیاکسیدانی، ضد التهابی و کاهش قند خون ALA را نشان داده است (40،39). یافته-های مطالعات حاکی از آن هستند که ALA عمل انسولین را از طریق اثر بر مسیر سیگنالینگ انسولین تقلید میکند. این اثر تحریکی با فعال کردن فسفاتیدیل اینوزیتول 3-کیناز (PI3-K) و فعالسازی /Aktپروتئین کیناز B در ارتباط است (41). همچنین درمان طولانی مدت با ALA اکسیداسیون گلوکز و هم تولید گلیکوژن را افزایش میدهد. علاوه براین، تحریک فسفریلاسیون تیروزین در گیرنده انسولین از دیگر نقش¬های اسید لیپوئیک میباشد و میتواند به عنوان یک عامل موثر در بهبود متابولیسم گلوکز و کاهش سطح آن در بیماران دیابتی نوع 2 عمل کند. در تایید این مطلب در مقالات دیگری نیز مطرح شده که استفاده ازALA چه در یک دوره کوتاهمدت و چه طولانیمدت، سبب بهبود مصرف گلوکز در بیماران دیابتی نوع 2 گردیده است (42). EL Midaoui و همکاران در مطالعه خود نشان دادند که رژیم غذایی حاوی ALA در موشهایی که به آنها گلوکز خورانده شده بود، باعث کاهش معنیدار سطح گلوکز و همچنین جلوگیری از ایجاد مقاوت به انسولین از طریق فعالسازی روندهای آنتیاکسیدانی میشود (43). بر اساس نتایج مطالعه Peth و همکاران، لیپوئیک اسید می¬تواند باعث بهبود متابولیسم گلوکز در عضلات اسکلتی و کل بدن در موشهای چاق Zucker مبتلا به مقاومت به شود (44). در مجموع درباره اثر تمرین و مکمل ALA بر میزان NLRP3 در آزمودنی¬های دیابتی مطالعات محدودی انجام شده است. از محدودیتهای تحقیق حاضر می¬توان به عدم اندازهگیری فاکتورهای مرتبط با آپوپتوز در سلولهای بتا اشاره کرد. همچنین، اندازه¬گیری شاخصهای استرس اکسیداتیو در تبیین و تفسـیر بهتر نتایج کمک نماید که در مطالعه حاضر بررسی نشد.
نتیجهگیری
با توجه به یافتههای تحقیق حاضر، به نظر میرسد دیابت با افزایش بیان ژن NLRP3 در بافت پانکراس همراه است و تمرین تناوبی شدید و متوسط به همراه مصرف مکمل آلفالیپوئیک اسید میتواند با کاهش سطوح گلوگز خون و ماومت به انسولین احتمالا باعث کاهش میزان NLRP3 بافت پانکراس و التهاب ناشی از مسیر سیگنالینگ NLRP3 را کاهش و کنترل کند. با وجود این، با توجه به مطالعات اندک انجام شده در این رابطه، درک اثرات فعالیت ورزشی بر فاکتورهای درگیر در التهاب ناشی از بیماری دیابت نیاز به پژوهشهای بیشتری دارد.
سپاسگزاری
این مقاله مستخرج از رساله دکتری دانشگاه آزاد اسلامی واحد ساری است. بدین وسیله نویسندگان از کلیه کسانی که در انجام این پژوهش یاری رساندند تشکر و قدردانی می-نمایند.
حامی مالی: ندارد.
تعارض در منافع: وجود ندارند.
التهاب مزمن یک عامل کلیدی در ایجاد دیابت است به طوریکه سطح بالاتری از پروتئینهای التهابی مانند اینترلوکین یک بتا (IL-1β) و اینترلوکین شش (IL-6) و پروتئین واکنش پذیر C پیشبینی کننده دیابت هستند (1). مطالعات نشان از آن دارند که سلولهای ایمنی میتوانند با بهکارگیری گیرندههای NLRs (نوعی از گیرندههای تشخیص الگو) الگوهای مولکولی مرتبط با پاتوژن و مرتبط با خطر را شناسایی و به القا پاسخهای التهابی منجر شوند. فعالسازی NLRs منجر به تعامل انفلامازوم NLRP3 با پروتئین تعدیل-کننده ASC میشود. این عمل منجر به فعالسازی پروکاسپاز-1 و تولید کاسپاز-1 میشود که تولید و ترشح IL-1β و IL-18 را به دنبال دارد (2). مطالعات نشان دادهاند فعال شدنNLRP3 یکی از مکانیسمهای کلیدی در مقاومت به انسولین است (3). یکی از مکانیسمهای احتمالی نقش اینفلامازوم در روند دیابت نوع دو این گونه است که اینفلامازومNLRP3 سیگنالهای خطر ایجاد شده در دیابت نوع 2 از جمله پلیپپتیدآمیلوئید جزیرهای،ATP (adenosine triphosphate) خارج سلولی و گونههای فعال اکسیژن را شناسایی کند (4). در افراد دیابتی افزایش تولید رادیکالهای آزاد و کاهش آنتی اکسیدانها باعث استرس اکسایشی میشود که این موضوع منجر به اثرات مخرب متعددی در دیابت میگردد. لذا مصرف آنتیاکسیدانها میتواند نقش بسزایی داشته باشد. مکمل آلفالیپوئیک اسید (ALA) یک آنتیاکسیدان قوی است و به عنوان کوفاکتور در کمپلکس آنزیمی دهیدروژناز میتوکندریایی در متابولیسم فعالیت دارد (5). این ماده از یک طرف میتواند بهطور مستقیم رادیکالهای پروکسیل تولید شده را از بین برده، از طرف دیگر با احیای آسکوربیل و کرومانوکسیل موجب افزایش قدرت سایر آنتیاکسیدانها گردد (5). تحقیقات نشان میدهد ALA با افزایش فسفریلاسیون تیروزین در سوبسترای 1 گیرنده انسولین و به دنبال آن، فعالسازی فسفاتیدیل اینوزیتول 3-کیناز، سرعت جابجایی انتقال دهندههای گلوکز به غشای پلاسمایی را رهبری میکند (6). ازطرف دیگر، در یک مطالعه مشخص گردید ALA می¬تواند باعث بهبود متابولیسم گلوکز در عضلات اسـکلتی در موشهای چاق و مبتلا به مقاومت انسولین نژاد زوکر شود (7). علاوه بر مداخلات تغذیهای، تمرین ورزشی تاثیرات بارزی بر کنترل و درمان دیابت دارد. با این حال، شدت بهینه تمرین در کاهش مسیرهای التهابی و بهبود عملکرد سلولهای بتا در دیابت به روشنی مشخص نیست. در این راستا، بعضی مطالعات گزارش کرده¬اند که شدت متوسط تمرین عملکرد سلولهای بتا را بیشتر از شدت بالای تمرین بهبود میبخشد (8) در حالیکه بعضی مطالعات تفاوتی بین دو شدت تمرینی گزارش نکردند (9،10). علاوه براین، بعضی مطالعات کاهش (13-11) و بعضی مطالعات عدم تغییر (14،15) NLRP3 را در نتیجه تمرینات ورزشی گزارش کردند. بنابراین، شناسایی مکانیسمهای مولکولی حاکم بر سازگاریهای تحریکشده توسط شدتهای مختلف تمرین در بافت پانکراس میتواند برای کنترل و درمان دیابت مفید باشد. از آنجا که شواهدی زیادی مبنی بر بررسی پاسخ NLRP3 بافت پانکراس به شدتهای مختلف تمرین در دسترس نیست و با وجود نتایج متناقض در رابطه با اثر تمرین بر NLRP3، و همچنین، با توجه به نقش آنتیاکسیدانی ALA، بررسی این موضوع که آیا مصرف ALA همراه تمرین ورزشی دارای اثر همافزایی بر کنترل برخی مسیرهای التهابی سلولهای بتا در دیابت است، حایز اهمیت می باشد. بنابراین هدف از این مطالعه بررسی تأثیر شدت تمرین ورزشی به همراه مصرف مکمل آلفالیپوئیک اسید بر بیان ژن NLRP3 پانکراس موشهای دیابتی بود.
روش بررسی
این مطالعه تجربی بر روی 35 سر موش نر نژاد ویستار با سن هشت هفته در مرکز ﭘﺮورش و ﻧﮕﻬﺪاری ﺣﯿﻮاﻧﺎت آزﻣﺎیﺸﮕﺎﻫﯽ هیستوژنوتک تهران انجام شد. معیار ورود به مطالعه شامل وزن 190 تا 220 گرم و سطح گلوکز پلاسمای بالاتر از 250 میلیگرم در دسیلیتر در گروه دیابت بوده و معیارهای خروج از مطالعه شامل مرگ در اواسط مطالعه و یا بیمار شدن حیوان و اجرا نکردن دو جلسه پیاپی تمرین هر موش در گروههای تمرینی بود. موشهای مورد مطالعه به تعداد پنج عدد در هر قفس از جنس پلیکربنات (30 × 15 × 15 سانتیمتر) در یک شرایط آب و هوایی کنترل شده (دمای 2±22 سانتیگراد، رطوبت 5±50 درصد، یک سیکل شب و روز (12:12) و با رژیم غذایی استاندارد و آب مورد نیاز در شرایط آزمایشگاهی نگهداری شدند. پس از آشنایی موشها با پروتکل تمرینی، 5 موش بهصورت تصادفی به عنوان گروه سالم جدا شد و 30 موش باقیمانده دیابتی شدند و بهصورت تصادفی در شش گروه: کنترل دیابت، تمرین تناوبی شدید، تمرین تناوبی متوسط، مکمل، مکمل+ تمرین تناوبی شدید، مکمل+ تمرین تناوبی متوسط قرار گرفتند. در تمام مراحل پژوهش، آب مورد نیاز حیوان به صورت آزاد در بطری 500 میلیلیتری ویژه حیوانات آزمایشگاهی در دسترس آنها بود. در این مطالعه برای دیابتی نمودن موشها از روش استرپتوزوتوسین (Streptozotocin) استفاده شد. به این صورت که با تزریق ml/kg 50 استرپتوزوتوسین به صورت داخل صفاقی، القای دیابت صورت گرفت. به منظور اطمینان از دیابتی شدن موشها، 48 ساعت پس از تزریق قند خون اندازه گیری شد و موشهای با قند خون بالای mg/dl 250 به عنوان موشهای دیابت در نظر گرفته شدند (10). دو هفته بعد از القا دیابت، برنامه تمرینی و مکملدهی انجام شد. گروه-های تمرینی پنج جلسه در هفته، به مدت شش هفته تمرین تناوبی انجام دادند. قبل از شروع پروتکل تمرینی، آزمودنیهای گروههای تمرین به منظور آشنایی با چگونگی فعالیت توسط نوارگردان (مخصوص فعالیت بدنی حیوانات آزمایشگاهی، ساخت ایران)، در یک هفته طی پنج جلسه، به مدت پنج دقیقه با سرعت هشت تا ده متر بر دقیقه با شیب صفر فعالیت داشتند. سپس، سرعت بیشینه دویدن هنگام حداکثر اکسیژن مصرفی برای هر رت و به منظور کنترل شدت تمرین تعیین شد. برای این منظور، بعد از 10 دقیقه گرم کردن با شدت پایین، رتها شروع به دویدن کردند و سرعت نوارگردان هر دو دقیقه یک بار دو متر بر دقیقه افزایش یافت تا حیوانات دیگر قادر به دویدن نباشند و به واماندگی برسند. سرعت نهایی رت به عنوان سرعت بیشینه در زمان رسیدن به حداکثر اکسیژن مصرفی جهت محاسبه شدتهای تمرینی استفاده گردید. از حیوانات هر دو هفته یک بار آزمون واماندهساز گرفته و شدت تمرین با توجه به مقادیر جدید آزمون تعیین میشد. برنامه تمرینی تناوبی با شدت بالا و تمرین تناوبی با شدت متوسط به مدت شش هفته و پنج جلسه در هفته اجرا شد. در هر دو پروتکل تمرینی، موشها ابتدا 5 دقیقه با سرعت کم (30-40 درصد سرعت بیشینه) و با هدف گرم کردن دویدند. هر جلسه تمرینی تناوبی با شدت بالا شامل 10 ست دویدن چهار دقیقهای با شدت 90-85 درصد سرعت بیشینه و دو دقیقه استراحت فعال (50-40 درصد سرعت بیشینه) بین هر مرحله تمرین بود. پروتکل تمرین تناوبی با شدت متوسط شامل 13 ست دویدن چهار دقیقهای با شدت 65-70 درصد سرعت بیشینه و 2 دقیقه استراحت فعال (50-40 درصد سرعت بیشینه) بین ستها بود (16). به منظور مکملدهی به گروههای مکمل، روزانه ﻣﯿﺰان 20 میلیﮔـﺮم به ازای هر کیلوگرم وزن بدن موشها مکمل آلفالیپوئیک اسید لیپوزومال (مکمل آلفالیپولئیک اسید ساخت شرکت Sigma-Aldrich کشور آمریکا) در متیل سلولز حل شده و یک ساعت بعد از تمرین بهصورت گاواژ و یک وعده در روز به موشها داده شد (17). برای لیپوزوم کردن از روش آب¬پوشانی لایه نازک استفاده شد، بدین صورت که ابتدا لسیتین فسفولیپید (L-a-a-phosphatidylcholine) در کلروفرم حل شد و محلول اول به دست آمد. سپس کلسترول در کلروفرم حل شد و محلول دوم به دست آمد. در مرحله بعد، دو محلول به ترتیب با نسبت چهار به یک با هم ترکیب شدند. سپس این ترکیب در دستگاه روتاری ، در دمای 50 درجه و سرعت rmp 150 و تحت خلا تبخیر شد و با تشکیل فیلم نازک لیپیدی، تبخیر حداقل به مدت دو ساعت ادامه یافت. سپس آلفالیپولئیک اسید را در آب مقطر حل کرده و به محلول اضافه کردیم. برای هموژنایز کردن سوسپانسیون و تولید نانو وزیکولها، نمونههای بهدست آمده به مدت 15 دقیقه با همگن ساز اولتراسوند، همگن شدند. سپس سوسپانسیون هموژن شده در مجاورت نیتروژن قرار گرفت و به مدت یک ساعت تحت حرارت انتقال چربی قرار گرفت. سپس محصول تولید شده سانترفیوژ شد و درنهایت یک سوسپانسیون شفاف از نانولیپوزومها تولید شد و تا زمان استفاده در دمای 4درجه سانتیگراد نگهداری شد (18). 48 ساعت پس از آخرین جلسه تمرین، در شرایط استراحت و ناشتا موشها با تزریق درون صفاقی ترکیبی از کتامین (mg/kg 70) و زایلازین (mg/kg 5-3) بیهوش شدند. نمونه خونی مستقیماً از قلب گرفته شد و سپس، قفسه سینه حیوان شکافته شده و بافت پانکراس موشها نمونهبرداری و پس از شستشو در سرم فیزیولوژیک، در نیتروژن مایع نگهداری شد. جهت سنجش بیان ژن NLRP3 مراحل مختلف انجام شد. ابتدا استخراج RNA صورت گرفت. بدین منظور سلول¬ها و بافتهای آماده شده در شرایط کاملاً استریل و روی یخ آماده شدند. میکروتیوبهای حاوی رسوب سلولی و یا بافت لیز شده را روی یخ قرار داده و به ازای هر 1 میلیون سلول و 50 میلی گرم بافت، 300 میکرولیتر ترایزول اضافه شد. 5 تا 10 ثانیه ورتکس کرده و آن را 5 دقیقه در دمای اتاق قرار داده شد. 200 میکرولیتر کلروفرم به آن اضافه و 15 ثانیه به خوبی مخلوط گردید. میکروتیوب را به مدت 5 دقیقه برروی یخ یا دمای 4 درجه سانتیگراد قرار داده و سپس در RPM 1200 در 4 درجه سانتیگراد به مدت 15 دقیقه سانتریفوژ شد. به میکروتیوبهای حاوی مایع شفاف به اندازه برابر با آن ایزوپروپانول اضافه شده و این ترکیب را به آرامی مخلوط کرده و به مدت 15 دقیقه در دمای 4 درجه سانتیگراد ا گردید. مخلوط در RPM 12000 در 4 درجه سانتیگراد، به مدت 15 دقیقه سانتریفوژ شد. فاز رویی را به آرامی و با استفاده از سمپلر زرد دور ریخته باید دقت شود که رسوب به همراه مخلوط رویی دور ریخته نشود. ml 1 اتانول 75 درصد به رسوب اضافه و خیلی کوتاه ورتکس گردید. محلول در RPM 7500 در دمای 4 درجه سانتیگراد، به مدت 8 دقیقه سانتریفوژ شد. فاز رویی را دور ریخته و به مدت 15 دقیقه اجازه میدهیم که رسوب نیمه خشک شود. پس از نیمه خشک شدن رسوب، μl20 تا μl 30 آب DEPC و یا TE به آن اضافه میکنیم. برای حل شدن رسوب میتوان میکروتیوبها را به مدت 15 دقیقه در دمای 55 تا 60 درجه سانتیگراد قرار داد. در ادامه به بررسی کمی استخراج RNA پرداخته شد. غلظت و خلوص RNA استخراج شده توسط اسپکتروفوتومتر نانو دراپ بررسی شد. جذب نوری نمونهها در طول موج 260 و 280 نانومتر اندازهگیری شده و غلظت آن براساس ضریب رقت برحسب ng/μl به دست آمد. بعد از این مرحله سنتز Cdna انجام شد. برای ساخت cDNAبعد از اندازهگیری OD نمونهها، با استفاد فرمول N1V1=N2V2 آنها را به غلظت ng/μl 1 رسانده و برای سنتز cDNA آماده شدند.μl 10 از RNA تیمار شده با Dnase (غلظتng/μl1 ) را درون میکروتیوب 0/2 ریخته و μl 10 از محلول کیت سنتز cDNA به آن اضافه شد، سپس به مدت 5 دقیقه در دمای 25 درجه سانتیگراد و به دنبال آن 60 دقیقه در 60 درجه سانتیگراد درون ترموسایکلر قرار داده شد. میکروتیوبها روی یخ خنک شده و به منظور انجام qPCR در دمای منفی 20 درجه سانتیگراد ذخیره شدند. برای طراحی پرایمرها در تکنیک Real-Time PCR به روش SYBER Green I در این مطالعه، پرایمرها پس از طراحی در نرمافزار آنلاین Primer3، در صفحه Primer BLAST بررسی شدند. جدول1 توالی پرایمرها را نشان میدهد. برای اندازهگیری گلوگز و انسولین پلاسما، بعد از بیهوش کردن موشها، نمونه خونی مستقیما از قلب جمع¬آوری و به لوله آزمایش حاوی EDTA منتقل شد. نمونه¬های بهدست آمده به سرعت به مدت 15 دقیقه و با سرعت 3000 دور در دقیقه سانتریفیوژ گردید و پلاسمای بهدست آمده در دمای 80- سانتیگراد نگهداری شد. سنجش گلوکز پلاسما به روش گلوکزاکسیداز و بهوسیله کیت تشخیص کمی گلوکز پلاسما شرکت پارس آزمون با حساسیت 5 میلیگرم در دسیلیتر انجام شد. انسولین سرم به روش الایزا و مطابق با استانداردهای کیت تجاری (ELIZA Diagnostic insulin Demeditec) ساخت کشور آلمان اندازه¬گیری شد.
تجزیه و تحلیل آماری
جهت بررسی طبیعی بودن توزیع دادهها از آزمون شاپیرو-ویلک وهمگنی واریانس گروهها از آزمون لون استفاده شد. ﺑﻪ ﻣﻨﻈﻮر ﺑﺮرﺳﯽ ﺗﻔﺎوتﻫﺎ از آزﻣﻮن ﺗﺤﻠﯿﻞ واریﺎﻧﺲ یﮏ ﻃﺮﻓﻪ و از آزﻣﻮن ﺗﻌﻘﯿﺒﯽ ﺗﻮﮐﯽ اﺳﺘﻔﺎده ﺷﺪ. ﺳﻄﺢ ﻣﻌﻨﯽداری 0/05 در نظر گرفته شد. تمامی عملیات آماری با نرمافزارversion 16 SPSS انجام گرفت.
ملاحظات اخلاقی
این مطالعه کلیه قوانین و مقررات بینالمللی کار با حیوانات آزمایشگاهی را رعایت و توسط کمیته اخلاق کار با حیوانات دانشکده تایید و کد اخلاق (IR.IAU.SARI.REC.1399.157) برای آن صادر گردید.
جدول 1: توالی پرایمرهای مورد استفاده

نتایج
نتایج مطالعه حاضر نشان داد که گلوگز پلاسما در تمام گروه¬ها به جز گروه دیابت+تمرین شدید+مکمل افزایش معنیداری نسبت به گروه کنترل سالم داشت (P=0/148) در مقایسه با گروه دیابت، تمرین متوسط(P=0/023) و همچنین ترکیب تمرین متوسط+مکمل(P=0/013) و تمرین شدید+مکمل(P=0/001) منجر به کاهش معنادار گلوگز شد. میزان انسولین در تمام گروه¬ها بهجز گروه دیابت+تمرین شدید+ مکمل کاهش معنیداری نسبت به گروه کنترل سالم داشت (P=0/089). در مقایسه با گروه دیابت، تمرین متوسط(P=0/0021) و تمرین متوسط+مکمل (P=0/018) و تمرین شدید+مکمل (P=0/001) منجر به افزایش معنادار انسولین شد (جدول 2). نتایج آزمون تحلیل واریانس یکراهه برای بیان ژن NLRP3 در جدول 3 نشان میدهد که بین گروه¬های مختلف در میزان بیان ژن نسبی NLRP3 تفاوت معناداری وجود دارد (P=0/0001). نتایج آزمون تعقیبی توکی نیز نشان داد که در گروه دیابت (P=0/0001)، دیابتی مکمل (P=0/001)و دیابتی تمرین متوسط (P=0/006) نسبت به گروه کنترل سالم افزایش معناداری در میزان بیان ژن نسبی NLRP3 مشاهده شد. این درحالی است که در گروه¬های مکمل(P=0/021) ، تمرین شدید(P=0/001) ، تمرین متوسط (P=0/009) ، تمرین متوسط+مکمل(P=0/003) و تمرین شدید+مکمل (P=0/0001) نسبت به گروه دیابت کاهش معناداری در میزان بیان ژن نسبی NLRP3 مشاهده شد. نکته جالب توجه در نتایج مشاهده این بود که بین تمرین شدید+مکمل (P=0/103) و تمرین متوسط+مکمل (P=0/089) نسبت به گروه سالم تفاوت معنی داری مشاهده نشد (نمودار 1).
جدول 2: مقایسه (انحراف معیار± میانگین) گلوگز و انسولین پلاسما در گروه سالم و گروههای دیابتی تحت تاثیر تمرین و مکمل

جهت مقایسه از آزمون تحلیل واریانس یکراهه استفاده شد.
* تفاوت معنیدار با دیابت، € تفاوت معنیدار با سالم
جدول 3: نتایج آزمون تحلیل واریانس یکراهه برای بیان ژن NLRP3

وجود تفاوت معنادار (05/0>p) بین گروه های تحقیق
.jpg)
نمودار 1: مقایسه میانگین و انحراف معیار با استفاده از آزمون توکی برای بیان ژن نسبی NLRP3 mRNA گروههای تحقیق.
a: تغییرات معنادار نسبت به گروه کنترل. b: تعییرات معنادار نسبت به گروه دیابت
بحث
یافتههای پژوهش حاضر نشان داد که دیابت نوع دو سبب افزایش قابل توجه گلوکز پلاسما شد که با افزایش بیان ژن NLRP3 بافت پانکراس نسبت به گروه کنترل سالم همراه بود. همسو با این پژوهش، Carlos و همکاران (2017) نشان دادند القای دیابت با استرپتوزوتوسین در موش ها سبب افزایش بیان ژن NLRP3 می¬گردد (19). Kim و همکاران (2016) گزارش کردند که افزایش بیان ژن NLRP3 پیشرفت دیابت را تسهیل می¬کند (20). مطالعات متعددی نشان دادند سرکوب ژنNLRP3 منجر به بهبود تحمل به گلوکز و حساسیت به انسولین و همچنین کاهش سطوح سایتوکین های التهابی سرم و بافتهای متابولیکی و از طرفی افزایش فعالیت مسیر سیگنالینگ PI3K-AKT انسولین موشهای چاق دیابتی میشود (21). از طرفی، عباسی و همکاران (2018) ارتباط مستقیمی بین اینفلامازومNLRP3 ، التهاب مزمن و مقاومت به انسولین را نشان دادند (12). فعالسازی اینفلامازوم NLRP3 در دیابت نوع دو منجر به تولید IL-1β و IL-18 می¬شود که باعث مقاومت به انسولین و اختلالات متابولیکی در بافت¬هایی از قبیل پانکراس می¬شود (12). مطابق با نتایج بدست آمده، هر دو نوع تمرین تناوبی با شدت متوسط و بالا باعث کاهش معنی¬دار بیان اینفلامازوم NLRP3 بافت پانکراس و همچنین کاهش گلوگز در مقایسه با گروه دیابتی شد بهطوریکه تمرین با شدت بالا منجر به کاهش بیشتر این ژن شد. این نتایج با کاهش سطح گلوگز در گروههای تمرینی در مقایسه با گروه دیابت همراه بود. مطالعات نشان داده¬اند که بلاک ژنهای NLRP3 و کاسپاز-1 منجر به بهبود تحمل به گلوکز و حساسیت به انسولین و همچنین کاهش سطوح سایتوکینهای التهابی سرم و بافتهای متابولیکی در موشهای در معرض رژیمهای پر چرب قرار گرفته میشود (22). علاوه براین، عواملی از قبیل هیپرگلیسمی، عدم تعادل ردوکس و عدم تعادل کلسیمی منجر به القاء استرس¬های شبکه آندوپلاسمی میشوند. استرسهای شبکه سارکوپلاسمی از طریق مسیرهای سیگنالینگ IRE-NF-kB ،CHOP و IRE-TRF2-ASK1 منجر به القاء اثرات التهابی و آپوپتوزی میشود. تنظیم منفی بیان فاکتورهای ذکر شده بهوسیله فعالیت ورزشی منجر به کاهش عوامل التهابی از قبیل اینفلامازوم NLRP3،1β-IL ، کاسپاز-1، پروتئینهای تعاملی تیورودوکسین، گونههای اکسیژنی فعال و دیگر عوامل القاء کننده التهاب می¬شود (23). بنابراین ممکن است کاهش سطح گلوگز بعد از هشت هفته تمرین منجر به کاهش بیان NLRP3 بافت پانکراس شده باشد. در تایید این نتایج، عباسی و همکاران (2018) نشان دادند که فعالیت ورزشی استقامتی با شدت متوسط و بالا باعث کاهش معنیدار بیان اینفلامازوم NLRP3 بافت چربی احشایی و کاهش سطوح گلوگز سرمی در مقایسه با گروه دیابتی شده است. نتایج تحقیق حاضر با نتایج تحقیقات Kim و همکاران (24)، Mardare و همکاران (25) وPea و همکاران (26) همخوانی دارد. Kim و همکاران (2019) گزارش کردند که 16 هفته تمرین هوازی با شدت متوسط (دویدن روی تردمیل با سرعت 10 تا 14 متر در دقیقه) و بالا (دویدن روی تردمیل با سرعت 14 تا 18 متر در دقیقه) منجر به کاهش بیان ژن NLRP3 بافت چربی موشهای چاق شد (24).Mardare و همکاران (2016) کاهش سطوح NLRP3 mRNA بافت چربی موشهای چاق را به دنبال 10 هفته تمرینات هوازی و مقاومتی گزارش کردند. در این مطالعه تمرین هوازی شامل دویدن روی تردمیل با شدت 80 درصد حداکثر اکسیژن مصرفی و تمرین مقاومتی شامل سه ست سه دقیقه¬ای انقباض ایزومتریک بود (25). کاهش بیان اینفلامازوم NLRP3 در افراد سالمند به دنبال هشت هفته تمرینات مقاومتی فزاینده در مطالعهPeña و همکاران (2017) گزارش شد (26). عباسی و همکاران (2018) نشان دادند که هشت هفته تمرین هوازی با شدت متوسط (سرعت 16-14 متر در دقیقه) و بالا (سرعت 22-20 متر در دقیقه) منجر به کاهش سطوح NLRP3 mRNA بافت چربی موشهای دیابتی شد ولی تمرین با شدت پایین (سرعت 8-5 متر در دقیقه) اثری بر آن نداشت (12). در مقابل،Zaidi و همکاران (2019) نتیجه گرفتند که 12 هفته تمرین هوازی اثری بر بیان ژن NLRP3 بافت چربی بیماران دیابتی نداشت (14). زارع و همکاران (2020) گزارش کردند که هشت هفته تمرین استقامتی با شدت 80 درصد حداکثر اکسیژن مصرفی اوج اثری بر NLRP3 موشهای چاق نداشت (15). تفاوت در نتایج مطالعات ذکر شده ممکن است به دلیل تفاوت در نمونه تحقیق، پروتکل تمرینی، آزمودنیها و بافت مورد هدف و روش اندازهگیری NLRP3 باشد. در مطالعهZaidi و همکاران (14) آزمودنیها بیماران مبتلا به بیماری شریان کرونری و دیابت بودند و بیان ژن NLRP3 در بافت چربی و لکوسیتهای در گردش اندازه گیری شد. پروتکل تمرینی سه جلسه در هفته و با شدت متوسط انجام شد که شامل دو جلسه فعایت هوازی و یک جلسه فعالیت مقاومتی بود. دو سوم تمرینات بهصورت گروهی و یک سوم تمرینات را هر آزمودنی در منزل اجرا کرد. با توجه به عدم تغییر وزن بدن بعد از تمرین، به نظر میرسد که شدت تمرین به اندازه کافی نبوده که بر سطوح NLRP3 بافت چربی اثرگذار باشد. در مطالعه زارع و همکاران (15)، موشها چاق و غیردیابتی بودند و NLRP3 به روش الایزا اندازهگیری شد. پروتکل تمرینی به مدت هشت هفته و با شدت 80 درصد اکسیژن مصرفی اوج بهصورت دویدن روی تردمیل اجرا شد. با توجه به اینکه در این مطالعه تمرین منجر به کاهش IL-1 شد، اگر اندازهگیری NLRP3 با بیان ژن یا پروتئین انجام میشد ممکن بود نتایج متفاوتی حاصل شود. تشکیل کمپلکس اینفلامازوم NLRP3 سیتوزولیک در دو مرحله انجام می¬شود: گام اول القاء نسخهبرداری اجزای اینفلامازوم از قبیل NLRP3 ، Pro IL-1β و Pro IL-18 از طریق فعالسازی سیگنالینگ NFkB وساطت شده بهوسیله گیرندههای شبه گذرگاهی (TLRs) است. در گام دوم، الیگومریزاسیون هموتیپیک NLRPها افزایش پیدا میکند و موجب شکلگیری اینفلامازوم فعال میشود که قابلیت تبدیل شکلهای نابالغ IL-1β و IL-18به شکلهای بالغ آن را دارد (27). مشخص نیست که اثرات مهاری تمرینات ورزشی بر فعال سازی اینفلامازوم NLRP3 در کدام یک از مراحل تشکیل این کمپلکس انجام میشود. نشان داده شده است تمرینات ورزشی از طریق کاهش فسفوریلاسیون IKKβ منجر به کاهش فعالسازی TLRs در بافتهای مختلف میشود (28). بنابراین، تمرین ممکن است مسیر اینفلامازوم NLRP3 را درگام اول مهار کند. همچنین گزارش شده است، تمرین گام اولیه فعالسازی اینفلامازوم NLRP3 در موشهای چاق را از طریق کاهش استرسهای شبکه آندوپلاسمی را مهار میکند (29). علاوه براین، محققین نشان دادند عملکرد و محتوای میتوکندریایی سلولهای بتا در بیماران مبتلا به دیابت کاهش پیدا میکند. گزارش شد تخریب میتوکندریایی یکی از علل فعال سازی اینفلامازومNLRP3 است. میتوفاژی از طریق حذف میتوکندری های آسیب دیده موجب بهبود هموستاز سلول میشود و به جلوگیری از افزایش التهاب ناشی از فعالسازی اینفلامازوم NLRP3 منجر میشود (30). مطالعات نشان دادند فعالیتهای ورزشی موجب افزایش چگالی و بهبود عملکرد میتوکندریایی سلولهای بتا پانکراس در افراد دیابتی میشود (31). میتوکندری نقش ممهی در تنظیم آپوپتوز سلولهای بتا ایفا میکند و استرس اکسایشی نیز به عنوان یک آغازگر مهم آپوپتوز در سلول های بتا میباشد (32). چندین سازوکار برای اثرات محافظتی تمرین های ورزشی روی آپوپتوز عضله مطرح شده است که شامل تغییر مستقیم در بیان پروتئنیهای مربوط به آپوپتوز، کاهش آزادسازی عوامل آپوپتوژنیک میتوکندری و تغییرات تولید گونه¬های فعال اکسیژن و وضعیت ضداکسایشی می¬باشد (31). به نظر میرسد در اثر تمرین ورزشی عملکـرد میتوکندریهای سلولهای بتا بهبود یافته و این عامل منجر به افزایش مقادیر عاملهای مهاری و کاهش عوامل تحریکی آپوپتوز شده باشد. این موضوع منجر به تحکیم دیواره میتوکندری، جلوگیری از رهاسازی سیتوکروم c، تنظیم کلسیم رها شده از سارکوپلاسمیک و کـاهش اثـرگونه¬های فعال اکسیژن ناشی از فعالیـت ورزشی، ایمنی سلول بتا را بالا میبرد و از آپوپتوز ناشی از استرس جلوگیری میکند. نتایج مطالعه حاضر نشان داد که مکمل ALA اثر همافزایی بر تمرین دارد و مصرف آن به همراه تمرین منجر به کاهش بیشتر NLRP3 بافت پانکراس و سطوح گلوکز پلاسما نسبت به مکمل یا تمرین به تنهایی شد. به نظرمی-رسد تمرین هوازی با شدت متوسط و بالا توانسته از طریق مکانیسم های سلولی وابسته به فعالیت ورزشی باعث کاهش سطح گلوکز در گروههای تمرینی شده باشد. فعالیت ورزشی باعث میشود GLUT-4 از جایگاههای ذخیرهای درون سلولی خود به جایگاههای غشاء پالسمایی و مجاری عرضی سارکولمایی نقل مکان کند (33). انتقال گلوکز با سیگنالهایی تنظیم میشود که با دوگانه تحریک انقباض ارتباط دارند. مهمترین این سیگنال¬ها افزایش کلسیم شبکه سارکوپلاسمی است. این احتمال وجود دارد که کلسیم رها شده در حین انقباض بهطور مستقیم با پروتئینهای SNARE که در انتقال وزیکول های GLUT-4 به سارکولما درگیرند وارد تعامل شوند. به علاوه، کلسیم از مسیرهای پیامرسانی حساس به کلسیم از قبیل ایزوفرم سنتی پروتئین کیناز C و کیناز وابسته به کلسیم یا کالمودولین عمل می¬کنند (34). در مجموع به نظر می¬رسد این نتایج، فعال شدن پروتئین کینازC در انتقال گلوکز عضلانی ناشی از تحریک انقباضی را نشان میدهند. با توجه به اینکه دیابت با افزایش فشار اکسایشی و آپوپتوز سلولهای بتا همراه است (35)، به نظر می رسد که ALA با ویژگیهای آنتیاکسیدانی خود اثرات تمرین ورزشی را تقویت میکند. در این رابطه، مطالعهUchendu و همکاران (2018) نشان داد که ALA منجر به افزایش سوپراکسید دسموتاز و کاتالاز و کاهش مالوندیآلدهید بافت پانکراس موشهای دیابتی شد، که عملکرد آنتیاکسیدانی ALA و توانایی آن در مهار فعالیت رادیکالهای آزاد و بهبود حالت ردوکس را تأیید میکند (36). نشان داده است که فعالسازی مسیر سیگنالینگ آدنوزین منوفسفات حلقوی (cAMP) بوسیله ALA افزایش می¬یابد که این موضوع منجر به افزایش بیان پروتئینهای آنتیآپوپتوزی BCL-2 و BCL-X1 و مهار فعالسازی کاسپازها می¬شود (37). مطالعات نشان دادهاند در افراد مبتلا به دیابت سطح ALA کاهش مییابد (38). چندین مطالعه هم خاصیت آنتیاکسیدانی، ضد التهابی و کاهش قند خون ALA را نشان داده است (40،39). یافته-های مطالعات حاکی از آن هستند که ALA عمل انسولین را از طریق اثر بر مسیر سیگنالینگ انسولین تقلید میکند. این اثر تحریکی با فعال کردن فسفاتیدیل اینوزیتول 3-کیناز (PI3-K) و فعالسازی /Aktپروتئین کیناز B در ارتباط است (41). همچنین درمان طولانی مدت با ALA اکسیداسیون گلوکز و هم تولید گلیکوژن را افزایش میدهد. علاوه براین، تحریک فسفریلاسیون تیروزین در گیرنده انسولین از دیگر نقش¬های اسید لیپوئیک میباشد و میتواند به عنوان یک عامل موثر در بهبود متابولیسم گلوکز و کاهش سطح آن در بیماران دیابتی نوع 2 عمل کند. در تایید این مطلب در مقالات دیگری نیز مطرح شده که استفاده ازALA چه در یک دوره کوتاهمدت و چه طولانیمدت، سبب بهبود مصرف گلوکز در بیماران دیابتی نوع 2 گردیده است (42). EL Midaoui و همکاران در مطالعه خود نشان دادند که رژیم غذایی حاوی ALA در موشهایی که به آنها گلوکز خورانده شده بود، باعث کاهش معنیدار سطح گلوکز و همچنین جلوگیری از ایجاد مقاوت به انسولین از طریق فعالسازی روندهای آنتیاکسیدانی میشود (43). بر اساس نتایج مطالعه Peth و همکاران، لیپوئیک اسید می¬تواند باعث بهبود متابولیسم گلوکز در عضلات اسکلتی و کل بدن در موشهای چاق Zucker مبتلا به مقاومت به شود (44). در مجموع درباره اثر تمرین و مکمل ALA بر میزان NLRP3 در آزمودنی¬های دیابتی مطالعات محدودی انجام شده است. از محدودیتهای تحقیق حاضر می¬توان به عدم اندازهگیری فاکتورهای مرتبط با آپوپتوز در سلولهای بتا اشاره کرد. همچنین، اندازه¬گیری شاخصهای استرس اکسیداتیو در تبیین و تفسـیر بهتر نتایج کمک نماید که در مطالعه حاضر بررسی نشد.
نتیجهگیری
با توجه به یافتههای تحقیق حاضر، به نظر میرسد دیابت با افزایش بیان ژن NLRP3 در بافت پانکراس همراه است و تمرین تناوبی شدید و متوسط به همراه مصرف مکمل آلفالیپوئیک اسید میتواند با کاهش سطوح گلوگز خون و ماومت به انسولین احتمالا باعث کاهش میزان NLRP3 بافت پانکراس و التهاب ناشی از مسیر سیگنالینگ NLRP3 را کاهش و کنترل کند. با وجود این، با توجه به مطالعات اندک انجام شده در این رابطه، درک اثرات فعالیت ورزشی بر فاکتورهای درگیر در التهاب ناشی از بیماری دیابت نیاز به پژوهشهای بیشتری دارد.
سپاسگزاری
این مقاله مستخرج از رساله دکتری دانشگاه آزاد اسلامی واحد ساری است. بدین وسیله نویسندگان از کلیه کسانی که در انجام این پژوهش یاری رساندند تشکر و قدردانی می-نمایند.
حامی مالی: ندارد.
تعارض در منافع: وجود ندارند.
References:
1- Sproston NR, Ashworth JJ. Role of C - reactive protein at Sites of Inflammation and Infection. Front Immunol 2018; 9: 754.
2- Groslambert M, Py BF. Spotlight on the NLRP3 Inflammasome Pathway. Inflamm Res 2018; 11: 359-74.
3- Vandanmagsar B, Youm YH, Ravussin A, Galgani JE, Stadler K, Mynatt RL, et al. The NLRP3 Inflammasome Instigates Obesity-Induced Inflammation And Insulin Resistance. Nat Med 2011; 17(2): 179-88.
4- Dixit VD. Nlrp3 Inflammasome Activation in Type 2 Diabetes: Is it Clinically Relevant? Diabetes 2013; 62(1): 22-4.
5- Golbidi S, Badran M, Laher I. Diabetes and Alpha Lipoic Acid. Front Pharmacol 2011; 2: 69.
6- Rochette L, Ghibu S, Muresan A, Vergely C. Alpha-Lipoic Acid: Molecular Mechanisms and Therapeutic Potential in Diabetes. Can J Physiol. Pharmacol 2015; 93(12): 1021-7.
7- Midaoui A, Fantus G, Boughrous A, Couture R. Beneficial Effects of Alpha-Lipoic Acid on Hypertension, Visceral Obesity, UCP-1 Expression and Oxidative Stress in Zucker Diabetic Fatty Rats. Antioxidants 2019; 8(12): 648.
8- Malin KS, Francois M, Eichner Z, Gilbertson N, He ston E, Fabris C. Impact of Short-Term Exercise Training Intensity on -Cell Function in Older Obese Adults with Prediabetes. J Appl Physiol 2018; 125(6): 1979-86.
9- Heiskanen MA, Motiani KK, Mari A, Saunavaara V, Eskelinen JJ, Virtanen KA, et al. Exercise Training Decreases Pancreatic Fat Content and Improves Beta Cell Function Regardless of Baseline Glucose Tolerance: A Randomised Controlled Trial. Diabetologia 2018; 61(8): 1817-28.
10- Holmes A, Coppey LJ, Davidson EP, Yorek MA. Rat Models of Diet-Induced Obesity and High Fat/Low Dose Streptozotocin Type 2 Diabetes: Effect of Reversal of High Fat Diet Compared to Treatment with Enalapril or Menhaden Oil on Glucose Utilization and Neuropathic Endpoints. J Diabetes Res 2015; 2015: 307285.
11- Lee J, Lee Y, LaVoy E, Umetani M, Hong J, Park Y. Physical Activity Protects NLRP3 Inflammasome-Associated Coronary Vascular Dysfunction in Obese Mice. Physiol Rep 2018; 6(12): 45-58.
12- Abbasi A, Faramarzi M, Ghatreh Samani M, Bbanitalebi E. The Effect of Different Intensities of Endurance Training on NLRP-3 Inflammasome Protein Expression in Visceral Adipose Tissue, Serum Glucose Levels and Insulin in Streptozotocin-Induced Diabetic Rats. Metabolism and Exercise, 2018; 7(1): 1-19. [Persian]
13- Khakroo Abkenar I, Rahmani-nia F, Lombardi G. The Effect of Different Intensities of Acute and Chronic Aerobic Activity on the Signaling Pathway of the Inflammasome NLRP3 Complex and TLR4 and Some Inflammatory Cytokines in Young Men. Practical Studies of Biosciences in Sport 2020; 8(16): 116-120. [Persian]
14- Zaidi H, Byrkjeland R, Njerve I, Akra A, Solheim S, Arnesen H, et al. Effects of Exercise Training on Inflammasome-Related Mediators and Their Associations to Glucometabolic Variables in Patients with Combined Coronary Artery Disease and Type 2 Diabetes Mellitus: Sub-Study of A Randomized Control Trial. Diab Vasc Dis Res 2019; 16(4): 360-8.
15- Zare Damirchi Z, Bashiri J, Narimani Rad MP, Hadi H. The Effect of Eight Weeks of Endurance Training and Olive Oil Supplementation on IL-1ß and NLRP3 Indices in Obese Male Rats. Yafte 2020; 22(3): 95-107. [Persian]
16- Faridnia M, Mohebbi H, Khalafi M, Moghaddami K, Khalafi M. The Effect of Interval and Continuous Training on the Content of Perilipin 1, ATGL and CGI -58 in Visceral Adipose Tissue of Obese Male Rats. SJKU 2019; 24(1): 78-89. [Persian]
17- Dworacka M, Chukanova G, Iskakova S, Kurmambayev Y, Wesołowska A, Frycz B. New Arguments for Beneficial Effects of Alpha-Lipoic Acid on the Cardiovascular System in the Course of Type 2 Diabetes. Eur J Pharm Sci 2018; 117: 41-7.
18- Karimi N, Bohlooli S, Mazani M. Nanoliposomal Formulation of Ecballium Elaterium Extract: Cytotoxic Evaluation Against Human Gastric Adenocarcinoma (AGS) Cell Line. Nanomedicine Research Journal 2016; 1(1): 9-14.
19- Carlos D, Costa FRC, Pereira CA, Rocha FA, Yaochite JN, Oliveira GG, et al. Mitochondrial DNA Activates the NLRP3 Inflammasome and Predisposes to Type 1 Diabetes in Murine Model. Front Immunol 2017; 8: 164.
20- Kim Y, Wang W, Okla M, Kang I, Moreau R, Chung S. Suppression of NLRP3 Inflammasome by Γ-Tocotrienol Ameliorates Type 2 Diabetes. J Lipid Res 2016; 57(1): 66-76.
21- Stienstra R, van Diepen JA, Tack CJ, Zaki MH, van de Veerdonk FL, Perera D, et al. Inflammasome Is a Central Player in the Induction of Obesity and Insulin Resistance. Proc Natl Acad Sci USA 2011; 108(37): 15324-9.
22- Freigang S, Ampenberger F, Weiss A, Kanneganti T-D, Iwakura Y, Hersberger M, et al. Fatty Acid-Induced Mitochondrial Uncoupling Elicits Inflammasome Independent IL-1 [Alpha] And Sterile Vascular Inflammation In Atherosclerosis. Nat Immunol 2013; 14(10): 1045-53.
23- Hong J, Kim K, Kim J-H, Park Y. The Role of Endoplasmic Reticulum Stress in Cardiovascular Disease and Exercise. Int J Vasc Med 2017; 2017: 2049217.
24- Kim Y, Pitriani P, Park G, Lee W. Moderate Intensity Exercise Has More Positive Effects on The Gene Expression of Inflammasome, M1, M2 Macrophage Infiltration and Brown Adipocyte Markers Compared to High Intensity Exercise in Subcutaneous Adipose of Obese Mice Induced by High Fat Diet. Life Science 2019; 29 (3): 303-10.
25- Mardare C, Krüger K, Liebisch G, Seimetz M, Couturier A, Ringseis R, et al. Endurance And Resistance Training Affect High Fat Diet-Induced Increase of Ceramides, Inflammasome Expression, and Systemic Inflammation in Mice. J Diabetes Res 2016; 2016: 4536470.
26- Mejías-Peña Y, Estébanez B, Rodriguez-Miguelez P, Fernandez-Gonzalo R, Almar M, de Paz JA, et al. Impact of Resistance Training on the Autophagyinflammation-Apoptosis Crosstalk in Elderly Subjects. Aging (Albany NY) 2017; 9(2): 408-18.
27- He Y, Franchi L, Núñez G. TLR Agonists Stimulate Nlrp3-Dependent IL-1β Production Independently of the Purinergic P2X7 Receptor in Dendritic Cells and in Vivo. Immunology 2013; 190(1): 334-9.
28- Oliveira AG, Carvalho BM, Tobar N, Ropelle ER, Pauli JR, Bagarolli RA, et al. Physical Exercise Reduces Circulating Lipopolysaccharide and TLR4 Activation and Improves Insulin Signaling in Tissues of DIO Rats. Diabetes 2011; 60(3): 784-96.
29- Goossens GH, Blaak EE, Theunissen R, Duijvestijn AM, Clément K, Tervaert JWC, et al. Expression of NLRP3 Inflammasome and T Cell Population Markers in Adipose Tissue are Associated with Insulin Resistance and Impaired Glucose Metabolism in Humans. Mol Immunol 2012; 50(3): 142-9.
30- Rovira-Llopis S, Apostolova N, Ban-uls S, Muntane J, Rocha M, Victor V. Mitochondria, the NLRP3 Inflammasome, and Sirtuins in Type 2 Diabetes: New Therapeutic Targets. Antioxid & Redox Signal 2018; 29(8): 749-90.
31- Peterson JM, Bryner RW, Sindler A, Frisbee JC, Alway SE. Mitochondrial Apoptotic Signaling is Elevated in Cardiac But Not Skeletal Muscle in the Obese Zucker Rat and is Reduced with Aerobic Exercise. J Appl Physiol 2008; 105(6): 1934-43.
32- Marin-Garcia J, Goldenthal MJ. Mitochondrial Centrality in Heart Failure. Heart Fail Rev 2008; 13(2): 137-50.
33- Pereira RM, Moura LP, Muñoz VR, Silva AS, Gaspar RS, Ropelle ER, et al. Molecular Mechanisms of Glucose Uptake in Skeletal Muscle at Rest and In Response to Exercise. Motriz- Revista De Educação Física 2017; 23: e101609.
34- Sylow L, Kleinert M, Richter EA, Jensen TE. Exercise-Stimulated Glucose Uptake [Mdash] Regulation and Implications for Glycaemic Control. Nat Rev Endocrinol 2017; 13(3): 133-48
35- EL-Sabbagh D, Dawood L, Abdallah AA, Hassan S. Effect of Alpha Lipoic Acid on Apoptotic Mechanisms and Oxidative Stress in Pancreatic Cells of High Fat Diet Induced Type II Diabetes Mellitus in Rats. Med J Cairo Univ 2019; 87(3): 1615-23.
36- Uchendu C. Chronic Co-Exposure to Chlorpyrifos and Deltamethrin Pesticides Induces Alterations in Serum Lipids and Oxidative Stress in Wistar Rats: Mitigating Role of Alpha-Lipoic Acid. Environ Sci Pollut Res 2018; 25(20):19605-11.
37- Kim SJ, Nian C, Widenmaier S, Mcintosh CH. Glucose-Dependent Insulinotropic Polypeptide-Mediated Up-Regulation of Β -Cell Antiapoptotic Bcl-2 Gene Expression is Coordinated by Cyclic AMP (Camp) Response Element Binding Protein (CREB) and Camp-Responsive CREB Coactivator 2. Mol Cell Biol 2008; 28 (5): 1644-56.
38- Mendoza-Núñez VM, García-Martínez BI, Rosado-Pérez J, Santiago-Osorio E, Pedraza-Chaverri J, Hernández-Abad VJ. The Effect of 600 Mg Alpha-Lipoic Acid Supplementation on Oxidative Stress, Inflammation, and RAGE in Older Adults with Type 2 Diabetes Mellitus. Oxidative Medicine and Cellular Longevity 2019; 3276958; 67-79.
39- Gorąca A, Huk-Kolega H, Piechota A, Kleniewska P, Ciejka E, Skibska B. Lipoic Acid-Biological Activity and Therapeutic Potential. Pharmacological Reports 2011; 63: 849-58.
40- Akbari M, Ostadmohammadi V, Tabrizi R, Mobini M, Lankarani KB, Moosazadeh M, et al. The Effects of Alpha-Lipoic Acid Supplementation on Inflammatory Markers among Patients with Metabolic Syndrome and Related Disorders: A Systematic Review and Meta-Analysis of Randomized Controlled Trials. Nutr Metabol 2018; 15(1): 39.
41- Yamawaki H, Kuramoto J, Kameshima S, Usui T, Okada M, Hara Y. Omentin. A Novel Adipocytokine Inhibits Tnf-Induced Vascular Inflammation in Human Endothelial Cells. Biochem Biophys Res Commun 2011; 408(2): 339-43.
42- Liu R, Wang X, Bu P. Omentin-1 Is Associated With Carotid Atherosclerosis In Patients With Metabolic Syndrome. Diabetes Res Clin Pract 2011; 93(1): 21-5.
43- El Midaoui A, de Champlain J. Prevention of Hypertension, Insulin Resistance, and Oxidative Stress by Alpha-Lipoic Acid. Hypertension 2002; 39(2): 303-7.
44- Peth JA, Kinnick TR, Youngblood EB, Tritschler HJ, Henriksen EJ. Effects of a Unique Conjugate of Alpha-Lipoic Acid and Gamma-Linolenic Acid on Insulin Action in Obese Zucker Rats. Am J Physiol Regul Integr Comp Physiol 2000; 278(2): 453-9.
نوع مطالعه: پژوهشي |
موضوع مقاله:
فیزیولوژی ورزش
دریافت: 1400/4/20 | پذیرش: 1400/8/12 | انتشار: 1401/2/15
دریافت: 1400/4/20 | پذیرش: 1400/8/12 | انتشار: 1401/2/15
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |







